2025年版《中国药典》已正式实施2个多月,其对生物制品生产用动物细胞基质的质量控制要求进行了重要修订。本次修订对生物制品生产企业和检测机构的影响路径和深度虽有差异,但都指向一个核心转变:从"遵循规定"到"证明科学性"。接下来,我们将详细解读修订的核心内容,以及行业应对策略。
一、核心修订:通则0234的结构性升级
2025年版最明显的结构性调整,是将2020年版的《生物制品生产检定用动物细胞基质制备及质量控制》通则一分为二:
-
通则0234:聚焦"生产用"动物细胞基质
-
通则0235:聚焦"检定用"动物细胞基质
这一拆分让标准更具针对性,其中通则0234(生产用)有三个关键修订值得关注:
- 适用范围扩展:
首次将昆虫细胞纳入监管范围,以适应新型生物技术产品(如某些病毒载体、重组蛋白)的生产需求,有利于杆状病毒表达系统等新技术路线的标准化。
- 监管理念进化:
全面引入风险评估策略。监管要求从部分"强制性描述"转变为"基于风险评估的指导",给予企业在检测项目设计上更大的科学决策空间。
- 检测技术更新:
在传统检测方法(如体外接种、动物接种法)基础上,明确允许采用基于核酸扩增方法或下一代测序技术,作为特定病毒检测的补充或替代方案,提升了检测的灵敏度与广度。
二、2025版 vs 2020版:多维度对比
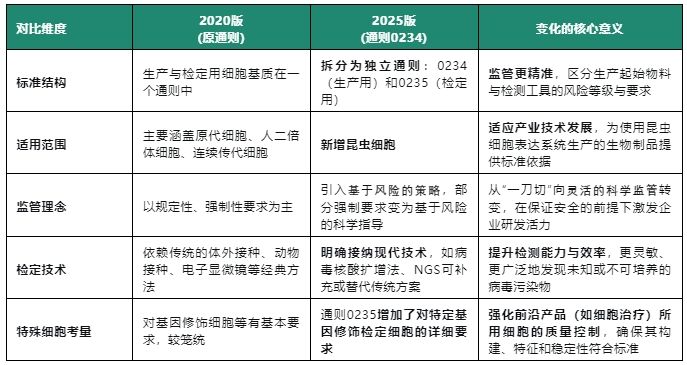
三、与国际药典及指导原则接轨
本次修订显著加强了与国际主流标准的协调对接,体现在:
1. 与ICH指导原则的深度协调
Ø 理念一致:引入的"风险评估"理念,与ICH Q9质量风险管理的核心思想完全一致。
Ø 技术要求同步:细胞历史、来源、细胞库(MCB/WCB)体系、鉴别、纯度(无菌、支原体、外源病毒)等核心要素的要求,与ICH Q5D用于生物制品生产的细胞基质的来源和鉴定高度契合。
Ø 标准互认:在通用检测方法上,中国药典与美国药典(USP)、欧洲药典(EP)和日本药典(JP)的相关章节已在ICH的推动下,通过药典讨论组(PDG)和ICH Q4B流程实现了部分标准的互认与协调。例如,微生物限度、无菌检查、内毒素检测等方面,药典相关章节已被认为可以互换使用。
2. 采纳WHO及国际前沿实践
Ø 修订明确遵循世界卫生组织(WHO)的相关技术指南。
Ø 引入NGS等先进技术用于病毒安全性检测,与国际上应对生物生产过程中外源因子污染风险的最新共识与实践同步。国际产业联盟(如CAACB)持续收集和分享此类数据,有利于完善风险控制策略。
3. 保留中国监管特色的优化:
Ø 在充分协调国际标准的同时,修订紧密结合我国生物制品监管体系和GMP全面实施的现状。如对异常毒性检查等项目的调整,既参考了国际"逐渐取消常规检查"的经验,也结合了我国医药发展的现状。
四、修订意义:监管更科学
-
监管理念升级:0234通则的修订,代表着我国生物制品监管标准从"符合性监管"向"科学性监管"和"发展性监管"的关键转型。
-
科学价值提升:以风险评估为基础,结合先进检测技术,使质量控制更精准、更高效。
-
产业创新激活:2025版药典的前瞻性(如纳入昆虫细胞)为技术路线创新铺平道路。监管策略的灵活性降低了不必要的成本,有利于激发行业活力。
4. 国际竞争力跃升:深度协调ICH、WHO等国际标准,显著提升了中国药典的国际地位和影响力,为中国生物医药产品的全球研发、申报和市场准入提供了便利。
义翘神州的贯彻标准
作为生物医药关键质量控制的第三方伙伴,义翘神州****安全检测实验室将2025版《中国药典》(ChP2025)通则0234的修订视为服务能力升级的战略拐点。这不是一次简单的"标准对标",而是将构建一个"技术引领、方案前瞻、服务增值"的新型服务体系。
我们已系统地完成从先进方法学验证到整体解决方案设计的全面升级,助力客户无缝应对从"规定性检查"到"科学性证明"的监管范式转变。我们为适应新规、赋能产业所完成的关键能力建设与服务升级,标志着我们已从传统的"检测执行者"转型为生物制品细胞基质质量控制的"科学合作伙伴"与"风险管控顾问"。
新规之下,我们的准备已经完成,只待与您携手同行。