目录
[1. 引言](#1. 引言)
[结果1: 盐胁迫下小麦根系单细胞转录组图谱的构建](#结果1: 盐胁迫下小麦根系单细胞转录组图谱的构建)
[结果5: 拟时序分析揭示根毛细胞的不同响应](#结果5: 拟时序分析揭示根毛细胞的不同响应)
[结果6:过表达 TaGSTU1-5B 通过清除活性氧提高耐盐性](#结果6:过表达 TaGSTU1-5B 通过清除活性氧提高耐盐性)
[结果7: 盐胁迫增强了多倍体小麦根系中的非对称基因表达](#结果7: 盐胁迫增强了多倍体小麦根系中的非对称基因表达)
放在前面
核心内容:本研究利用snRNA测序技术在单细胞分辨率下构建了盐胁迫下小麦根系的转录组图谱,系统揭示了盐敏感与耐盐品种的差异化响应机制。研究揭示了根毛细胞是盐胁迫响应的关键细胞类型,耐盐品种DK通过增强代谢重编程和细胞修复能力,相较于依赖快速应激信号的CS表现出更强耐性,进一步验证了TaGSTU1-5B基因通过清除活性氧增强耐盐性的作用机制,并揭示了盐胁迫会特异性增强六倍体小麦A/D主导型亚基因组同源基因的不对称表达。该研究为解析小麦耐盐机制提供了单细胞水平的见解,为作物耐盐遗传改良奠定了关键理论基础与基因资源。
OA文章链接:https://pubmed.ncbi.nlm.nih.gov/41133438/
公众号解读:https://mp.weixin.qq.com/s/1i6GNJyBLq8c967zBef3CA?scene=1
摘要
土壤盐渍化严重威胁小麦的产量与品质。根系是植物响应盐胁迫的关键器官,但其在细胞类型水平上的分子机制尚不明确。本研究对盐敏感品种(CS)和耐盐品种(DK)在盐胁迫条件下的根尖进行了首次单细胞核RNA测序分析,成功获取了188,270个高质量根部细胞的表达谱。通过已报道的标记基因及参考图谱,我们鉴定并验证了17种细胞类型。
细胞类型特异性分析发现,根毛细胞与盐胁迫的关联最为显著,其品种特异性的转录变化可能与DK品种优异的耐盐性密切相关。对根毛细胞的基因差异分析表明,CS品种倾向于快速的应激信号传导和渗透调节物质积累,而DK品种则更侧重于代谢重编程和细胞修复机制。
拟时序分析锁定 TaGSTU1-5B 为提高小麦耐盐性的关键候选基因,后续过表达实验证实该基因能通过介导活性氧(ROS)清除来显著增强小麦的耐盐能力。此外,亚基因组分析揭示盐胁迫增强了多倍体小麦根系中同源基因(homeologs)的非对称表达,且A和D亚基因组占优势的同源基因与盐响应的关联度更高。本研究首次构建了盐胁迫下小麦根系的单细胞图谱,揭示了细胞类型及品种特异性的盐响应模式,为理解小麦耐盐与适应性的分子基础提供了全新见解。
1. 引言
盐渍化是威胁全球农业生产力最严峻的非生物胁迫之一。它不仅对作物的生长、发育和产量产生负面影响,还会损害土壤健康并破坏生态平衡(Munns and Gilliham 2015; Morton et al. 2019)。目前,全球约20%的可耕地正遭受盐渍化困扰,由此造成的经济损失每年估计超过270亿美元(Qadir et al. 2014; Munns et al. 2020)。随着气候变化的持续、灌溉措施的不当以及不可持续的耕作方式,预计到2050年,超过50%的可耕地将被盐渍化(Lord 2024)。因此,解析植物响应和抵抗盐胁迫的分子机制,对于开发优质耐盐作物新品种至关重要,这也是应对盐渍化挑战和人口增长压力的关键。
为了应对这些挑战,先进的基因组学工具不可或缺。单细胞核RNA测序(snRNA-seq)技术是一种新兴的前沿高通量测序方法,能够在单细胞分辨率下解析个体细胞的转录组。该技术可以揭示细胞异质性、获取细胞类型特异性信号、构建细胞图谱,并明确器官中各类细胞的特征与状态(Zhang, He, et al. 2023; Tan et al. 2024; Li et al. 2024)。因此,snRNA-seq已被广泛应用于生物学和医学研究,在理解细胞类型多样性、细胞间通信、等位基因表达以及细胞发育轨迹方面推动了重大进展(Tang et al. 2009; Zhong et al. 2018; Farrell et al. 2018; Shao et al. 2020; Wang, Sun, et al. 2023)。在植物研究领域,snRNA-seq首先应用于拟南芥(Shulse et al. 2019),随后扩展到多种物种和组织,包括水稻根系(Liu et al. 2021)、玉米发育中的幼穗(Xu et al. 2021)、杨树分化中的茎部木质部(Xie et al. 2022)、番茄茎尖(Tian et al. 2020)、棉花色素腺体(Sun et al. 2023)以及小麦根系(Zhang, Li, et al. 2023; Du, Zhang, et al. 2025)。这些研究彰显了snRNA-seq在解析植物复杂性状和胁迫响应中的重要价值。
值得注意的是,根系是感知并响应盐环境的关键部位,snRNA-seq为高分辨率揭示细胞类型特异性的胁迫响应提供了强有力的手段------而这一领域目前仍探索不足(Zhu et al. 2025)。近期利用snRNA-seq开展的研究已为植物响应各种环境胁迫提供了重要见解(Liu et al. 2021; Wendrich et al. 2020)。例如,该技术已被用于研究玉米根系受真菌侵染过程中的细胞类型特异性转录调节网络(Cao et al. 2023)、烟草根系对入侵响应的细胞和分子机制(Jia et al. 2025)、玉米根系的时空热应激响应(Wang, Wang, et al. 2025)、水稻根系的土壤胁迫响应(Zhu et al. 2025)、拟南芥根尖的渗透响应(Liu et al. 2024),以及棉花和不结球蔓菁的根系响应(Li et al. 2024; Liu, Kang, et al. 2025)。这些前期成果凸显了snRNA-seq在理解不同植物物种应激机制方面的广泛适用性和有效性(Zhu et al. 2025)。尽管取得了这些进展,但在小麦等主要作物中,单细胞水平的应激响应研究仍然匮乏。
普通小麦(Triticum aestivum L. )是关乎全球粮食安全的重要主粮作物,年产量超过7.7亿吨,全球种植面积超过2.2亿公顷,为人类提供了约20%的每日热量和蛋白质摄入(IWGSC 2018; Tadesse et al. 2019)。此外,小麦表现出比水稻和玉米更强的固有耐盐性,使其特别适合在干旱和半干旱地区的盐渍地或边际土地上种植(Mujeeb-Kazi et al. 2019; Naeem et al. 2020)。在响应盐胁迫的研究中,Zheng等证明了TaHAG1 在增强耐盐性中起关键作用(Zheng et al. 2021);Wang等发现TaSPL6-D 的变异通过激活TaHKT1;5-D 赋予植物耐盐性,同时能保持产量相关性状(Wang et al. 2024);另一项研究则报道了关键基因TaGPAT6通过合成角质和木栓质单体形成有效的扩散屏障来增强耐盐性(Wang, Chi, et al. 2025)。然而,尽管已有大量关于盐相关数量性状位点(QTLs)、候选基因和分子通路的研究,但在单细胞水平上,小麦耐盐的内在机制仍不十分明确(Liu, Wang, et al. 2025)。因此,深入理解小麦耐盐性的分子基础,不仅有助于培育耐盐品种,还能为植物普遍的应激响应提供启示。
在本研究中,我们对耐盐和盐敏感的小麦品种在盐胁迫0小时、3小时和8小时后的样本进行了snRNA-seq分析,旨在鉴定单细胞水平的转录组图谱。随后,我们系统地研究了不同的细胞群、表达模式和调控网络,以表征关键的功能候选基因。值得注意的是,通过对候选基因TaGSTU1-5B进行过表达的功能验证,证实了其在增强小麦耐盐性方面的正向作用。本项工作代表了小麦在盐胁迫下的首次单细胞核转录组研究,为这一全球重要作物的盐响应分子和细胞机制提供了新见解。我们的研究结果为未来的功能基因组学研究和耐盐小麦品种的选育铺平了道路。
结果1: 盐胁迫下小麦根系单细胞转录组图谱的构建
为了验证两个小麦品种(DK961和CS)的耐盐性,我们对其耐盐表型进行了鉴定。对两个品种根系的相对干重和相对根长进行的统计分析显示,DK品种的相对根长和相对干重均显著高于CS品系(图 S1A--D)。这些结果进一步证实了DK为耐盐品种,而CS为盐敏感品种。
为了剖析小麦根系细胞对盐分动态转录响应,我们利用三叶期两个小麦品种的根尖构建了高分辨率的单细胞核转录组(snRNA-seq)图谱,这两个品种分别是盐敏感品种"中国春"(Chinese Spring, CS)和耐盐品种"德抗961"(Dekang 961, DK,通过表型评估筛选)。实验设计包括每个品种的三种处理条件:正常对照(不含NaCl;CS_0h, DK_0h)、3小时盐处理(200 mM NaCl;CS_3h, DK_3h)以及8小时盐处理(200 mM NaCl;CS_8h, DK_8h)(图 1A)。在对细胞核分离方案进行严格优化后(Du, Chen, et al. 2025),我们从12个数据集中生成了201,273个单细胞核转录组,平均每个样本包含16,773个细胞核。在剔除双细胞、低质量细胞核(线粒体基因含量 > 5%)以及酶解受损细胞后,最终获得了188,270个高置信度细胞核,每个细胞核检测到的基因中位数为4766个(图 S1E--K 和表 S1)。
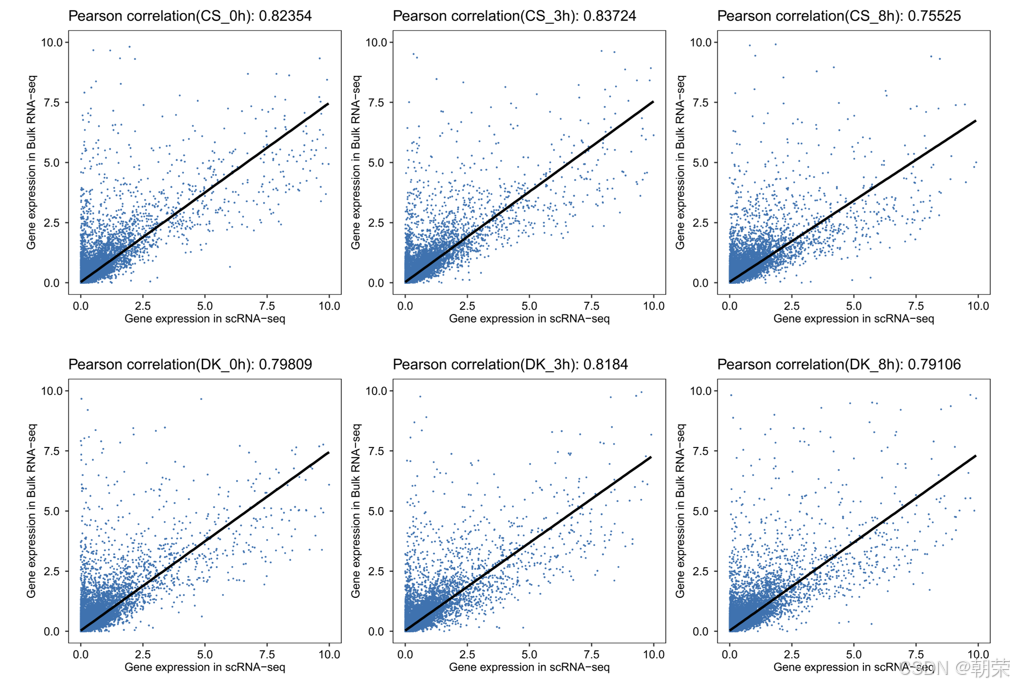
为了验证snRNA-seq数据的可靠性,我们将其与大批量转录组(bulk RNA-seq)数据集进行了交叉验证。匹配样本间的皮尔逊相关系数(PCCs)范围在0.76至0.84之间(图 S2A),表现出强一致性,证实了snRNA-seq数据的整体可靠性。此外,snRNA-seq数据集的样本间相关性分析显示,条件匹配的样本比两个品种间的样本具有更高的转录相似性(图 S2B 和 S3A,B),这表明品种的遗传背景对基因表达的影响可能比盐胁迫处理更为显著,反映了品种特异性特征和耐盐机制的多样性。
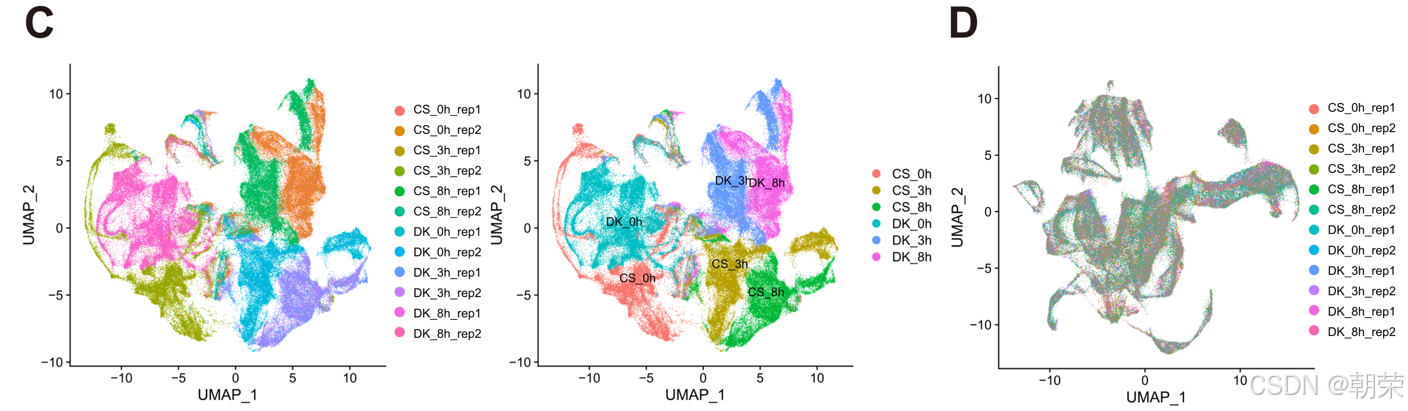
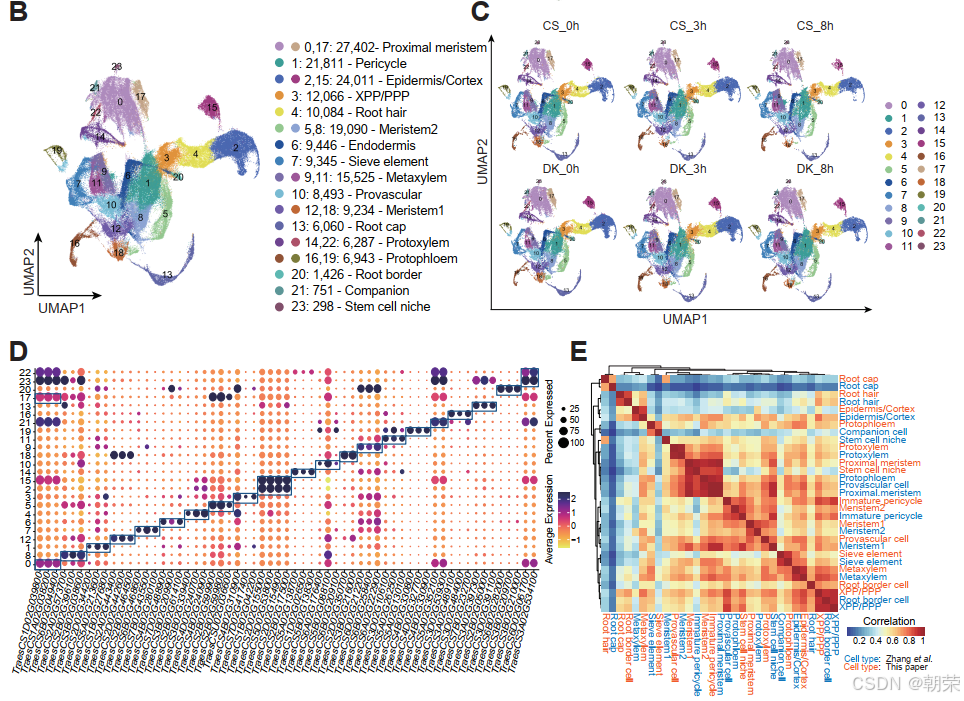
为了消除多样本snRNA-seq工作流中固有的技术批次效应(图 S3C,D),我们采用典型相关分析(CCA)整合数据集,随后通过均匀流形近似与投影(UMAP)进行嵌入分析(图 1B,C 和 S4A,B)。该分析划分出24个细胞簇,共同代表了正常和盐胁迫条件下小麦根尖的细胞图谱。此外,我们鉴定并可视化了具有高度限制性表达模式的细胞簇特异性标记基因(图 1D 和 S4C),进一步验证了聚类结果的稳健性。
综上所述,本研究建立了详尽且可靠的小麦根系盐胁迫响应单细胞转录组图谱,为研究小麦耐盐性中保守的和品种特异性的调节机制提供了宝贵的资源和见解。
结果2:根系细胞类型的鉴定与验证
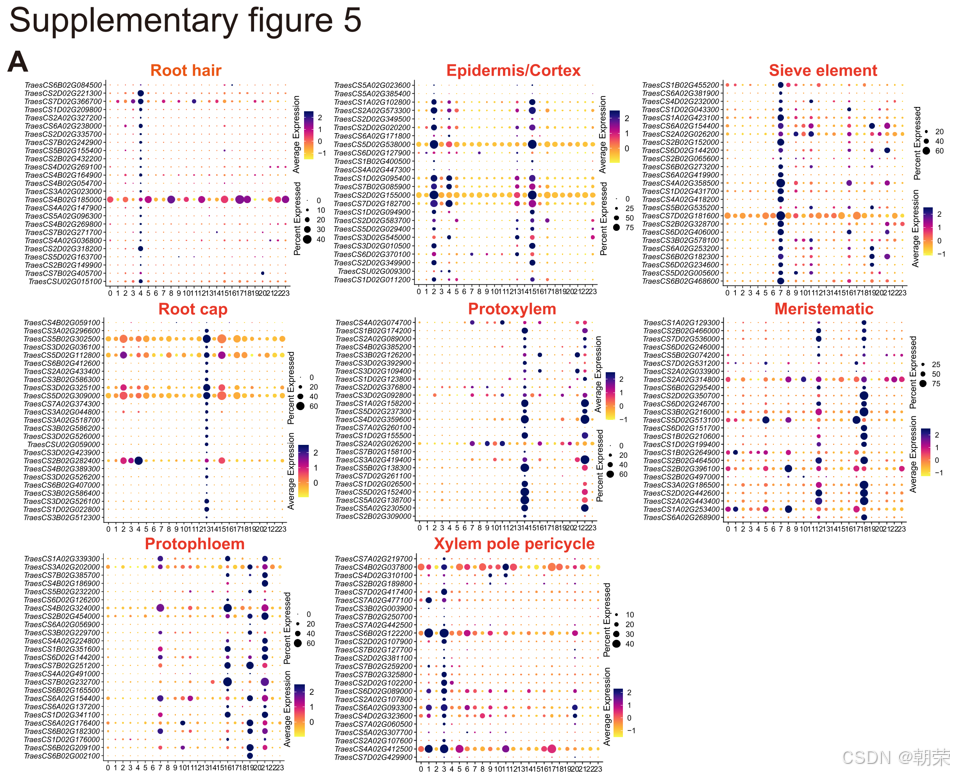
我们对24个转录细胞簇进行了系统的注释。首先,通过挖掘植物单细胞转录组注释精选库scPlantDB数据库(He et al. 2024),鉴定了保守的标记基因。通过分析这些标记基因在各细胞簇中的特异性表达模式(表 S2),我们精确注释了关键的细胞谱系,包括:根毛(root hair,细胞簇4)、表皮/皮层(epidermis/cortex,细胞簇2, 15)、根冠(root cap,细胞簇13)、筛管分子(sieve elements,细胞簇7)、原生木质部(protoxylem,细胞簇14, 22)、分生组织细胞(meristem cells,细胞簇5, 8, 12, 18)、木质部/韧皮部原始周鞘(XPP/PPP,细胞簇3)、干细胞生态位(stem cell niche,细胞簇23)、原生韧皮部(protophloem,细胞簇16, 19)以及周鞘(pericycle,细胞簇1)(图 S5A,B;补充信息)。
同时,通过在我们的数据集中检查参考snRNA-seq图谱(Zhang, He, et al. 2023)中前列标记基因的表达模式,我们验证了先前鉴定的16个细胞簇的身份,并发现了额外的细胞类型,包括:原形成层细胞(provascular cells,细胞簇10)、内皮层(endodermis,细胞簇6)、近端分生组织(proximal meristem,细胞簇0, 17)、根边缘细胞(root border cells,细胞簇20)、伴胞(companion cells,细胞簇21)以及后生木质部(metaxylem,细胞簇9, 11)。此外,根据参考图谱中分生组织2(meristem2)标记基因在细胞簇12和18中的特异性表达,我们将分生组织亚群进一步细分为分生组织1(meristem1,细胞簇5, 8)和分生组织2(meristem2,细胞簇12, 18)(图 S6A,B;方法部分)。与参考图谱的交叉验证显示,匹配的细胞类型之间具有极强的转录一致性,进一步支持了我们注释的可靠性(图 1E 和 S7A,B;补充信息)。
此外,为了证实细胞类型划分的生物学相关性,我们对每个细胞簇特异性上调的差异表达基因(up-DEGs)进行了基因本体(GO)富集分析(表 S3 和 S4)。每个细胞簇中富集程度前15名的显著生物学过程(BP)与其注释细胞类型的生理功能高度一致。例如,被鉴定为近端分生组织的细胞簇0和17,富集了诸如姐妹染色单体分离(GO:0000819)、染色体组织(GO:0051276)、DNA拓扑结构变化(GO:0006265)和核糖体生物合成(GO:0042254)等条目,这与其活跃的细胞生长和分裂功能相符。同样,被注释为根毛细胞的细胞簇4,富集了根毛伸长(GO:0048767)和根系发育调节(GO:2000280)等条目。被鉴定为后生木质部细胞的细胞簇9和11,则在生长素稳态和生长素外流相关条目中表现出显著富集,反映了它们在木质素沉积中的作用。这些结果共同证明了我们细胞类型注释的可靠性(图 S8A,B;补充信息)。
这些结果确认了我们细胞类型注释的稳健性,并描绘了不同细胞谱系中由盐胁迫诱导的转录重编程过程,突出了不同细胞类型在应对渗透挑战时的特异性适应性响应(图 1)。
结果3:CS和DK根系中细胞类型特异性的盐胁迫响应
为了在单细胞分辨率下研究保守及品种特异性的细胞类型响应,我们对比了CS和DK在对照组(0h)与盐处理组(3h、8h)之间的细胞类型比例变化(图 2A,S9A--C 和表 S5)。两个品种表现出一些共同的响应,包括根毛和分生组织2(meristem2)群体显著减少(Student's t-test, p < 0.05),而原生韧皮部和未成熟周鞘群体显著扩张(Student's t-test, p < 0.05)(图 S9A--C,S10A 和 S11A),这表明它们在应对渗透胁迫时存在保守的机制。
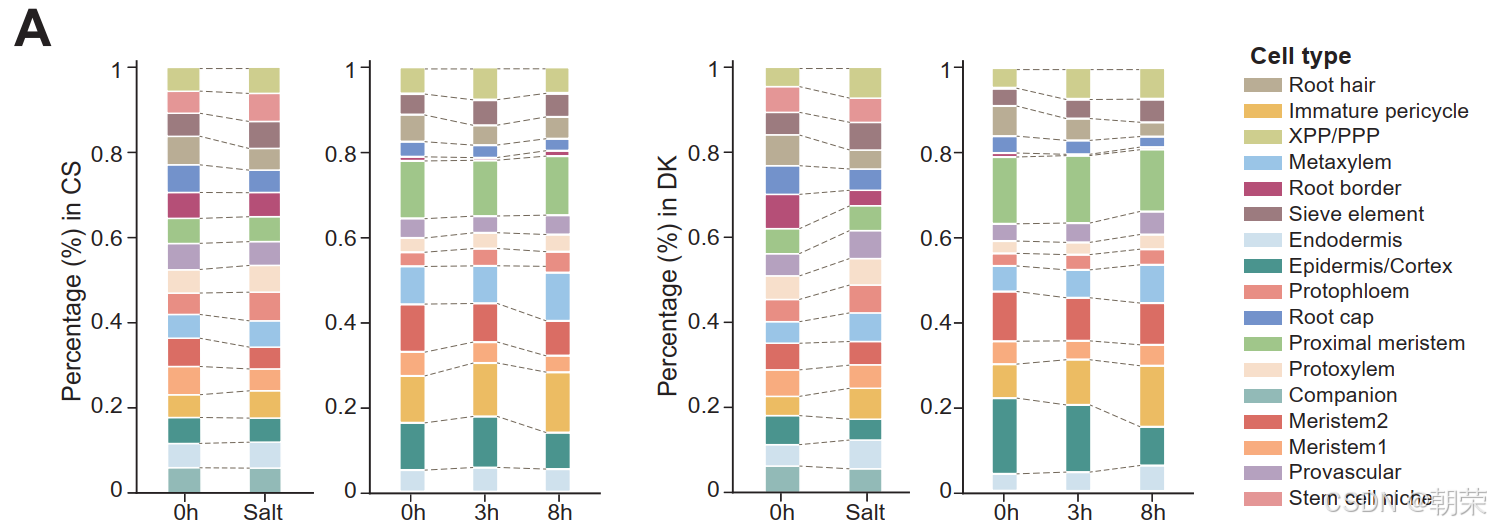
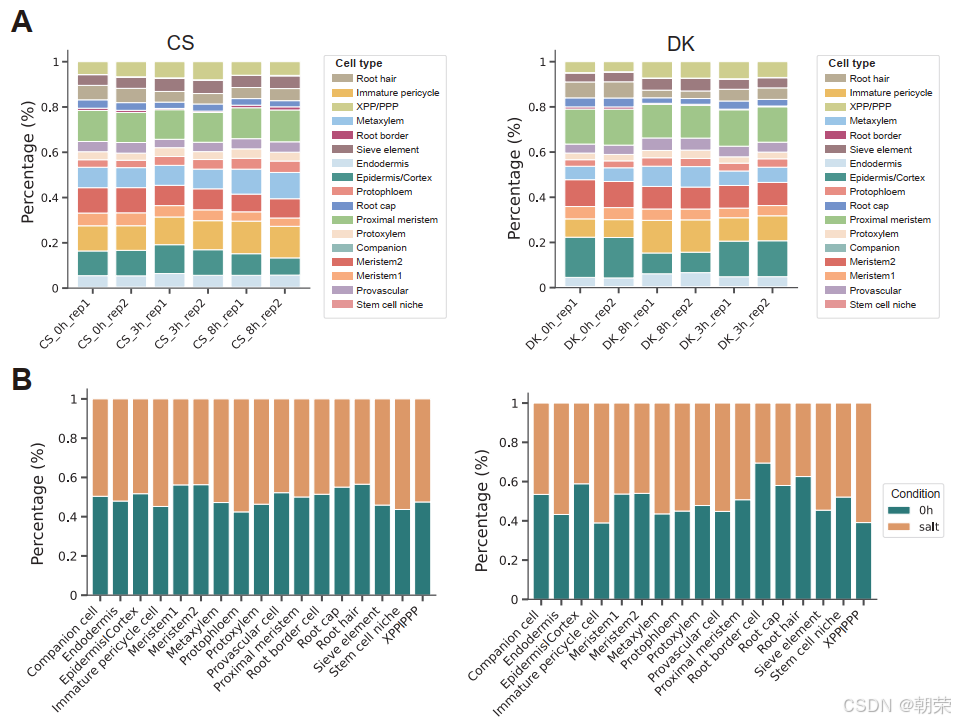
值得注意的是,DK在盐适应过程中(3h到8h的变化)表现出独特的动态特征:其表皮/皮层和根毛比例持续下降,而内皮层、原形成层和筛管分子群体显著增加(Student's t-test, p < 0.05)。这些变化可能反映了DK通过调整根部结构和功能来增强其耐盐性与适应性,而这些调整在CS中并未观察到(图 S12A 和 S13A)。这些品种特异性的变化可能与DK更强的耐盐性有关。
对细胞类型特异性上调差异表达基因(up-DEGs)的富集分析(图 S8A,B)进一步明确了与盐胁迫响应相关的细胞类型。与渗透和离子稳态相关的排名前10的生物学过程(BP),包括水运输(GO:0006833)、细胞水分稳态(GO:0009992)、离子跨膜运输(GO:0034220)和盐胁迫响应(GO:0009651),在内皮层、根边缘细胞和根毛细胞中显著富集,证明了它们在盐胁迫下调节水分和离子的关键作用(Li et al. 2024; Zhou et al. 2024)。相反,表皮/皮层、XPP/PPP、根冠和根毛细胞则在缓解氧化应激过程(如:内质网应激响应,GO:0034976)和结构强化通路(如:植物型细胞壁生物合成,GO:0009832)中表现出富集(Wang et al. 2024; Liu et al. 2024)。这些结果凸显了表皮/皮层、根毛和内皮层细胞在响应盐胁迫中的关键作用。
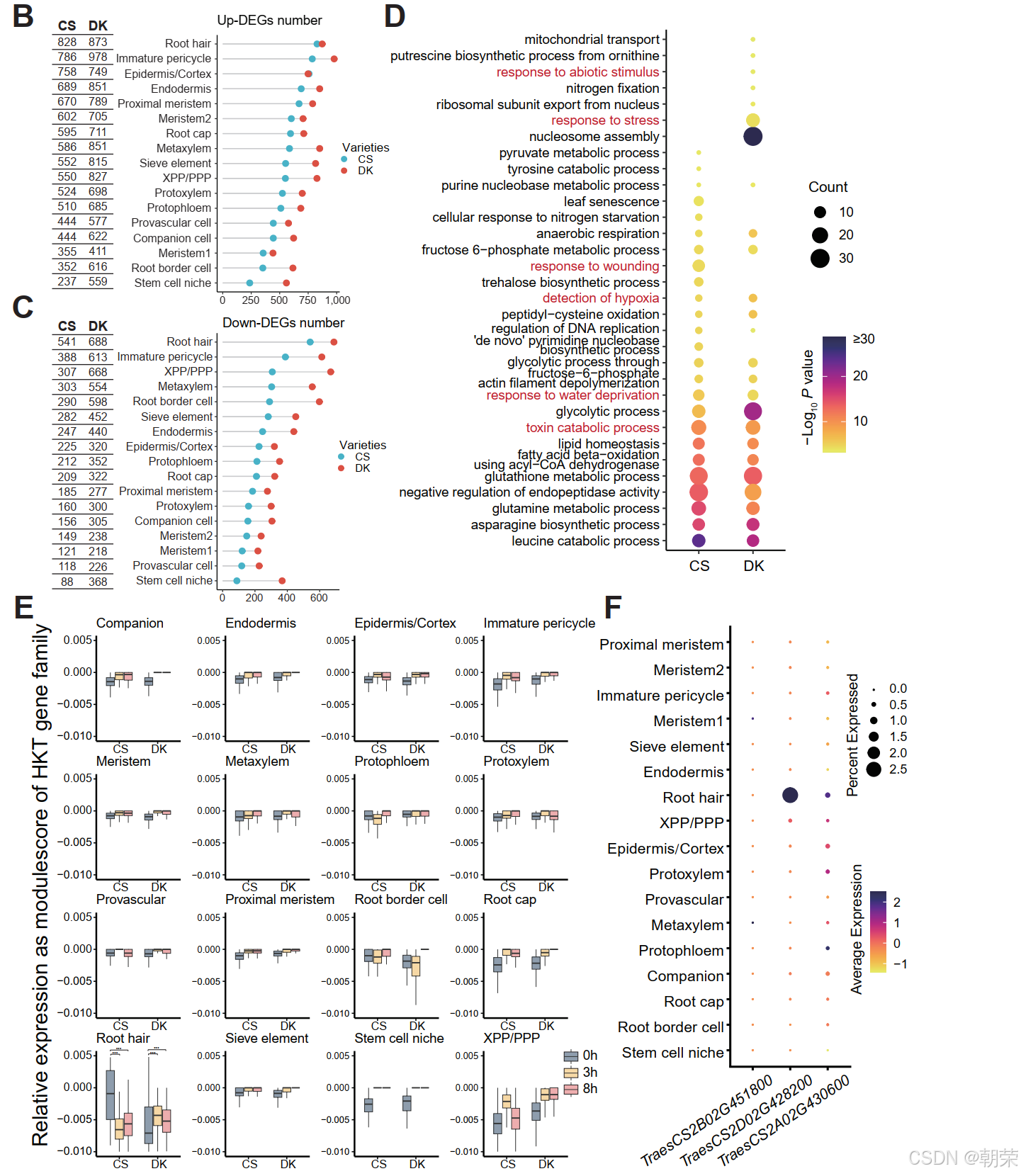
为了锁定盐胁迫响应细胞类型,我们计算了每个细胞类型在不同盐胁迫条件下的差异表达基因(DEGs)(图 2B,C 和 S14A--C;表 S6)。每个细胞类型的DEG数量量化了胁迫下的细胞异质性变化(Micali et al. 2023)。根毛细胞在盐敏感品种(CS)中表现出最多的上调/下调DEGs,而在耐盐品种(DK)中则显示出最高总数的DEGs,这表明根毛对盐胁迫具有强烈的转录响应。有趣的是,与CS相比,DK在所有细胞类型中均表现出更广泛且更显著的转录重编程(更高的DEG计数),这暗示DK可能拥有一种更高效的基因表达调节机制来应对盐胁迫,这可能促成了其卓越的耐性。
此外,通过GO和KEGG分析对盐响应上调DEGs进行功能表征(图 2D 和 S14D;表 S7 和 S8)显示,两个品种在与耐盐性相关的关键生物学过程(排名前25)中具有共同的富集特征,包括水分亏缺响应(GO:0009414)、毒素分解代谢过程(GO:0009407)和缺氧检测(GO:0001666)(Li et al. 2024)。值得注意的是,DK在应激响应(GO:0006950)和非生物刺激响应(GO:0009628)中表现出显著富集,这些过程与耐盐性密切相关。此外,DK还特异性地激活了磷酸戊糖途径(ko00030),据报道该途径在植物耐盐机制中起着核心作用。这些发现共同强调了根毛在植物盐胁迫响应和耐受中的核心地位。
HKT 基因家族是公认的参与盐响应和耐受的调节因子(Wang et al. 2024; Gholizadeh et al. 2024; Hua et al. 2024)。我们进一步系统地评估了小麦 HKT 基因家族在不同细胞类型和处理下的表达活性(图 2E)。具体而言,显著的盐诱导 HKT 表达变化仅在CS和DK的根毛细胞中被观察到(Student's t-test, p < 0.0001),其中 TaHKT1-D (TraesCS2D02G428200)(Hua et al. 2024)在根毛中表现出细胞类型特异性的高表达(图 2F)。这些发现结合前述分析,有力地支持了这一结论:根毛细胞在小麦根系响应盐胁迫中扮演着最重要的角色。这种细胞类型特异性的响应/适应机制可能在小麦抵御盐碱环境的能力中发挥关键作用,为未来旨在增强作物耐盐性的遗传改良策略提供了宝贵见解。
结果4:CS和DK根毛细胞在盐胁迫下的差异基因表达模式
除了细胞水平的分析外,我们进一步在基因水平上研究了根毛细胞中盐胁迫响应基因的差异表达模式。首先,我们鉴定了每种细胞类型在三个不同盐胁迫阶段的差异表达基因(DEGs):初始盐胁迫(0h vs. 3h)、适应性盐胁迫(3h vs. 8h)和持续盐胁迫(0h vs. 8h)。在所有细胞类型中,根毛细胞表现出的DEG数量最多(图 S15A 和表 S9),证实了其在盐胁迫响应中的核心作用。
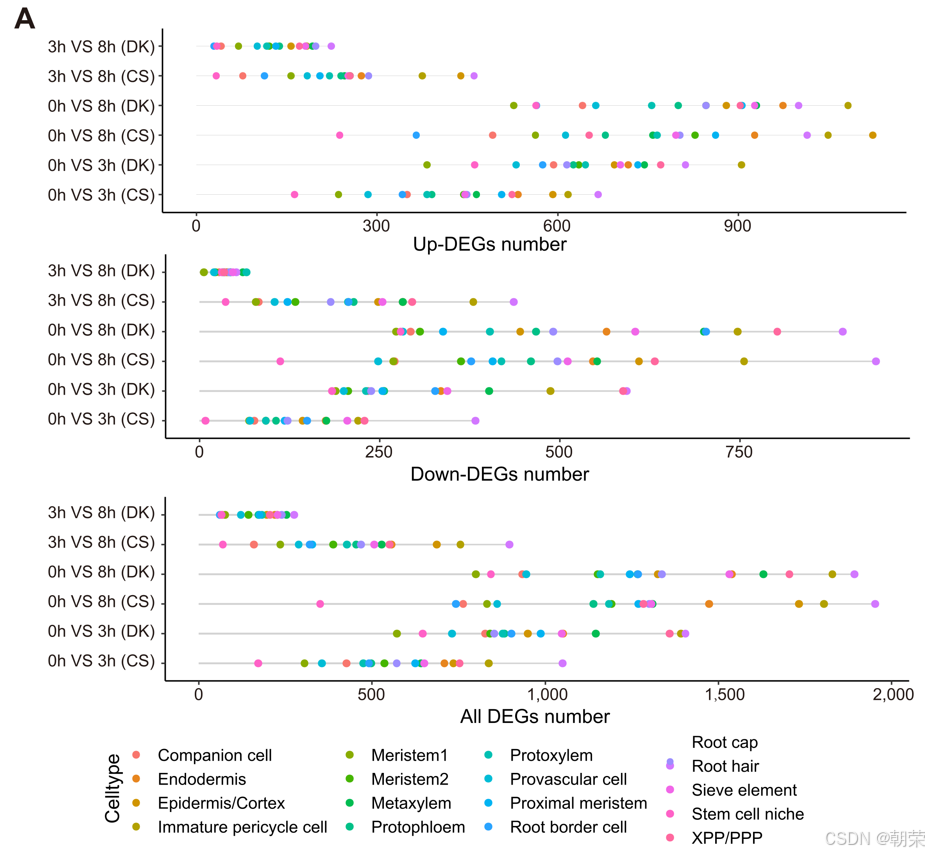
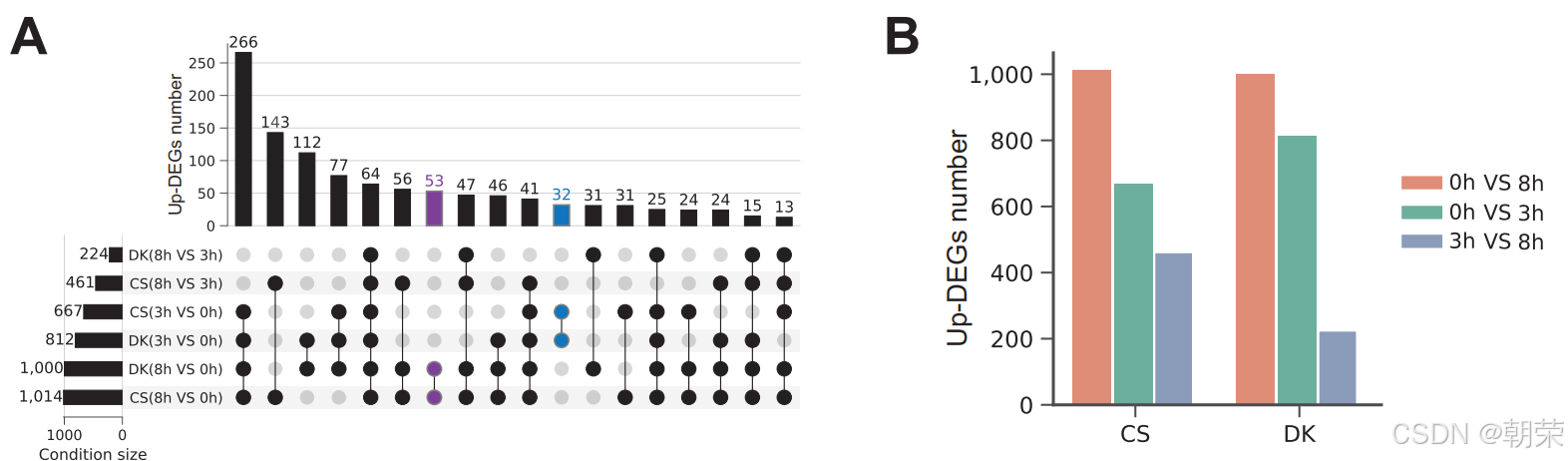
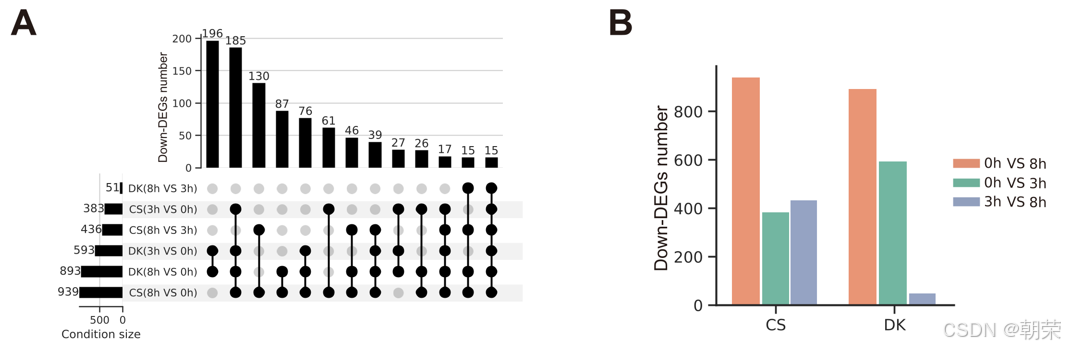
对DEG分布的进一步分析(图 3A,B 和 S16A,B)显示,两个品种在初始盐胁迫阶段的上调DEGs数量均多于适应阶段。这一模式反映出根毛细胞在面临突发盐胁迫时具有显著的细胞异质性和快速应急响应机制,而其基因表达在适应过程中趋于稳定。有趣的是,虽然在持续胁迫下CS(1014个)和DK(1000个)的上调DEGs数量相似,但在初始盐胁迫阶段,DK的上调DEGs数量高于CS,这表明DK具有更快、更强劲的转录响应,可能有助于其更迅速地适应高盐环境。
为了研究保守性和品种特异性的响应,我们开展了两方面的分析。一方面,为了鉴定保守的盐胁迫响应功能,我们对四个对照组(初始、适应、持续及盐胁迫状态下)共有的上调DEGs进行了GO和KEGG分析。这些组分别产生了508、147、691和396个共有上调DEGs(图 3C--F)。初始阶段的响应富集在应激响应(GO:0006950)、非生物刺激响应(GO:0009628)、水分亏缺响应(GO:0009414)和缺氧检测(GO:0001666)等生物学过程(BP),突出了其在胁迫/刺激响应、抗氧化防御和渗透调节中的作用(图 3C)。相比之下,适应阶段的特征是富集在细胞能量供应相关的BP,包括内肽酶负调节(GO:0030407)、木聚糖分解代谢过程(GO:0033644)、固氮作用(GO:0015979)和淀粉生物合成过程(GO:0005982)(图 3D)。同样,共有下调DEGs(四个对照组分别为256/520/38/219个基因)(图 S16C--J)富集在根毛发育和细胞修复功能上。这些结果彰显了CS和DK在不同阶段响应盐胁迫的保守功能机制,并展示了初始响应与适应阶段之间截然不同的功能侧重点。
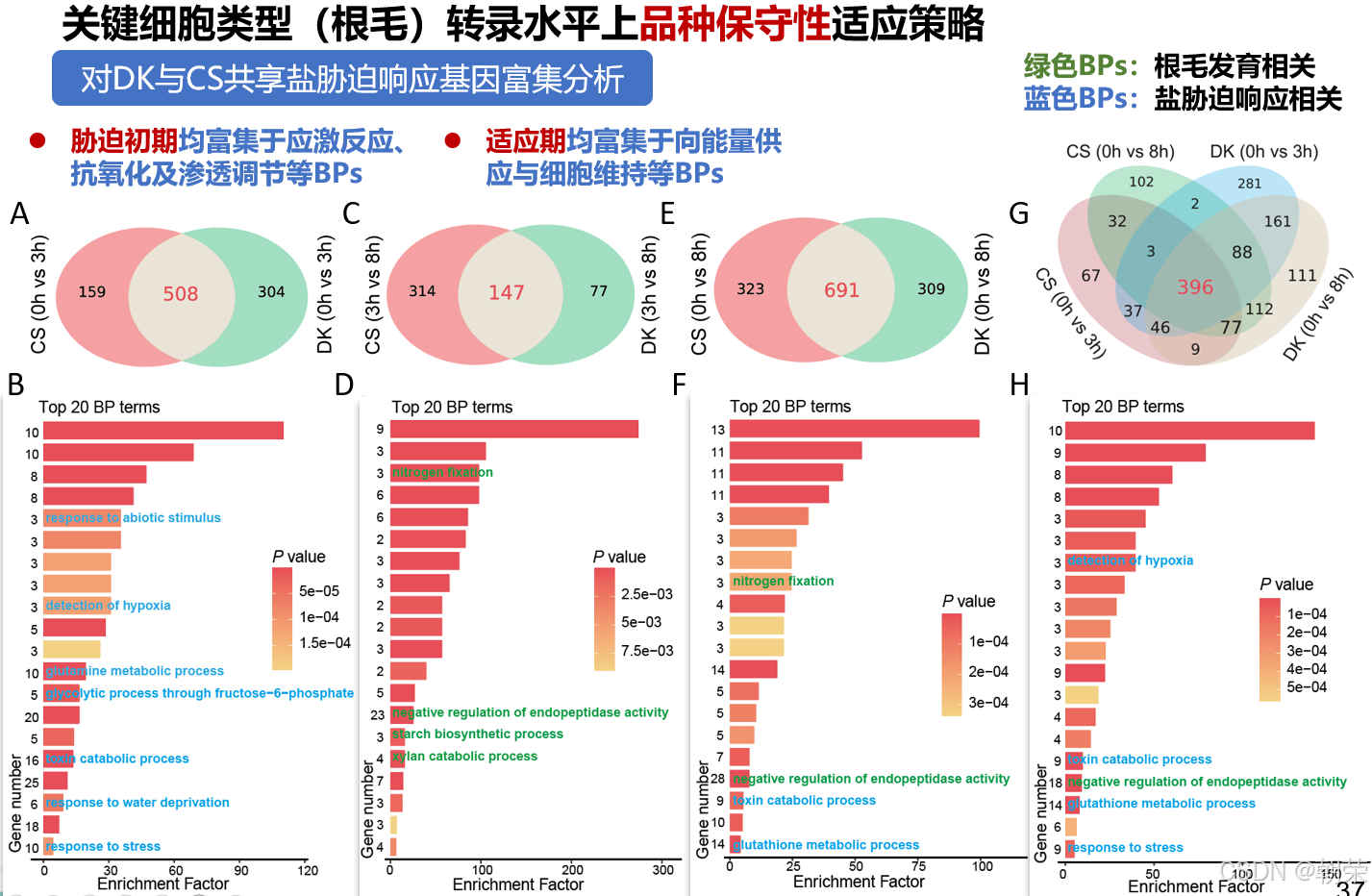
另一方面,我们通过在根毛中进行富集分析研究了品种特异性的响应(图 3G 和 S17A--C)。在初始胁迫期间,两个品种的上调DEGs均富集在水分亏缺响应、脱落酸(ABA)响应(GO:0009737)和应激响应中。然而,在适应期间,富集功能转向了海藻糖生物合成、固氮作用和木聚糖分解代谢等过程,反映了从应激信号传导向细胞发育和细胞维持的转变。有趣的是,在盐胁迫下,谷胱甘肽代谢成为两个品种的关键通路,根毛中谷胱甘肽相关基因(GSTU 基因家族)显著激活(图 S18A)。
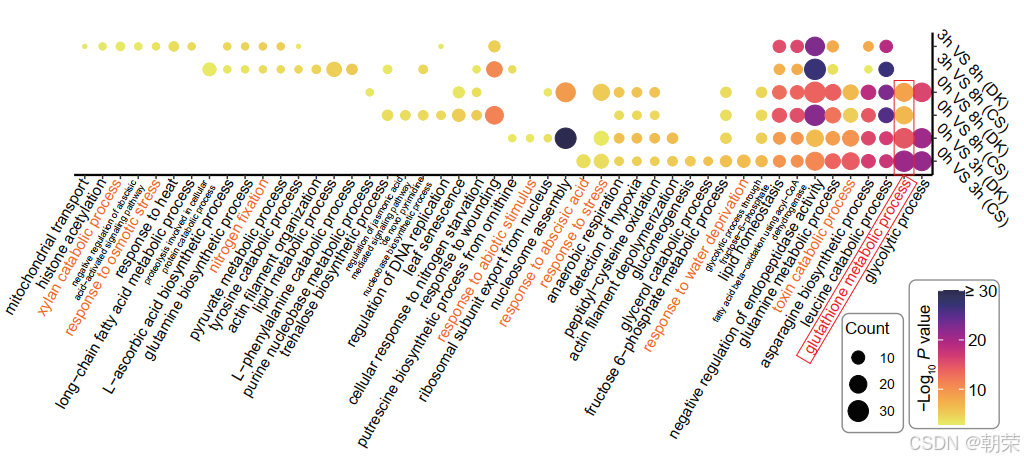
尽管存在这些保守通路,但在0h vs. 3h和3h vs. 8h的比较中,CS和DK重叠的上调DEGs分别仅有32个和53个(图 3A),表明胁迫响应基因存在巨大的品种差异。为了进一步剖析这些差异,我们根据表达谱将所有显著的DEGs划分为不同的表达模式:5种上调模式(图 3H)、4种下调模式(图 3I)和5种其他模式(图 3J)。具体而言,up_1、up_2和up_3随盐胁迫时间的延长表达水平不断升高,其中up_1与生长调节相关,up_2与抗氧化防御相关,up_3与养分积累相关。这些模式在CS中更为显著,暗示其依赖增强能量代谢、应激信号传导和渗透调节物质积累来应对盐胁迫。然而,DK占主导的模式up_4和up_5富集在碳水化合物代谢(up_4)、能量代谢、应激响应和细胞修复(up_5)中(图 3H),突显了其强调胞内活动和细胞修复以应对盐胁迫的策略。
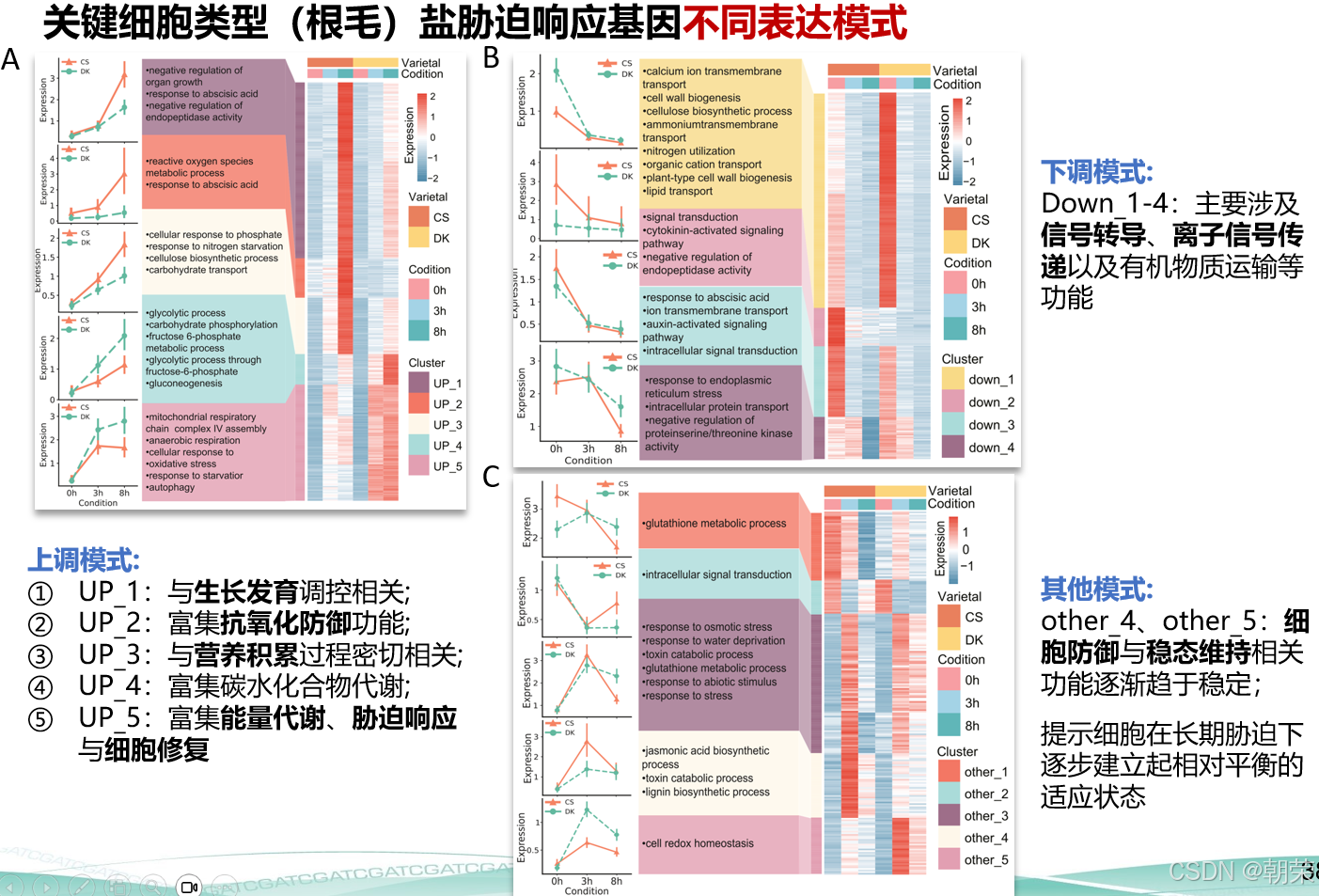
这些发现揭示了盐敏感品种CS优先考虑快速的应激信号传导和渗透调节物质积累,而耐盐品种DK则侧重于代谢适应和细胞修复。这种遗传和功能上的分歧为基因水平上盐胁迫响应的动态过程和基因型差异提供了宝贵的见解。
结果5: 拟时序分析揭示根毛细胞的不同响应
在盐胁迫条件下,根毛细胞的数量显著减少(图 2A),这一现象对植物根系生长和耐盐性具有重要影响。为了深入研究这一过程中基因表达和生理特性的动态变化及其潜在的调节机制,我们利用 Monocle2 进行了轨迹分析(Qiu et al. 2017)。鉴于根毛起源于表皮细胞的分化(Zhang, He, et al. 2023; Li et al. 2024),我们利用细胞簇 4(根毛)和 15(表皮/皮层)构建了分化轨迹,以阐明 CS 和 DK 根毛对盐胁迫的动态响应。
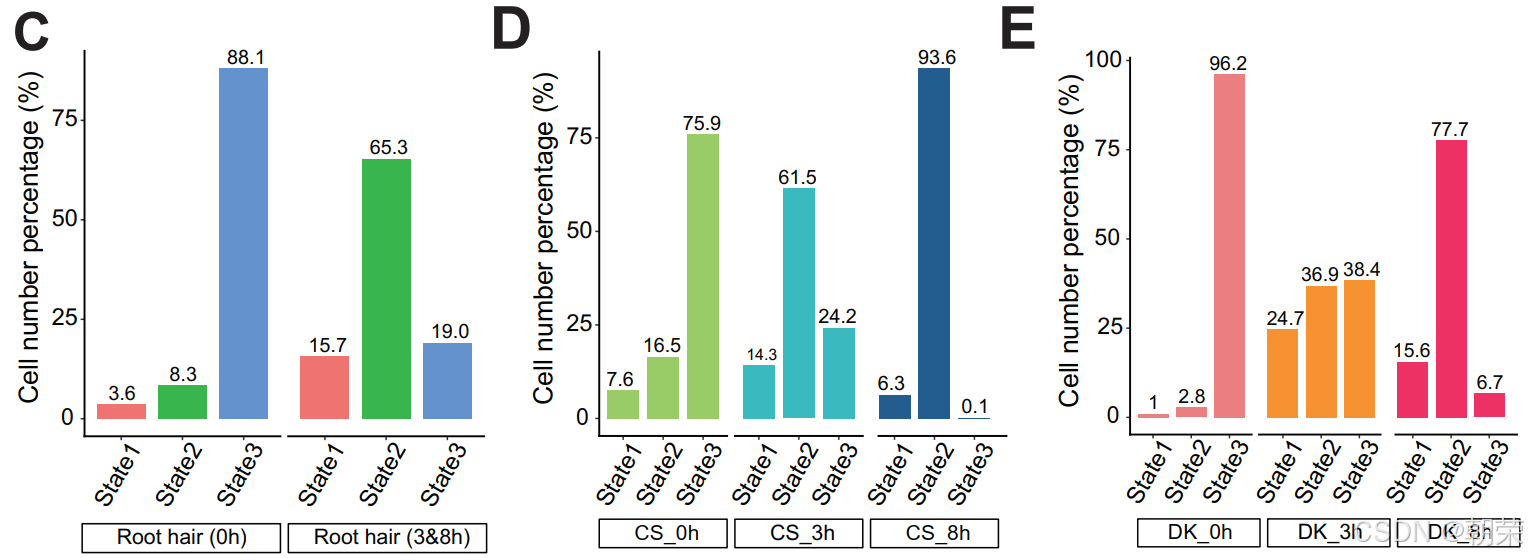
拟时序轨迹分析将表皮细胞置于起点,并延伸代表初始根毛状态(状态1)。随后,轨迹分叉为两个分支,代表根毛的两种不同生理状态:状态2和状态3(图 4A 和 S19A--C)。将六个组别中的根毛细胞分布映射到拟时序轨迹上(图 4B 和 S19D,E)发现,正常条件与盐胁迫条件下的细胞分布并不均衡。具体而言,正常条件下 88.1% 的根毛细胞集中在状态3,而 65.3% 的盐胁迫细胞位于状态2(图 4C 和 S20A)。这些发现表明,状态3代表正常发育后期的根毛细胞,而状态2则反映了盐胁迫诱导的生理转变。
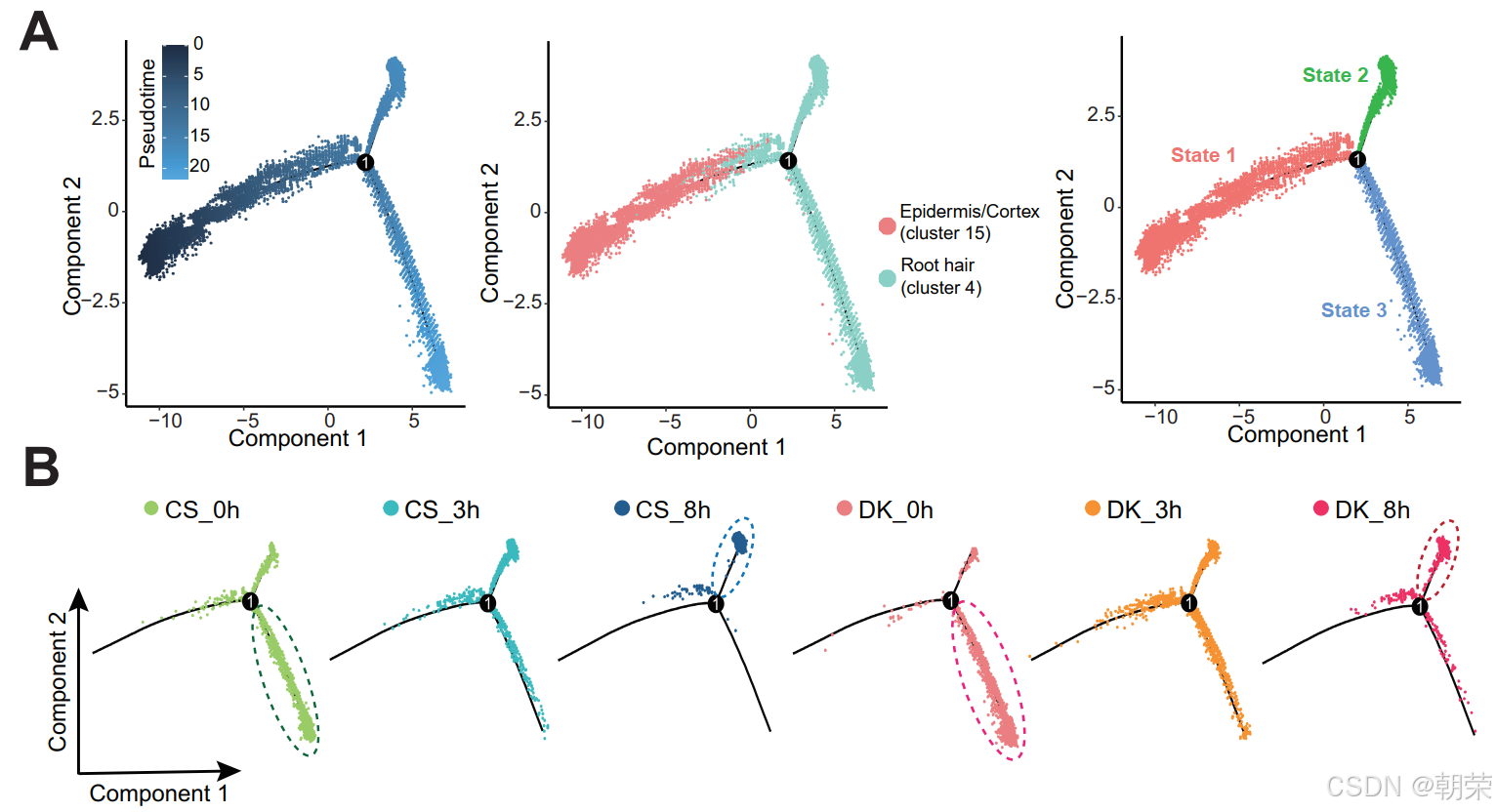
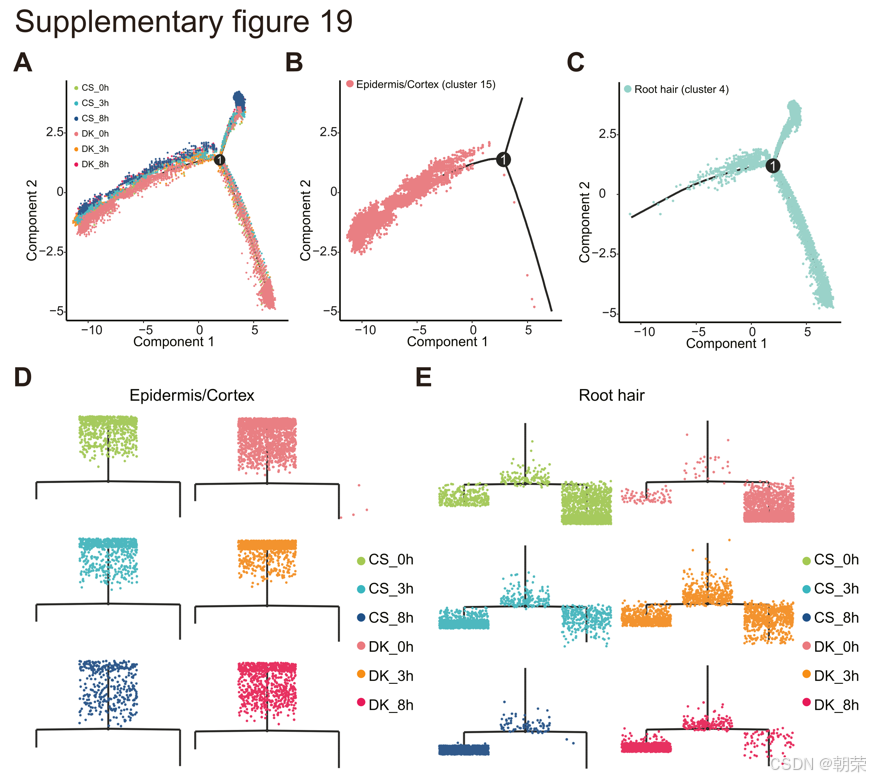
在正常条件下,DK 根毛表现出更高的发育成熟度,处于状态3的细胞比例为 96.2%,而 CS 为 75.9%(图 4D,E 和 S20B--E)。然而,在盐胁迫下,随着胁迫时间的延长,向状态2转变的根毛细胞比例逐渐增加。值得注意的是,这种转变在 CS(93.6%)中比在 DK(77.7%)中更为显著,表明 CS 根毛更容易受到盐胁迫的影响,这与其盐敏感表型一致。这些发现证明了 CS 和 DK 之间存在截然不同的盐胁迫响应模式,DK 在胁迫条件下表现出更优异的发育稳定性,表明其比 CS 具有更强的耐盐性,这一结论与该领域的现有认知相吻合。
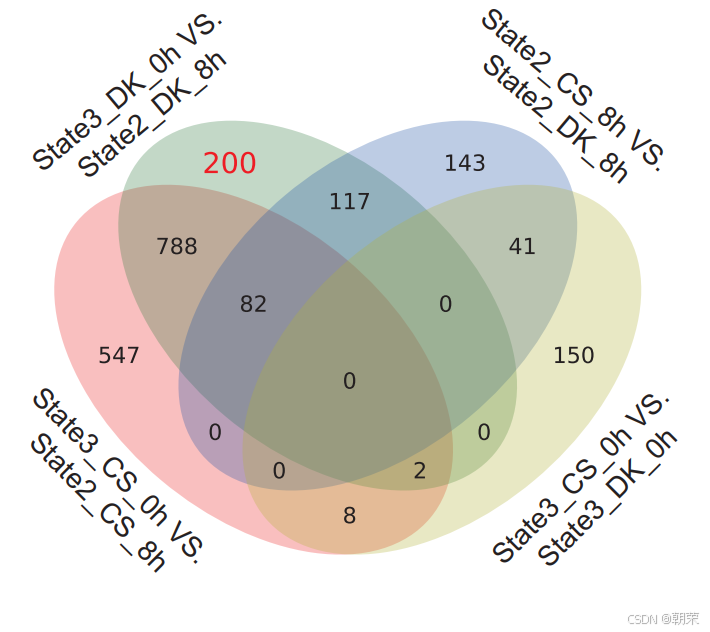
为了鉴定驱动这些差异响应的关键基因,我们分别对处于状态3的 CS_0h 细胞与处于状态2的 CS_8h 细胞,以及处于状态3的 DK_0h 细胞与处于状态2的 DK_8h 细胞进行了差异表达分析,以鉴定盐响应差异基因(DEGs)。此外,我们还比较了 0h 和 8h 时间点 CS 和 DK 处于状态3的细胞之间的 DEGs,以阐明品种间差异(图 4F)。结果显示,有 200 个 DK 特异性的上调 DEGs 对盐胁迫产生响应。
值得注意的是,在按折叠倍数排序的前10个基因中,只有 TaGSTU1-5B (TraesCS5B02G426400) 与盐胁迫响应机制表现出显著的功能相关性(表 S10),该基因在谷胱甘肽代谢(ko00480)、谷胱甘肽转移酶活性(GO:0004364)、谷胱甘肽代谢过程(GO:0006749)和毒素分解代谢过程(GO:0009407)中显著富集。鉴于谷胱甘肽作为抗氧化剂在清除活性氧(ROS)及赋予植物胁迫耐性方面的关键作用(Kumar and Trivedi 2018),我们将 TaGSTU1-5B 鉴定为助力 DK 增强盐胁迫抗性的潜在基因。这一发现强调了该基因在盐胁迫下介导抗氧化防御机制的潜在作用,进一步突显了 TaGSTU1-5B 在应对环境逆境分子响应中的重要性。
结果6:过表达 TaGSTU1-5B 通过清除活性氧提高耐盐性
我们利用特异性引物从耐盐品种 DK 的根部 cDNA 中扩增了 TaGSTU1-5B 的全长编码序列。序列分析表明,TaGSTU1-5B 基因包含一个 669 bp 的编码序列,编码一个分子量为 25.0 kDa 的蛋白,该蛋白是水稻 OsGSTU1 的同源蛋白。系统发育分析显示,小麦 TaGSTU1-5B 蛋白与小麦祖先种及水稻 OsGSTU1 亲缘关系密切(图 S21A)。结构域搜索显示,TaGSTU1-5B 蛋白及其同源蛋白均包含两个保守结构域:谷胱甘肽 S-转移酶 N 端结构域和谷胱甘肽 S-转移酶 C 端样结构域(图 S21B)。
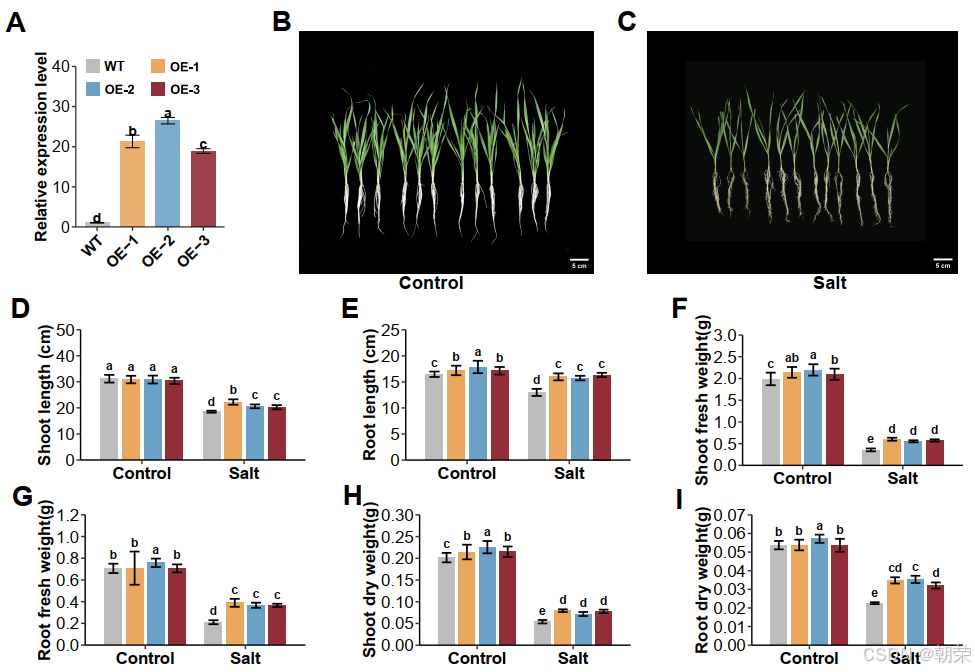
为了验证 TaGSTU1-5B 在耐盐性中的作用,我们构建了其过表达载体并转化小麦,获得了转基因株系。与野生型(WT)相比,三个过表达株系(OE)中 TaGSTU1-5B 的表达水平显著升高(图 5A)。随后,我们比较了 OE 株系和 WT 株系在正常及盐胁迫条件下的形态特征。在正常条件下,两者未表现出显著差异(图 5B);而在盐胁迫条件下,OE 和 WT 株系的生长均受到抑制,但 OE 株系的受抑制程度显著低于 WT(图 5C)。统计分析显示,过表达株系的地上部长度和根长均显著大于 WT 株系(图 5D, E)。此外,过表达株系的鲜重和干重也显著高于 WT(图 5F-I)。这些结果表明,过表达 TaGSTU1-5B 增强了小麦的耐盐性。
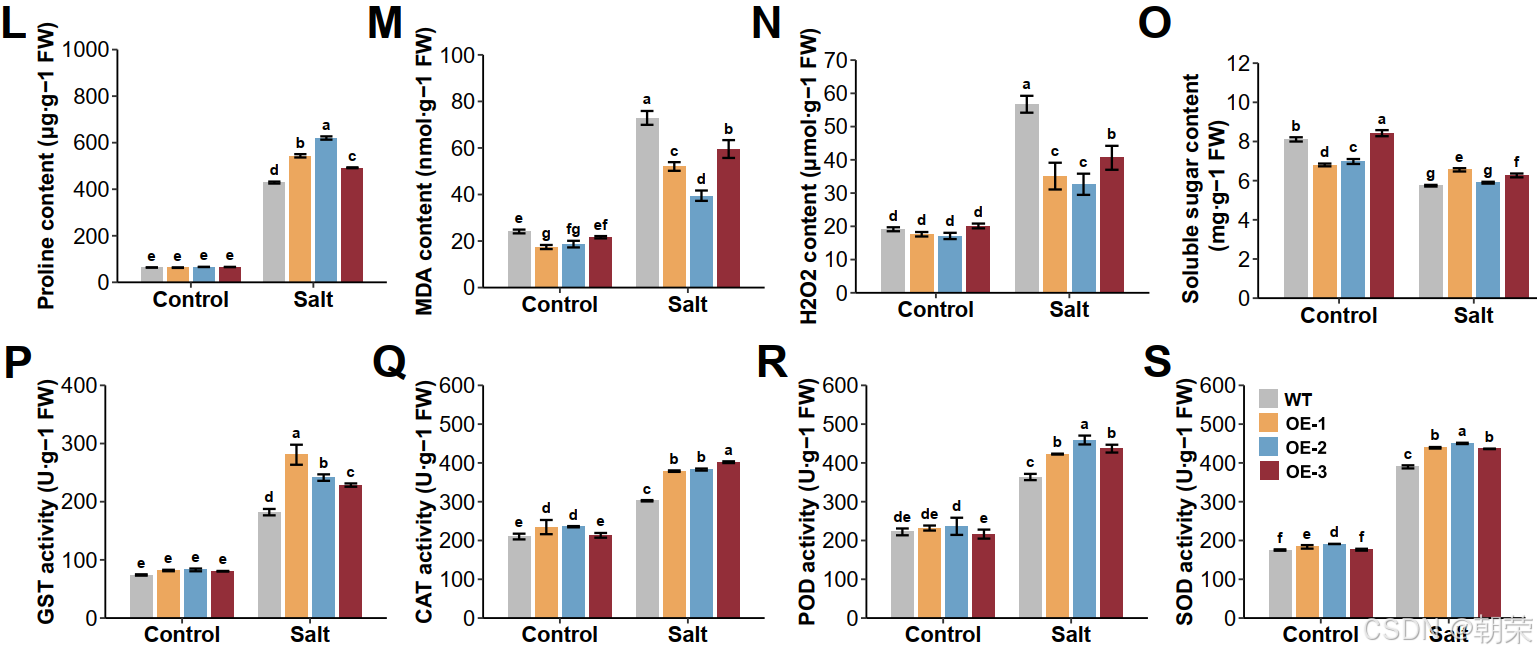
为了阐明 TaGSTU1-5B 的功能,我们进一步测量并比较了 OE 和 WT 株系的生理指标。NBT(氮蓝四唑)和 DAB(二氨基联苯胺)染色结果显示,在盐胁迫处理 48 小时后,OE 株系积累的 O_2\^{·-}(超氧阴离子)和 H_2O_2(过氧化氢)少于 WT 株系,而在正常条件下观察不到显著差异(图 5J, K)。此外,我们还研究了盐处理 48 小时后的多项生理指标。结果显示,盐胁迫处理后,OE 株系的脯氨酸和可溶性糖含量更高,而 MDA(丙二醛)和 H_2O_2 含量更低(图 5L-O)。酶活性测定表明,OE 株系的 GST、CAT、POD 和 SOD 活性也比 WT 株系显著提高(图 5P-S)。这些结果证明,过表达 TaGSTU1-5B 通过增强活性氧(ROS)的清除能力,进而提高了小麦的耐盐性(表 S11)。
结果7: 盐胁迫增强了多倍体小麦根系中的非对称基因表达
作为一种异源六倍体物种,小麦表现出复杂的基因组间相互作用,因此构建单细胞分辨率下的非对称转录图谱具有重要意义。为了探究盐胁迫下的非对称转录现象,我们首先分析了大批量转录组(bulk RNA-seq)数据,观察到约33.49%的小麦同源三体基因(即在A、B、D基因组上均有拷贝的基因)表现出不平衡表达模式,这与之前的研究结果一致(Ramírez-González et al. 2018)(图 6A 和表 S12)。
此外,我们解析了 CS 和 DK 根系中的非对称基因表达,发现表现出不平衡表达模式的同源基因比例在 17 种细胞类型中存在差异,范围在 45.4% 到 53.3% 之间(图 6B、S22A-F 和 S23A;表 S13)。这些结果有力地支持了这一观点:非对称基因表达水平在不同发育阶段和细胞类型中具有高度的异质性。值得注意的是,特定的细胞类型,包括中柱细胞生态位(SCN)、根边缘细胞和伴胞,在 CS 和 DK 中均表现出最高比例的不平衡表达基因(图 6B-D)。
有趣的是,我们的分析还揭示了一个此前未见报道的现象:持续的盐胁迫暴露逐渐提升了 CS 和 DK 中不平衡表达同源基因的比例,这在 bulk RNA-seq 和 snRNA-seq 数据集中均得到了趋势一致的证实(图 6A-D)。显著的是,与 CS 相比,DK 中这种不平衡表达比例的增幅明显更高(图 6B-D 和 S23A),这暗示亚基因组转录的不对称性可能作为一种盐适应的调节机制,潜在地支撑了 DK 优异的应激耐受性。
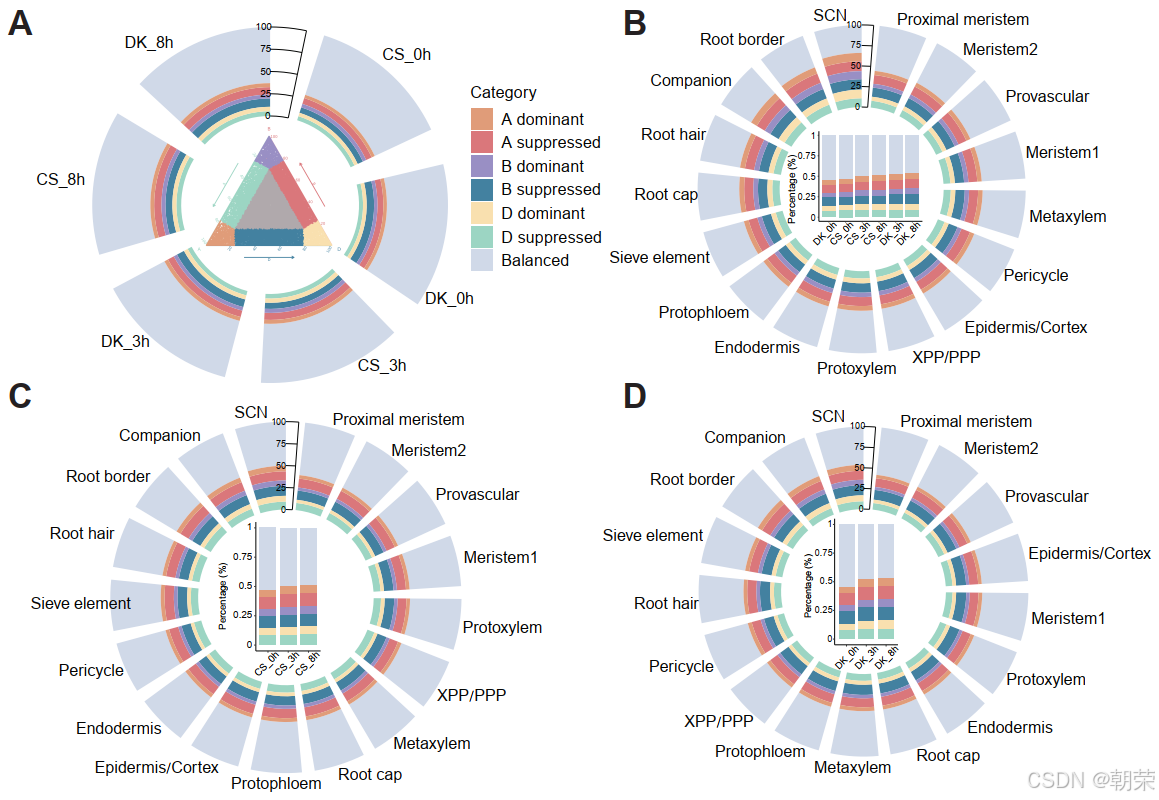
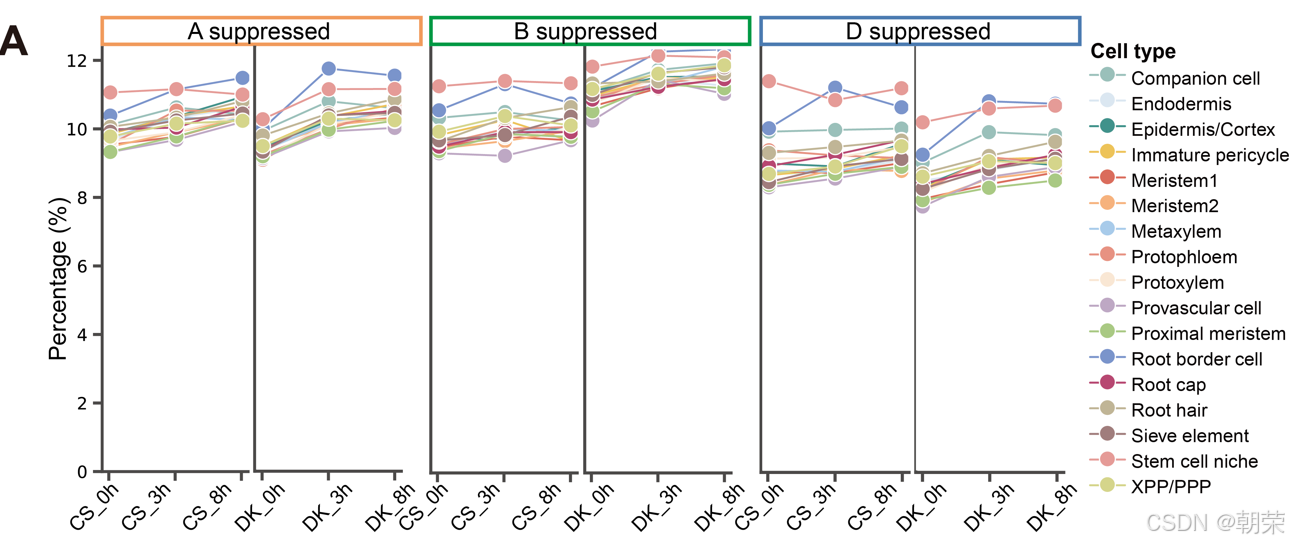
为了剖析这种关联,我们系统地量化了跨细胞类型的五种表达模式(A/B/D 优势型和 A/B 抑制型)。值得注意的是,耐盐品种在胁迫条件下始终表现出比 CS 更高比例的这些模式(图 6E),这在特定的转录偏好与增强的耐盐性之间建立了直接联系。随着盐胁迫时间的延长,两个小麦品种中 A/B/D 优势型模式的比例均呈现上升趋势。然而,与 CS 相比,DK 在大多数细胞类型中这三种优势模式的增加更为显著。相比之下,A/B/D 抑制型模式的比例在整个胁迫过程中保持相对稳定(图 6F 和 S24A)。这些结果表明,A、B 和 D 优势模式流行率的增加可能在增强小麦耐盐性中发挥关键作用,从而促成了 DK 中观察到的更强的应激抗性。
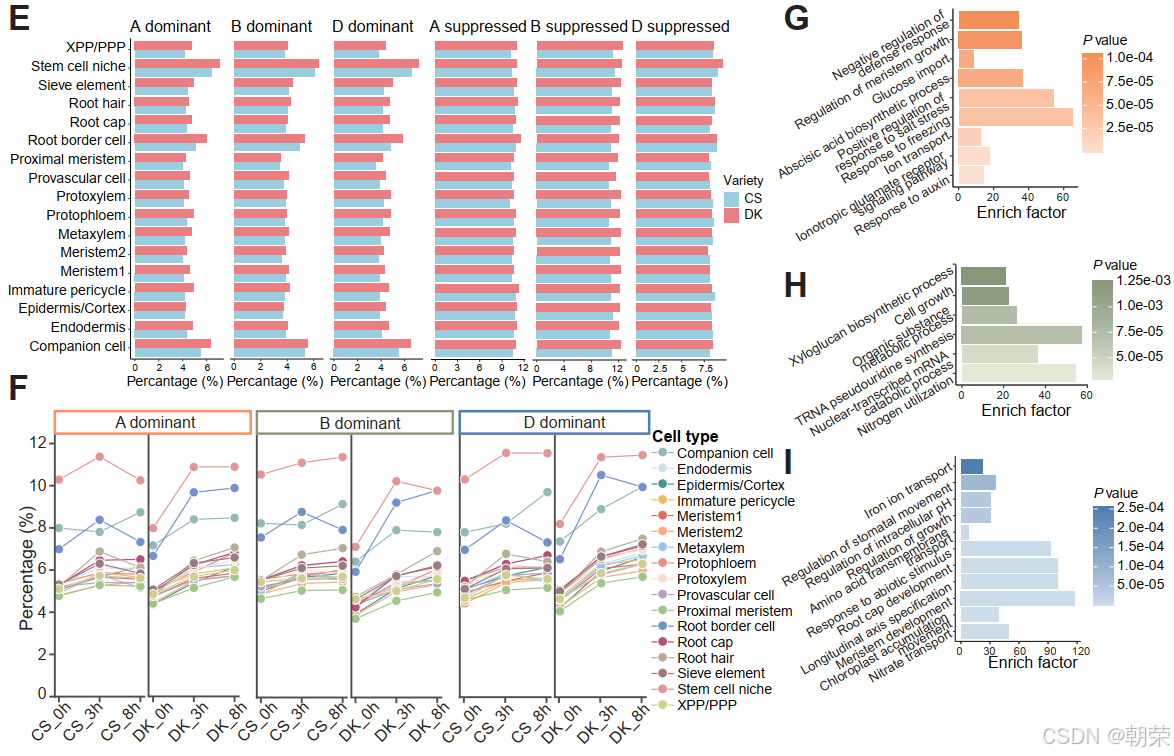
为了进一步阐明盐胁迫响应的内在机制,我们对从 0h 的平衡状态转变为 3h 的 A/B/D 优势状态的基因集进行了富集分析。在 CS 和 DK 中转换为 D 优势型的基因,富集在与根冠发育和纵轴特化相关的功能中,这与之前关于 D 优势基因与根系发育密切相关的报道一致(Zhang, He, et al. 2023; Wang et al. 2018)。同时,与盐胁迫响应相关的过程,如非生物刺激响应、铁离子转运和胞内 pH 调节也显著富集,表明 D 优势基因不仅在促进根系生长方面起关键作用,还可能通过调节离子稳态和胞内环境来增强耐盐性。
同样,转换为 A 优势型的基因在离子转运、盐胁迫响应正调节、防御响应负调节和生长素响应方面表现出显著富集,证明这些基因通过维持离子平衡和调节植物激素信号传导来贡献于耐盐性。相比之下,转换为 B 优势型的基因与盐胁迫相关功能没有显著关联,表明这些基因可能不是小麦盐胁迫响应的关键驱动因素(图 6G-I 和 S24B-G)。
这些发现揭示了耐盐小麦品种(DK)通过增强盐胁迫响应基因在优势模式下的表达不对称性,建立了更高效的适应性调节机制。值得注意的是,A 和 D 亚基因组优势似乎与盐胁迫期间更强的转录响应相关,暗示它们潜在参与了耐盐机制。这些观察结果突显了亚基因组特异性调节活动与增强应激耐受性之间的可能联系,为未来探索小麦适应盐渍环境的分子基础提供了参考框架。
讨论
土壤盐渍化是一个严峻的全球性问题,严重限制了农作物的生产力(Du, Zhang, et al. 2025)。与玉米、水稻等其他谷物相比,小麦表现出更高的耐盐性,这使其成为理解植物盐胁迫响应及培育耐盐品种的宝贵模型。特别地,根系在感知、适应和耐受盐胁迫中发挥着至关重要的作用。深入阐明小麦根系响应盐胁迫的分子机制,对于培育耐盐品种具有核心意义(Wang, Zhao, et al. 2023; Dissanayake et al. 2024)。在本研究中,我们利用优化后的 snRNA-seq 方法(Du, Chen, et al. 2025),构建了首个盐胁迫下小麦根系的单细胞核转录组图谱,为理解盐敏感品种(CS)和耐盐品种(DK)的细胞类型特异性响应提供了高分辨率的视角(Chao et al. 2006)。
通过对 188,270 个高质量根部细胞核进行分析(图 1A, B),我们利用四重注释法从 24 个细胞簇中鉴定了 17 种不同的细胞类型(图 1B)。两个品种均表现出保守的盐胁迫响应,包括根毛和分生组织细胞数量的减少,以及原生韧皮部和未成熟周鞘细胞群的扩张(图 2A)。然而,耐盐品种 DK 展现出独特的适应性:表皮/皮层和根毛细胞比例持续下降,同时伴随着内皮层和维管细胞群的增加(图 S8)。值得注意的是,根毛细胞表现出最强烈的转录响应(图 2B-D),这与先前关于拟南芥和不结球蔓菁中根毛在早期胁迫感知中作用的研究结果一致(Liu, Kang, et al. 2025; Wang et al. 2008; Wang and Li 2008)。
我们的数据进一步揭示了根毛细胞在时间和基因型上的不同响应策略(图 3C-F)。虽然两个品种共享核心的胁迫响应通路,但它们表现出截然不同的功能偏好:CS 侧重于快速的应激信号传导和渗透调节物质的生物合成,而 DK 则倾向于代谢重编程和细胞修复(图 3G-I)。这些发现表明,DK 增强的耐盐性可能源于其在细胞水平上采取了更具适应性且更持久的响应策略。
本研究的一个关键创新点是利用拟时序轨迹分析(图 4)来鉴定 DK 特异性的适应机制。我们发现参与谷胱甘肽代谢的基因 TaGSTU1-5B 是耐盐性的候选调节因子。通过过表达进行的功能验证确认了其在增强耐盐性方面的作用,这为小麦改良提供了一个极具前景的靶点------而此前这一发现从未在单细胞分辨率下得到证实(图 5)。
此外,我们揭示了异源六倍体小麦在盐胁迫下亚基因组表达调节的新模式(Ramírez-González et al. 2018; IWGSC 2018)。结合 bulk RNA-seq 和 snRNA-seq 的分析(图 6A-D)显示,持续的盐胁迫逐渐扩大了 CS 和 DK 中不平衡表达基因的比例------这是一个此前从未被报道的新发现。对非对称表达状态发生改变的基因进行富集分析(图 6G-I)表明,A 或 D 亚基因组优势基因的上调与耐盐性的增强相关,强调了亚基因组调节在小麦应激适应中的作用。
需要指出的是,实验室受控环境下的均质盐胁迫可能无法完全模拟盐分与其他环境问题之间复杂的相互作用(Ryu et al. 2019)。我们选择了具有代表性的盐敏感和耐盐小麦品种来鉴定耐盐性的细胞类型特异性和品种特异性机制,这确保了结果的可比性和相关性。此外,盐胁迫处理采用的固定时间点可能遗漏了早期或恢复阶段的动态转录变化;盐胁迫效应通常需要时间积累(Julkowska and Testerink 2015),从而产生更明显的细胞和基因水平异质性(Munns and Tester 2008; Shavrukov 2013)。因此,所选的 0h、3h 和 8h 时间点有效反映了特定阶段内的盐胁迫响应,并为未来的动态分析奠定了基础。