肿瘤mRNA疫苗
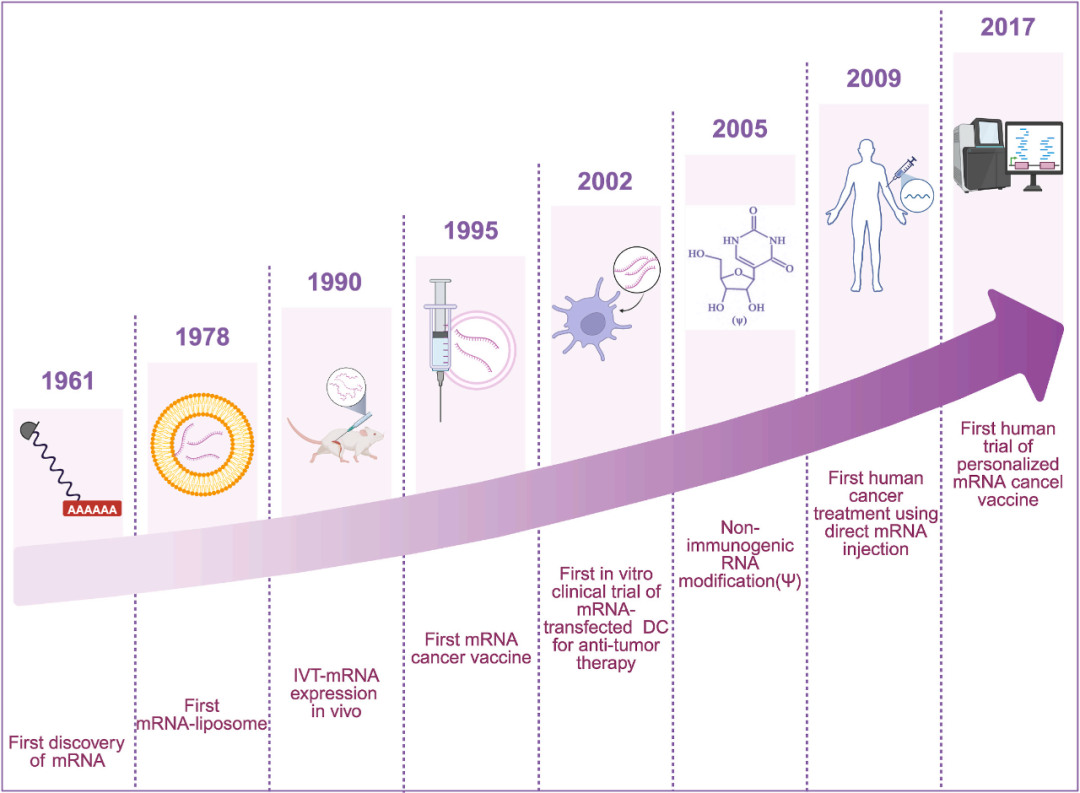 tumor mRNA疫苗的发展历程【1】
tumor mRNA疫苗的发展历程【1】
其中,tumor mRNA疫苗异军突起,成为近些年瞩目的焦点。 tumor mRNA疫苗是一种通过递送编码 tumor抗原的mRNA至人体细胞,诱导免疫系统特异性攻击癌细胞的创新疗法。相比多肽疫苗和DC疫苗,mRNA疫苗不依赖佐剂、生产成本低、可高效递送多种抗原、不受患者HLA分型限制,还能同时激活细胞免疫与体液免疫,也不会存在DNA疫苗整合宿主基因组导致突变的风险,其多价设计也有望解决 tumor异质性和耐药问题 【1】。 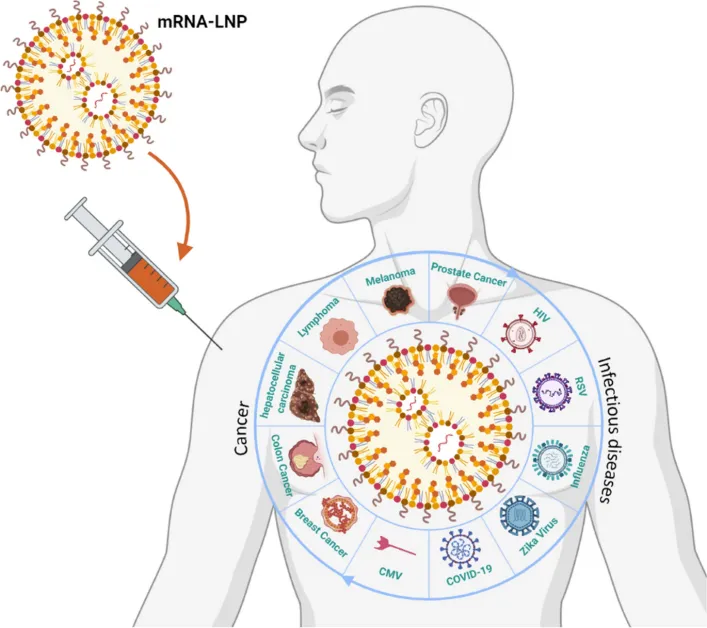 tumor mRNA疫苗需要高效的递送载体和合适的输注方式才可发挥作用。目前,递送载体主要有病毒载体、病毒样颗粒载体和脂质纳米颗粒(LNP)载体,LNP应用最广泛 ,能保护mRNA免于降解,延长体内循环时间 【2】。 肿瘤新抗原
tumor mRNA疫苗需要高效的递送载体和合适的输注方式才可发挥作用。目前,递送载体主要有病毒载体、病毒样颗粒载体和脂质纳米颗粒(LNP)载体,LNP应用最广泛 ,能保护mRNA免于降解,延长体内循环时间 【2】。 肿瘤新抗原
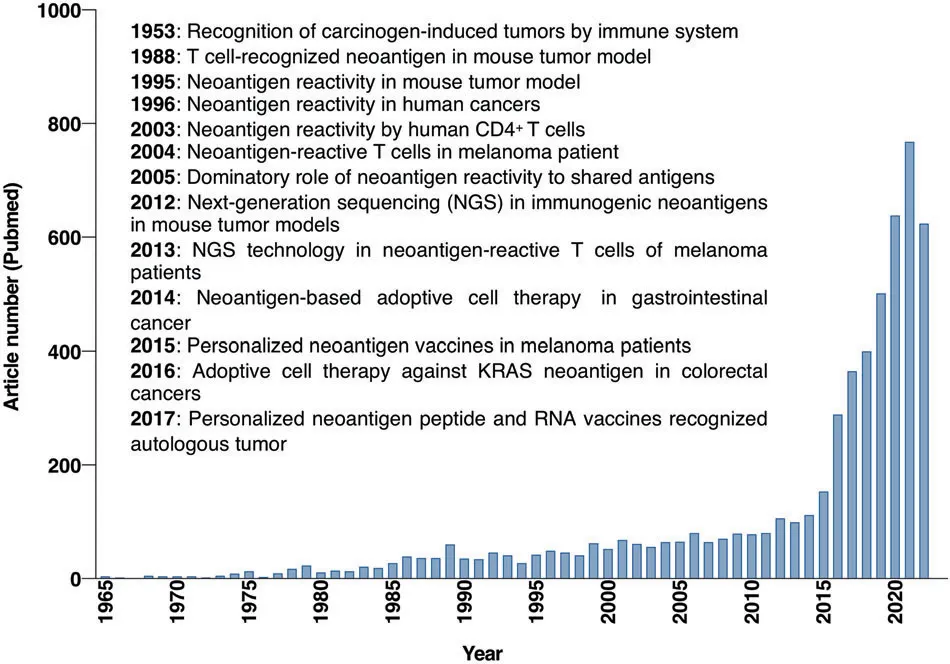
tumor 新抗原的发展历程【3】 tumor mRNA疫苗分为个性化疫苗与通用型疫苗两种。其中个性化 tumor mRNA疫苗根据个人的突变分布和HLA表型选择更高免疫原性的tumor新抗原 ( Neoantigen ) 组合,实现精准医疗【2】。 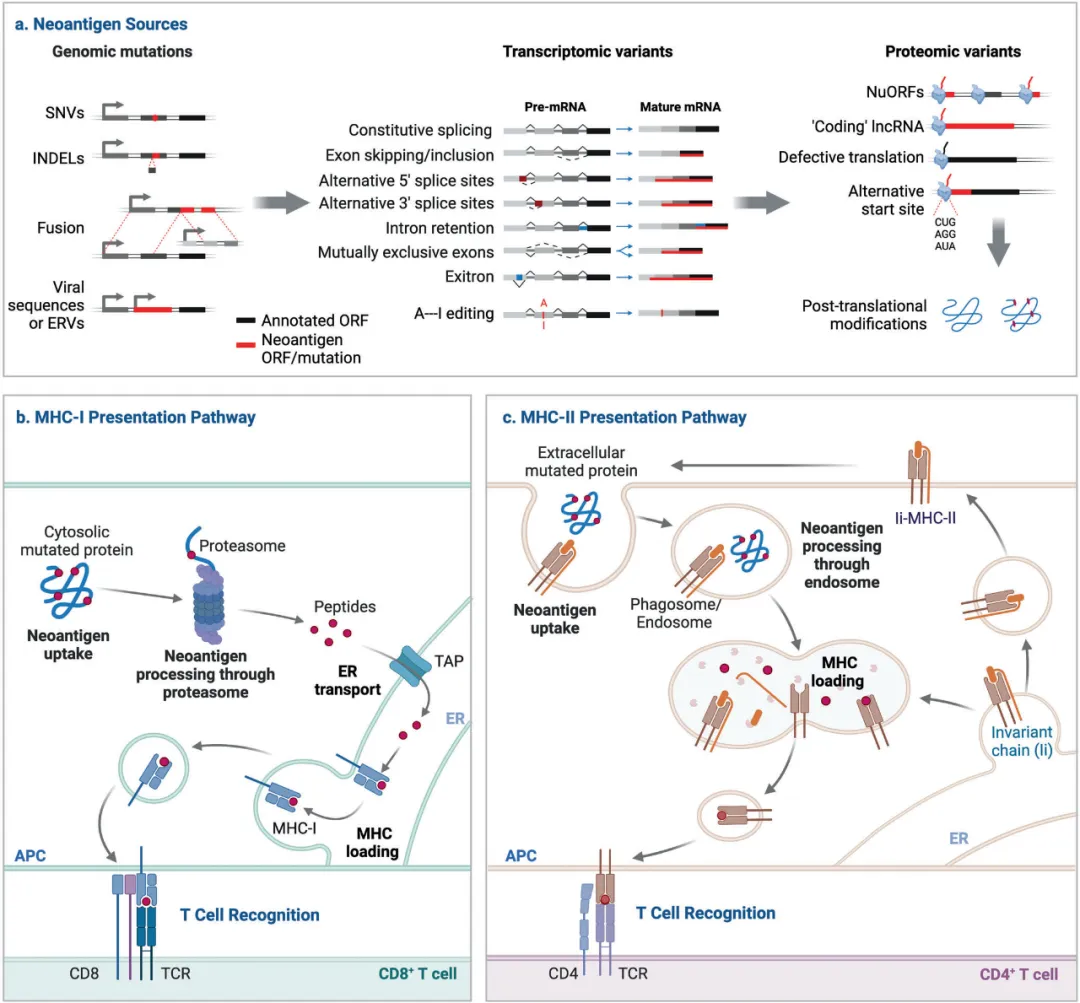 新抗原的产生与抗原呈递【3 】 tumor新抗原是由于tumor细胞基因组突变(SNVs、InDels、Fusions)、异常转录变异体或翻译后修饰而产生的异常蛋白质片段,在正常细胞中不存在3。免疫系统能够将其识别为"非己"物质,从而激活T细胞发动精准攻击。 tumor 新抗原优势在于:
新抗原的产生与抗原呈递【3 】 tumor新抗原是由于tumor细胞基因组突变(SNVs、InDels、Fusions)、异常转录变异体或翻译后修饰而产生的异常蛋白质片段,在正常细胞中不存在3。免疫系统能够将其识别为"非己"物质,从而激活T细胞发动精准攻击。 tumor 新抗原优势在于:
- 精准靶向tuomr细胞 :新抗原源于tumor特有突变,仅表达在cancer细胞表面,显著降低对正常组织的脱靶毒性风险。
- 激活双重免疫应答 :mRNA疫苗递送的新抗原可同时诱导CD8⁺和CD4⁺ T细胞活化,产生强效且持久的抗tumor免疫。
- 高度个体化设计 :基于患者特异性突变谱定制新抗原组合,克服tumor异质性并兼容PD-1等联合疗法提升疗效。
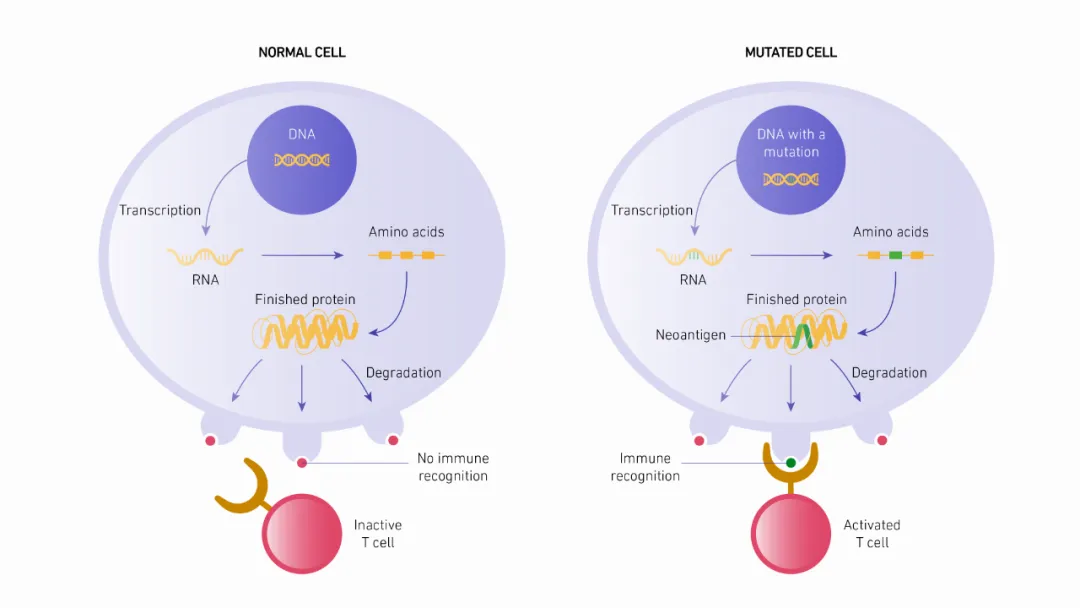
图源自Technology Networks
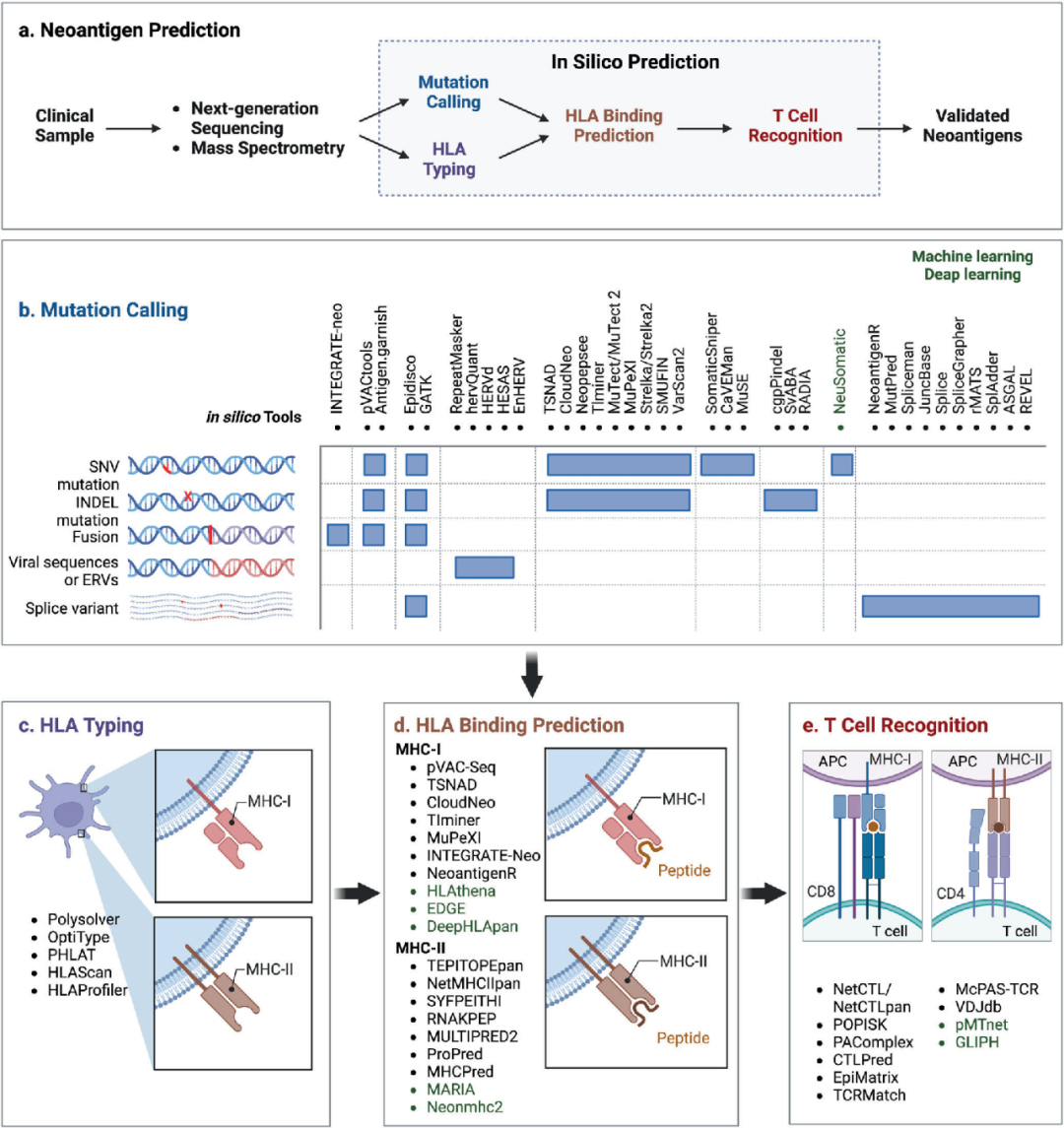
肿瘤新抗原预测流程【3】
个性化肿瘤mRNA疫苗如何发挥作用?
个性化tumor mRNA疫苗即通过基因测序靶向预测并筛选患者 tumor新抗原,将选定新抗原序列整合至mRNA载体,通过LNP包封从而制备mRNA疫苗。疫苗通过LNP递送编码 tumor新抗原的mRNA至抗原呈递细胞( 如树突状细胞 )摄取,在胞质内翻译表达新抗原蛋白;蛋白酶体将新抗原蛋白降解为短肽段( 抗原表位 ),与主要组织相容性复合体Ⅰ( MHC-Ⅰ )结合,呈递至细胞表面,被T细胞受体识别,激活CD8+T细胞,进一步分化为细胞毒性T淋巴细胞,直接杀伤 tumor细胞 。同时分泌的抗原还可能进入MHC-Ⅱ呈递途径,激活CD4+T细胞,促进B细胞产生 tumor特异性抗体,进一步增强免疫反应【2】。 
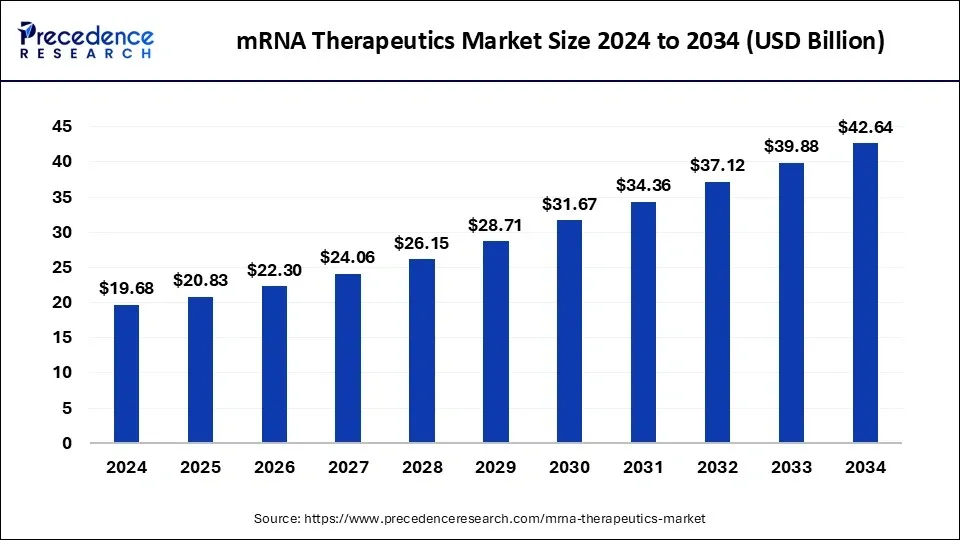
当前AI技术正在革新个性化 tumor mRNA疫苗。早在2016年,Moderna 便引入AI进行个性化 tumor mRNA疫苗序列设计,在2023年与OpenAI全面合作;BioNTech 在2023年收购InstaDeep进一步深化AI赋能;2025年初,美国星际之门 计划开启(软银、OpenAI、甲骨文等顶尖科技巨头领衔),注资5000亿美金,甲骨文CEOLarry Ellison在发布会上表示,计划落地后将助力AI增效,将个性化tumor mRNA疫苗的开发时间压缩至48小时。这种策略不经有望克服 tumor 异质性带来的治疗障碍,还可能大幅压缩患者等待时间。 Precedence Research 报告显示,预计到2034年,全球mRNA疗法市场规模将达426.4亿美元。
2025年8月8日,国家自然科学基金委员会发布赋能药物创新的RNA基础研究重大研究计划2025年度项目指南"关于发布赋能药物创新的RNA基础研究重大研究计划2025年度项目指南的通告 "。指南开篇强调"面向RNA药物创制的国家重大需求"。2025年拟资助(培育项目30-40项 × 80万/项 + 重点支持项目3-5项 × 300万/项 ),申请书提交日期为2025年9月15日-2025年9月22日16时。
https://www.nsfc.gov.cn/publish/portal0/tab434/info95398.htm




为****全面推进 tumor mRNA疫苗的研究与产业化发展。 表观生物与珲信生物达成战略合作协议。双方将聚焦 tumor mRNA疫苗技术及其相关产品领域,展开深度战略合作。期望携手为推动中国生物医药产业的创新与发展贡献一份力量,造福 tumor 患者。
我们正式推出从tumor新抗原预测到mRNA-LNP制剂制备的一站式服务:****
个性化tumor mRNA疫苗开发方案
一 肿瘤新抗原发现 1. 经典方案
- tumor组织:WES(15 G)+mRNA-seq(10G)
- 全血:WES(10 G)
分析内容: 体细胞突变(Mutations)、单核苷酸突变(SNVs)、插入/缺失(InDels)、融合基因(Fusions)
2 . 全基因组方案
- tumor组织:WGS(90 G)+WES(15 G)+mRNA-seq(10 G)
- 全血:WGS(90 G)+WES(15 G)
**分析内容:**Mutations、SNVs、InDels、Fusions、结构变异(SVs)、拷贝数变异(CNVs)、异常可变剪接(Junctions)
3. 联合翻译组方案
- tumor组织:WES(15 G)+longRNA-seq(15 G)+Ribo-seq(100 M)
- 正常组织:longRNA-seq(15 G)+Ribo-seq(100 M)
- 全血:WES(10 G)
**分析内容:**Mutations、SNVs、InDels、Junctions、Fusions、tumor特异性翻译事件
二 质粒构建 NeoDesign序列优化与设计 →基因合成 →载体构建 →质粒生产
三 mRNA批生产 模版制备 → ******体外转录(**IVT) →纯化与质控 →批次扩增
四 mRNA-LNP制剂批生产 LNP配方设计 ****→****mRNA-LNP封装 →纯化与浓缩 →GMP生产
五 质检交付4 mg mRNA-LNP制剂(供8次注射,GMP级,可用于IIT或者临床前研究)
研究方案与案例
经典方案:WES+mRNA-seq
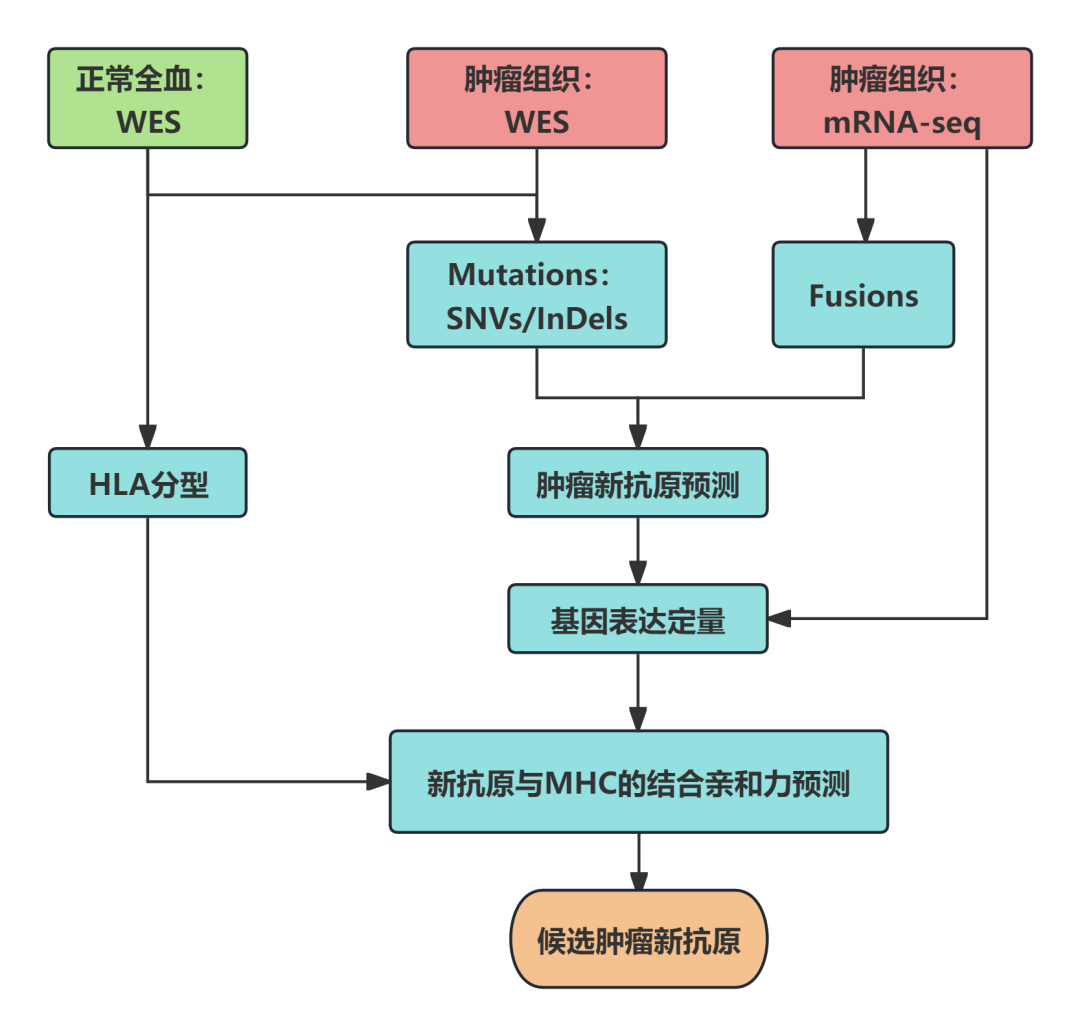
WES全外显子测序专注编辑蛋白质的区域,即外显子组。这部分虽然只占整个基因组的1~2%,但包含了大约85%的致病突变[4]。WES检测突变,mRNA-seq检测突变基因的转录表达水平。
优势: 成本较低,分析流程成熟。
局限: WES无法发现非编码区突变或较大结构变异,错过潜在的新抗原来源;mRNA-seq不能直接证明突变蛋白被翻译或呈递。
📑研究案例:
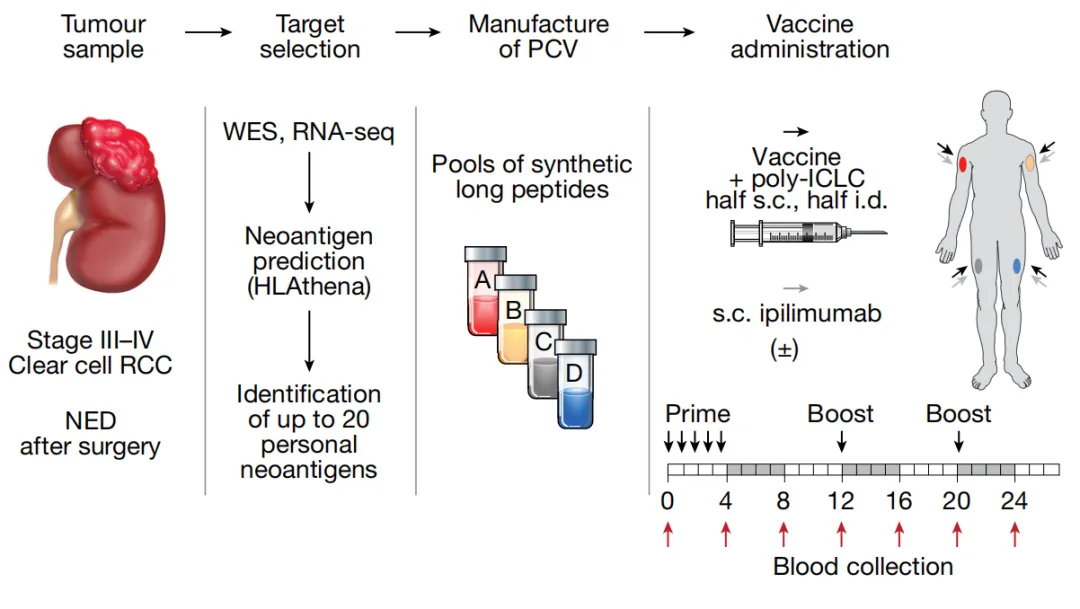
****1. 《Nature》A neoantigen vaccine generates antitumour immunity in renal cell carcinoma **[5]**
通过WES和RNA测序识别体细胞突变,优先选择驱动基因突变、高表达、克隆性突变等高质量新抗原,设计成15-33个氨基酸的合成长肽并分为4个肽池制备疫苗。结果显示,中位随访40.2个月后无一例患者复发,所有患者均产生了针对疫苗抗原的T细胞免疫反应,包括对VHL、PBRM1、BAP1等关键驱动基因突变的反应,77.8%的患者检测到抗自体tumor反应性,证明了个性化新抗原疫苗在低突变负荷tumor中的可行性和免疫原性。
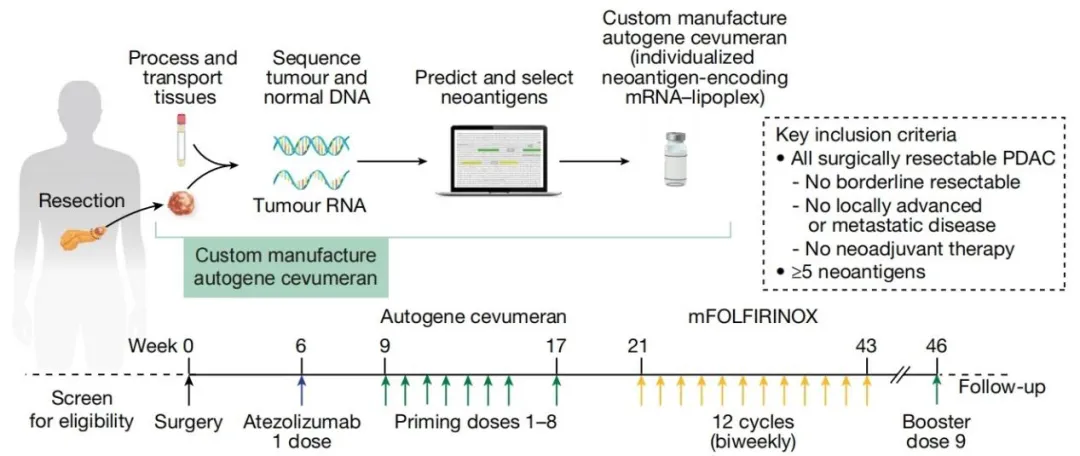
****2. 《Nature》Personalized RNA neoantigen vaccines stimulate T cells in pancreatic cancer **[6]**
这项研究使用WES识别体细胞突变、RNA-seq确认突变基因表达、HLA分型确定限制性元件,结合生物信息学算法预测和排序新抗原免疫原性,成功开发出个体化mRNA新抗原疫苗治疗胰腺cancer。研究还创新性地运用TCR Vβ测序开发CloneTrack方法追踪疫苗扩增的T细胞克隆,并通过单细胞RNA/TCR测序深入分析T细胞功能,证明了该疫苗能有效激活新抗原特异性T细胞应答并显著延长患者无复发生存期。
全基因组方案:WGS+WES+mRNA-seq
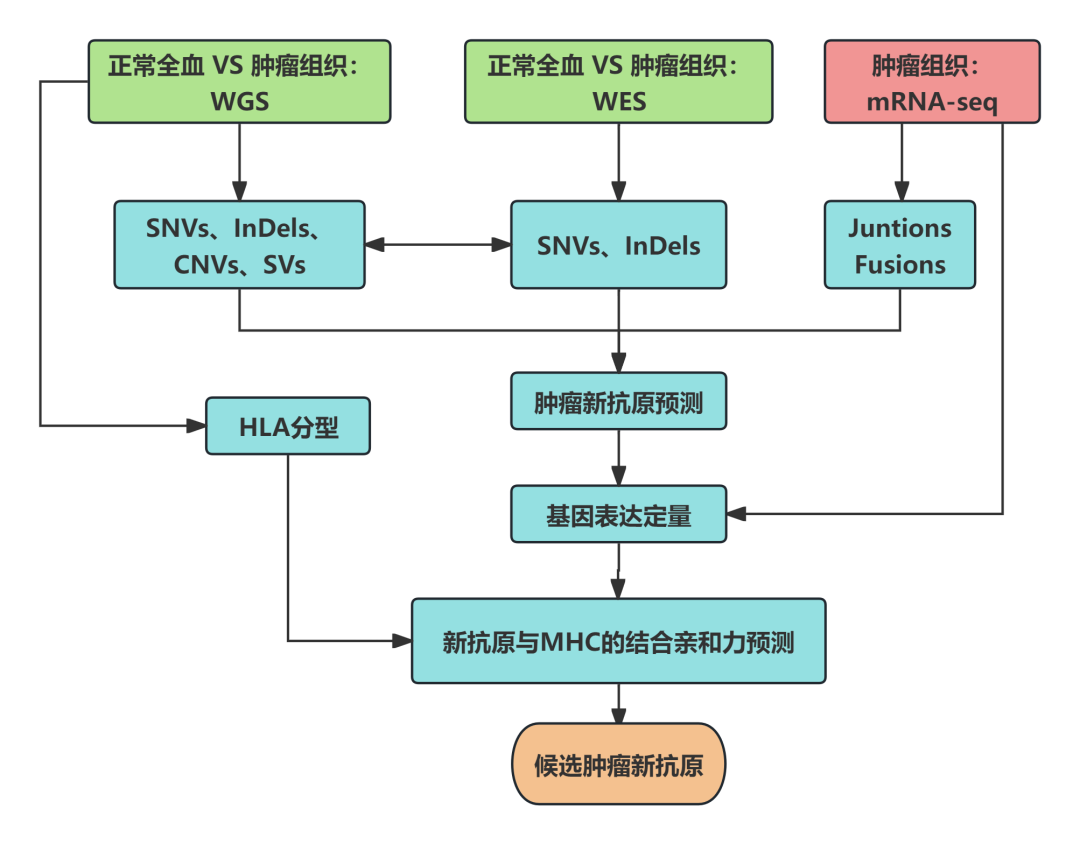
WGS覆盖全基因组,可以检测非编码区、SVs和CNVs,能发现WES遗漏的内部SV、基因融合断点和可变剪接位点[7,8]。
优势: 检测全基因组范围所有突变,包括非编码区的新抗原。
局限: 成本稍高、数据量大、分析时间延长
📑研究案例:
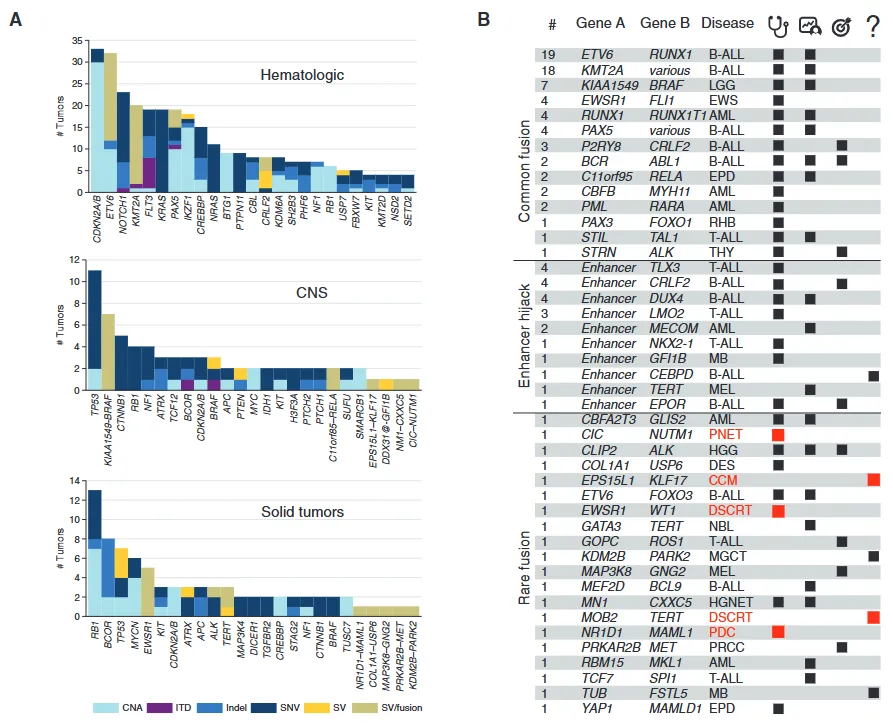
****1. 《Cancer Discovery》Genomes for Kids: The Scope of Pathogenic Mutations in Pediatric Cancer Revealed by Comprehensive DNA and RNA Sequencing **[9]**
这项研究通过三组学联合分析(WGS、WES、RNA-seq)对309例儿童cancer患者进行综合突变分析。研究在体细胞突变层面检出平均每例3个致病性变异,包括基因融合(36%)、增强子劫持(8%)和微缺失(15%)等复杂结构变异;在胚系突变分析中发现18%患者携带cancer易感变异,其中55%与tumor发生直接相关。三组学联合的核心优势在于WGS检测结构变异和非编码区突变,WES精确识别编码区点突变,RNA-seq验证功能影响和异常表达,相互补充实现了比单一测序平台更全面的突变谱解析,最终86%患者获得临床可操作的基因组信息。
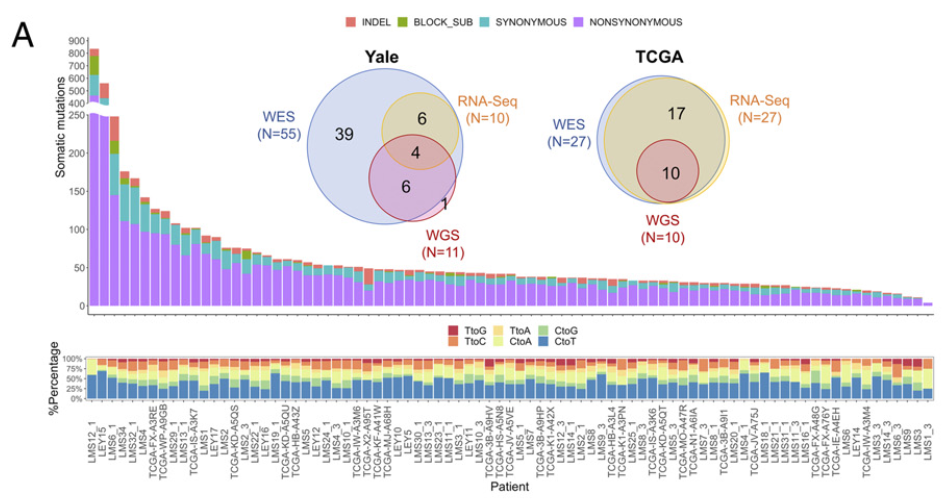
****2. 《PNAS》Integrated mutational landscape analysis of uterine leiomyosarcomas **[10]**
这篇研究采用WGS、WES和RNA-Seq三种测序技术的整合分析策略,对83例子宫平滑肌肉tumor进行了全面的基因组学分析。研究通过联合突变分析识别了体细胞SNV、InDel、CNV、Fusion和SV等多层次基因组改变,发现TP53(43.9%)、ATRX(30.4%)、PTEN(4.9%)和新识别的MEN1(6.1%)为显著突变的驱动基因。突变特征分析揭示25%的tumor具有同源重组修复缺陷(HRD)特征,2%具有微卫星不稳定(MSI)特征,76%的样本存在染色体复杂重排。
联合翻译组方案:WES+longRNA-seq+Ribo-seq
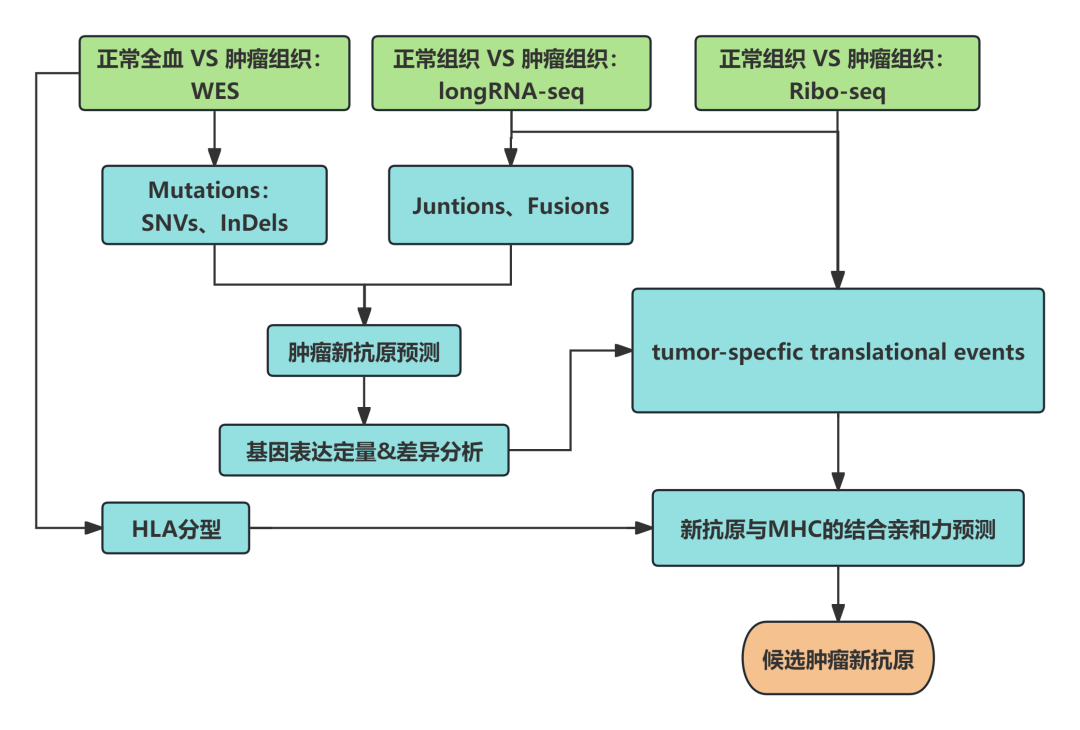
2025年5月,麻省理工在《Science 》发表了关于胰腺cancer隐秘抗原的文章,该研究发现了胰腺cancer中由HLA-I分子呈递的非典型抗原肽,这些抗原主要来源于lncRNA、UTR及内含阅读框,具有高度的癌症特异性[11]。longRNA-seq可用时检测mRNA和lncRNA;Ribo-seq可提供突变肽段真实翻译的证据;过滤掉未翻译的突变肽段;鉴定难以识别的非经典开放阅读框等;发现遗漏的潜在新抗原等[12]。
优势: 最大限度挖掘新抗原来源,可发现非经典ORF翻译出的肽段;增强候选新抗原的可信度,降低假阳性率[13]。
局限: 样本要求严格,成本稍高,数据分析复杂。
📑思路参考:
****1. 《Science》:Pancreatic cancer-restricted cryptic antigens are targets for T cell recognition **[11]**
该研究首次系统性地证明了胰腺cancer中存在大量cancer特异性的隐性抗原,这些来源于非编码基因组区域的肽类分子具有良好的免疫原性,可作为新的免疫治疗靶点。这为突变负荷较低的胰腺cancer等实体tumor提供了全新的免疫治疗策略,有望扩大cancer免疫治疗的适用范围,特别是对传统免疫检查点抑制剂治疗无效的患者群体。
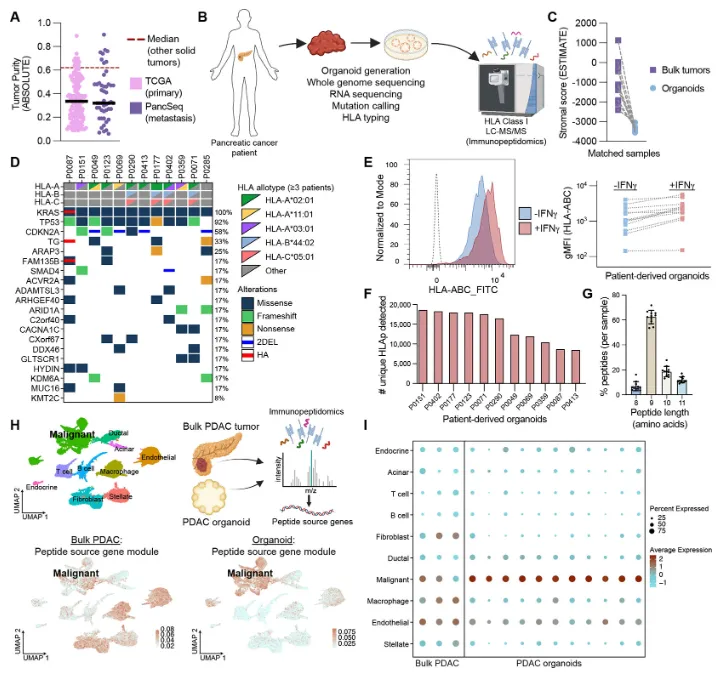
****2. 《Nat Biotechnol》:Unannotated proteins expand the MHC-I-restricted immunopeptidome in cancer **[12]**
这项研究通过结合核糖体分析和质谱技术,发现了数千个来自未注释开放阅读框(nuORFs)的MHC-I呈递肽段,证明nuORFs可作为癌症特异性抗原的重要来源,通过体细胞突变和cancer富集翻译两种机制扩展了潜在的新抗原库,为cancer免疫治疗提供了新的靶点和策略。
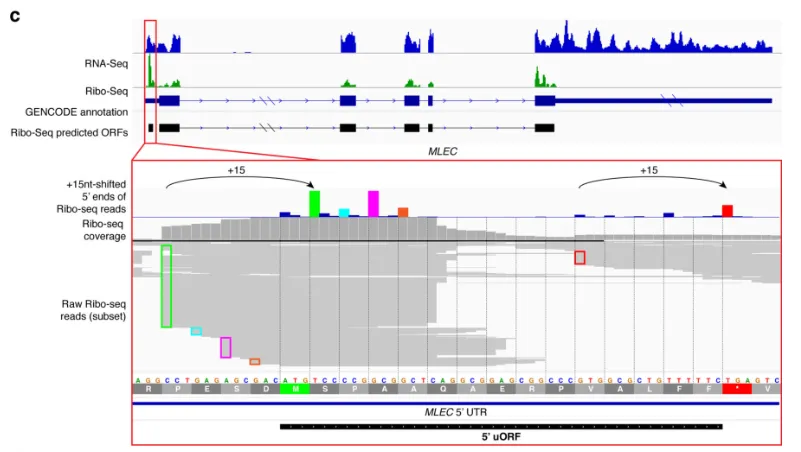
****3. 《Nat Commun》:Global proteogenomic analysis of human MHC class I-associated peptides derived from non-canonical reading frames **[14]**
该研究首次系统性地证明了约10%的人类MHC-I类呈递肽段来源于基因组的非编码区域或非规范翻译,这些隐性肽段具有独特的生物学特征和免疫学性质,显著增加了免疫肽组的复杂性,扩展了CD8+ T细胞免疫监视的范围。
NeoDesign序列优化与设计
多价tumor新抗原mRNA疫苗(如结合20-30个抗原肽)可增强免疫原性,但序列设计面临挑战:多肽随机组合和同义密码子会产生海量序列选项,导致linker过多、意外新抗原生成、复杂蛋白结构和mRNA不稳定等问题。这些可能降低疫苗的安全性和效能(如免疫逃逸或降解加速)。
NeoDesign **[15]** 工具可从多肽组合生成的序列池中选择最优蛋白序列,并为后续mRNA序列设计提供指导。
候选的tumor新抗原 输入NeoDesign(通常10-30个),输出最优蛋白序列和λ建议。NeoDesign的流程分为四个模块:
-
Library Construction(库构建)
-
Optimal Path Filtering(最优路径过滤)
-
Linker Addition(连接子添加)
-
λ-Evaluation(λ评估)
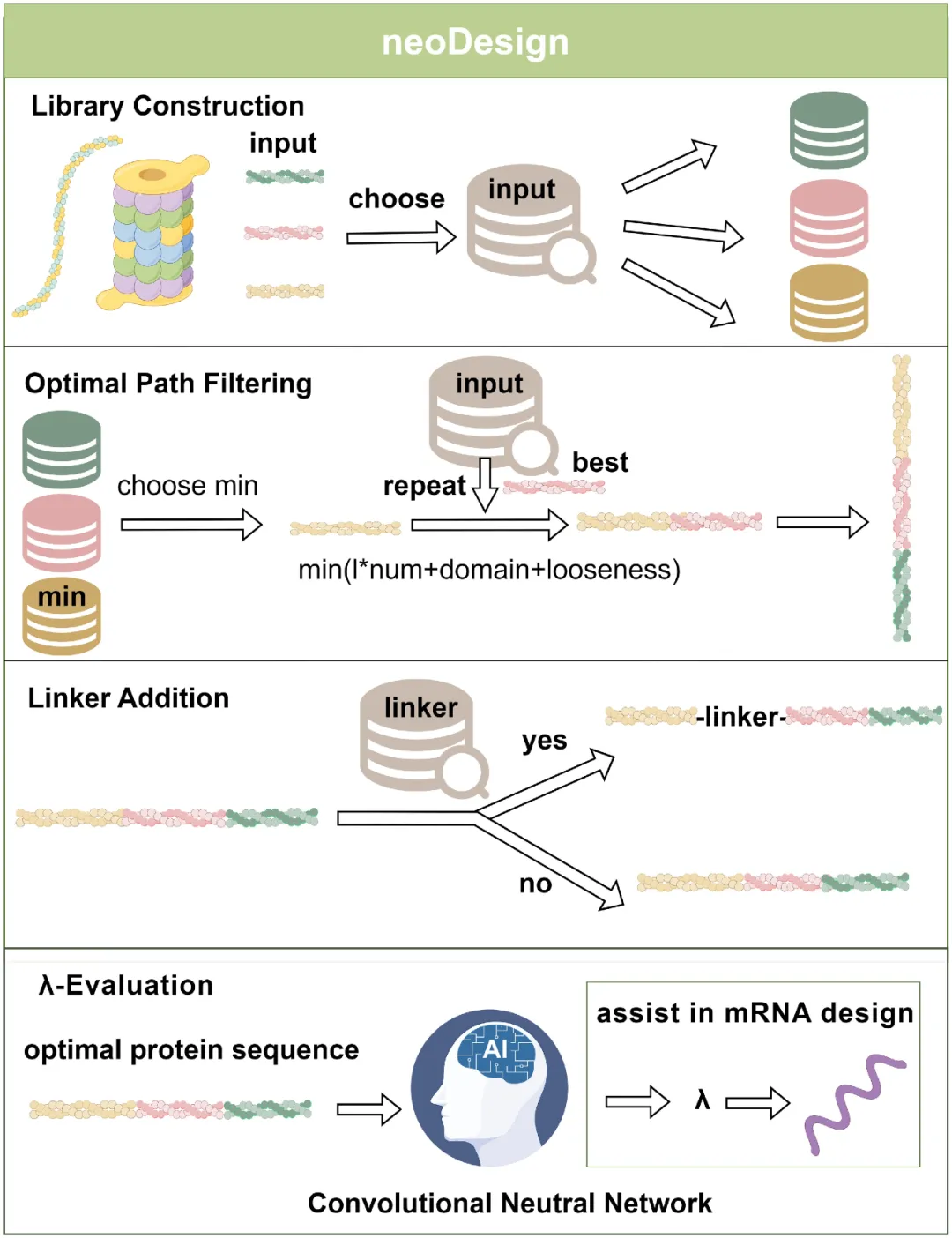
NeoDesign的架构****[15]****
生产流程
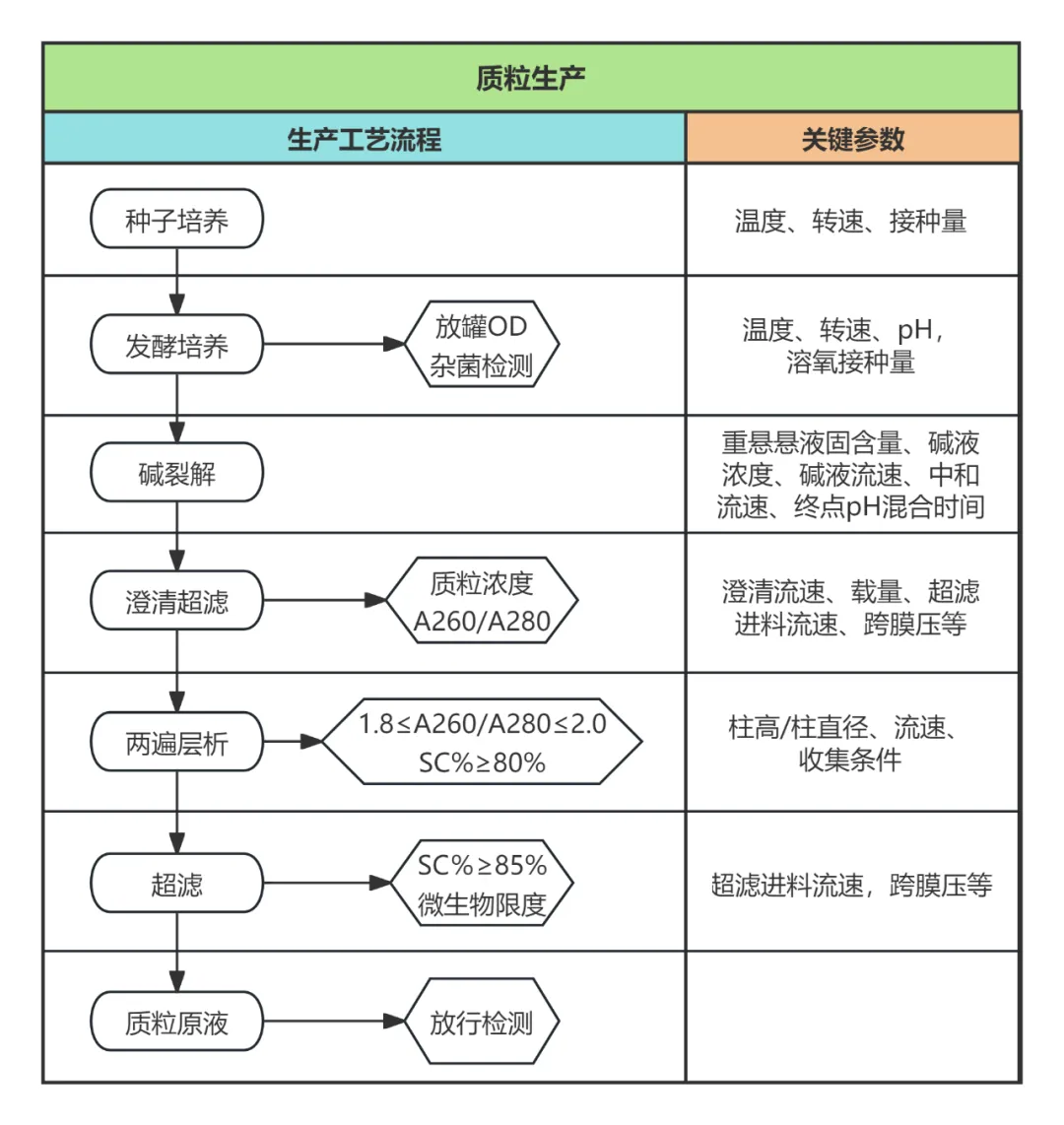
质粒生产
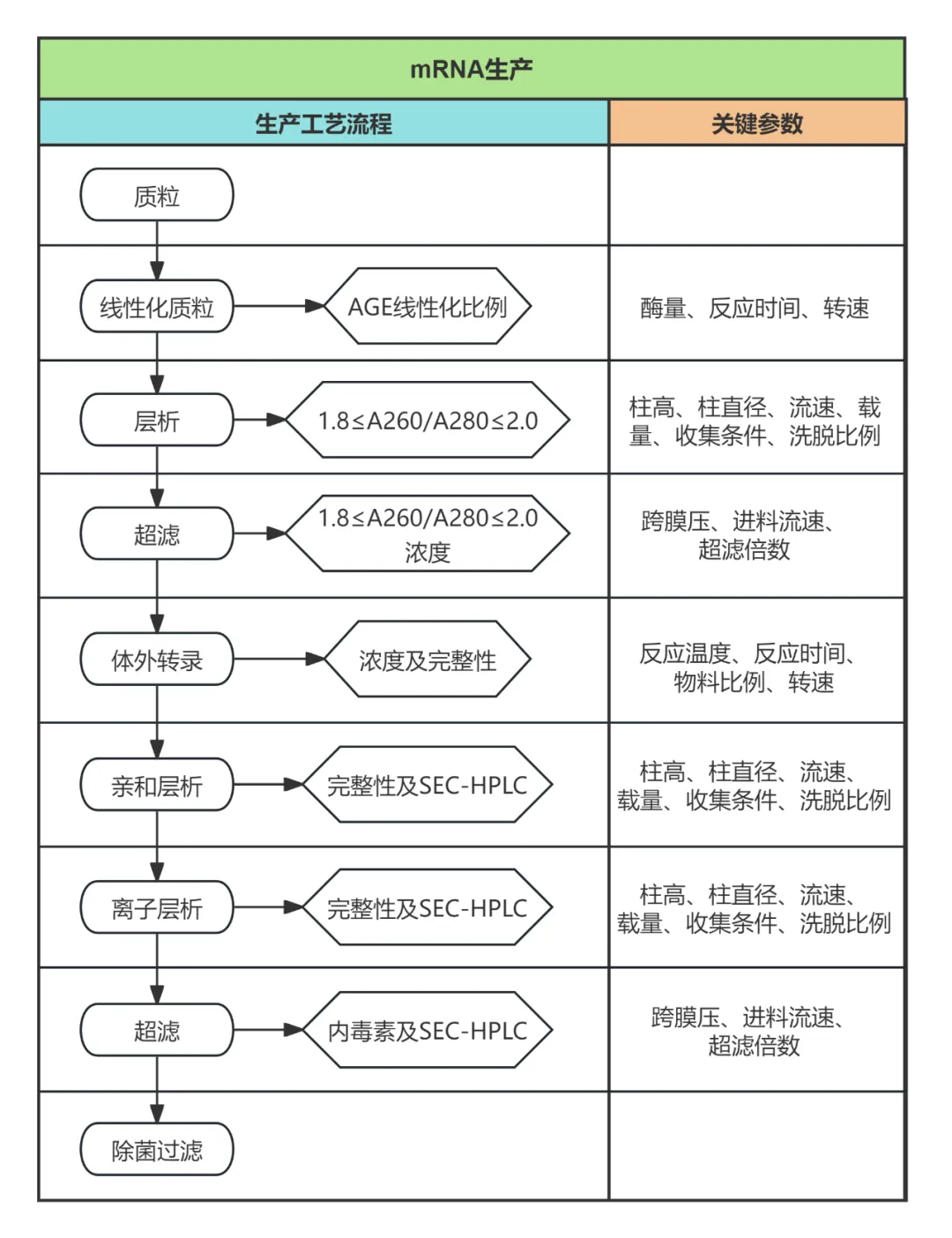
mRNA生产
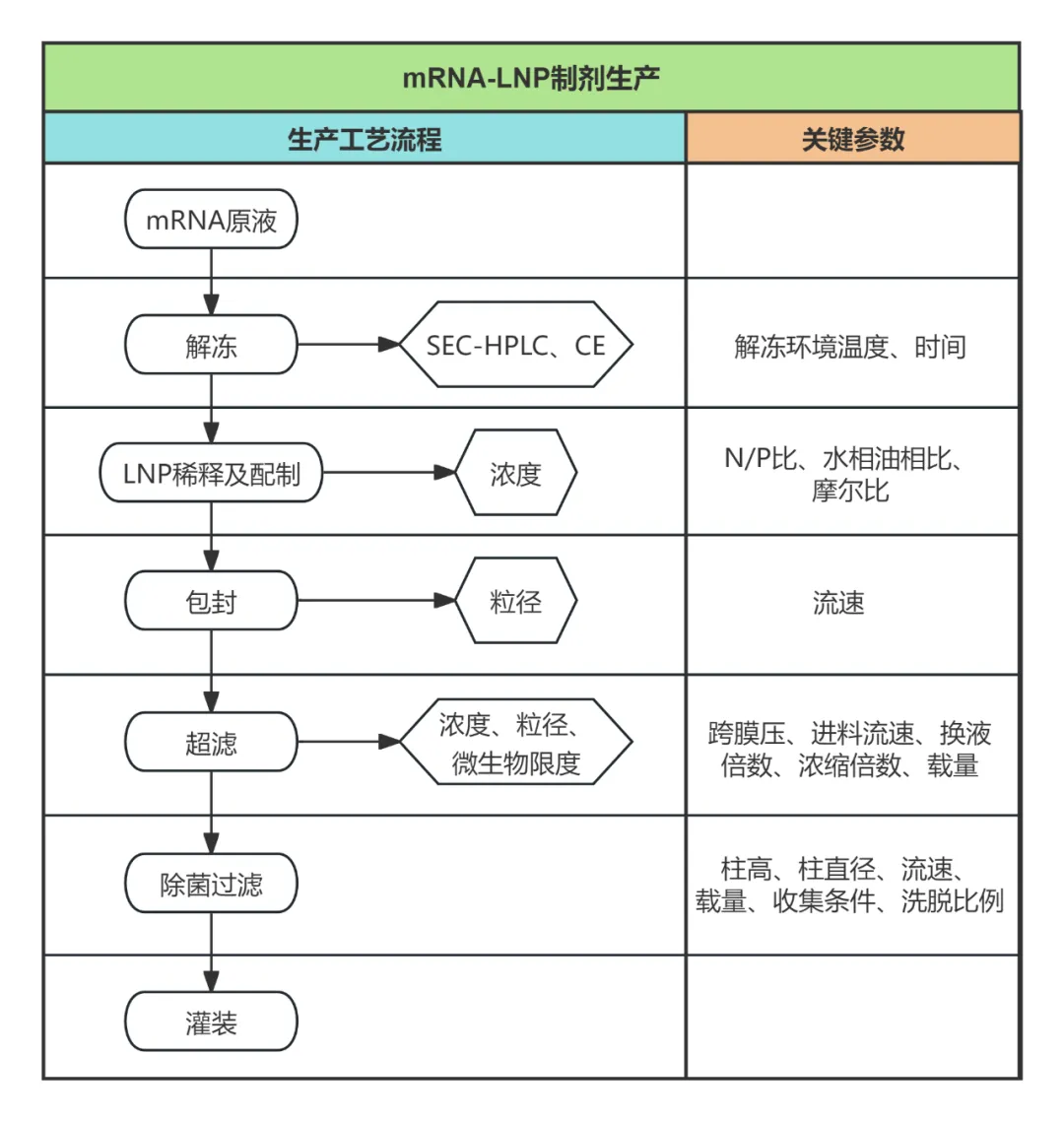
mRNA-LNP生产
参考文献:
1 Li H, Min L, Du H, Wei X, Tong A. Cancer mRNA vaccines: clinical application progress and challenges. Cancer Lett. 2025;625:217752. doi:10.1016/j.canlet.2025.217752 2 Kon E, Ad-El N, Hazan-Halevy I, Stotsky-Oterin L, Peer D. Targeting cancer with mRNA-lipid nanoparticles: key considerations and future prospects. Nat Rev Clin Oncol. 2023;20(11):739-754. doi:10.1038/s41571-023-00811-9 3 Xie N, Shen G, Gao W, Huang Z, Huang C, Fu L. Neoantigens: promising targets for cancer therapy. Signal Transduct Target Ther. 2023;8(1):9. Published 2023 Jan 6. doi:10.1038/s41392-022-01270-x 4 Chen Q, Yan W, Duan E. Epigenetic inheritance of acquired traits through sperm RNAs and sperm RNA modifications. Nat Rev Genet. 2016;17(12):733-743. doi:10.1038/nrg.2016.106 5 Braun DA, Moranzoni G, Chea V, et al. A neoantigen vaccine generates antitumour immunity in renal cell carcinoma. Nature. 2025;639(8054):474-482. doi:10.1038/s41586-024-08507-5 6 Rojas LA, Sethna Z, Soares KC, et al. Personalized RNA neoantigen vaccines stimulate T cells in pancreatic cancer. Nature. 2023;618(7963):144-150. doi:10.1038/s41586-023-06063-y 7 Richters MM, Xia H, Campbell KM, Gillanders WE, Griffith OL, Griffith M. Best practices for bioinformatic characterization of neoantigens for clinical utility. Genome Med. 2019;11(1):56. Published 2019 Aug 28. doi:10.1186/s13073-019-0666-2 8 Nguyen BQT, Tran TPD, Nguyen HT, et al. Improvement in neoantigen prediction via integration of RNA sequencing data for variant calling. Front Immunol. 2023;14:1251603. Published 2023 Sep 4. doi:10.3389/fimmu.2023.1251603 9 Newman S, Nakitandwe J, Kesserwan CA, et al. Genomes for Kids: The Scope of Pathogenic Mutations in Pediatric Cancer Revealed by Comprehensive DNA and RNA Sequencing. Cancer Discov. 2021;11(12):3008-3027. doi:10.1158/2159-8290.CD-20-1631 10 Choi J, Manzano A, Dong W, et al. Integrated mutational landscape analysis of uterine leiomyosarcomas. PNAS. 2021;118(15):e2025182118. doi:10.1073/pnas.2025182118 11 Ely ZA, Kulstad ZJ, Gunaydin G, et al. Pancreatic cancer-restricted cryptic antigens are targets for T cell recognition. Science. 2025;388(6747):eadk3487. doi:10.1126/science.adk3487 12 Ouspenskaia T, Law T, Clauser KR, et al. Unannotated proteins expand the MHC-I-restricted immunopeptidome in cancer. Nat Biotechnol. 2022;40(2):209-217. doi:10.1038/s41587-021-01021-3 13 Katsikis PD, Ishii KJ, Schliehe C. Challenges in developing personalized neoantigen cancer vaccines. Nat Rev Immunol. 2024;24(3):213-227. doi:10.1038/s41577-023-00937-y 14 Laumont CM, Daouda T, Laverdure JP, et al. Global proteogenomic analysis of human MHC class I-associated peptides derived from non-canonical reading frames. Nat Commun. 2016;7:10238. Published 2016 Jan 5. doi:10.1038/ncomms10238 15 Yu W, Yu H, Zhao J, et al. NeoDesign: a computational tool for optimal selection of polyvalent neoantigen combinations. Bioinformatics.2024;40(10):btae585.