Biology and applications of CRISPR--Cas12 and transposon-associated homologs
摘要:
CRISPR相关的Cas12蛋白是一个高度多样化的核酸靶向蛋白集合。所有Cas12变体都使用RNA引导和一个单一的核酸酶结构域来靶向互补DNA(或在少数情况下靶向RNA)。Cas12效应蛋白的高度变异性可以通过一系列来自不同转座子相关TnpB样祖先的独立进化事件来解释。尽管在基本结构和功能上具有相似性,但这导致了Cas12效应蛋白在大小、结构域组成、引导RNA结构、靶标识别和干扰策略 方面出现了前所未有的变异。在这篇综述中,我们比较了天然和工程化改造的Cas12及TnpB变体的独特分子特征。此外,我们概述了已建立的基因组编辑和诊断应用,并讨论了未来潜在的发展方向。
**Cas12效应蛋白:****是指**V型CRISPR-Cas系统中的效应核酸酶。**是一类在细菌和古菌中负责执行"靶向切割DNA"任务的蛋白质机器。
一. 核心职责是什么?
在细菌的CRISPR免疫系统里,Cas12蛋白有两个关键作用:
- RNA引导:它会结合一条专门设计的CRISPR RNA(crRNA),这条RNA像"GPS导航"一样,引导它去识别特定的DNA序列。
- DNA切割:一旦通过crRNA找到匹配的靶DNA,Cas12就会激活其内部的RuvC核酸酶结构域,像"手术刀"一样切断该DNA。
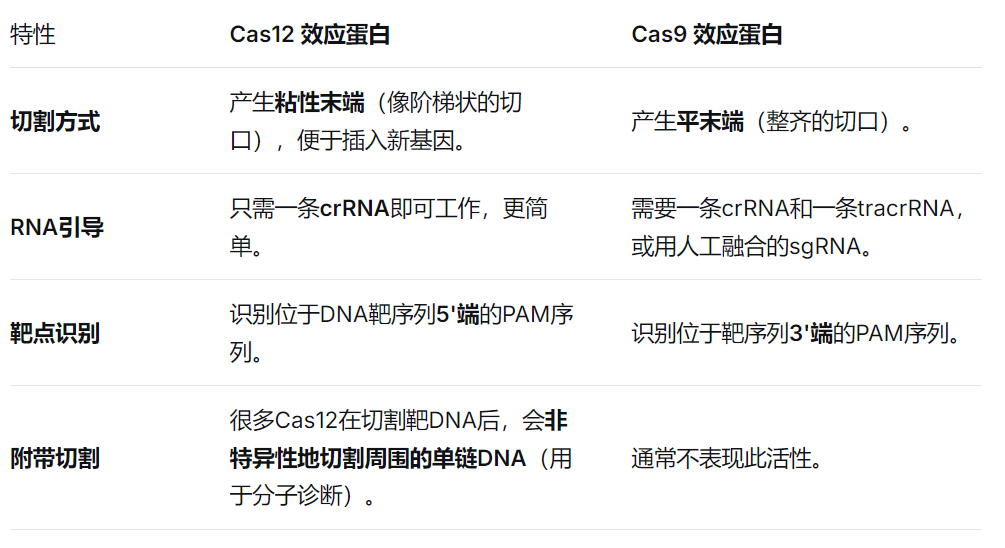
二. 它和著名的Cas9有什么区别?
这是理解Cas12的关键。Cas9(II型系统)和Cas12(V型系统)都是单蛋白DNA切割器,但Cas12有几个独特优点:
三. Cas12家族包括了哪些成员?
Cas12是一个极其多样化的超家族,并且还在不断扩张。文章中指出目前已有14个已充分鉴定的亚型(A-N)。常见的包括:
- Cas12a (曾用名Cpf1):最著名、应用最广的Cas12蛋白。
- Cas12b (曾用名C2c1):另一种常用的编辑器。
- Cas12f (曾用名Cas14):非常小型的Cas12蛋白(~400-700个氨基酸),易于递送。
- Cas12k:失活的Cas12,用于引导转座子进行大片段DNA插入。
四. 它与TnpB是什么关系?
TnpB是Cas12的进化祖先。TnpB是一种由IS200/IS605转座子编码的更小、更原始的RNA引导核酸酶。在进化长河中,TnpB基因被"驯化"并招募到CRISPR阵列旁,经过一系列结构域的扩展和功能优化,最终演化成了今天我们看到的各种复杂而高效的Cas12效应蛋白。可以说,Cas12是TnpB的"高级专业版"**。
总结
Cas12效应蛋白**是指一类体积可小、能产生粘性末端、通常只需crRNA引导、且具有附带切割活性的V型CRISPR效应核酸酶家族。它们是从更原始的转座子蛋白TnpB进化而来的强大DNA编辑工具,在基因编辑、碱基编辑和核酸检测等领域具有重要应用价值。
问题1:Cas12效应蛋白基本结构是什么?
所有Cas12效应蛋白都共享一个源自其祖先TnpB的核心骨架,整体呈"双叶"结构:
-
识别叶 :负责识别和结合引导RNA。包含WED结构域和REC1结构域。
- 在更复杂的Cas12中,识别叶会扩展出REC2、PI(PAM互作)等额外结构域,以增强识别能力。
-
核酸酶叶 :负责切割DNA。
-
RuvC结构域:这是Cas12唯一且最核心的催化结构域,包含保守的"D-E-D"(天冬氨酸-谷氨酸-天冬氨酸)催化三联体,负责切割DNA双链。
-
TNB结构域:插入在RuvC中,辅助结合靶DNA。
-
此外,Cas12蛋白通常还会包含一个或多个锌指结构域,起结构稳定作用。
问题2:Cas12效应蛋白的变异有哪些?
Cas12最具魅力的特点就是其极端多样性 。这种多样性源于其祖先TnpB在不同细菌和古菌中经历了几十次独立的进化事件。主要变异体现在:
-
大小变异 :从微型的Cas12f (400-700 aa) 到巨大的Cas12b (1100-1500 aa),差异巨大。
-
结构域组成变异:
-
微型 :如Cas12f,缺乏许多结构域,必须形成二聚体才能工作。
-
中型:如Cas12a,拥有基本的WED、REC1、RuvC和PI结构域。
-
大型:如Cas12b,插入了更多的REC和结构域,相互作用更复杂。
-
-
引导RNA变异:
-
依赖tracrRNA型:如Cas12b,需要一长一短两个RNA分子。
-
不依赖tracrRNA型:如Cas12a,只需要一个经过加工的短crRNA即可。
-
-
功能变异:
-
标准核酸酶:切割DNA双链(如Cas12a)。
-
切口酶:主要切割单链(如Cas12i)。
-
失活/结合蛋白 :失去切割能力,仅结合DNA用于基因调控 (Cas12m)或引导转座(Cas12k)。
-
RNA靶向蛋白:专门切割RNA(Cas12g、Cas12a2)。
-
-
PAM偏好性变异:不同亚型识别完全不同的PAM序列(如TTTN、TTN、CCY等)。
问题3:天然和改造Cas12和TnpB的区别有哪些?特征是什么?为什么要改造?
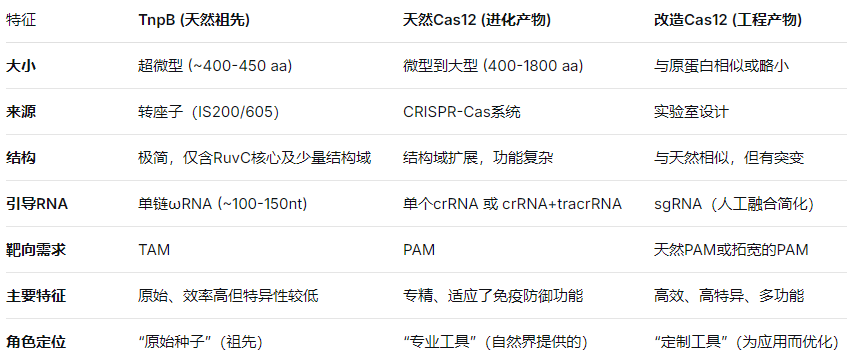
改造Cas12的核心逻辑与改造所有CRISPR工具一致,即克服天然版本的局限性,将其从"大自然的设计"优化为"人类应用的工具"。主要驱动力和追求的目标如下:
-
追求更小体积 :天然Cas12a很大(>1200 aa),远超AAV病毒载体的包装极限(~4.7kb)。通过改造微型Cas12f、Cas12n,或筛选更小的祖先TnpB,并用它们构建碱基编辑器 或基因调控器 ,实现高效的单AAV递送,这是体内基因治疗的关键。
-
追求更高活性 :许多天然Cas12(尤其是微型变体)在37°C(人类体温)下活性很低。通过理性设计和定向进化,引入正电氨基酸(增强DNA/RNA结合)等,可大幅提升其在人类细胞中的编辑活性。
-
追求更高特异性 :天然Cas12可能容忍向导RNA与靶点间的错配,导致脱靶效应 。通过突变那些稳定"非目标链"的氨基酸,可"破坏"其容错能力,让系统对错配更敏感,从而显著提升编辑的精准度和安全性。
-
追求更广的靶向范围 :每种天然Cas12都有其特定的PAM需求,这限制了可编辑的基因位点。通过对PAM互作结构域进行饱和突变 ,可开发出能识别更简并或非经典PAM的变体,极大地拓宽了基因组的靶向范围。
-
追求更多新功能:这是最富创造性的改造方向。
-
碱基编辑器 :将失活的dCas12 融合脱氨酶,实现单碱基的精确替换(C→T或A→G),无需产生DNA双链断裂。
-
引导编辑器 :将Cas12切口酶 融合逆转录酶,实现小片段的精确替换、插入或删除。
-
基因调控器 :将dCas12 融合转录激活/抑制因子,用于调控特定基因的表达水平。
-
诊断工具 :利用某些Cas12强大的附带切割活性,开发超灵敏的核酸检测平台(如DETECTR)。
-
总结
可以说,TnpB是Cas12的"原始引擎",天然Cas12是"各具特色的车型",而改造Cas12则是为满足特定需求(如更小、更快、更准、功能更多)进行的"赛车化改装"。
你之前的文档中关注的Cas12f、TnpB 等,都属于"微型"类别,它们最核心的改造动机就是突破AAV递送瓶颈 ,以便用于体内治疗。而改造Cas12a 则主要是为了拓宽PAM和做功能融合(碱基/引导编辑)。
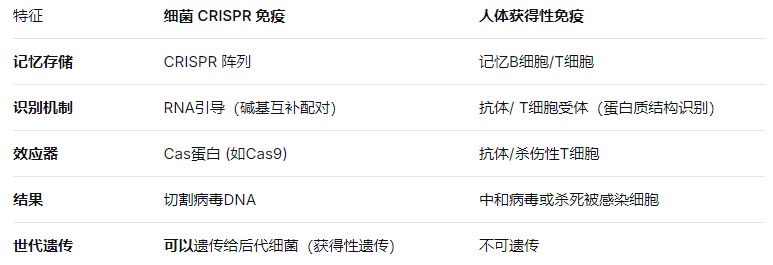
问题4、CRISPR免疫系统是什么?
是细菌和古菌(古生菌)特有的一种适应性免疫系统。你可以把它想象成细菌世界里的"疫苗档案系统"或"基因手术刀"。核心比喻:细菌的"通缉令"系统
1. 第一步:获取"通缉犯"信息 (适应阶段 - Adaptation)
-
当病毒(噬菌体)首次入侵细菌时,细菌会"抓获"一段病毒的DNA片段。
-
这段片段会被切割下来,作为"通缉犯照片"插入到细菌自己基因组的特定区域------CRISPR阵列中,成为新的间隔序列。下次再遇到这个病毒,就能立刻认出它。
2. 第二步:制作"子弹" (表达与加工 - Expression & Processing)
-
这个CRISPR阵列会被转录成一条长链RNA前体。
-
细菌的机器会把它切割成许多小段的CRISPR RNA,这就是"子弹"。每颗"子弹"上都带有那张"通缉犯照片"。
3. 第三步:执行打击 (干扰阶段 - Interference)
-
效应蛋白(如Cas9、Cas12)会拿起这颗"子弹"(crRNA)。
-
当复合物在细菌内遇到与"子弹"序列完全匹配的病毒DNA时,效应蛋白就会激活。
-
Cas9/Cas12会切断病毒的DNA,从而消灭病毒,保护细菌。
组成部分:两大核心元件
1. CRISPR阵列:基因组的"记忆库"。由一系列高度重复的序列(重复序列)和中间捕获的病毒独特序列(间隔序列)交替组成。间隔序列就是历史感染记录。
2. Cas基因 :编码执行具体功能的蛋白质。根据系统类型不同,编码的Cas蛋白也不同:
-
Cas9 (II型系统):单一蛋白,像"狙击手",进行精确切割。
-
Cas12(V型系统):单一蛋白,与Cas9类似但特性不同(如产生粘性末端)。
-
Cas3 (I型系统):多蛋白复合体,像"粉碎机",会"边走边吃",降解大片段的DNA。
-
革命性的基因编辑工具:科学家利用它的"RNA引导,蛋白切割"原理,开发成了今天强大的CRISPR/Cas基因编辑技术,让我们能以前所未有的精确度修改基因。
-
抗病毒应用:利用CRISPR系统设计专门攻击耐药菌的工程噬菌体,用于对抗"超级细菌"。
-
基础研究:研究它帮助我们理解了细菌与病毒之间数十亿年的"军备竞赛"进化史。
总结
CRISPR免疫系统是原核生物用来对抗病毒等入侵者的一种获得性免疫系统。它通过将入侵者的DNA片段存储在自己的基因组(CRISPR阵列)中,然后利用这些存储的信息(通过crRNA)引导Cas蛋白精确地识别并摧毁再次入侵的相同病毒DNA。
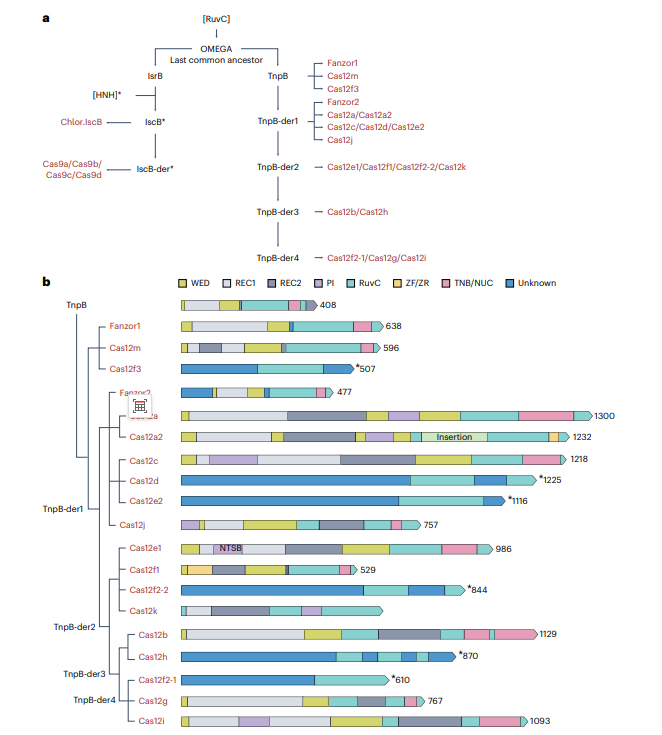 **图1 | OMEGA核酸酶向Cas9和Cas12的进化。
**图1 | OMEGA核酸酶向Cas9和Cas12的进化。
a. 示意图系统发育树,展示了OMEGA最后共同祖先的进化方向:(左分支) 向IsrB、IscB、IscB衍生型以及单系群Cas9进化;(右分支) 向TnpB、TnpB衍生变体、Fanzor以及多系群Cas12进化。所有核酸酶都具有RuvC样核酸酶 结构域,而只有左下分支的核酸酶(IscB、IscB衍生型和Cas9;用星号\*标记)拥有第二个HNH样核酸酶结构域。
b. Cas12蛋白的系统发育树及其结构域结构示意图。星号(\*)表示基于多个序列和预测结构比对估计的、细节较少的结构域架构。
1. TnpB和Cas12变体的进化
-
共同祖先:Cas9和Cas12的系统发育都与小型转座子编码蛋白相关。
-
TnpB的角色:TnpB原是IS200/IS605转座子的辅助蛋白。其生物学作用是帮助转座子维持和扩散:在DNA复制过程中,TnpA切除转座子,TnpB使用ωRNA引导链特异性识别切除位点并产生双链断裂,通过同源重组修复来"复制"转座子。
-
OMEGA系统:这些具有核酸酶活性的转座子相关蛋白统称为"专性移动元件引导活性核酸酶",包括原核的TnpB、IscB和真核的Fanzor。它们与Cas12机制相似,使用ωRNA作为引导,需要靶点邻近基序,由其RuvC结构域切割DNA双链。
2. 结构域架构
-
基本结构:所有OMEGA及衍生核酸酶都具有包含识别叶和核酸酶叶的双叶结构 。
-
TnpB较小 (~480 aa),RNA引导较长(100-120 nt);Cas12更大(400-1800 aa),RNA引导较短。
-
进化趋势:从TnpB进化到Cas12,识别叶通过扩增REC1、插入REC2或PI结构域等方式扩展,以增强对靶DNA和引导RNA的结合能力,从而允许引导RNA缩短。
-
独特案例:Cas12f1通过形成不对称同源二聚体来弥补结构域的缺失;Cas12h丢失了tracrRNA并获得Cas3。
3. 引导RNA
-
TnpB:使用单一的ωRNA,长约100-150 nt,包含高度结构化的部分(含假结)和可变的引导部分。
-
Cas12的两种进化路径:
(1) 将ωRNA截短为tracrRNA和来自CRISPR阵列的crRNA(如Cas12b/c/g/k/l等)。
(2) 将ωRNA序列缩减为能形成发夹结构的crRNA,无需tracrRNA,由Cas蛋白自身加工(如Cas12a、Cas12i、Cas12j等)。
4. PAM/TAM与靶标识别
-位置与偏好:所有靶向dsDNA的Cas12和TnpB都需要位于靶序列5'端的PAM或TAM,通常富含T碱基。
- 识别机制:主要通过PI、WED或REC结构域与PAM/TAM碱基发生特异性相互作用。
5. RuvC核酸酶活性
-
单一结构域切割双:与Cas9不同,Cas12和TnpB仅凭一个RuvC结构域依次切割非目标链和目标链,产生粘性末端。
-
失活变体:Cas12c2、Cas12k、Cas12m等因DED催化三联体退化而失去切割活性,转变为仅结合DNA的蛋白(用于基因沉默或引导转座)。
-
RNA靶向变体:Cas12g和Cas12a2可靶向单链RNA。
6. 附带切割活性
- 多数Cas12和TnpB在特异性识别靶标后,其RuvC结构域会被激活,非特异性地切割单链DNA (反式切割),这一特性被开发为诊断工具(如DETECTR)。
- 应用
-
基因组编辑:
-
天然变体:Cas12a是应用最广的V型效应器,已进入治疗血液疾病的临床试验。Cas12b、Cas12f、TnpB、Fanzor等也在真核细胞中表现出编辑活性,但通常需要优化。
-
工程化改造:
-
提高活性:引入带正电氨基酸以增强DNA结合。
-
增强特异性:突变参与结合非目标链的氨基酸,以破坏错配耐受性。
-
改变PAM:通过定向进化或理性设计位点饱和突变。
-
优化温度:如将嗜热BhCas12b改造为适合37°C工作的变体。
-
碱基编辑与引导编辑:
-
由于Cas12只有一个核酸酶结构域,难以像Cas9那样制成切口酶,因此碱基编辑器主要使用失活的dCas12融合脱氨酶。
-
已开发出基于Cas12a的引导编辑系统(如REDRAW、niCPE)。
-
基因调控:使用失活的dCas12融合转录激活/抑制结构域(如VPR),实现多重基因调控。小型Cas12f或TnpB在此类应用中有递送优势。
-
分子克隆:利用Cas12a切割产生的特定粘性末端,开发了无限制性内切酶的克隆方法(CCTL)。
-
诊断:利用Cas12的附带切割活性,结合等温扩增技术,开发了高灵敏度的核酸检测平台(如DETECTR)。
-
**引导转座**:Cas12k失活,与Tn7-like转座子形成复合物,实现RNA引导的大片段DNA靶向整合(CAST系统)。
8. 展望
-
Cas12家族的多样性源于从TnpB的多次、独立进化。
-
更小型的Cas12、TnpB及Fanzor变体在AAV或LNP递送方面具有巨大优势,有望推动体内基因治疗的发展。
-
尽管面临免疫原性等挑战,Cas12和OMEGA效应器的巨大潜力将持续推动生物技术创新。
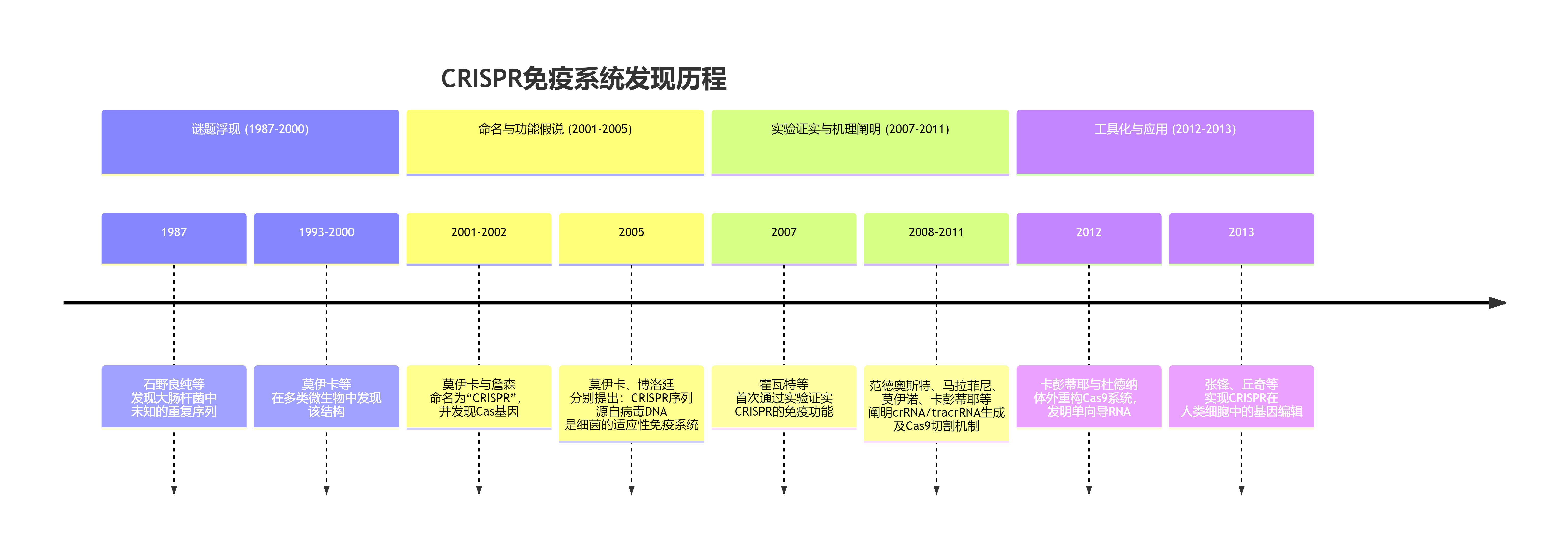
第二部分:主要技术路线总结
这篇综述虽然没有进行新的实验,但它系统地归纳了从转座子元件发现和改造新型基因编辑工具的技术路线。
其核心思想可以概括为:"寻根溯源(从进化源头挖掘)、解析机制(结构与生化)、工程化改造(优化性能)"。
主要技术路线如下图所示:
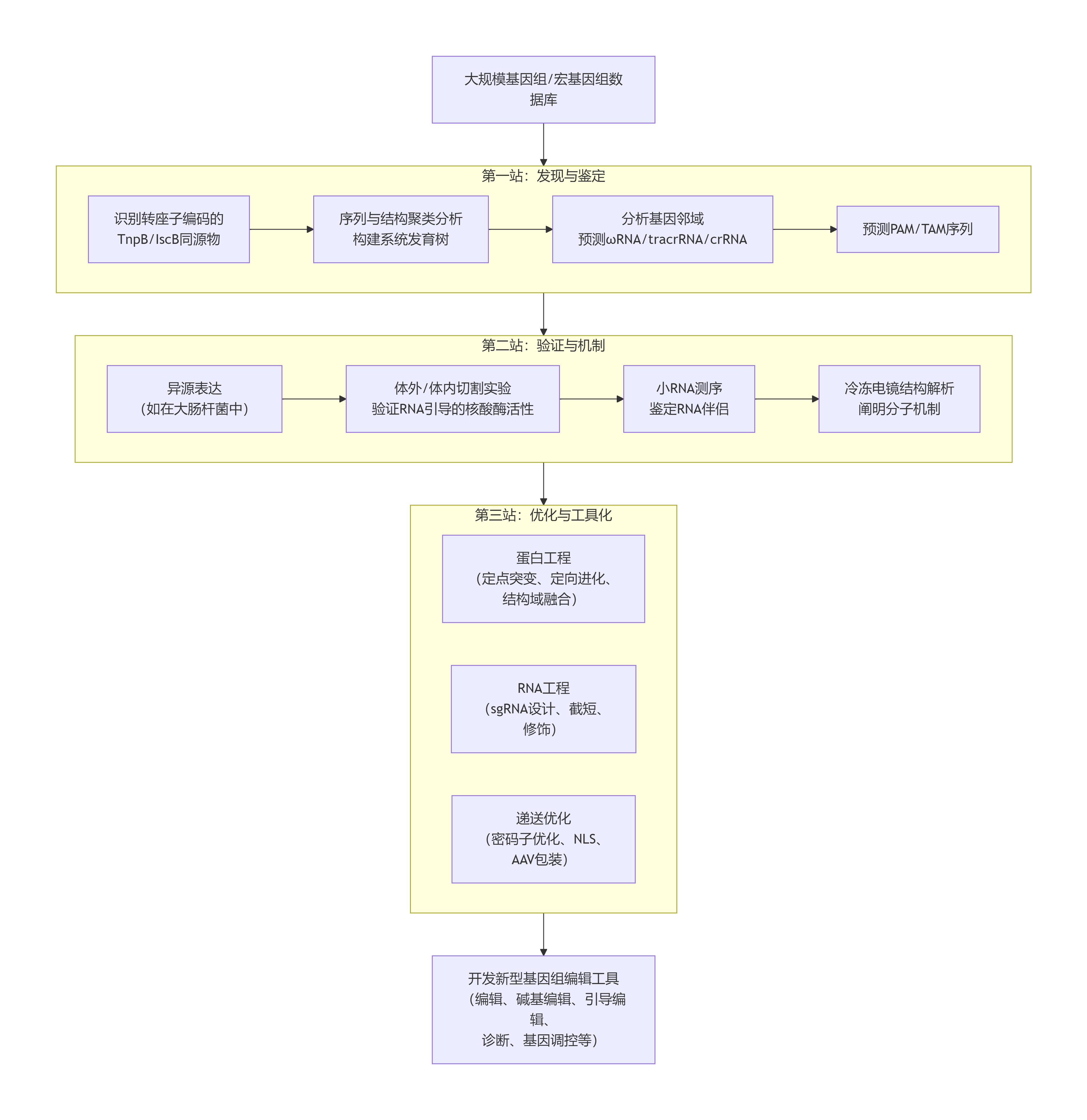
技术路线详解:
1. 第一步:发现与鉴定------从进化源头挖掘
(1)数据驱动:利用日益庞大的公共数据库(NCBI、JGI等),收集细菌、古菌及宏基因组中的序列数据。
(2)进化为指导:不局限于已知的CRISPR系统,而是追溯其进化祖先------IS200/IS605转座子家族。重点寻找编码TnpB或IscB的基因座。
(3)序列与结构分析:使用HMM、BLAST等工具进行同源搜索,通过序列比对和AlphaFold等AI结构预测工具进行系统发育分析,将序列分类为不同的TnpB和Cas12亚型。
(4)基因邻域分析:通过分析目标基因的上下游序列,预测其功能元件:
RNA伴侣 :若附近有CRISPR阵列则预测为crRNA/tracrRNA;若附近有转座子末端则预测为ωRNA。
PAM/TAM:通过保守序列模式预测其识别的靶点旁侧基序。
2. 第二步:验证与表征------确认功能与机制
(1)高通量筛选:在模式生物(如大肠杆菌)中异源表达候选系统,构建靶标库(如带随机PAM的质粒),通过质粒清除实验快速筛选出有功能的系统并确定其TAM。
(2)生化验证:纯化效应蛋白和其RNA,在体外重建RNA引导的DNA切割反应,证实其独立活性。
(3)测序鉴定RNA:通过小RNA测序,明确与效应蛋白结合的RNA序列,确定其形态(是单一的ωRNA,还是tracrRNA-crRNA对)。
(4)结构生物学:利用冷冻电镜技术解析效应蛋白-RNA-靶DNA三元复合物的结构,从原子水平阐明其靶标识别、PAM/TAM识别和DNA切割的分子机制。
- 第三步:工程化改造------优化以适用于应用
(1)蛋白工程:
* 提高活性:在蛋白表面或活性中心附近引入带正电的氨基酸(精氨酸),增强与带负电DNA骨架的结合。
* 增强特异性:突变RuvC结构域中参与稳定非目标链的氨基酸,使蛋白对向导与靶标间的错配更敏感。
* 扩展PAM:对PAM互作结构域进行定点饱和突变或定向进化,识别非经典的PAM序列。
* 温度驯化:突变嗜热蛋白表面残基,使其在中温(37°C)下具有更高活性。
* 功能融合:将失活的dCas12融合到脱氨酶(做碱基编辑)、逆转录酶(做引导编辑)、或转录激活因子(做基因调控)上,赋予其新功能。
(2)RNA工程:
* 嵌合体设计:将天然的tracrRNA和crRNA融合为一个人工的单链引导RNA,简化应用。
* 截短与修饰:删减RNA中不必要的茎环结构以缩小尺寸,或对RNA骨架进行化学修饰以提高稳定性和编辑效率。
- 第四步:应用落地------工具化与场景适配
(1)递送是关键:对于体内应用,优先选择小型化的变体(如TnpB、Cas12f、Cas12n),以便能包装到AAV病毒载体或脂质纳米颗粒中。通过密码子优化、添加核定位信号等方式使其在真核细胞中高效工作。
(2)场景化验证:在植物、动物细胞、小鼠模型乃至临床样本中验证其在基因组编辑、碱基编辑、诊断、大片段DNA插入等方面的实际效能。
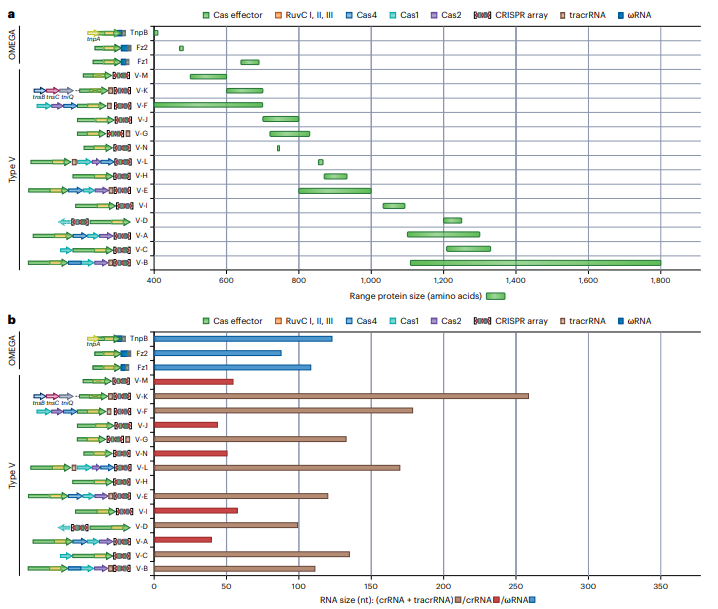
a, b, y轴表示OMEGA和V型亚型。x轴分别表示效应蛋白的大小(以氨基酸为单位)(a)和其伴随的RNA种类的大小(以核苷酸为单位)(b);其中,tracrRNA/scoutRNA用棕色表示,crRNA用红色和菱形表示,ωRNA用蓝色表示。在V-H型中未发现tracrRNA,因此也没有可用的crRNA长度数据。
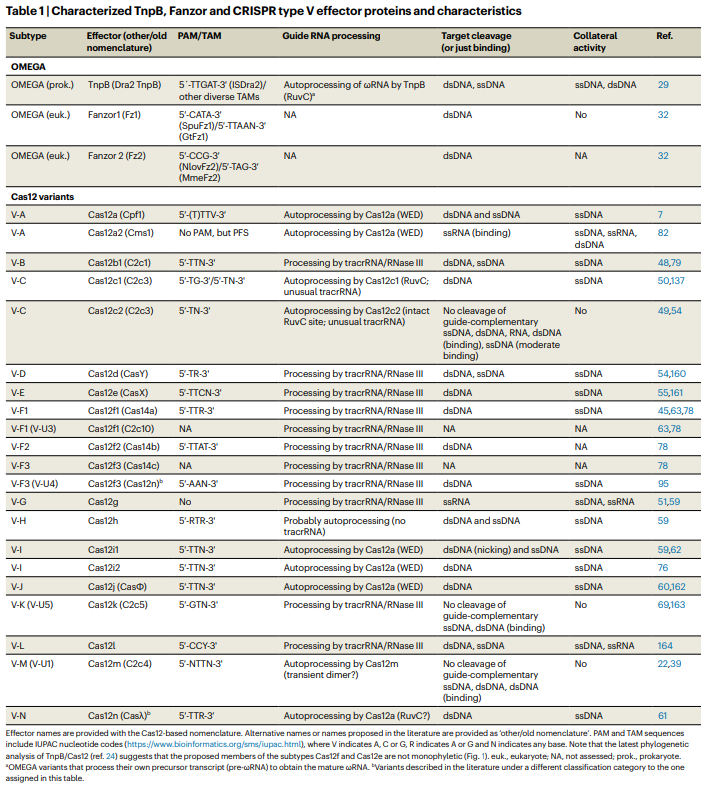
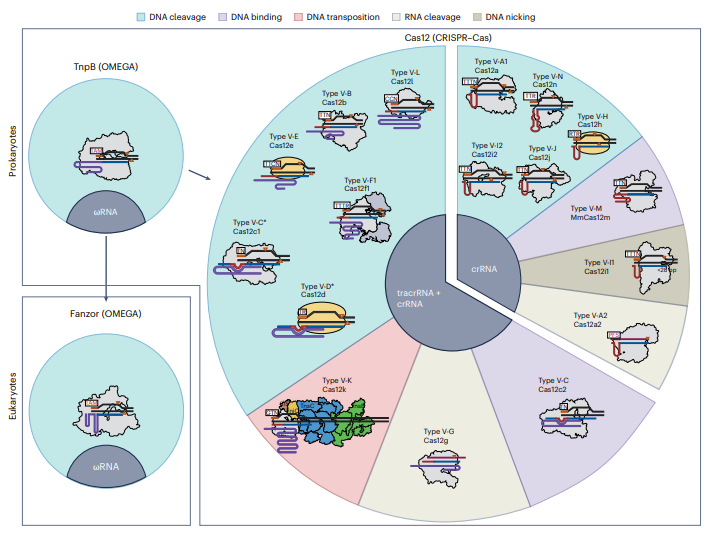
图3 | Cas12变体的不同活性。
Cas12效应蛋白根据其伴随的RNA种类(是一个tracrRNA/crRNA对,还是仅仅一个单一的crRNA)进行分组,并根据其dsDNA切割、dsDNA结合、RNA引导的DNA转座、RNA切割或DNA切口酶活性进行分类。
有crRNA伴随的效应蛋白可以在没有宿主因子帮助的情况下加工它们的前体crRNA。星号(*)表示那些有特定tracrRNA(在某些情况下称为scoutRNA)伴随的效应蛋白,并且它们可以在没有宿主因子帮助的情况下加工自身的前体crRNA。
具有实验解析结构的Cas12效应蛋白以灰色表示。在Cas12f1同源二聚体的情况下,第二个亚基以深灰色描绘。
伴随Cas12k的Tn7样CRISPR相关蛋白和核糖体蛋白S15分别以棕色(S15)、黄色(TniQ)、蓝色(TnsC)和绿色(TnsB)表示。
以下是为不同Cas12变体轮廓界定所使用的蛋白质数据库(PDB)ID:6I1L (Cas12a1),8D49 (Cas12a2),5U30 (Cas12b),7VYX (Cas12c1),7V94 (Cas12c2),7C7L (Cas12f),6XMG (Cas12g),6W5C (Cas12i),7LYS (Cas12j),8EA3 (Cas12k),7YOJ (Cas12l),8HHL (Cas12m2),8DC2 (Cas12n),8H1J (TnpB) 和 8GKH (Fanzor)。
没有实验解析结构的核酸酶以黄色表示。
Cas12i1被归入DNA切口酶类别,尽管当crRNA-DNA异源双链长度≥28 bp时,它也能够切割dsDNA。Cas12f2和Cas12f3虽未在图中描绘,但它们具有与Cas12f1相同的功能,尽管尚未证明它们能形成二聚体。
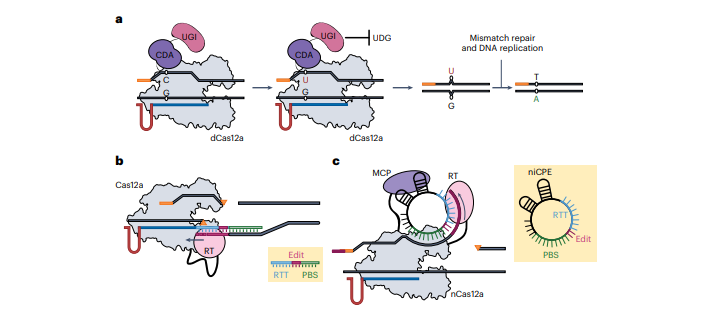
图4 | 基于Cas12a的碱基编辑器(BEs)和引导编辑器(PEs)。
a, 一个基于胞嘧啶脱氨酶(CDA)和dCas12a的碱基编辑器示例。在此,dCas12a与胞嘧啶脱氨酶以及一个尿嘧啶DNA糖基化酶抑制剂(UGI)融合。UGI可阻止尿嘧啶DNA糖基化酶(UDG)切除U-G中间体,从而提高碱基编辑效率。
b, REDRAW类型的基于Cas12a的引导编辑器(PE)。Cas12a与逆转录酶(RT)融合,并连接一个引导编辑向导RNA(pegRNA)。该pegRNA包含了引导RNA、逆转录模板(RTT)以及一个3'端的目标链引物结合位点(PBS),从而实现对目标链的编辑。
c, 另一种基于Cas12a的引导编辑器设计,采用了经过工程化改造的MS2-pegRNA。在这种情况下,Cas12a切口酶与MS2外壳蛋白(MCP)融合,MCP会与pegRNA上的MS2茎环结构相互作用。同时,该Cas12a切口酶也与逆转录酶(RT)融合。环状的pegRNA包含PBS区域,用于结合非目标链,随后将根据RTT的设计对该链进行编辑。