口腔炎症(如牙周炎、种植体周围炎)影响全球近一半人口。为什么有些炎症会迅速破坏组织(快速进展型),而有些则发展缓慢?过去几十年,科学界对牙周炎的研究主要集中在"细菌如何激发免疫细胞(如巨噬细胞、T细胞)引发炎症"这一线性逻辑上。然而,作为组织基底的"结构性细胞"(上皮细胞和间质基质细胞)长期被认为是被动受害者。然而,近期的空间多组学证据指出,结构性细胞绝非无辜的旁观者。它们不仅能建立物理屏障,还能主动协调免疫细胞的招募。在慢性病灶中,结构性细胞甚至会形成"炎症记忆",主动维持和放大局部的免疫攻击。临床上,种植体周围炎(Peri-implantitis)和重度牙周炎(Stage III/Grade C)是最具破坏性的两种快速进展型黏膜炎症。它们发生在解剖位置相邻、但生物学环境迥异的微型生态位中,却殊途同归地导致了软硬组织的极速崩塌。这暗示着背后存在一个共通的、宿主驱动的分子开关。
近期,一项发表在《Nature Communications》上的研究,通过整合单细胞转录组 测序 、激光捕获显微切割( LCM)+微生物基因组测序 、Xenium 空间转录组 、Phenocycler-Fusion ( PCF) 空间 单细胞 蛋白组等,揭示了快速发展的口腔炎症(如种植体周围炎、重度牙周炎)的核心驱动力并非完全依赖细菌负荷,而是由宿主自身的血管内皮细胞发生代谢重编程(CD38介导的NAD+耗竭)所引发的"血管病变"。

研究首先用传统的组织学染色揭示了健康牙龈结构紧密,普通牙周炎有局部破坏,而种植体周围炎则呈现出大面积的基质降解和深层免疫细胞浸润。种植体周围炎的病灶面积在水平宽度还是垂直深度上都显著大于普通牙周炎。在种植体周围炎的病灶中,研究者敏锐地观察到大量"血管样结构"散布在炎症区域。这暗示血管正在疯狂增生或发生改变。
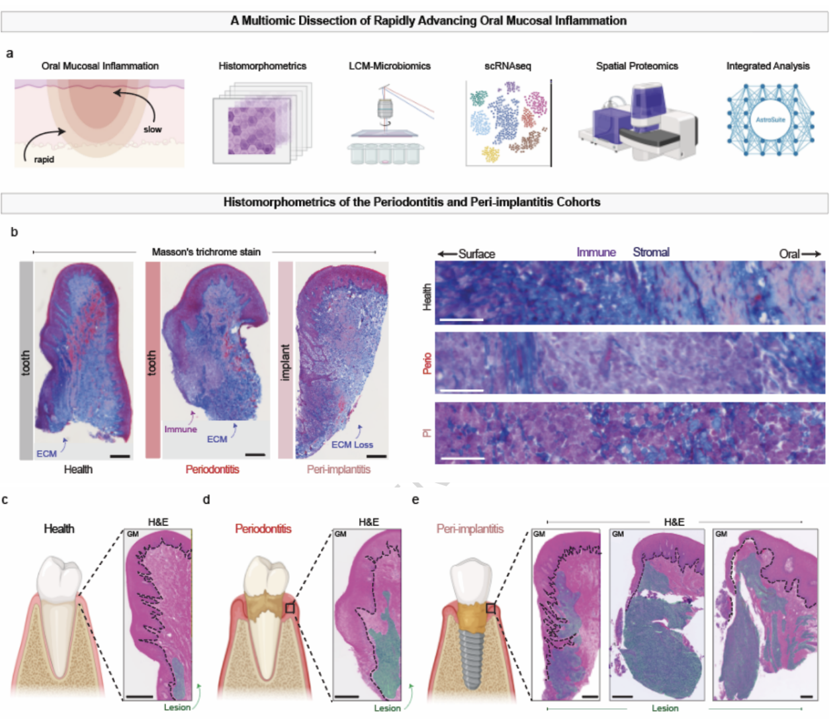
常规思维定式认为哪里的炎症重,哪里的细菌就一定多。而接下来研究者通过激光捕获显微切割技术(LCM),把牙龈组织切片上的"上皮区"和"基质区"分别切下来,进行微生物全基因组测序。统计学显示,不管是上皮区还是基质区,无论是细菌总量还是菌群多样性,普通牙周炎组织的细菌负荷竟然显著高于极具破坏力的种植体周围炎。研究者由此推断,种植体周围炎病灶的扩张,必然是由宿主自身失调的内在机制主导。
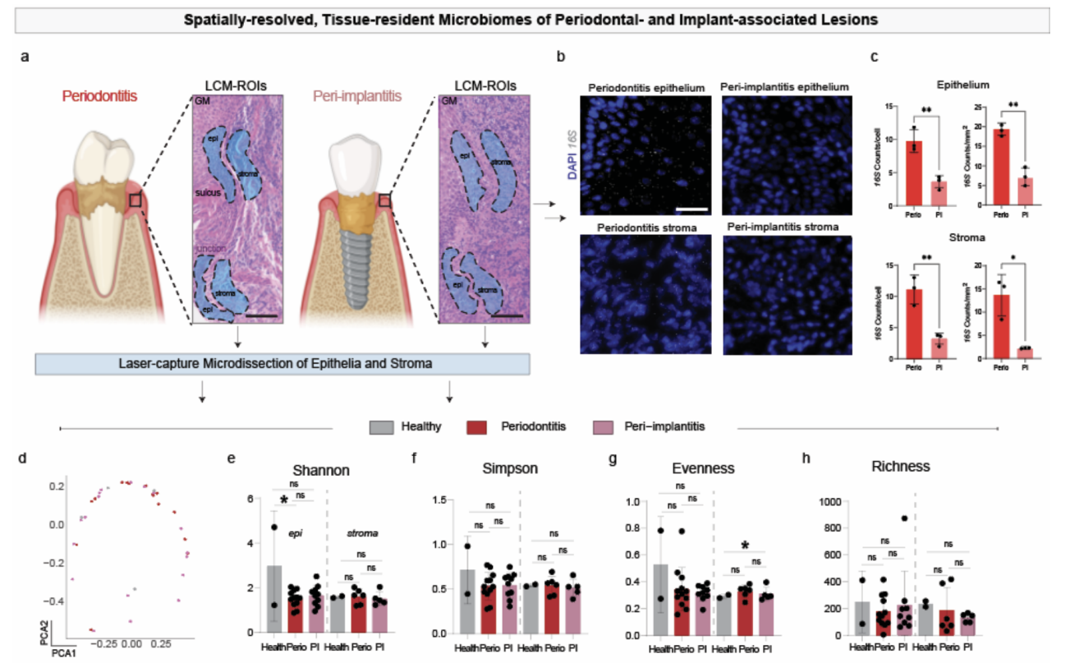
研究者利用 sc RNA-seq 分析, 发现 了 在种植体周围炎中,血管内皮细胞的基因表达谱发生了最为剧烈的扰动 。通路富集分析显示,这些内皮细胞中与线粒体氧化磷酸化(OXPHOS)和电子传递链相关的基因被严重抑制,而与NAD+代谢及Sirtuin信号通路相关的基因却被异常激活。这表明内皮细胞正处于极度的代谢应激和能量枯竭状态。进一步细分发现了高表达TNFRSF6B和ICAM1的****毛细血管后微静脉(** **PC-VECs)****变化最为剧烈。内皮-间质转化和缺氧通路在PC-VECs中被激活。
为了在组织原位解析空间分子特征,研究者对 6例 种植体周围炎 样本进行了 Xenium 5K空间转录组分析 。在空间原位定义了不同内皮细胞亚型,尤其是验证了NAD+代谢 通路 在PC-VECs中被显著激活,特别是NAD+的消耗酶CD3 8在PC-VECs中被特异性地大量诱导表达。
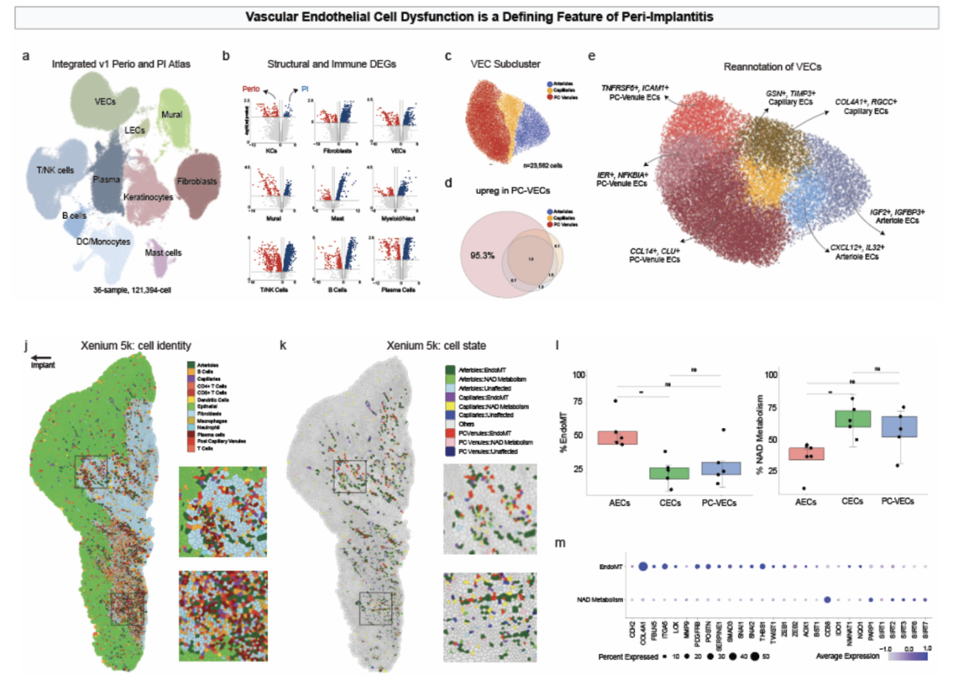
为了原位解析种植体周围炎的细胞空间互作关系,特别是分析表达 CD3 8的内皮细胞和其他细胞类型组成的空间生态位,研究者利用PCF空间单细胞蛋白组分析了健康、普通牙周炎和种植体周围炎,总共15例样本,通过检测32种抗体 ,定义了上皮、血管内皮、免疫细胞等的亚型和功能状态。
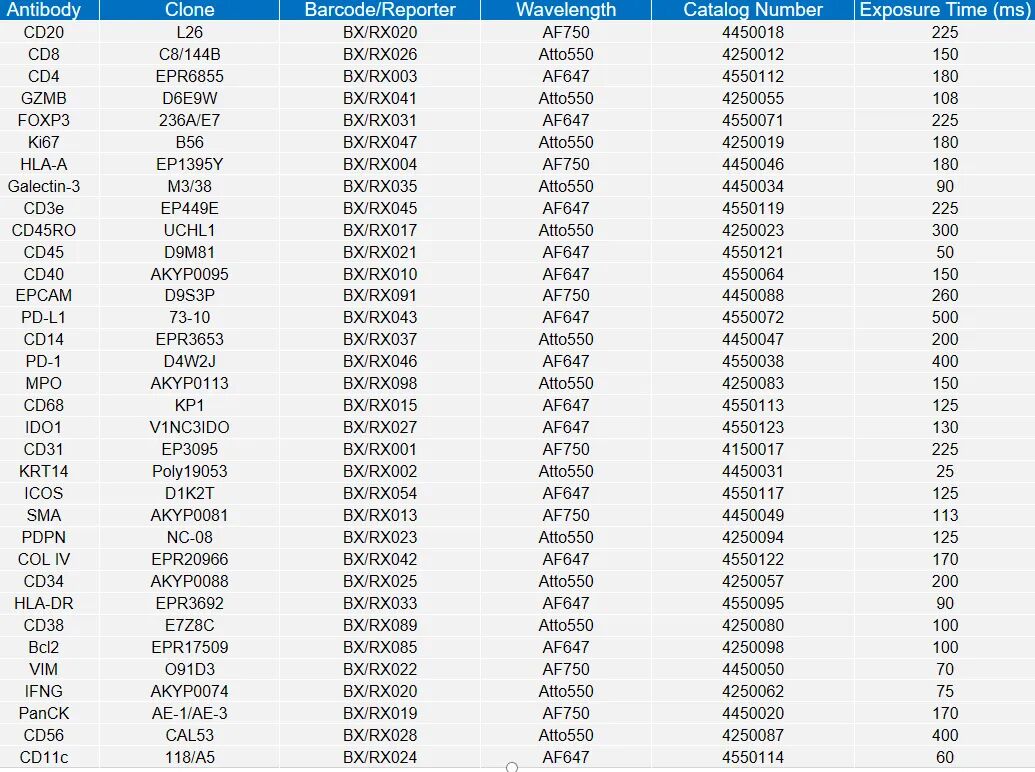
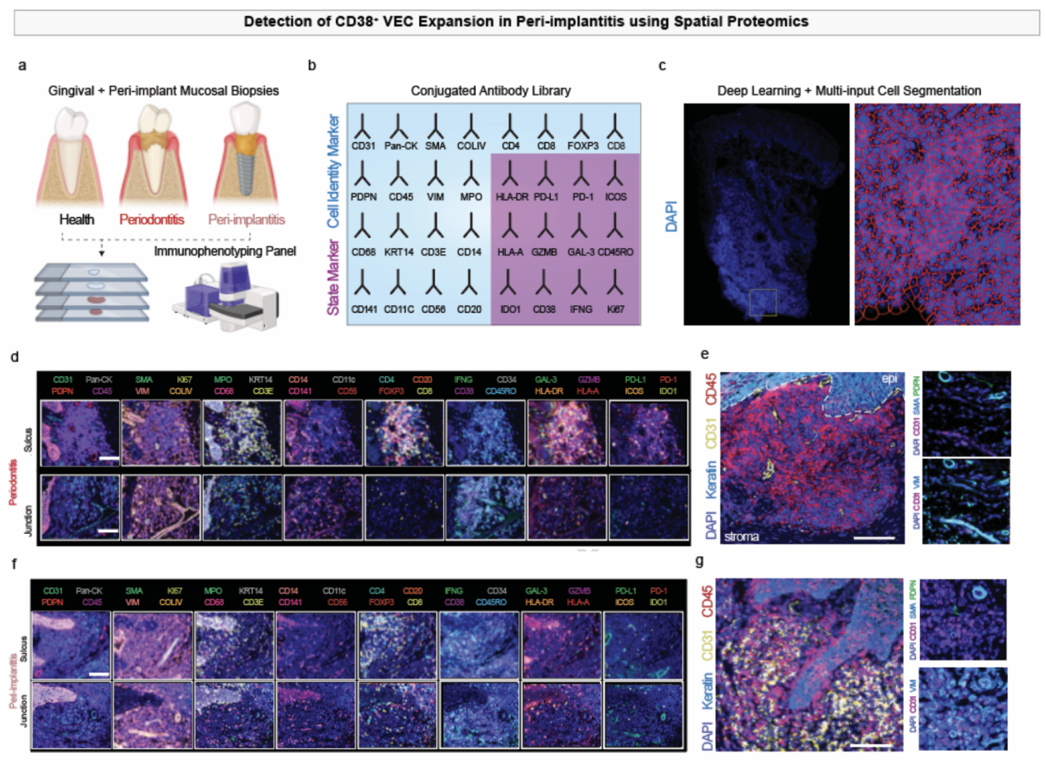
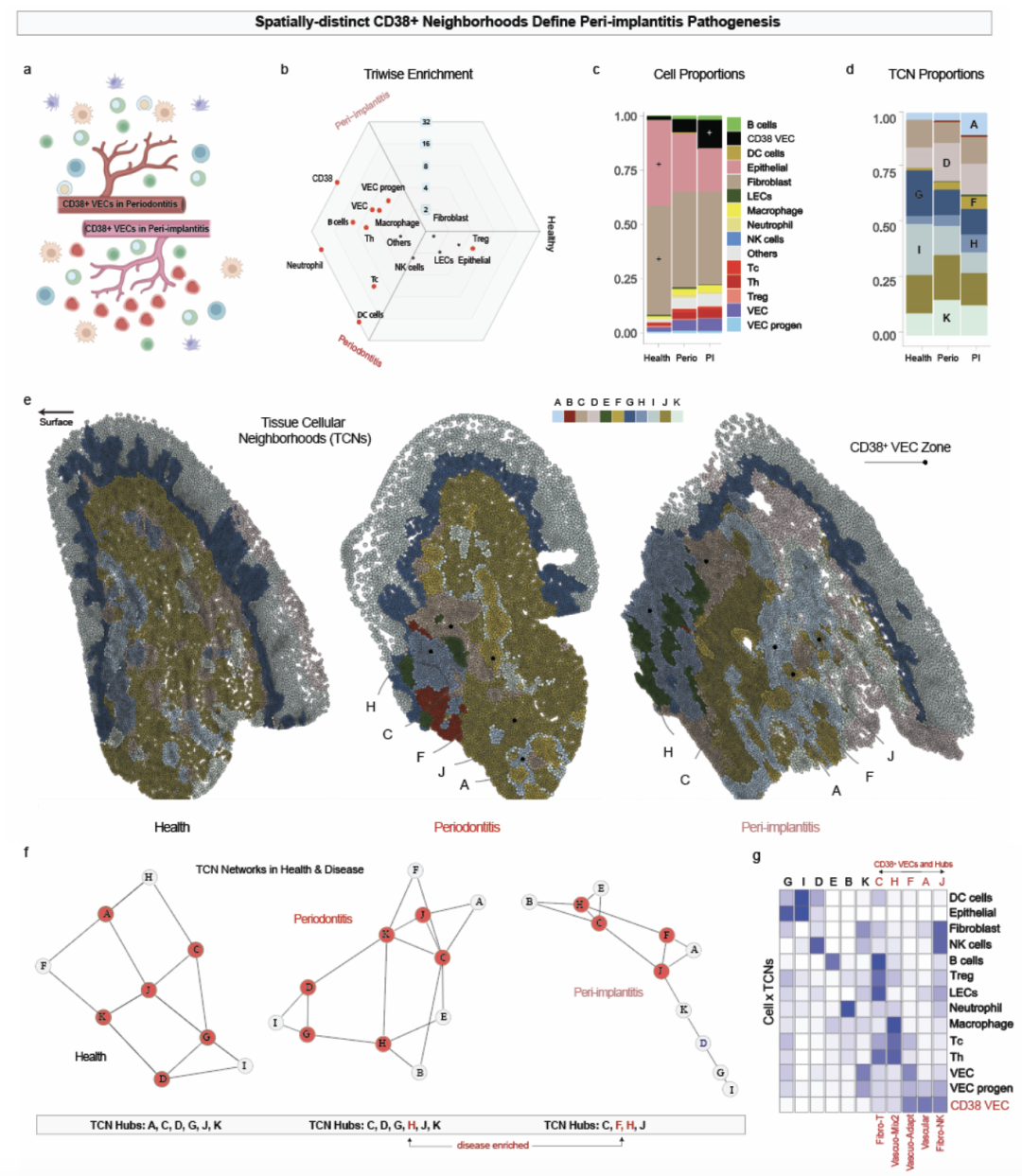
PCF空间单细胞蛋白组发现了,D38+内皮细胞的扩张和健康内皮细胞(CD34+)的耗竭,几乎是种植体周围炎独有的病理特征。细胞邻域分析揭示了这些病态的CD38+内皮细胞并没有孤立存在,而是与CD8+ T细胞、CD4+T细胞和巨噬细胞形成了极其紧密的空间生态位。
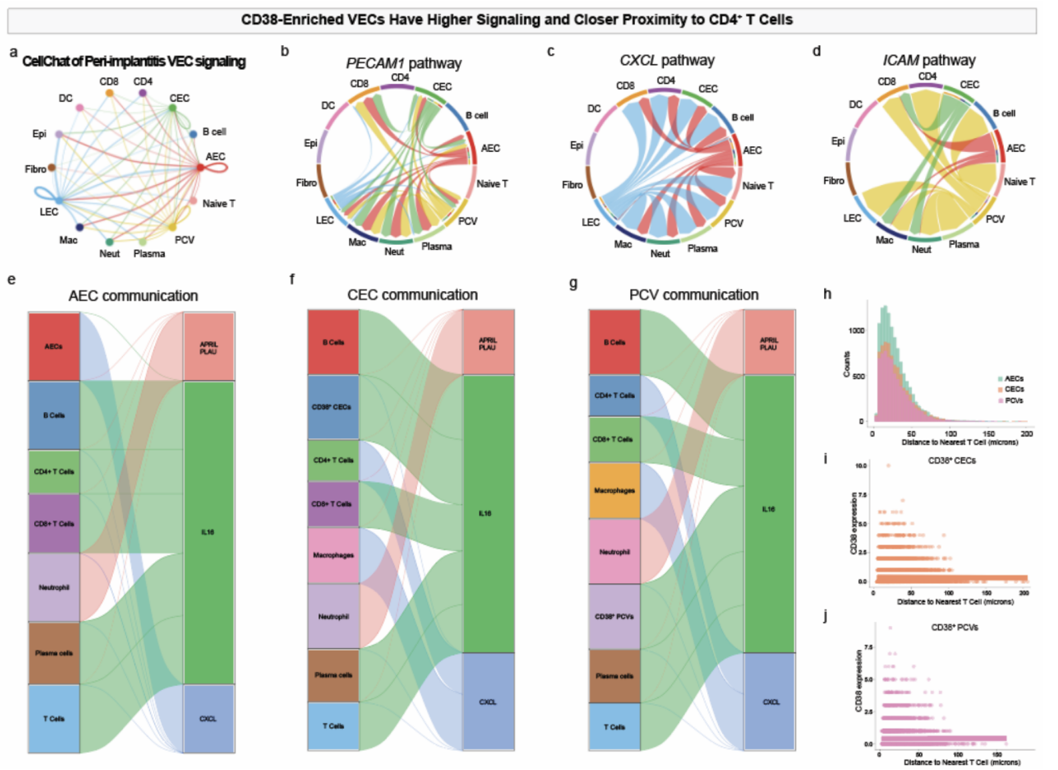
基于PCF空间单细胞蛋白组发现的空间互作关系,研究者又分析了Xenium空间转录组数据。通过受体-配体分析,揭示了高表达CD38的血管内皮细胞与相邻的CD4+ T细胞之间,存在着异常活跃的 IL-16 信号通路传导。
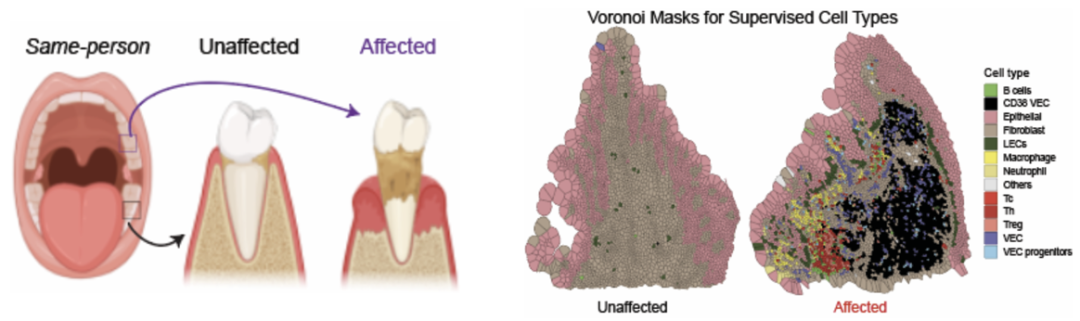
最后研究者也利用PCF空间单细胞蛋白组分析了重度牙周炎(Grade C)患者的患病部位和健康组织。结果发现了患病部位的细菌量并无显著差异,但同样出现了局灶性的 CD38+内皮细胞扩张,且空间排布模式与种植体周围炎类似。这些结果佐证了CD38介导的血管病变是快速进展性口腔炎症的通用底层原因。
总结与讨论
这项研究通过多维度的空间组学技术证明了快速破坏性牙周炎和种植体周围炎的真正引擎,是局部微血管的内皮细胞发生了代谢紊乱(NAD+耗竭与CD38上调),进而呈现出促炎的特征,通过物理拉近和细胞因子(如IL-16)招募免疫细胞,最终导致组织的快速崩解。这项研究也为药物开发提示了新的靶点。通过靶向CD38或补充NAD+前体,恢复内皮细胞的代谢稳态,阻断其对免疫细胞的异常招募,或许是阻断快速进展型口腔炎症的潜在策略。
| 参考文献
Easter, Q.T., Huynh, K.L.A., Stolf, C.S. et al. CD38⁺ endothelial remodeling marks spatially patterned vasculopathy in rapidly advancing periodontitis and peri-implantitis. Nat Commun (2026). https://doi.org/10.1038/s41467-026-72452-2