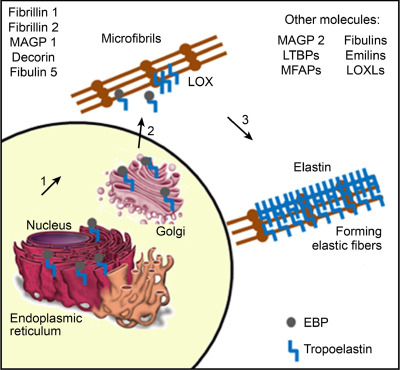
弹性蛋白(Elastin)是一类在生物体中广泛存在的重要结构蛋白,其特征在于具有优异的弹性与可逆伸缩能力。在重组蛋白表达体系中,重组弹性蛋白及其衍生形式(如弹性蛋白样多肽,Elastin-like Polypeptides, ELPs)因其独特的结构特性和理化行为,成为实验研究中常见的一类蛋白模型。
一、弹性蛋白的基本结构特征
天然弹性蛋白是一种高度疏水且富含重复序列的结构蛋白,其核心结构由多种短肽重复单元组成。典型序列通常以Val-Pro-Gly-Val-Gly(VPGVG)为基本重复单元,这一结构赋予其独特的柔性与弹性行为。
在重组表达体系中,弹性蛋白通常以模块化重复结构存在,不同重复次数与序列组合会直接影响蛋白的分子量、构象稳定性以及溶液行为。
从空间结构角度来看,弹性蛋白并不形成稳定的三级结构,而是以高度动态的无规卷曲(random coil)或部分有序结构存在,这种结构特征是其功能性质的基础。
二、重组弹性蛋白的序列特性
重组弹性蛋白最显著的特征在于其高度重复的氨基酸序列。这类序列通常具有以下特点:
富含疏水性氨基酸(如缬氨酸、脯氨酸)
含有甘氨酸,增加主链柔性
重复单元规则排列,形成周期性结构
这种序列设计使蛋白在水溶液中表现出独特的构象动态性,同时对温度、离子强度等环境因素具有敏感响应。
此外,不同氨基酸替换(如X位点变化)可改变蛋白整体亲水/疏水性质,从而影响其溶解性与相变行为。
三、弹性蛋白样多肽(ELP)的分子特性
弹性蛋白样多肽(ELP)是基于天然弹性蛋白重复序列设计的重组蛋白,其典型结构为(VPGXG)ₙ,其中X可为除脯氨酸外的任意氨基酸。
ELP最突出的特性是其可逆相变行为,即在特定温度(转变温度,Tt)以上发生从可溶状态向聚集状态的转变。这一现象源于分子内外疏水相互作用的变化。
从技术角度看,这种温度响应行为反映了蛋白分子在溶液中的构象变化及分子间作用力的动态平衡。
四、溶液行为与相变机制
重组弹性蛋白在溶液中的行为具有明显的环境依赖性。其核心机制可以归纳为"疏水作用驱动的可逆聚集":
在低温条件下,蛋白以可溶单体或小分子聚集体存在
温度升高时,疏水相互作用增强,导致蛋白分子发生聚集
当温度降低后,聚集体重新解离,恢复溶解状态
这一过程被称为"反向温度转变"(inverse temperature transition),是ELP类蛋白的典型特征。
此外,蛋白浓度、盐浓度及溶液pH等因素也会影响相变温度及聚集行为。
五、蛋白折叠与构象动态
与典型球状蛋白不同,重组弹性蛋白通常不形成稳定的紧密折叠结构,而是呈现高度柔性的构象。这种"无固定结构"状态使其在溶液中具有较大的构象自由度。
从分子层面来看,这种动态结构允许蛋白在不同环境条件下快速调整构象,从而实现可逆的物理变化。
同时,这类蛋白的折叠过程不依赖经典的折叠路径,而更接近于统计构象分布的变化过程。
六、分子间相互作用
重组弹性蛋白的聚集与解聚过程主要依赖以下几类相互作用:
疏水相互作用:驱动蛋白分子聚集
氢键作用:稳定局部结构
静电相互作用:影响分子间排斥或吸引
这些作用力在不同环境条件下表现出不同权重,从而决定蛋白在溶液中的状态。
例如,在高盐环境中,离子屏蔽效应会增强疏水作用,从而降低相变温度。
七、分子量与重复次数的影响
重组弹性蛋白的分子量通常由重复单元数量决定。随着重复次数增加,蛋白的整体性质会发生系统性变化:
分子量增加 → 聚集倾向增强
相变温度降低
溶液黏度增加
这种规律性变化使弹性蛋白成为研究蛋白质结构-功能关系的典型模型体系之一。
八、表达体系中的结构表现
在原核表达系统中,重组弹性蛋白通常表现出较好的可溶性,但其具体状态仍取决于序列设计与表达条件。
由于其结构较为柔性且缺乏复杂折叠需求,相较于多结构域蛋白,弹性蛋白更容易以可溶形式存在。然而,在高浓度或特定环境下,仍可能发生可逆或不可逆聚集。
从实验角度看,这类蛋白在表达体系中的表现,体现了序列特性与细胞环境之间的直接关系。
九、重组弹性蛋白的分子本质
综合来看,重组弹性蛋白的核心特征可归纳为:
高度重复的氨基酸序列
动态无规卷曲结构
温度依赖的可逆相变行为
以疏水相互作用为主导的分子间作用
这些特征共同决定了其在溶液中的行为模式,并构成其在实验体系中的基础性质。