在现代生命科学研究中,重组蛋白(Recombinant Protein)与抗体(Antibody)是两类基本的生物大分子工具。它们在分子结构、表达系统、功能特性与实验应用中存在显著差异。理解这些差异,有助于在实验设计、数据分析与试剂选择中做出更精准的技术判断。
一、基础概念与分子构成
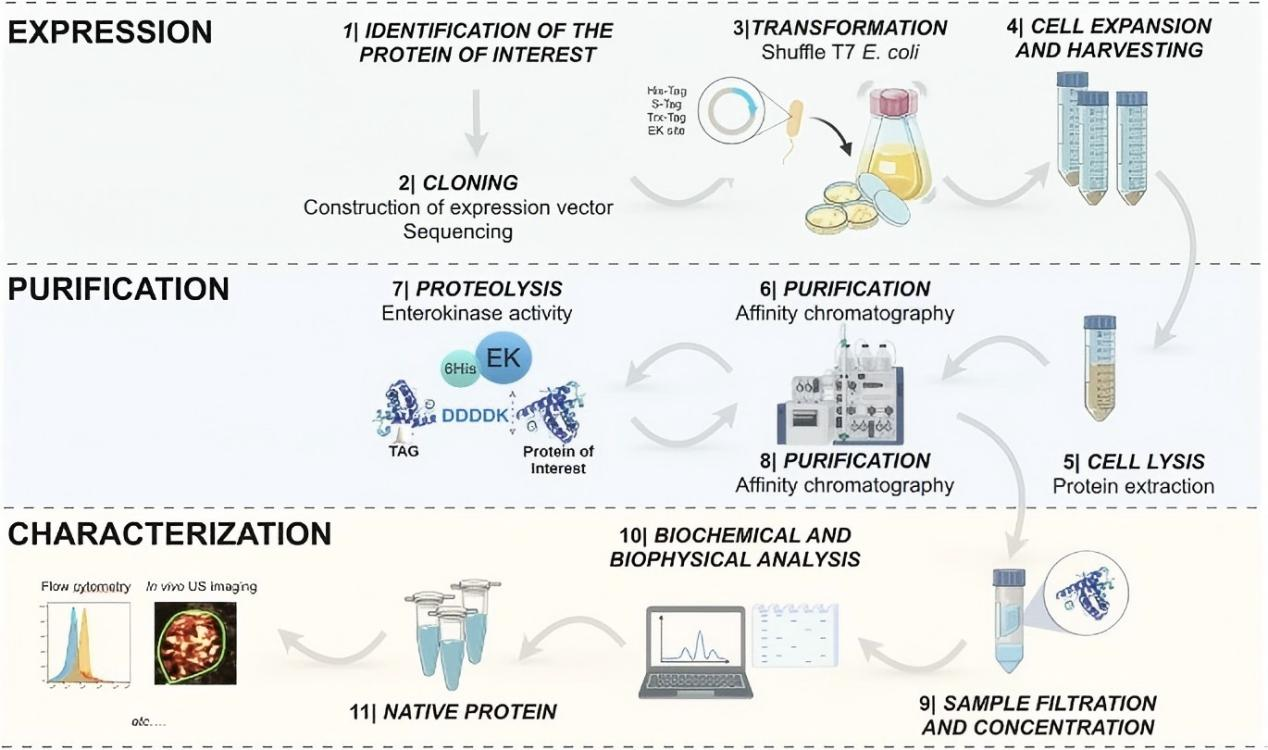
重组蛋白通常指通过基因工程技术获得的特定蛋白质,其氨基酸序列完全由目标基因编码。利用常见的蛋白表达系统,如原核表达、真核表达,可获得具有特定结构的目标蛋白。重组蛋白可包括酶、结构蛋白、信号分子或融合蛋白,常伴有标签以便于蛋白纯化与检测。
抗体是一类天然产生的免疫球蛋白分子(如 IgG、IgM),由两条重链和两条轻链通过二硫键连接构成。抗体具有高度的抗原结合特异性,可识别并结合特定的分子表位(Epitope),在免疫检测和分子识别中发挥核心作用。
二、分子结构差异
重组蛋白从结构上来讲可能是单链或多链,取决于目标蛋白的天然状态或构建设计。它们的三级结构受氨基酸顺序和后期折叠控制。在表达与分析中,重组蛋白的结构特点直接影响其可溶性蛋白比例与稳定性。
抗体结构则具有特定的恒定区(Fc)与可变区(Fab),其中可变区提供抗原识别功能,恒定区调节免疫效应。抗体天然的二硫键和重轻链构象,使其在体外与体内具有特有的稳定性与亲和特性。
三、表达系统及可溶性表达
重组蛋白的表达可根据实验需求选择不同系统。原核表达系统(如大肠杆菌)适合表达不需要复杂后期修饰的重组蛋白,表达速度快,成本低。真核表达系统(如酵母、昆虫细胞、哺乳细胞)适合表达需要糖基化修饰或复杂构象的蛋白。重组蛋白在表达过程中经常面对的技术考量是可溶性蛋白表达与合理的构象折叠,这直接关系到蛋白纯化效率与下游实验效果。
抗体分子由于本身的多链结构及糖基化要求,一般需在真核细胞系统中表达(如哺乳细胞系),以确保完整结构与高亲和性表位的形成。
四、蛋白纯化与标签策略
在重组蛋白表达后,常借助标签策略(如 6×His、GST、FLAG)以便在亲和层析中进行高效蛋白纯化。这些技术提高了目标蛋白的回收率与纯度,同时兼容下游结构分析、功能测定与比对实验。
抗体的纯化一般利用蛋白 A/G 亲和层析,结合抗原亲和柱进行选择性洗脱,以获得高纯度抗体。这种纯化策略基于抗体 Fc 或 Fab 与捕获介质的特异性结合特性。
五、功能与实验应用差异
重组蛋白在实验中常作为标准品、结构分析样品、功能性蛋白试剂或标签融合蛋白,用于信号通路研究、分子互动鉴定和定量比较。
抗体因其高特异性,可用于多种检测平台,例如 Western Blot 用于识别特定目标蛋白,免疫沉淀(IP)用于捕获蛋白复合物,免疫荧光和免疫组化(IHC)用于定位分子或细胞标记,以及 ELISA 用于定量检测抗原或抗体。
尽管两者在实验室应用中常相互配合,彼此的功能特征与技术定位却各自侧重不同。
六、抗原结合特异性与亲和力
重组蛋白本身不一定具有抗原识别能力,它通常作为实验对象或配合试剂用于结构和功能研究。抗体的核心功能则是识别和结合特定表位。这种高亲和力和高特异性是抗体技术的关键属性,使其成为免疫分析和分子检测的基础工具。
七、稳定性与储存条件
重组蛋白在不同的表达系统中可能具有不同的稳定性,例如在高盐或 pH 变化条件下其构象可能影响可溶性蛋白比例和聚集状态。常用分析方法如 SDS-PAGE、动态光散射(DLS)等用于评估蛋白状态。
抗体表现出相对较高的热稳定性和长期保存能力,在常用的储存缓冲体系中能维持其结合活性,使免疫实验更具可重复性。
八、实验输出与数据解读
在实验设计中,选择使用重组蛋白还是抗体取决于研究目的。若目的是研究蛋白本身的结构、活性或互作,则重组蛋白是直接对象;若目的是检测或定位特定蛋白,则抗体作为识别试剂是首选。理解两者技术特性,可以帮助研究者合理安排实验流程、优化参数设定,并明确数据解读的生物学意义。