01
文献学习

今天分享的文献是由复旦大学附属中山医院孙惠川、 徐彬团队联合 天津医科大学肿瘤医院宋天强、 上海交通大学医学院附属瑞金医院陈拥军教授等团队 于2026年2月26日在肝病学领域顶刊 《 Hepatology 》 (中科院1区top,IF=16.8) 上发表的研究"Deep learning-assisted tumor radiomic dynamics on MRI predict pathological complete response in HCC undergoing immune-based therapy followed by hepatectomy"即基于深度学习辅助MRI肿瘤影像组学动态变化预测接受免疫治疗序贯肝切除术的肝细胞癌患者的病理完全缓解,该研究旨在探索基于MRI影像组学特征的动态变化预测肝细胞癌(HCC)患者在接受免疫联合靶向治疗后行肝切除术前的病理完全缓解(pCR)。研究构建了基于基线、术前和"delta"(变化)影像组学特征的多种机器学习模型,并验证其预测性能。结果显示,delta影像组学模型显著优于传统影像评估方法,结合AFP动态变化后预测能力进一步提升。该研究为术前无创评估pCR提供了新工具。
创新点:①首次构建基于多时点MRI的影像组学动力学模型 ,动态捕捉肿瘤对免疫治疗的演变过程。②结合血清AFP动态变化与影像组学特征 ,构建双模态融合模型,显著提升pCR预测准确性。③引入病灶级与患者级分层分析策略,解决多灶性HCC异质性对疗效评估的干扰。
临床价值:①实现术前无创预测pCR ,避免依赖术后病理,为手术时机和策略提供依据。②识别转化治疗中获益最大的患者 ,助力个体化治疗决策,避免不必要手术。③模型结合影像与血清指标,提升疗效评估全面性,适用于多中心推广。
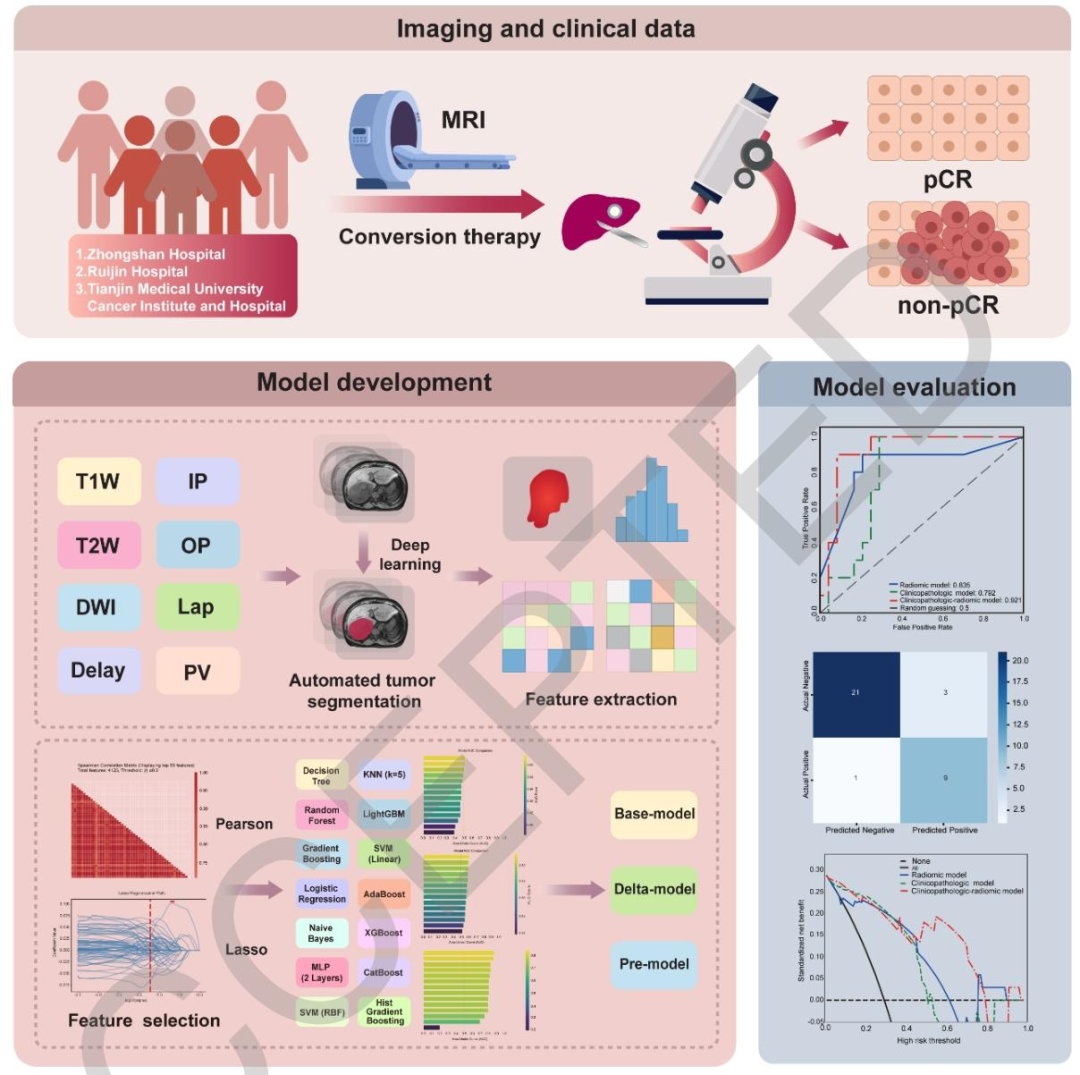
图 1:研究整体流程图
①数据收集阶段 :纳入影像数据 (MRI多序列:T1WI同相位IP、T2WI反相位OP、DWI弥散加权、门脉期PV、延迟期Delay等)+临床结局数据(pCR/non-pCR分组),并标注研究对象为接受转化治疗后行肝切除术的HCC患者;
②影像处理阶段 :对MRI影像进行自动化肿瘤分割 (AI算法)→定量特征提取(影像组学特征,含纹理、形状、一阶统计量等);
③模型构建与评估阶段 :通过Pearson相关性分析、LASSO回归进行特征筛选,最终构建三类影像组学模型(Base-model基线模型、Delta-model动态变化模型、Pre-model术前模型),并完成模型训练与效能评估。
02
研究背景和目的
研究背景
肝细胞癌(HCC)是全球范围内发病率位居第六、癌症相关死亡原因位居第三的恶性肿瘤,严重威胁人类健康。对于早期HCC患者,手术切除是主要的根治性手段,但临床上面临的严峻挑战是,超过70%的患者在初诊时已处于中晚期,失去了直接手术切除的机会 。近年来,以靶向治疗(如酪氨酸激酶抑制剂)联合免疫治疗(如PD-1/PD-L1抑制剂)为基础,并结合肝动脉化疗栓塞(TACE)或肝动脉灌注化疗(HAIC)等局部治疗手段的转化治疗方案取得了显著进展,使得部分初始不可切除的HCC患者获得了降期后手术的机会。在此背景下,病理学完全缓解(pCR)成为评估转化疗效的核心指标 ,研究表明,达到pCR的患者术后无进展生存期和总生存期显著优于未达到pCR的患者。然而,pCR的明确诊断目前完全依赖于术后对切除标本的病理学评估,在术前无法获知。现有的影像学评估方法,如基于单一参数(强化程度)的mRECIST标准,难以全面捕捉肿瘤内在的异质性及治疗过程中的动态演变,导致影像学评估与病理学反应之间存在显著偏差。因此,临床上迫切需要一种能够在术前无创、精准地预测pCR的工具,以弥补现有评估手段的不足。影像组学作为一种能从医学影像中高通量提取人眼无法识别的定量特征,并结合人工智能算法进行深度分析的新技术,为全面量化肿瘤微环境的时空异质性、动态监测治疗反应提供了可能,为攻克这一临床难题开辟了新的方向。
研究目的
本研究的主要目的是开发并验证一种基于多序列MRI的动态影像组学模型,用于在术前预测初始不可切除的肝细胞癌(uHCC)患者在接受免疫联合靶向为基础的转化治疗后,能否达到病理学完全缓解(pCR) 。研究团队旨在通过整合患者在基线和术前两个时间点的多序列MRI影像数据,提取并筛选出能够稳定反映肿瘤治疗响应动态变化的影像组学特征(特别是变化量"delta"特征 ),结合血清肿瘤标志物(如AFP)的动态变化,运用多种机器学习算法构建和优化预测模型。研究的核心目标在于:第一,系统性比较基线模型、术前模型和delta动态模型在预测pCR性能上的优劣 ,验证捕捉肿瘤动态演变特征的增量价值;第二,探究影像组学特征与血清AFP动态反应(AFP response)在预测效能上的协同作用 ,构建融合影像与血清标志物的双模态联合预测模型,以期达到最高的预测精度;第三,在病灶层面和患者层面分别验证模型的预测能力 ,尤其针对多发性HCC患者,解决肿瘤异质性带来的评估难题。最终,本研究旨在提供一种无创、精准、可解释的术前评估工具,用以辅助临床医生甄别出能从转化治疗中获得最大病理学获益的患者,从而为后续的个体化治疗决策(如手术时机的选择、手术方式的优化,乃至未来探索"观察等待"策略的可行性)提供强有力的数据支持和科学依据。
03
数据和方法
研究数据
总样本量: 154例患者(159个病灶)
训练集:78例(中山医院)
内部测试集:32例(中山医院)
外部验证集:44例(天津肿瘤医院、瑞金医院)
**数据来源:**三家三甲医院(2019--2025年)
**影像数据:**多序列MRI(T2WI、DWI、T1WI、动脉期、门脉期、延迟期等)
临床数据: AFP、PIVKA-II、肝功能、治疗方案等
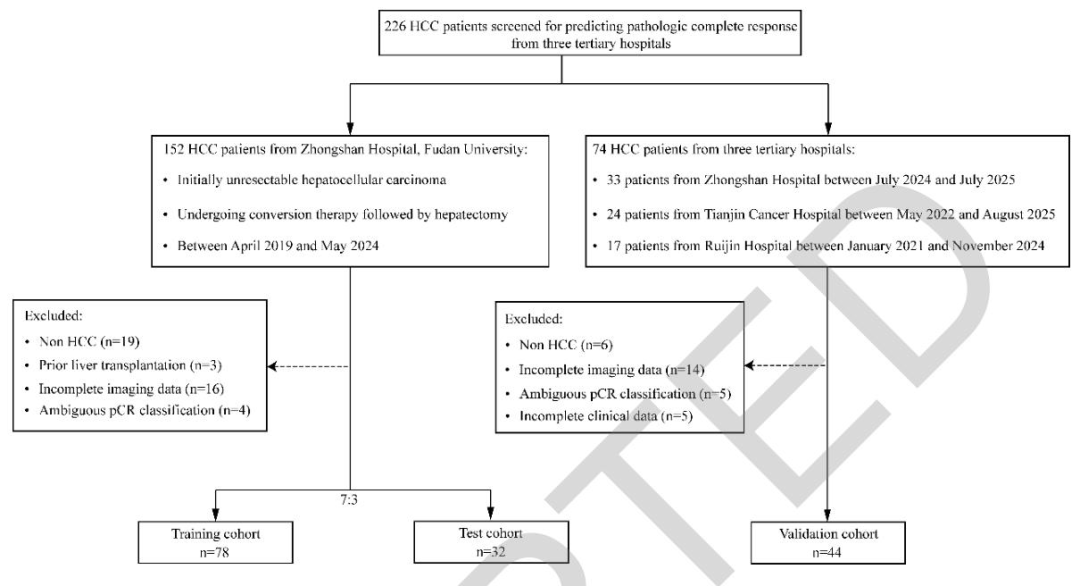
图 2:患者纳入与分组流程图
技术方法
**数据预处理:**图像配准、归一化、N4偏置场校正
肿瘤分割: AI自动分割 + nnU-Net辅助,ICC筛选高重复性特征
特征提取: PyRadiomics提取2264个特征(一阶、形状、纹理等)
特征筛选: ICC、t检验、LASSO、随机森林
模型构建: 14种机器学习模型对比,最终选择MLP
模型评估: AUC、准确性、敏感性、特异性、PPV、NPV、校准曲线、DCA
AFP动态定义: log10(术前AFP)/log10(基线AFP)
04
实验结果
**pCR率:**训练集32.1%,测试集31.2%,验证集45.5%
AFP动态: pCR患者AFP下降更显著(p < 0.05)
delta影像组学模型显著优于传统模型:
测试集AUC:0.835 vs 基线0.483 / 术前0.685
验证集AUC:0.783 vs 基线0.434 / 术前0.506
结合AFP后预测性能进一步提升:
测试集AUC:0.920,验证集AUC:0.857
SHAP分析: AFP响应和影像组学评分为最重要预测因子
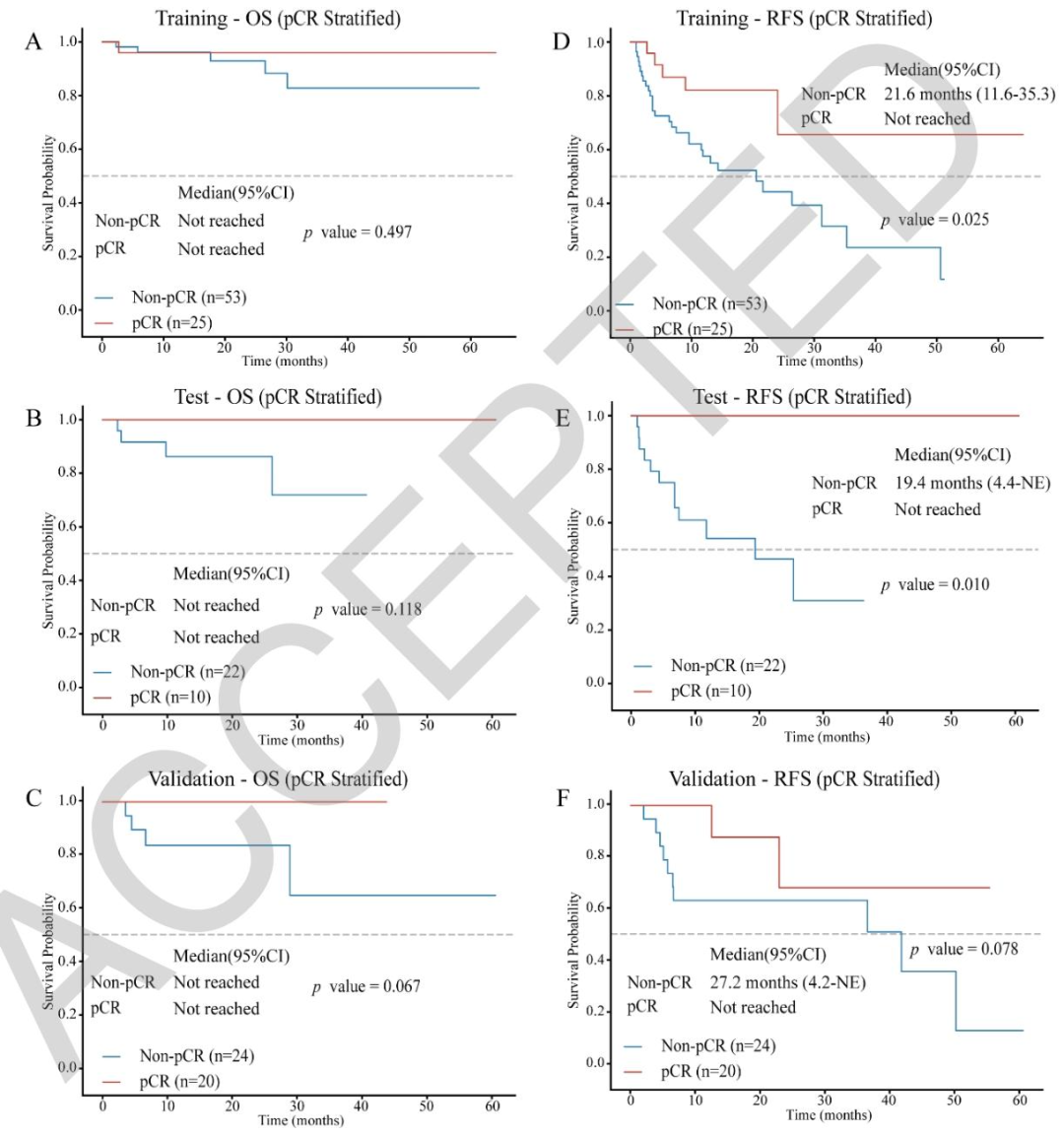
图 3:不同患者队列按pCR状态分层的生存分析图
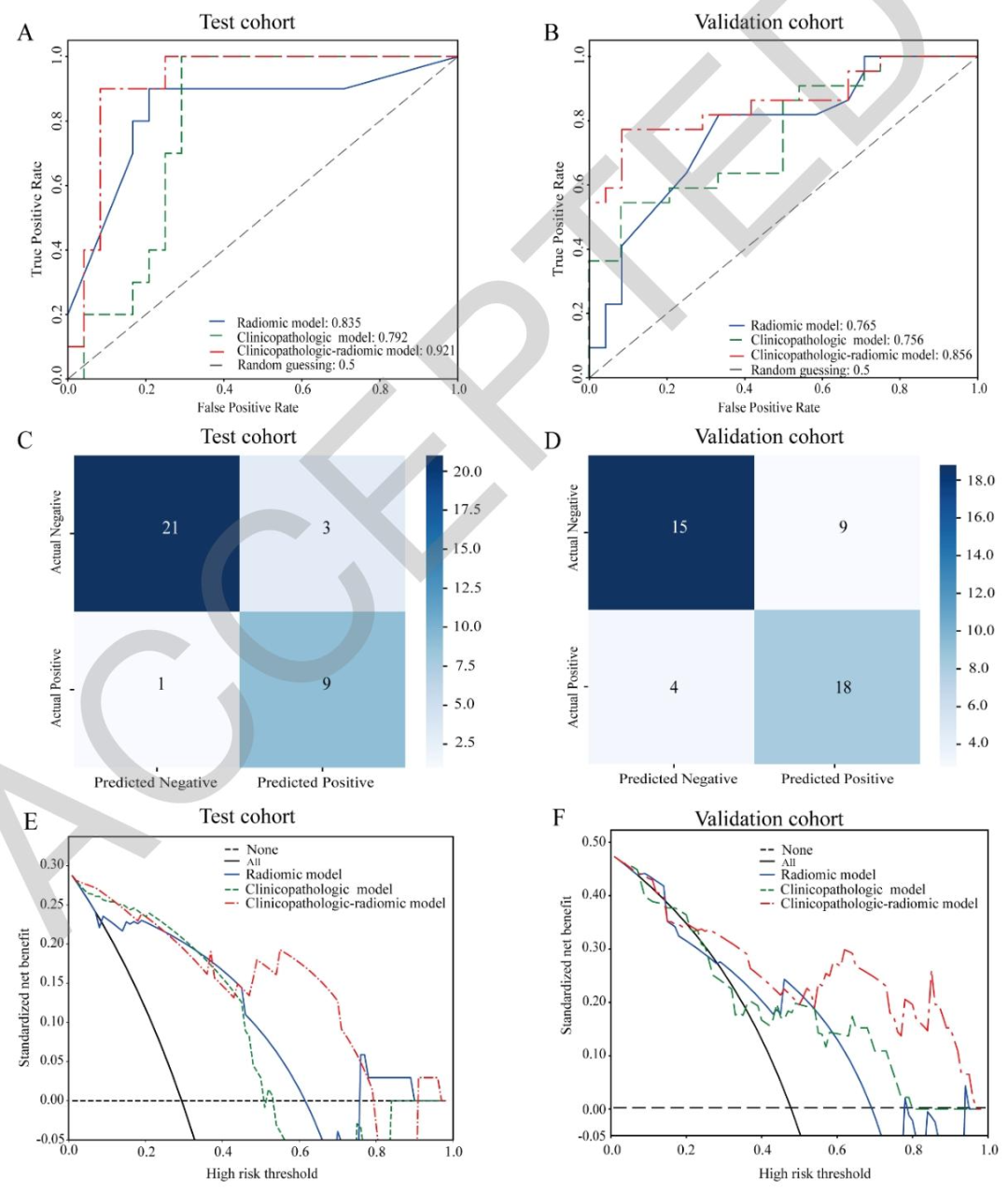
图 4:整合临床-影像组学联合模型的效能评估图
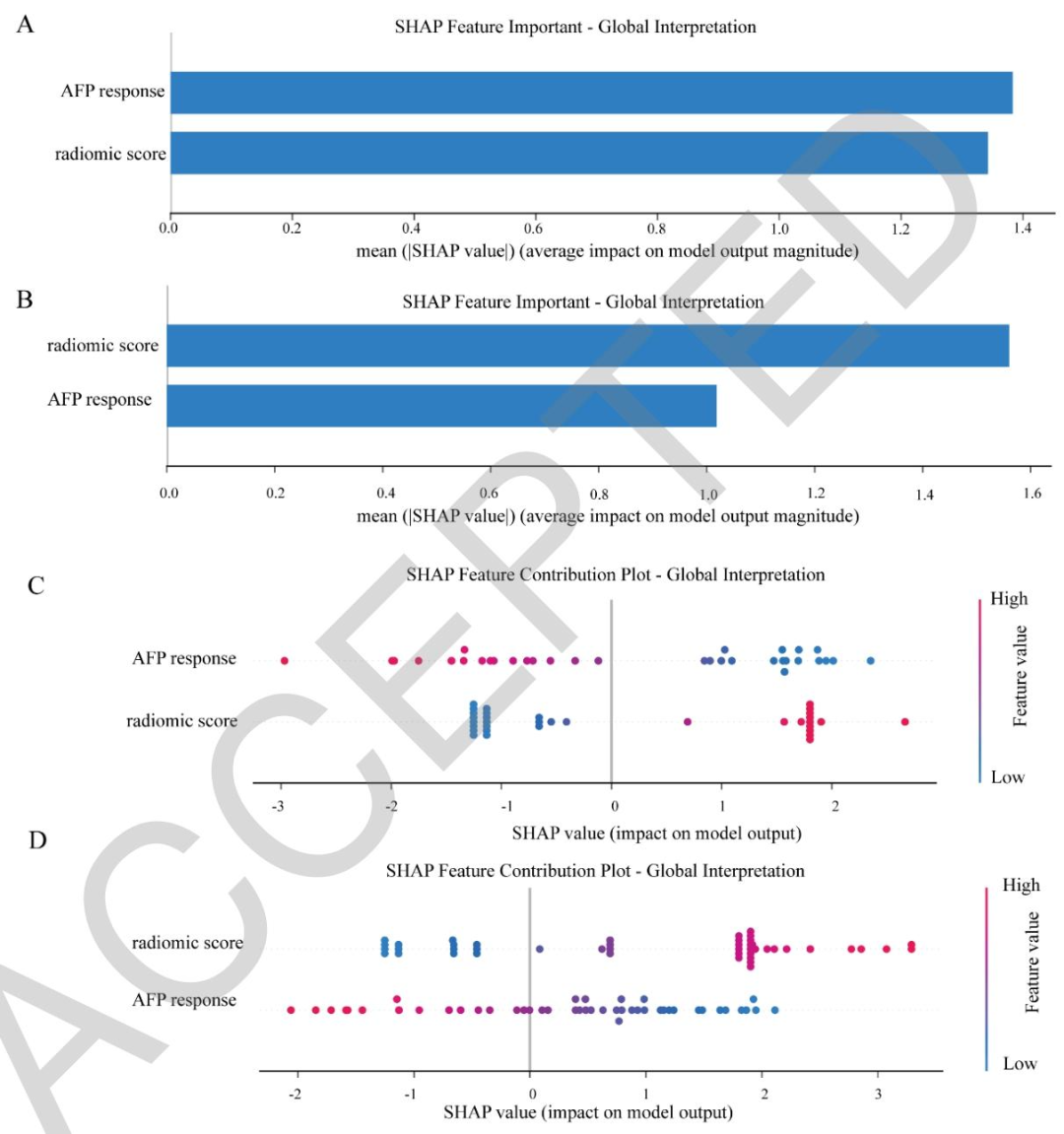
图 5:联合模型的SHAP分析图
05
研究结论
该论文通过多中心回顾性研究,首次构建并验证了基于MRI的影像组学-临床融合模型 ,用于预测初始不可切除肝细胞癌(uHCC)患者在接受免疫联合靶向治疗后、手术前的病理完全缓解(pCR) 。研究发现,相较于单一的基线或术前影像模型,动态变化影像组学(delta radiomics)模型能更准确地捕捉治疗过程中的肿瘤异质性演变 ,在测试集和验证集中预测病灶水平pCR的AUC分别达到0.835和0.783,显著优于传统mRECIST评估标准。进一步将动态影像组学特征与血清AFP对数比值(AFP response)相结合 ,构建的联合模型在预测患者水平pCR时表现最优,测试集AUC高达0.920,验证集为0.857,校准度和临床净获益均良好。SHAP分析显示,AFP反应与影像组学评分是贡献最大的预测因子。该研究证实,动态影像组学联合血清生物标志物可无创、精准地评估转化治疗后的pCR,为筛选可能避免手术或实施"等待观察"策略的极佳响应者提供了可靠工具,具有指导个体化治疗的潜力。
参考文献:Zhou SQ, Wang LN, Wu LF, Sun LY, Yang YC, Yang ZY, Wang ZY, He T, Li F, Chen LL, Li H, Zhu XD, Shen YH, Huang C, Ji Y, Gao Q, Zhou J, Jia F, Chen YJ, Song TQ, Xu B, Sun HC. Deep learning-assisted tumor radiomic dynamics on MRI predict pathological complete response in HCC undergoing immune-based therapy followed by hepatectomy. Hepatology. 2026 Feb 26. doi: 10.1097/HEP.0000000000001724.