在诱导多能干细胞(iPSC)研究中,从体细胞重编程到规模化生产,涉及多个关键技术环节,包括重编程、培养扩增、基因编辑、定向分化及最终产业化应用等。本文对iPSC全流程进行系统梳理,帮助理解各环节核心技术要点。 :contentReferenceoaicite:0{index=0}
一、重编程
在iPSC研究中,重编程是实现体细胞向iPSC转化的核心步骤。通过导入关键转录因子或结合小分子调控,可逆转体细胞分化命运,激活多能性基因表达。
经典Yamanaka四因子包括:
- Oct4
- Sox2
- Klf4
- c-Myc
此外,Nanog、Lin28等因子也可辅助提升重编程效率。
目前重编程技术主要分为:
1. 整合型方法
- 逆转录病毒
- 慢病毒
优点:效率高
缺点:存在基因组插入风险
2. 非整合型方法(主流)
- mRNA转染
- 仙台病毒
- 游离质粒
特点:
- 无基因组整合
- 安全性更高
- 更适合临床应用
二、培养扩增
iPSC维持培养依赖稳定的培养体系,包括培养基、细胞因子和基质材料等。
关键影响因素
- 细胞多能性维持
- 基因组稳定性
- 扩增效率
- 批次一致性
常见培养要素
- FGF-2(bFGF)
- TGF-β1
- 无动物源培养体系
培养基质
层粘连蛋白(如LN521)常用于iPSC培养,可提供更接近体内环境的生长条件:
- 支持干性维持
- 提高扩增效率
- 适配2D/3D培养体系
三、细胞解离与传代
iPSC扩增过程中,细胞解离方式对状态影响较大:
常见方法
- 胰蛋白酶/EDTA(贴壁细胞)
- 温和酶解(球体解离)
关键点
- 降低细胞损伤
- 保持多能性
- 提高存活率

四、基因编辑
基因编辑技术可用于构建疾病模型或功能研究:
- CRISPR-Cas9
- 转基因技术
- 突变模型构建
- 基因表达调控
应用包括:
- 遗传病研究
- 药物筛选
- 功能验证
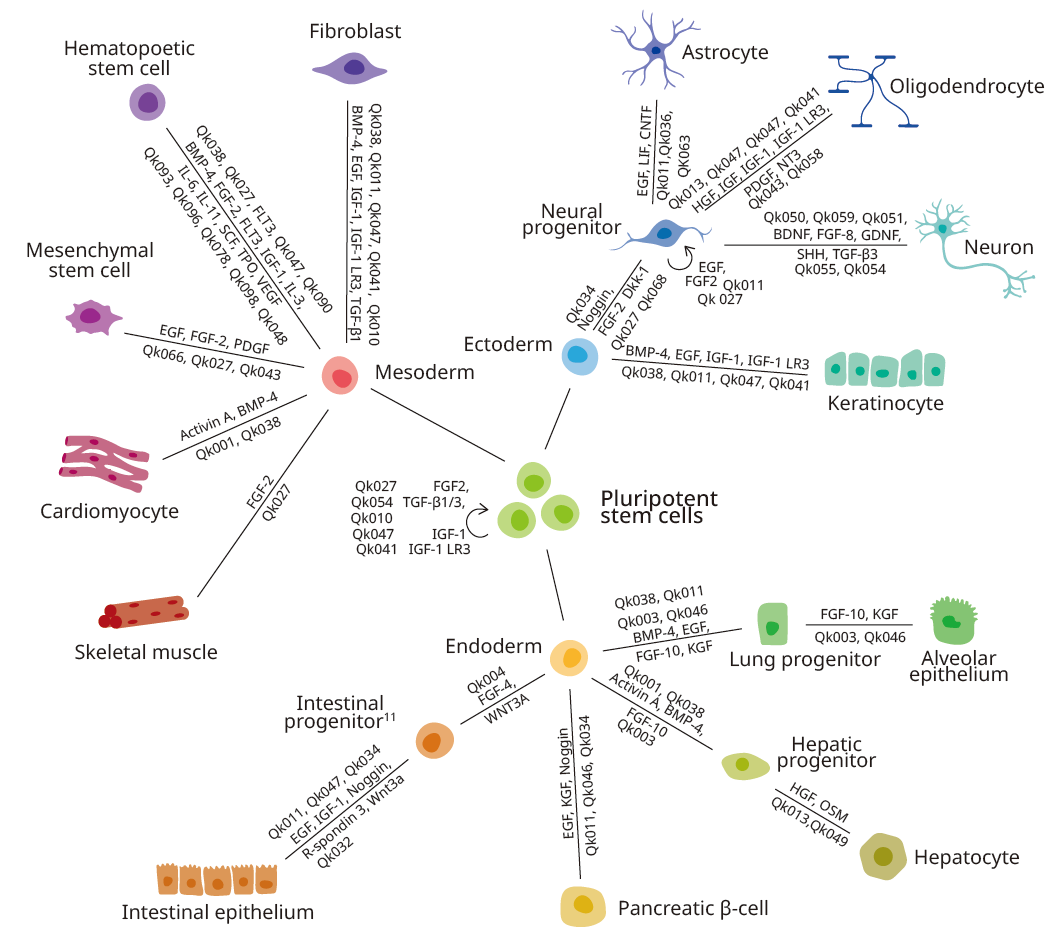
五、定向分化
iPSC可分化为多种功能细胞:
- 神经细胞
- 心肌细胞
- 肝细胞
- 胰岛细胞
分化依赖:
- 生长因子组合
- 小分子调控
- 信号通路调节
六、细胞表征
iPSC质量评估包括:
- 三胚层分化能力
- 多能性标志物检测
- 流式分析
- 免疫荧光
七、工艺开发(规模化培养)
iPSC产业化依赖生物反应器系统:
特点:
- 可放大生产
- 控制剪切力
- 保持细胞一致性

八、制剂与灌装
细胞治疗产品需要满足:
- GMP规范
- 无菌操作
- 高一致性
关键设备包括:
- 自动化灌装系统
- 冻存容器
九、保存与运输
细胞保存面临挑战:
- 冻存损伤
- 冷链成本
新技术趋势:
- 常温保存
- 水凝胶封装
- 提高细胞活性保持

FAQ(提高CSDN通过率关键模块)
Q1:iPSC与ESC的主要区别?
A:iPSC来源于体细胞重编程,而ESC来源于胚胎。
Q2:为什么非整合技术更受欢迎?
A:避免基因组突变风险,更适合临床应用。
Q3:培养过程中最容易出问题的环节?
A:解离和传代阶段,容易影响细胞活性。
Q4:iPSC可以分化成哪些细胞?
A:几乎所有体细胞类型,如神经、心肌、肝细胞等。
Q5:产业化最大挑战是什么?
A:批次一致性和规模化生产能力。
延伸阅读
https://www.mine-bio.com/iPSC/?utm_source=csdn\&utm_medium=referral\&utm_campaign=ipsc_article
本文基于iPSC相关公开资料由其中国提供商上海曼博生物整理,仅用于科研信息分享。上海曼博生物可提供iPSC诱导多能干细胞培养体系、生长因子及相关解决方案产品,支持干细胞研究与细胞治疗应用。