抗生素滥用导致多重耐药微生物在全球蔓延,但新型抗生素的研发进展缓慢,亟需找到替代抗生素的新型防御策略。抗菌肽(AMPs)作为天然防御分子,具有低耐药潜力和广谱活性。德国小蠊(Blattella germanica)生活方式较为复杂,作为携带多种病原体的昆虫,其肠道微生物组为挖掘新型AMPs提供了独特资源。
2024年Microbiome一篇文章通过跨学科策略揭示了昆虫共生微生物中AMPs的医学潜力,为抗感染药物开发提供了新方向。

期刊:Microbiome
影响因子:15.1
发表时间:2024
1、研究背景
AMP是一类进化形成的大分子,通过破坏细菌细胞膜实现抗菌作用,但AMPs本身临床应用较为困难,需要评估其在体内稳定性及潜在的毒性影响。哺乳动物或昆虫在进化的过程中,肠道微生物群落可能会编码高度选择性的AMP来对抗病原微生物,而不会对宿主造成细胞毒性。
2、研究背景
研究设计开发了深度学习工具"AMPIdentifier",并基于该工具分析了B. germanica的6个生长阶段的12个样本的肠道微生物组数据,从结果中筛选抗菌肽进行体外实验验证。
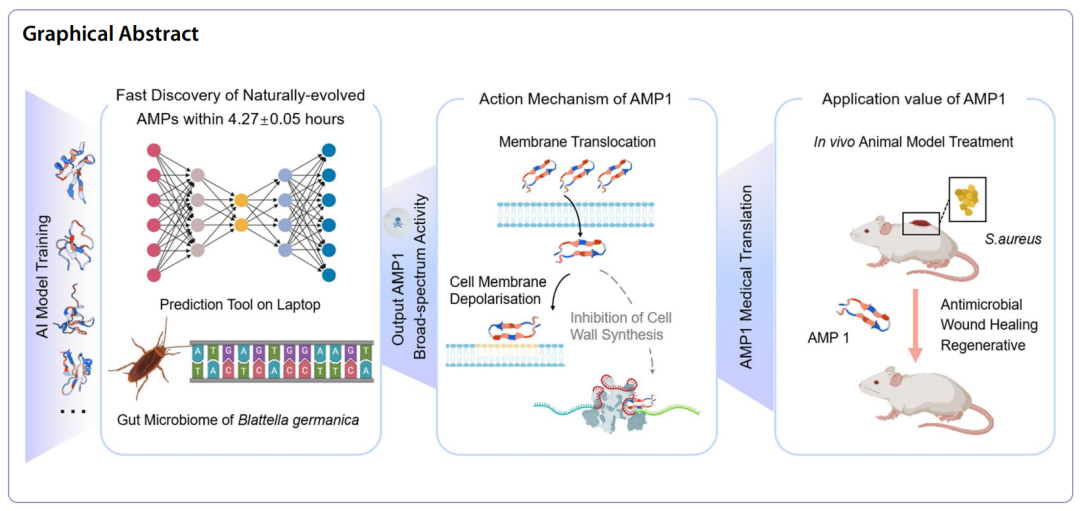
3、主要结果
(1)来自蟑螂肠道微生物群的潜在AMP
研究基于深度人工学习策略开发的AMPidentifier工具,对德国小蠊肠道微生物进行AMP预测,共获得565,655个潜在肽,其中79种肽被预测为潜在抗菌肽。最终筛选了5种肽用于进一步实验验证。
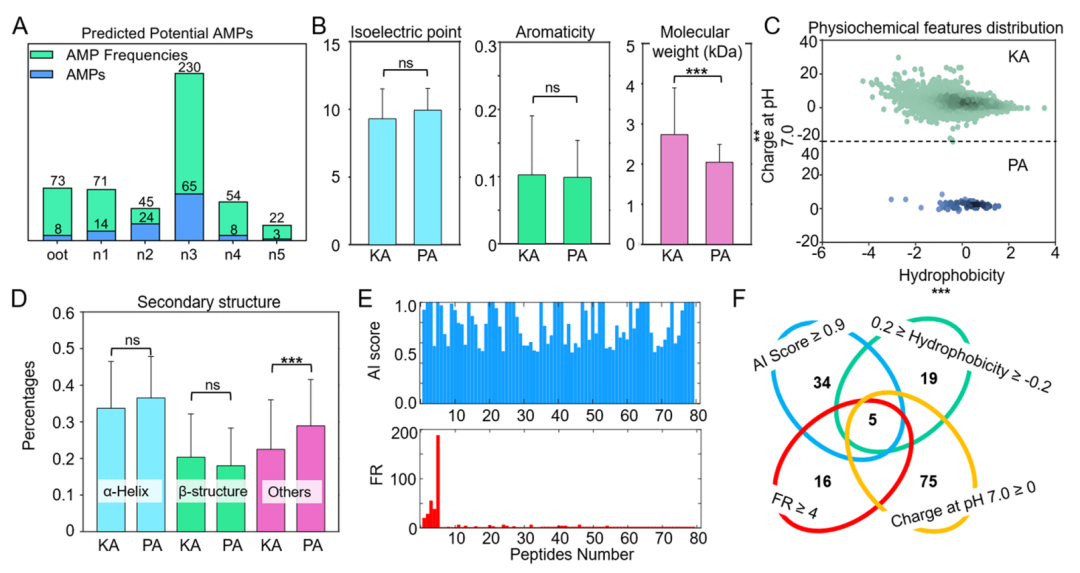
图1.软件预测及AMP筛选
(2)潜在抗菌活性AMP的体外验证
针对上一步获得的5个AMP进行体外验证,发现其中AMP1具有广谱抗菌活性,对枯草杆菌23 857、金黄色葡萄球菌6538和大肠杆菌25404有显著效果。此外AMP1具有低毒性,在100uM的浓度下,哺乳动物C2C12细胞的平均存活率为87.0±8.4%。
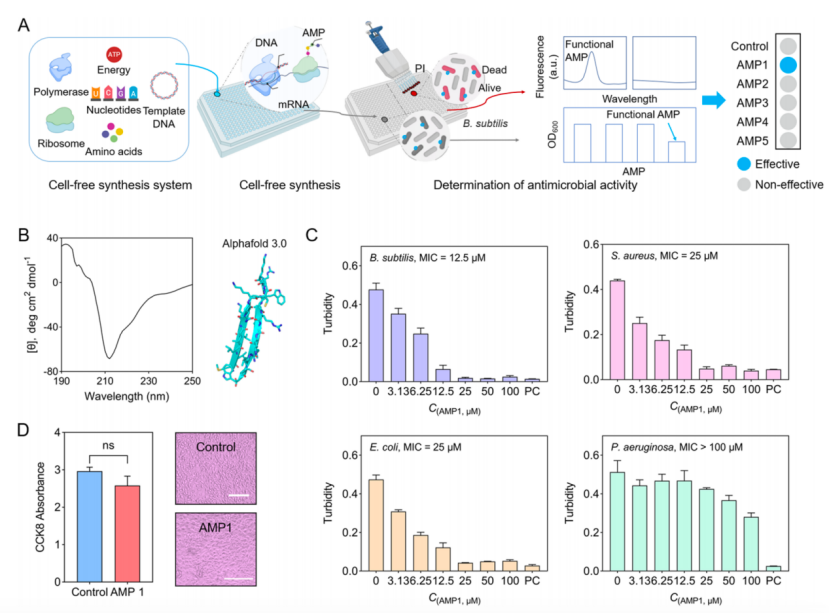
图2 体外验证AMP抗菌效果及细胞毒性
(3)AMP1的抗菌机制
研究结合共聚焦显微镜观察AMP1的抗菌机制,发现AMP1可以在1分钟内迅速渗透到细胞中,并随着时间的推移在细胞内逐渐积累。结合扫描电镜发现AMP1可能具有抑制细胞壁合成的细胞内靶点,此外还会导致膜去极化。同时还发现AMP1携带两个Trp残基,这一基团可能与AMP1稳定性和抗菌效力有关。
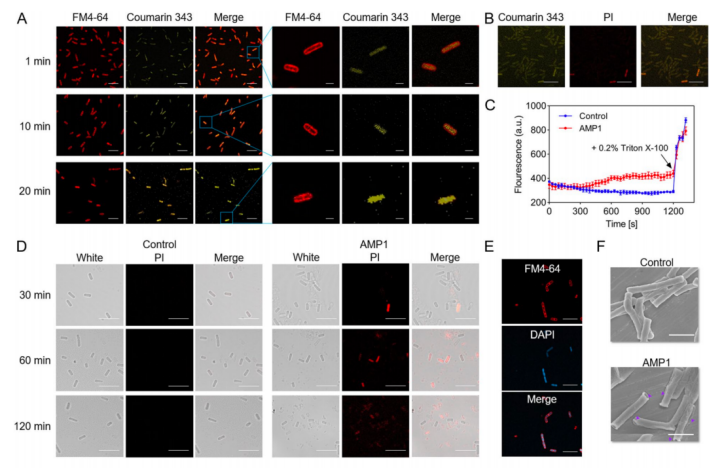
图3 AMP1的作用机制
(4)动物实验验证
动物模型中,AMP1显著促进金黄色葡萄球菌感染伤口的愈合,疗效媲美万古霉素。这一点和以往研究相同,AMP在体内能够利用免疫调节和组织再生功能,抗菌效果比体外更好。
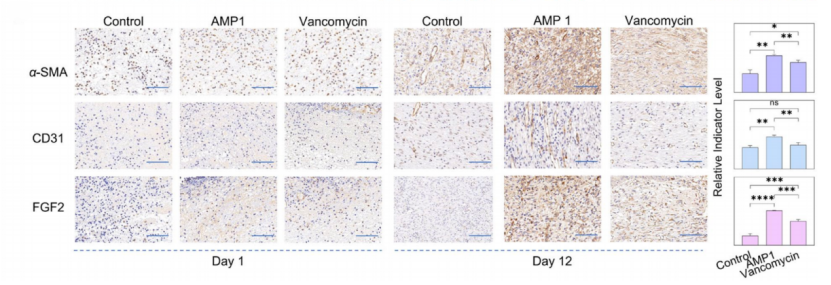
图4 动物模型抗菌效果
3、研究总结
本研究开发并展示了通过软件从微生物组数据中挖掘新型AMPs的可能性,为抗菌药物研发带来了新的方向。但挖掘出的AMP作用机制、稳定性及分子靶点仍需要进一步探讨及优化,探索其在更复杂动物模型中的应用。
利用现有的肠道和环境宏基因组数据进行AMP挖掘,可以抗菌药物研发带来了新的方向。凌恩生物新推出基于宏基因组的AMP分析,根据 Cell 论文(doi:10.1016/j.cell.2024.05.013)的方法,进行AMPs 的鉴定并分析AMP在宏样本中的分布、丰度。感兴趣的老师快来联xi吧~
参考文献
Chen, S., Qi, H., Zhu, X. et al. Screening and identification of antimicrobial peptides from the gut microbiome of cockroach Blattella germanica. Microbiome 12, 272 (2024). https://doi.org/10.1186/s40168-024-01985-9