我国对医疗器械的监管体系建立在严格的风险分级管理 原则之上。根据《医疗器械监督管理条例》及相关法规,医疗器械的管理类别是依据其风险程度由低到高,依次划分为第一类(I) 、第二类(II) 和第三类(III)。风险程度是判定分类的基础,确保监管要求与产品可能对人体造成的危害相匹配。
制定医疗器械分类目录的核心依据在于产品的使用风险。分类的判定遵循国家药品监督管理局(NMPA)颁布的《医疗器械分类规则》(NMPA令第15号) 指导下的目录分类制度。在分类实践中,NMPA参照国际通行的分类标准,但明确要求必须"从严掌握"。这一原则意味着,在分类存在不确定性时,监管机构通常倾向于采取风险程度更高的分类,以最大限度地保障公众健康和安全。
分类等级的划分,直接决定了监管机构对资源的分配和管理力度的侧重。对风险等级最高的第三类医疗器械,国家药品监督管理局(NMPA)实行集中、严格的国家级注册管理,并且强制要求实施医疗器械唯一标识(UDI)制度。相反,风险较低的第一类医疗器械则仅需在省级药品监督管理部门进行备案。
这种分级管理体系是监管资源有效利用的关键策略。通过将最严格的审批和上市后监管资源集中于III类器械,例如要求其生产、流通、使用全流程可追溯,监管机构能够有效控制植入人体、支持生命或具有潜在严重危险的器械。因此,分类等级不仅是风险的标签,也是监管深度和资源投入的决定性因素。
医疗器械三类划分的风险定义与区别判定
医疗器械分类的核心在于其对人体可能造成的伤害程度,以及为保证其安全有效性所需采取的控制措施。
A. 第一类医疗器械(I类:低风险)
第一类医疗器械是指通过常规管理足以保证其安全性、有效性的医疗器械。这类器械通常结构简单、功能单一,不与人体深度接触或只做暂时性接触,风险等级最低。
典型案例: I类医疗器械的实例包括听诊器、灌肠套件、乳胶手套、绷带、床上用品、外科口罩和灌注牙科注射器等。

管理要求: I类器械实行产品备案管理。境内产品向所在地的省级药品监督管理部门备案。备案流程相对简化,并且不要求提交临床评价资料,其目的是提高管理效率并确保基本安全。
B. 第二类医疗器械(II类:中度风险)
第二类医疗器械是指对其安全性、有效性应当加以控制的医疗器械。这些器械具有一定的潜在风险,但通常可以通过技术标准、规范和省级监管机构的注册审批程序来有效控制。
典型案例: II类器械的实例包括血压计、体温计、助听器、注射器(非一次性无菌)、输血装置和电动轮椅等。此外,预期明确用于某种疾病治疗的医疗器械,其分类应不低于第二类。
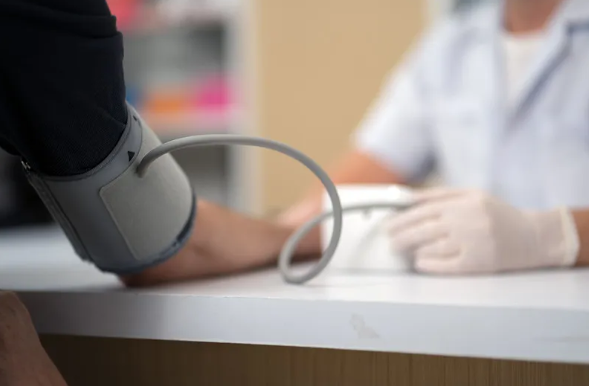
管理要求: II类器械实行产品注册管理,由省级药品监督管理部门负责审批和颁发注册证。
C. 第三类医疗器械(III类:高风险)
第三类医疗器械具有最高的风险,是指植入人体;用于支持、维持生命;或对人体具有潜在危险,对其安全性、有效性必须严格控制的医疗器械。
这类器械的风险升级主要源于其高侵入性、长期植入性,或一旦失效将导致严重甚至危及生命的后果。
典型案例: III类器械包括植入式心脏起搏器、人工晶状体、血管支架、血液透析装置、齿科植入材料、医用可吸收缝合线、以及一次性使用无菌注射器和输液器等。
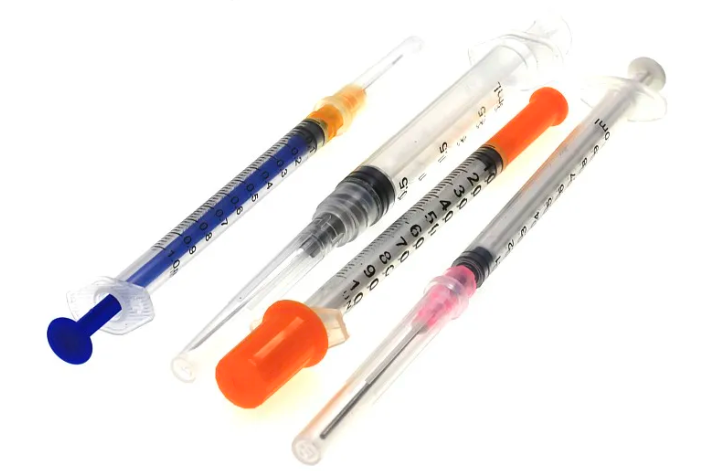
管理要求: III类器械实行产品注册管理,由国家药品监督管理局(NMPA)负责集中审评审批。这类器械的上市要求最为严格,并且自2022年6月1日起,III类医疗器械已强制实施唯一标识(UDI),以保障生产、流通、使用的全流程追溯。
D. III类的风险升级机制分析
对第三类医疗器械的判定,其核心逻辑在于临床使用的后果严重性,而非仅是产品的技术复杂度或结构。例如,一次性使用无菌注射器和输液器,尽管在结构上可能相对简单,但由于它们直接接触血液循环系统,并且必须以无菌形式提供,一旦无菌屏障失效或产品质量存在缺陷,可能引发严重的系统性感染或危及生命。因此,其风险等级被提升至III类。这种判定机制清楚地表明,监管关注的焦点是风险发生时对患者造成的不可逆损伤程度,从而将高风险路径(如接触血液循环系统或中枢神经系统)与必需的无菌性结合的产品,其分类自动跃升至最高级别。
医疗器械分类标准与管理要求对比
|-----------|----------|---------------|----------|----------------------|--------------------------------------------|
| 类别 | 风险等级 | 安全有效性控制要求 | 管理方式 | 典型产品示例 | 经营要求 |
| 第一类 (I) | 低风险 | 常规管理足以保证 | 备案管理 | 听诊器、绷带、外科口罩 | 无需办理许可证或备案,只需在营业执照经营范围中增加"医疗器械相关内容"即可合法经营。 |
| 第二类 (II) | 中度风险 | 应当加以控制 | 注册管理+许可 | 体温计、助听器、心电图机 | 需办理《第二类医疗器械经营备案凭证》(非许可证),向市级药监部门备案。 |
| 第三类 (III) | 高风险 | 必须严格控制 | 严格注册+许可 | 植入式起搏器、血管支架、一次性无菌输液器 | 必须办理《医疗器械经营许可证》,审批严格,需现场核查。 |
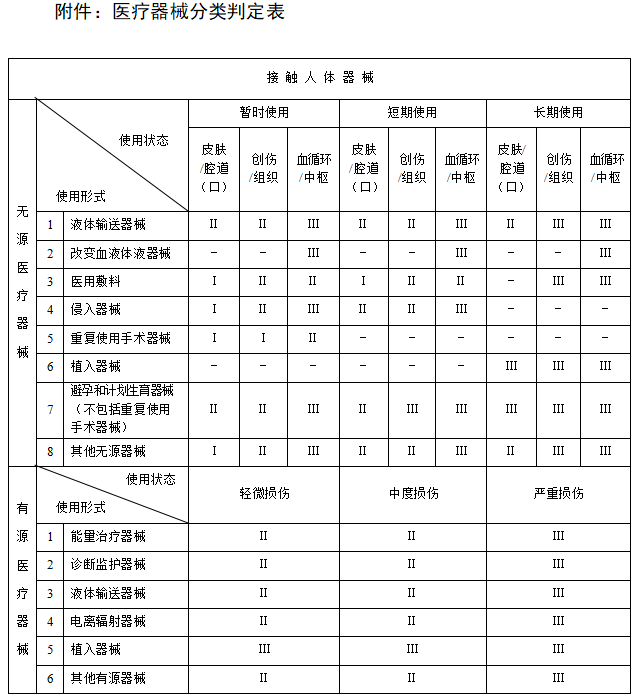
国家出台的**《医疗器械分类规则》**,具体内容请见下表,里面对医疗器械的种类进行了详细的约束和说明,便于医疗器械的监管和约束。
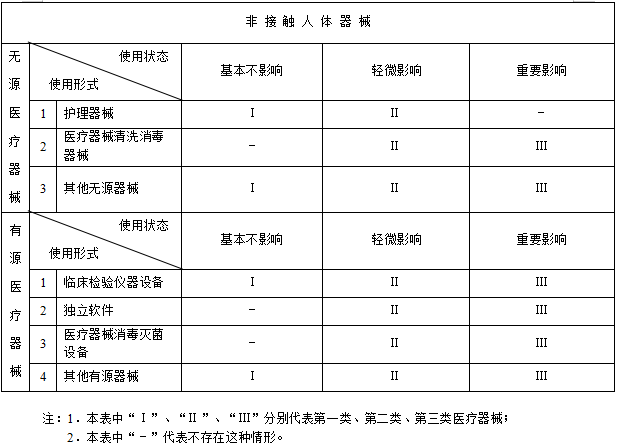
🔎 审批信息查询途径
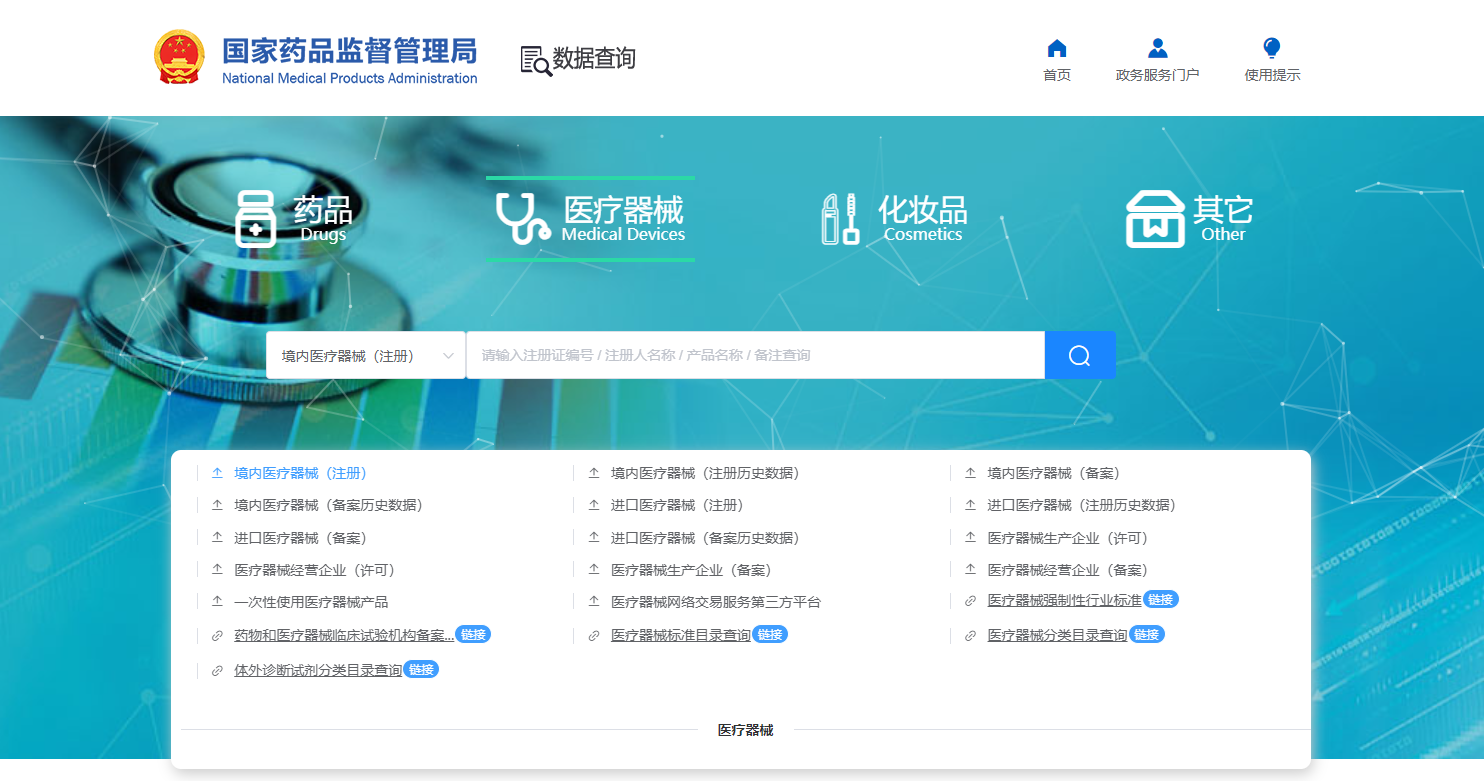
想要了解 III 类医疗器械的审批和上市情况, 我们可以通过国家药品监督管理局网站查询,这是查询任何在中国境内合法上市医疗器械的首要且最权威的渠道。
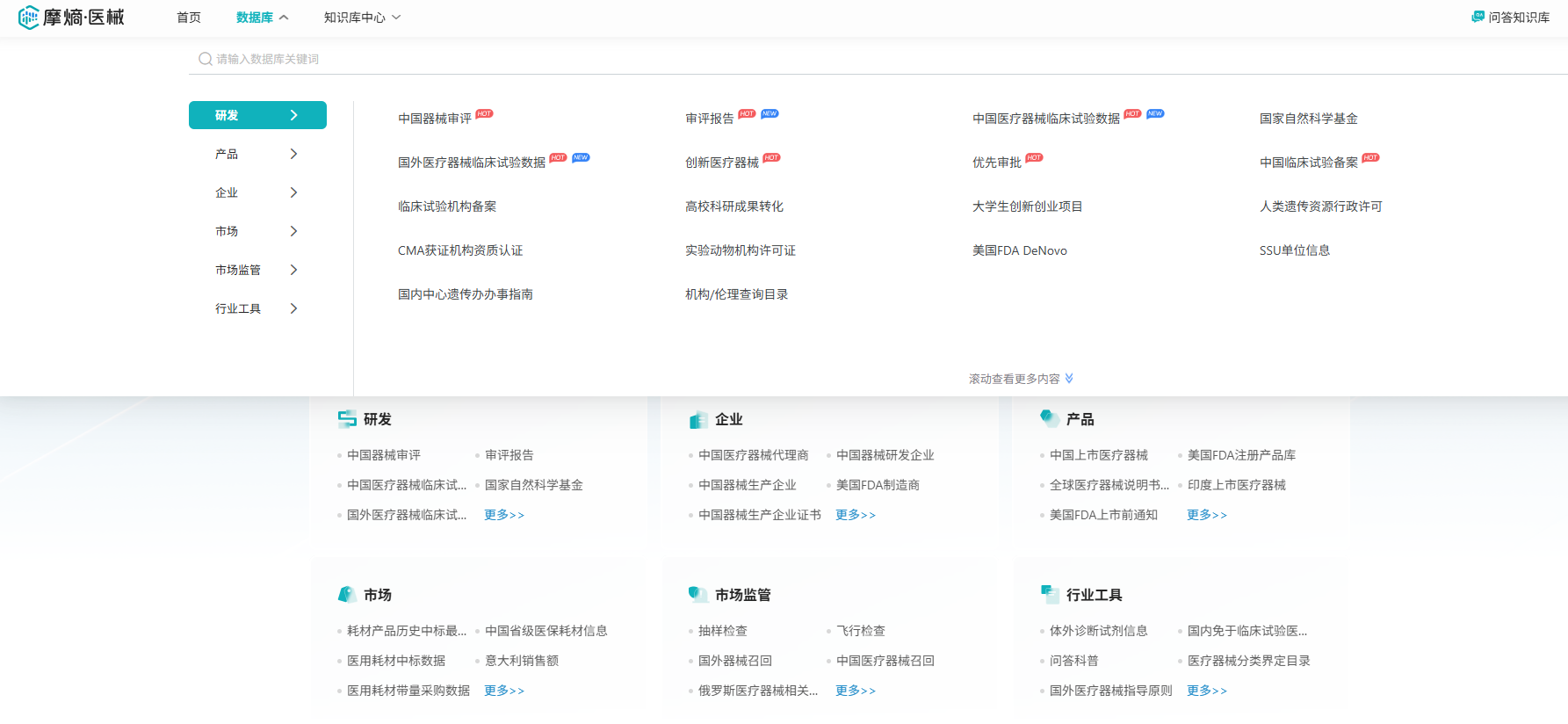
当然,我们也可以使用专业第三方医械查询平台 ,在复杂的医疗器械行业中,信息的专业性、整合性和时效性至关重要。传统的官方或通用查询方式往往难以满足行业用户对深度数据分析和高效信息获取的实际需求。因此,选择专业第三方医械查询平台已成为行业趋势,这类平台的核心优势在于:
- 更懂行业用户: 它们专注于医疗器械垂直领域,提供的服务和功能设计能够精准契合研发、生产、注册、市场、投资等环节的实际需求。
- 人性化体验: 提供优化、便捷的查询入口和界面,极大地提升了用户查找和获取数据的效率。
- 深度数据整合与分析: 不仅仅是简单的数据罗列,而是将碎片化的信息进行关联和结构化,提供一站式的数据解决方案。
以摩熵医械为例,这类专业平台专注于医疗器械数据领域,整合生物医药全产业链的上下游数据资源,全面覆盖医疗器械从研发到上市的全生命周期。
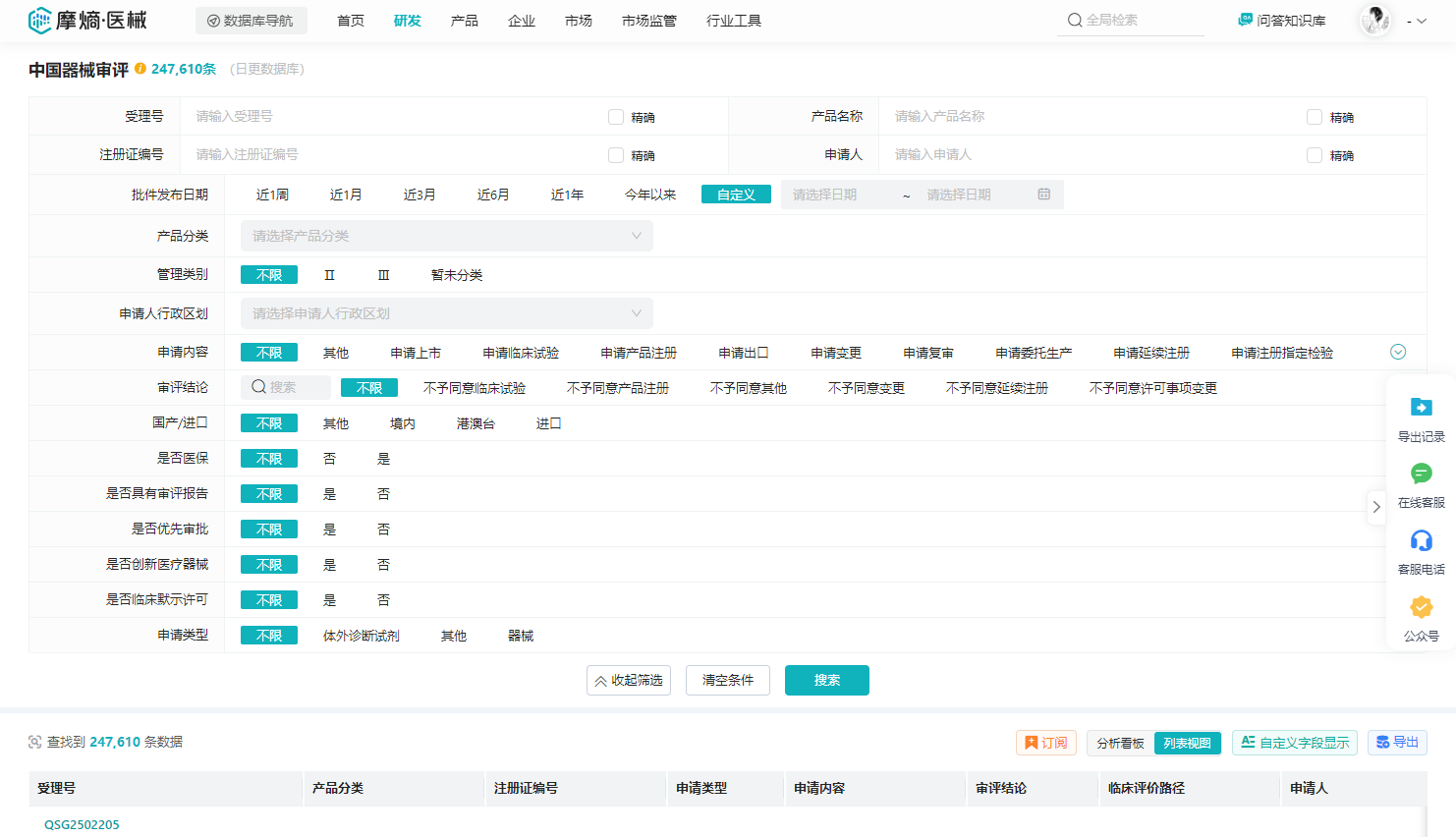
摩熵医械的核心价值之一是提供中国器械审评数据库 等高价值数据服务,旨在帮助用户了解医疗器械上市前审批的申请内容。此数据库是由国家药品监督管理局(NMPA)与国家药品监督管理局医疗器械技术审评中心(CMDE)等多个部门的官方数据整合而成的。目前,数据库中收录了超过24万+的数据。可以利用平台快速查询 目标产品的审评状态、申请内容、审评结论等信息,并能实时跟踪器械的研发进展和申报动态。 这将有助于企业进行科学立项,及时调整产品销售策略,以规避风险。
摩熵医械平台超越了单一维度查询的局限性,实现了数据的智能关联与深度整合。
- 关联维度: 平台能够将特定的医疗器械产品信息与相关的行业标准、生产企业资质、专利信息、临床试验数据等进行多维度的智能匹配和关联。
- 用户效益: 这种一站式、深度整合的数据解决方案,极大地提高了信息检索的效率和准确性,为医疗器械行业的研发人员、质量/注册(QA/RA)团队、生产管理以及市场经营人员节省了大量宝贵的时间,让用户能够将精力聚焦于核心业务而非繁琐的信息整理。
结语
中国医疗器械分类体系是一个基于风险、多维度考量的严谨系统。它明确区分了低风险的I类器械、中度风险的II类器械和高风险的III类器械。分类判定不仅依赖于产品的物理结构和功能,更关注其预期用途、侵入人体程度、使用时限以及是否包含无菌、药物或可吸收等高风险特征。遵循"最高风险"原则是确保监管安全阀的关键。
面对复杂的分类体系,医疗器械企业应采取以下策略以确保合规:
① 早期介入分类界定: 在产品概念设计和研发初期,企业应利用《分类规则》进行内部预判,并对新颖或跨界(如药械组合)产品积极向监管部门申请官方预分类界定。提前锁定产品类别是确保后续注册路径清晰、高效的关键战略步骤。
② 精准限定预期用途: 在准备I类或II类备案/注册资料时,必须严格按照目录要求撰写"产品描述"和"预期用途"。任何模糊或超出目录范围的描述都可能被视为试图规避高风险监管,从而触发分类升级。
③ 遵循从高原则: 当产品设计复杂或由多个组件构成时,必须主动识别并采取风险程度最高的管理类别进行注册和管理,以满足NMPA"从严掌握"的监管要求。
④ 关注上市后合规投入: 对于确定为III类或II类的高风险产品,企业必须投入资源建立和维护符合UDI要求的系统,并确保在流通环节依法取得相应的经营许可或备案,实现产品的全生命周期合规管理。