在原核表达系统中,如何高效启动目标基因的转录是重组蛋白生产的关键环节。异丙基-β-D-硫代半乳糖苷(IPTG)作为一种经典的诱导剂,凭借其稳定性和高效性,已成为实验室最广泛使用的诱导工具。
一、诱导原理:基于乳糖操纵子的调控机制
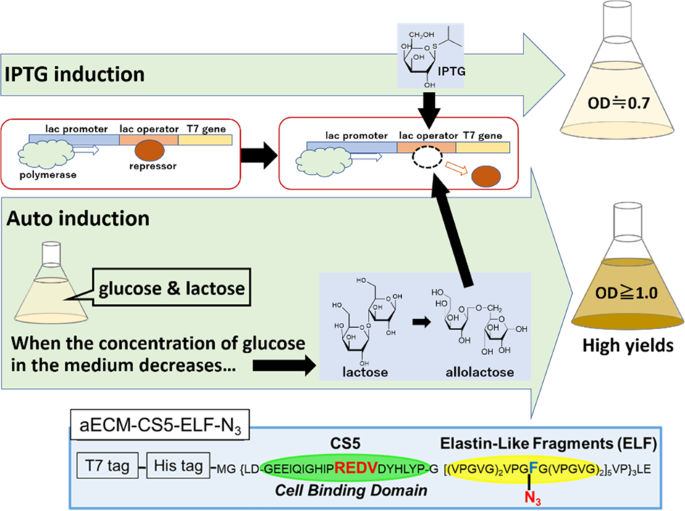
IPTG的诱导机制源于大肠杆菌的乳糖操纵子模型。在自然状态下,当培养基中缺乏乳糖时,由调节基因编码合成的Lac阻遏蛋白会与操纵基因结合,阻碍RNA聚合酶与启动子的结合,从而抑制结构基因的转录。
IPTG的结构中含有硫苷键,使其无法被细胞代谢降解,具有极高的化学稳定性。当IPTG进入细胞后,会与Lac阻遏蛋白发生变构结合,导致阻遏蛋白的空间构象发生改变,使其从操纵基因上解离下来。这一过程解除了对转录的抑制,RNA聚合酶得以顺利通过启动子,驱动下游目的基因的高效转录与翻译。
在实际应用中,T7启动子驱动的原核表达系统最为常见。宿主菌株如BL21(DE3)染色体上整合了受lacUV5启动子控制的T7 RNA聚合酶基因,IPTG的加入能够同步激活T7 RNA聚合酶的表达,从而实现目标蛋白的高水平生产。
二、标准实验流程
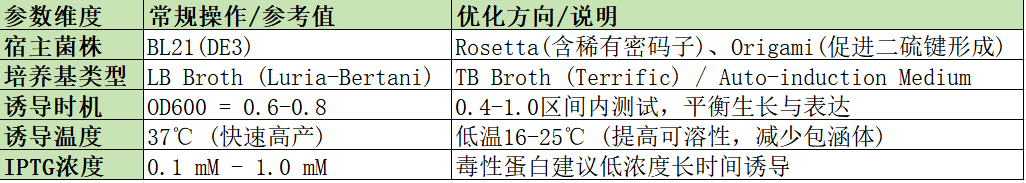
为了获得理想的蛋白产量,优化诱导条件是关键。以下是以BL21(DE3) 感受态细胞为宿主的标准操作参考:
1. 菌株与质粒准备
将构建好的表达载体转化至表达宿主菌中。由于T7表达系统的普及,市面上常见的BL21(DE3)及其衍生菌株(如Rosetta、Tuner)均能很好地配合IPTG发挥作用,因为它们染色体上整合了受lacUV5启动子控制的T7 RNA聚合酶基因。
2. 培养与扩增
挑取单克隆接种于含有对应抗性的LB培养基中,在37℃下振荡培养过夜。随后按1:50至1:100的比例转接至新鲜培养基中,继续培养至对数生长期。通常通过测定OD600值来监测菌液密度,当OD600达到0.6-0.8时,菌体处于代谢旺盛的对数期,此时最为适合诱导。
3. 添加诱导剂
加入IPTG至预设的终浓度。根据不同的蛋白特性,浓度梯度通常在0.1 mM至1.0 mM之间。值得注意的是,较低浓度的IPTG(如0.1-0.4 mM)往往有助于减缓蛋白合成速率,从而促进蛋白正确折叠,减少包涵体的形成。
4. 降温诱导
这是影响蛋白可溶性的重要环节。高温(37℃)易导致蛋白合成过快而形成无活性的聚集体;而低温(16℃-25℃)诱导虽然会延长诱导时间(通常12-24小时),但能显著提高可溶性蛋白的产量。
5. 细胞收集与裂解
诱导结束后,通过离心收集菌体沉淀。弃去上清后,可使用缓冲液重悬菌体,并通过超声破碎或高压匀浆等方式细胞裂解,释放胞内蛋白,以便进行后续的纯化步骤。
三、 关键试剂参数对比
在实际操作中,除了上述参数,培养基的选择也影响产量。TB培养基(Terrific Broth)因其营养更丰富,通常比LB培养基能获得更高的菌体湿重和蛋白总量。