在生命科学研究中,重组胶原蛋白(Recombinant Collagen)作为一种关键的生物大分子,因其独特的结构特点和在细胞外基质研究中的重要性而被广泛关注。
一、胶原蛋白分子构成与分类
胶原蛋白(Collagen)是动物体内最丰富的多肽类结构蛋白,具有三股螺旋的独特构象,其基本单元为由三个α链通过特定氨基酸序列缠绕形成的三螺旋结构。这种结构由重复的 GlyXY 序列(其中 X 和 Y 多为脯氨酸或羟脯氨酸)构成,是胶原特有的分子标志。根据氨基酸组成与链型差异,可划分为多种类型,例如 I 型、II 型和 III 型等,每种类型在生物体中的分布与功能各异。
与天然来源的胶原蛋白相比,重组蛋白提供了可控的氨基酸序列、可预测的分子量和易于引入标签的优势,使得下游分析如质谱鉴定、结构解析和功能比对等实验更加精确可靠。
二、表达系统选择与分子构建考虑
重组胶原蛋白的表达系统需兼顾蛋白折叠、后期修饰以及分子稳定性等多项技术要求。无论在真核还是原核系统中表达,核心目的均是确保产物能正确折叠为三螺旋结构,同时保留胶原特有的生物理化性质。
在分子构建阶段,引入适配的标签技术(如 6×His、FLAG 或 GST 标签)成为常见实践,便于后续的检测与纯化操作。这些标签在不干扰蛋白折叠与功能的前提下,可极大提升实验效率。
此外,针对不同研究需求,可设计不同长度的氨基酸序列,例如构建仅含胶原重复片段的短链多肽用于结构分析,或构建更接近全长的重组胶原用于细胞模型研究。
三、蛋白结构与性质分析
重组胶原蛋白的结构与性质分析是理解其功能的基础。在蛋白表达后,蛋白分析技术如 SDSPAGE、Western blot 及质谱分析等成为验证表达产物质与量的核心手段。通过这些技术,可确认目标蛋白的分子量、标签存在性以及可能的降解产物情况。
鉴于胶原蛋白三股螺旋结构的热稳定性特征,差示扫描量热法(DSC)和圆二色谱(CD)等光谱技术常用于评估蛋白的构象状态与热变性曲线。这类分析可以帮助研究者理解不同条件下蛋白的稳定性变化,从而为实验条件设定提供依据。
四、细胞外基质与体外模型中的应用
作为细胞外基质的核心成分之一,重组胶原蛋白在体外模型构建中具有重要作用。利用其良好的生物相容性与三维支架特性,可用于建立细胞培养基底、构建三维细胞培养模型,或作为与其他 ECM 蛋白组合使用的基底分子。
在这些应用场景中,重组胶原的批次一致性和可控性较天然提取胶原更优,有助于减少实验变量,提高数据可重复性。需要指出的是,实验设计中关注胶原分子与细胞表面受体的相互作用是理解细胞行为(如黏附、迁移等)的关键。
五、常见技术考虑与实验参数设置
在使用重组胶原蛋白进行实验时,一些技术参数需要认真考量:
蛋白浓度与溶液制备:根据应用目的优化浓度范围,例如用于基底涂层时的浓度通常高于用于结构分析的浓度。
溶液稳定性:重组胶原蛋白在溶液中的稳定性受 pH、温度和离子强度影响明显,需根据具体实验条件调整缓冲体系。
蛋白聚集状态:由于胶原分子的亲水性与三股螺旋特性,容易形成高分子聚集体。通过动态光散射(DLS)等技术监测聚集情况,有助于判断溶液状态。
六、生物合成机制与分子特性
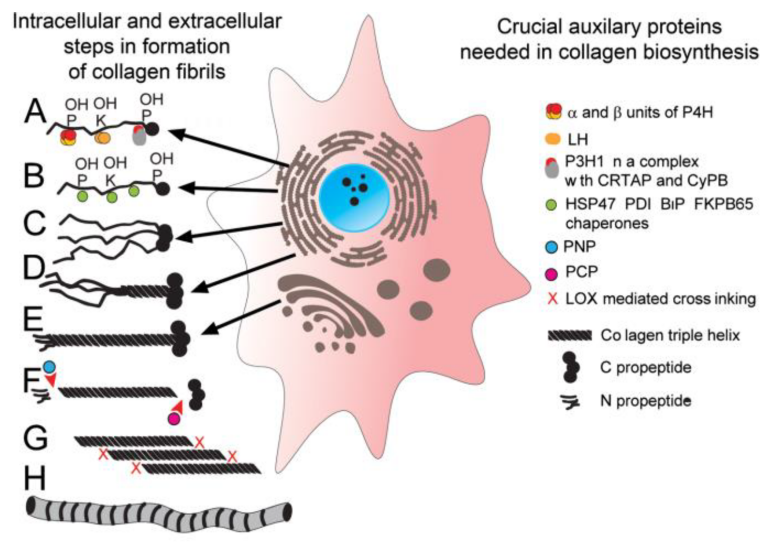
理解胶原蛋白的生物合成机制有助于解释其分子行为。天然胶原蛋白在生物体内经历前体合成、信号肽切除、羟基化等一系列后期修饰,这些修饰对三螺旋稳定性有深远影响。重组系统尽管不完全模拟天然生物合成路径,但在设计表达构建时考虑到氨基酸序列与可能的修饰位点,可以使重组产物更贴近天然特性。
从分子特性上看,胶原蛋白的重复 GlyXY 序列赋予其独有的结构刚性和弹性,这种特性在生物材料研究、细胞行为研究等领域有着广泛的应用价值。在实验层面,通过对这些序列的分析与比对,研究者可以更好地理解胶原分子的力学特性以及在不同环境下的行为表现。