01
文献学习

今天分享的文献是由北京大学第一医院马永蔌、田孝东、杨尹默、陈凯等团队于2026年3月24日在《Cancer Letters》(中科院1区top,IF=10.1)上发表的研究"A Deep Learning Pathomic Signature Predicts Survival and Recurrence in Pancreatic Ductal Adenocarcinoma Independent of CA19-9"即一种基于深度学习的病理组学特征可独立于CA19-9预测胰腺导管腺癌的生存与复发,该研究开发并验证了一种基于深度学习(DeepSurv)的病理组学特征模型(PCPSDL),用于预测胰腺导管腺癌(PDAC)患者的总体生存(OS)和无复发生存(RFS)。模型基于常规H&E染色切片提取病理组学特征,在内部和外部(TCGA)数据集中均表现出良好的预测性能,尤其在CA19-9阴性患者中仍能有效进行风险分层。结合转录组和多重免疫组化分析,揭示了高风险评分与免疫抑制微环境及基底样上皮细胞状态的关联。
创新点:①首次建立针对PDAC的深度学习病理组学模型 ,同时预测总生存期与无复发生存期,填补了术后精准风险分层工具的空白 。②在CA19-9阴性患者中仍能有效分层预后 ,HR达9.26,突破传统血清标志物的应用局限 。③结合转录组与多重免疫组化揭示生物学机制 ,将高风险与免疫抑制微环境及基底样表型直接关联,提升模型可解释性。
临床价值:①仅需常规H&E切片即可实现精准预后预测 ,成本低、可推广 ,适合在各级医院落地应用。②为CA19-9阴性患者提供独立的预后判断依据 ,填补临床管理盲区 ,指导个体化辅助治疗决策。③构建可视化诺模图 ,实现1、3、5年生存与复发风险的个体化量化评估 ,直接辅助临床决策。
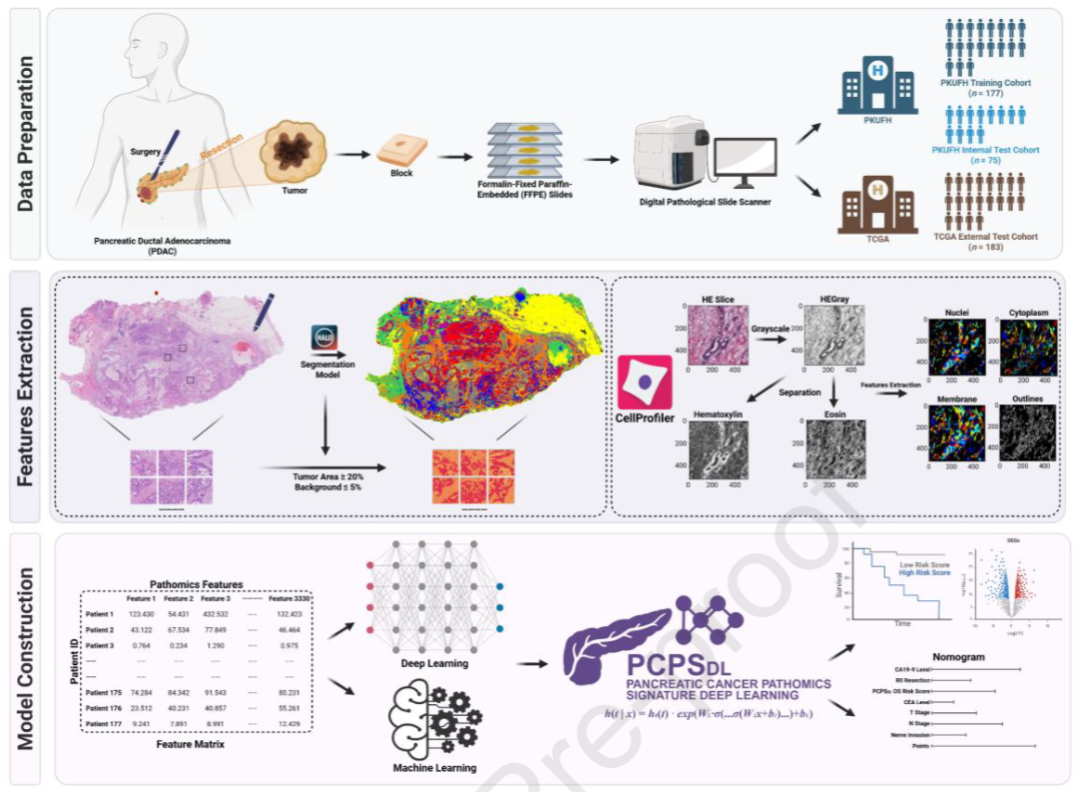
图 1:胰腺导管腺癌病理组学深度学习模型(PCPSDL)构建流程示意图
数据准备
内部队列:北京大学第一医院(PKUFH)252例PDAC患者,7:3分为训练集(177例)+内部测试集(75例);
外部验证:TCGA数据库183例PDAC患者;
数据来源:病理确诊后的H&E染色全切片病理图像(WSI)。
特征提取
HALO软件自动分割肿瘤区域,筛选肿瘤占比≥20%的有效图像块;
CellProfiler开源软件高通量定量提取3330个病理组学特征(核、胞质、胞膜、纹理、强度等);
构建「患者-病理组学特征」矩阵。
模型构建与转化
基于DeepSurv深度学习框架构建OS(总生存)、RFS(无复发生存)预测模型;
高低风险分层+肿瘤微环境(TME)差异分析;
整合临床变量,构建可视化预后列线图。
02
研究背景和目的
研究背景
胰腺导管腺癌(PDAC)是一种预后极差的消化系统恶性肿瘤,其5年生存率仅为13% ,超过半数的患者在初诊时已处于局部进展期或发生远处转移,即便接受根治性手术,近50%的患者在术后12个月内出现复发或转移 。当前临床上主要依赖血清生物标志物CA19-9进行术后监测,但约10%的患者因Lewis抗原阴性而呈现CA19-9不表达 ,导致该群体缺乏有效的血清学评估手段。尽管近年来基于空间转录组、单细胞测序等高通量技术构建的预测模型层出不穷,但其临床转化受限于样本处理复杂、成本高昂、跨中心可重复性差 等问题。传统病理学评估主要依赖人工判读肿瘤分化程度、间质比例等有限特征,仅利用了全切片图像中不足1%的信息 。虽然人工智能辅助病理模型发展迅速,但多数模型存在"黑箱 "问题,缺乏生物学可解释性,且未在CA19-9阴性等临床挑战性人群中进行充分验证。因此,亟需开发一种兼具高预测性能、生物学可解释性、且适用于CA19-9阴性患者的新型预后评估工具。
研究目的
本研究旨在开发并验证一种基于深度学习 的胰腺导管腺癌病理组学特征模型(PCPSDL),该模型利用常规苏木精-伊红染色全切片图像 提取定量病理特征,实现对患者总生存期和无复发生存期的精准预测 。研究的核心目标包括:第一,构建并验证PCPSDL模型在内部和外部独立队列中的预测性能与泛化能力;第二,重点评估模型在CA19-9阴性这一临床难点人群中的风险分层效能 ,为缺乏血清学标志物的患者提供可行的预后评估工具;第三,通过整合转录组分析、肿瘤微环境免疫细胞解析及多重免疫组化技术,揭示模型风险评分背后的生物学基础 ,包括与免疫抑制性微环境、基底样上皮细胞状态的关联;第四,增强模型的可解释性 ,通过SHAP分析阐明关键病理特征的贡献权重;第五,将PCPSDL风险评分与临床病理变量整合,构建可视化的列线图预测工具,为临床个体化治疗决策提供有力支持,从而推动该模型向临床实践转化。
03
数据和方法
研究数据
内部数据集:北京大学第一医院(PKUFH)252例PDAC患者(训练177,内部测试75)。
外部验证:TCGA数据库183例PDAC患者。
数据模态:H&E染色全切片图像(WSI)、临床病理变量、转录组数据(TCGA)、多重免疫组化(mIHC)。
技术方法
图像处理:HALO自动分割肿瘤区域,筛选肿瘤含量≥20%的图像块。
特征提取:CellProfiler提取3,330个病理组学特征(核、质、膜形态、纹理等)。
模型构建:DeepSurv(MLP)构建OS和RFS预测模型,结合5折交叉验证和贝叶斯超参数优化。
生物学分析:
差异表达基因(DESeq2/edgeR)与GO/KEGG富集分析。
CIBERSORT免疫细胞浸润分析。
Ecotyper识别肿瘤生态型。
mIHC验证免疫细胞比例。
统计与可解释性:SHAP分析特征贡献,构建诺模图,C-index、AUC评估模型性能。
04
实验结果
模型性能:
OS的C-index:训练0.74,内部测试0.64,外部测试0.62。
RFS的C-index:训练0.77,内部测试0.61,外部测试0.64。
风险分层:高风险组OS和RFS显著更差(P < 0.001)。
CA19-9阴性患者:PCPSDL仍能有效分层(OS HR = 9.26,P < 0.001)。
生物学关联:
高风险与基底样上皮状态、免疫抑制(M2/M1 TAM升高)、CD8⁺ T细胞浸润增加但功能失调相关。
低风险与免疫活跃生态型(CE8)相关。
诺模图:1、3、5年OS和RFS预测AUC分别达0.87、0.78、0.91和0.80、0.70、0.85。
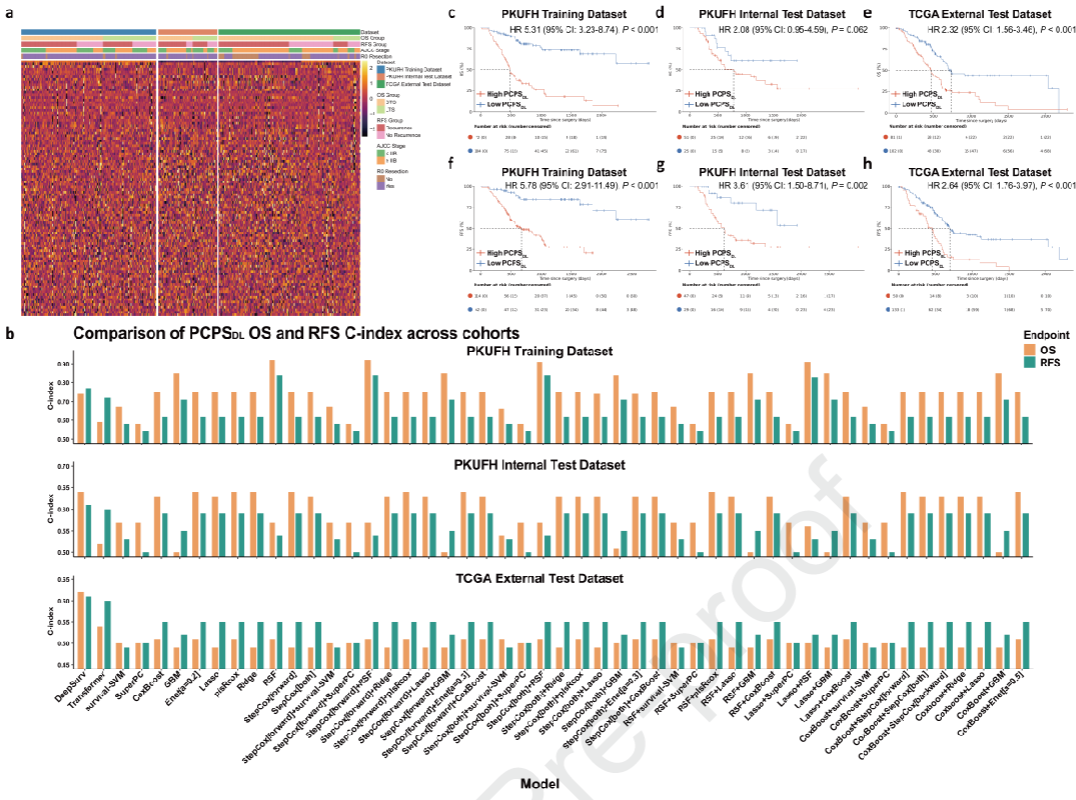
图 2:PCPSDL模型性能及风险分层Kaplan-Meier生存曲线

图 3:PCPSDL OS模型对不同CA19-9/CEA水平患者的生存风险分层预测
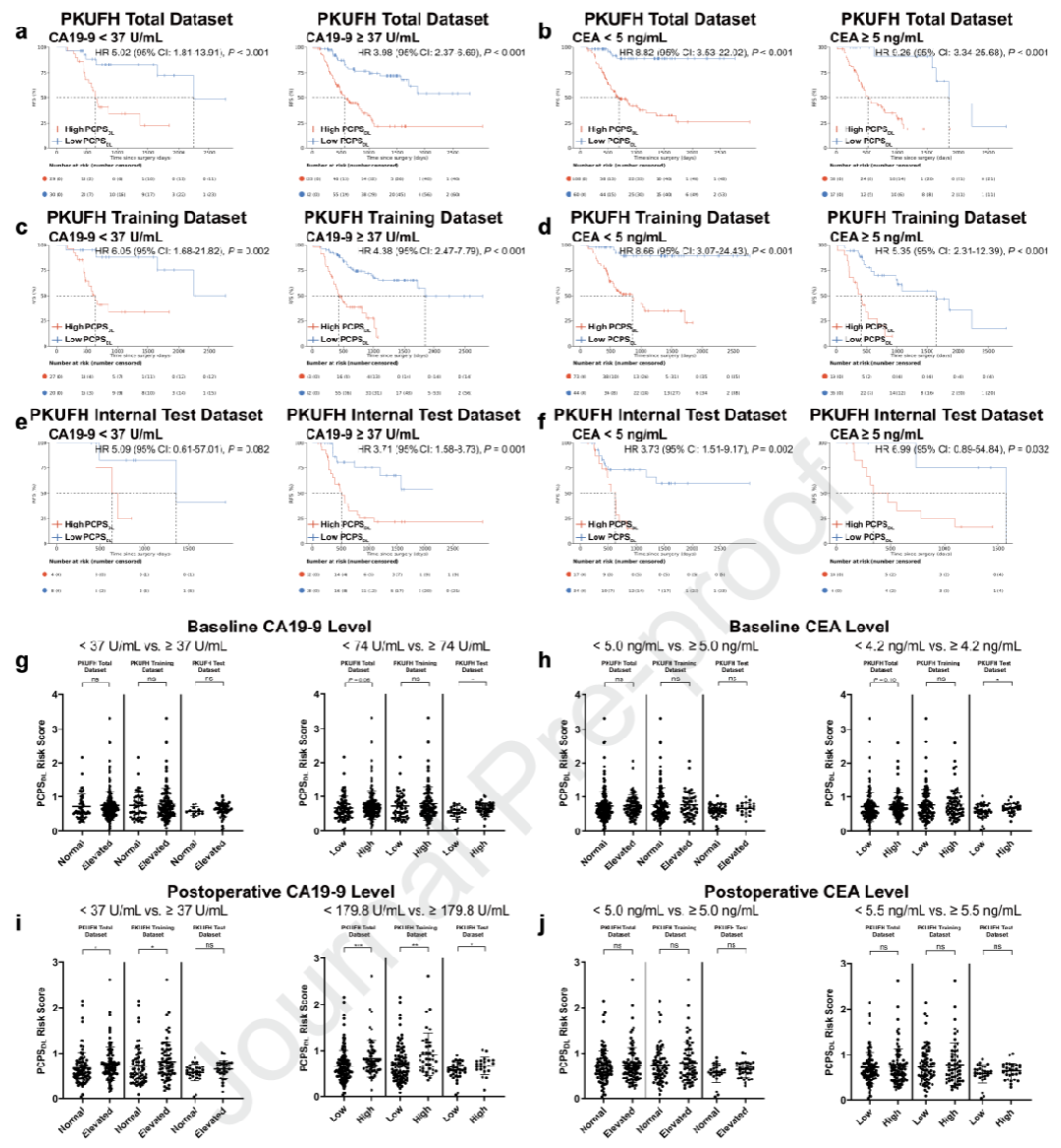
图 4:PCPSDL RFS模型对不同CA19-9/CEA水平患者的复发风险分层预测
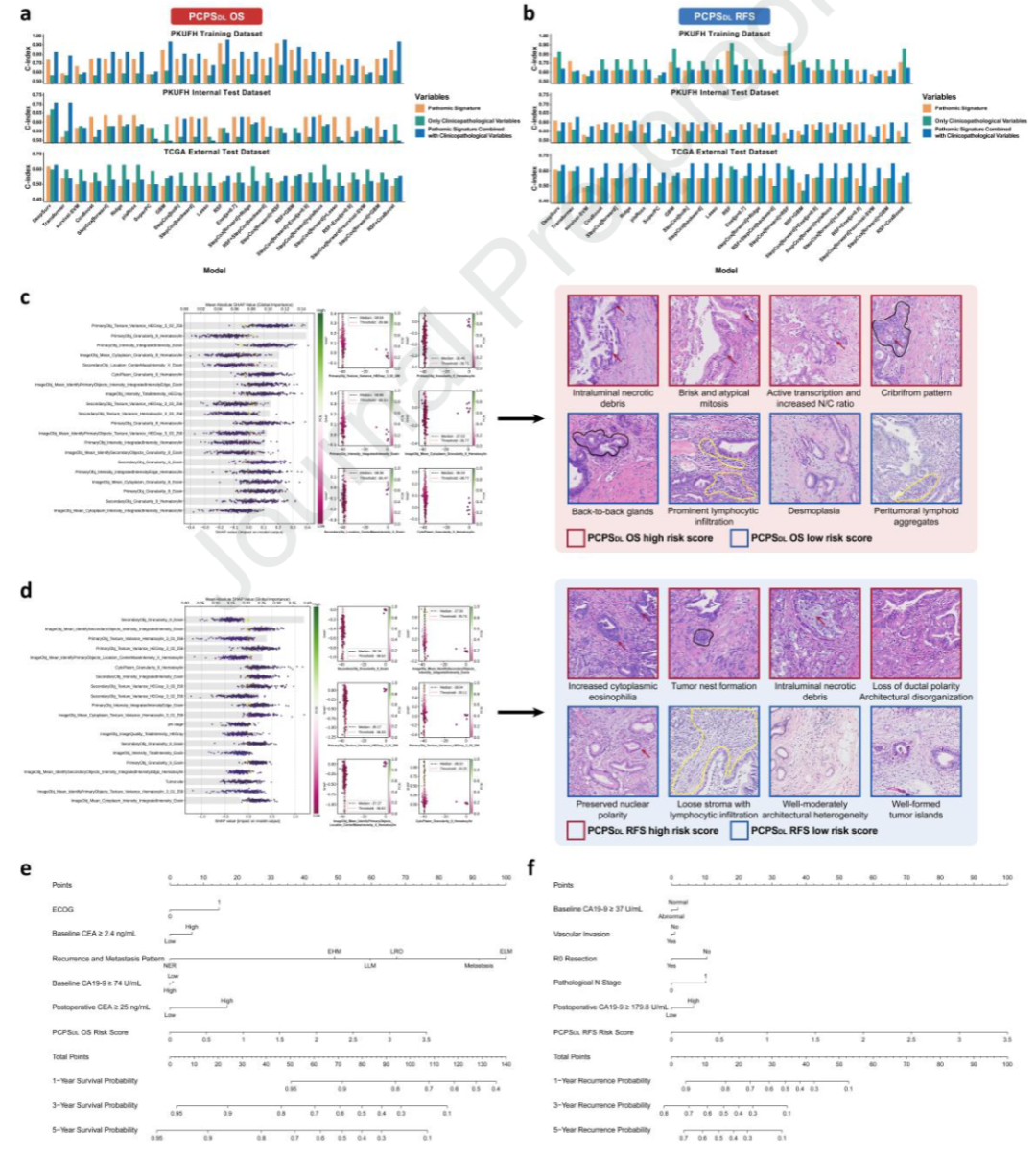
图 5:临床变量增益、模型可解释性(SHAP)与列线图构建
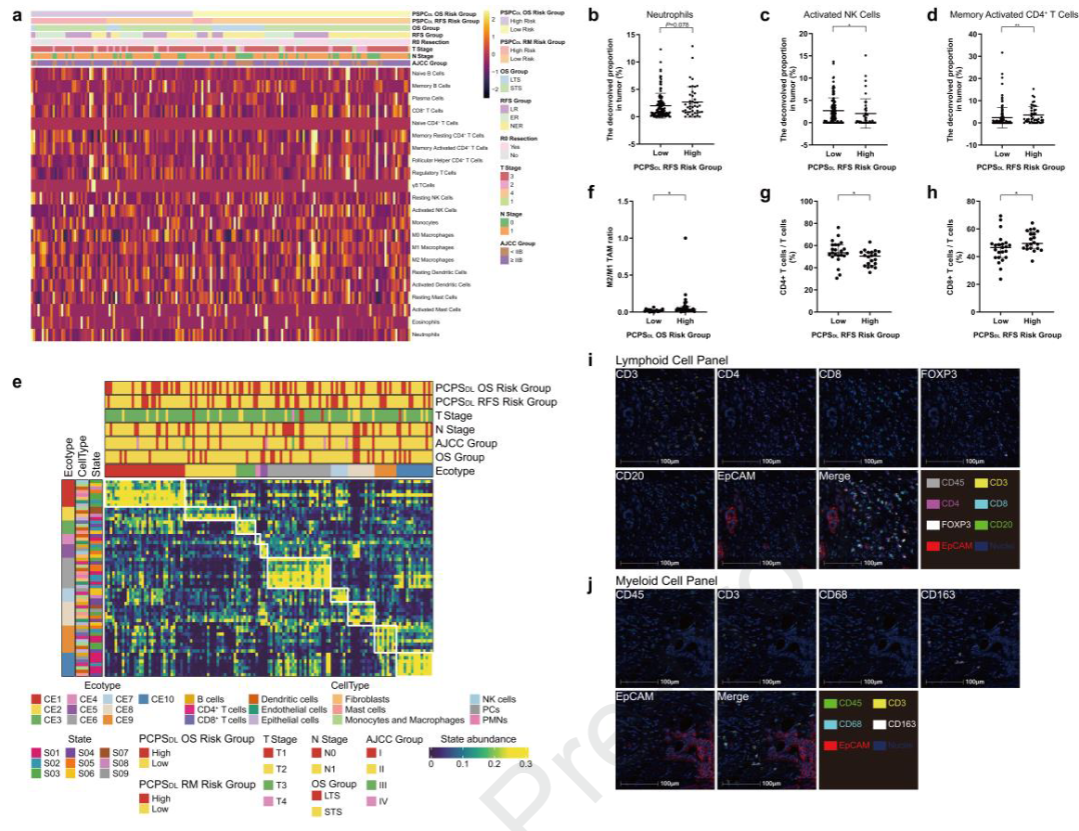
图 6:PCPSDL定义的高低风险组肿瘤微环境(TME)表征
05
研究结论
该研究成功构建并验证了一种基于深度学习及常规H&E染色切片的胰腺导管腺癌病理组学特征模型 ,命名为PCPSDL。该模型在内部与外部验证集中均能稳健预测患者的总生存期与无复发生存期 ,其关键优势在于在CA19-9阴性这一临床棘手亚组中仍能实现有效风险分层 ,显著区分高低风险患者的预后。通过多组学与多重免疫组化分析,研究揭示高风险评分与免疫抑制性微环境 及基底样上皮细胞状态 密切相关,赋予模型明确的生物学解释性。此外,结合临床变量构建的列线图进一步提升了模型的临床应用价值。总体而言,PCPSDL作为一项独立于传统血清标志物的、可解释性强的预后工具,为胰腺导管腺癌,尤其是缺乏有效标志物患者的个体化治疗与术后管理提供了新的策略。
参考文献:Yang B, Liu X, Wei J, Xu L, Zhang J, Fan M, Hou Y, Zhang F, Chen Y, Liu W, Li Y, Liu Z, Chen K, Tian X, Yang Y, Ma Y. A Deep Learning Pathomic Signature Predicts Survival and Recurrence in Pancreatic Ductal Adenocarcinoma Independent of CA19-9. Cancer Lett. 2026 Mar 24:218452. doi: 10.1016/j.canlet.2026.218452.