An acetyltransferase family required for biosynthesis of diverse marine carotenoids
一个参与多种海洋类胡萝卜素生物合成的乙酰转移酶家族

研究意义
全球约半数的光合作用发生在海洋中。海洋真核藻类可合成特异性类胡萝卜素,以实现在水下环境的高效光能捕获。尽管这类色素的多步生物合成途径已有部分解析,但对于岩藻黄质及其他主要海洋类胡萝卜素形成所必需的共同乙酰化步骤 ,仍未见相关研究。本研究鉴定出负责这一关键修饰反应的长期未知酶。结果表明,不同藻类谱系通过进化调整该酶的底物特异性,形成了多样化的色素谱,进而造就了海洋生态系统中光合色素的高度多样性。该发现解答了藻类生物学领域长期存在的科学问题,并为提升作物捕光效率、开发高价值类胡萝卜素可持续来源开辟了广阔前景。
摘要
包括硅藻、定鞭藻、甲藻在内的有色藻门藻类是海洋初级生产力的主要贡献者,在维持海洋生态系统与全球碳循环的同时,可合成岩藻黄质、多甲藻素等一系列结构丰富的乙酰化类胡萝卜素。这些色素可优化藻类光合捕光效率,并对人类具有营养保健价值,但其生物合成途径尚未完全阐明,尤其是共有的乙酰化修饰步骤。本研究通过对三角褐指藻(Phaeodactylum tricornutum )中 39 个候选基因进行筛选,鉴定出一种具有叶黄素乙酰转移酶(XACT)活性的酶,该酶是上述乙酰化修饰不可或缺的关键因子。在三角褐指藻及真眼点藻微拟球藻( Nannochloropsis oceanica )中敲除 XACT 后,叶黄素乙酰化过程完全消失。系统发育分析显示,XACT 仅存在于能够合成乙酰化叶黄素的有色藻门生物中。对三角褐指藻、微拟球藻、褐藻长囊水云( Ectocarpus siliculosus ) 、甲藻 ** 共生藻(Symbiodinium tridacnidorum )** 及一种定鞭藻来源的重组 XACT 进行体外酶活检测,结果证实其均对丙二烯型类胡萝卜素前体具有催化活性,但表现出谱系特异性的底物偏好性,这也解释了不同谱系藻类类胡萝卜素结构的多样性。三角褐指藻 XACT 具有宽泛的底物特异性,促使我们重新分析岩藻黄质合成途径中其他关键酶的底物特异性,结果表明硅藻中岩藻黄质的生物合成并非线性途径,而是多分支途径。水云来源的 XACT 则表现出显著狭窄的底物谱,为褐藻岩藻黄质合成途径中两个此前争议步骤的先后顺序提供了关键证据。本研究填补了海洋类胡萝卜素生物合成领域长期存在的研究空白,并证实相关酶的宽泛底物特异性是驱动藻类类胡萝卜素结构多样性的重要因素。
海洋藻类在地球碳循环与海洋初级生产力中发挥着至关重要的作用。其中,有色藻(光合不等鞭毛类生物,如硅藻和褐藻)、定鞭藻及甲藻在海洋浮游植物群落中占据主导地位,是全球固碳作用的主要贡献者。它们在生态上的成功源于独特的光合适应机制,包括拥有与陆生植物截然不同的色素组成。值得注意的是,其捕光复合体中类胡萝卜素与叶绿素的比值显著更高,并且能够合成陆生植物所缺乏的特异性类胡萝卜素,如岩藻黄质、多甲藻素和无隔藻黄质酯(图 1 及补充附录表 S1)。这些独特的色素,尤其是岩藻黄质和多甲藻素,表现出优异的绿光吸收效率,这是对海洋环境蓝绿光光谱的重要适应。除了在光生理过程中不可或缺的作用外,这类藻类来源的类胡萝卜素因其对人类健康具有显著的营养与药用潜力,也日益受到广泛关注。
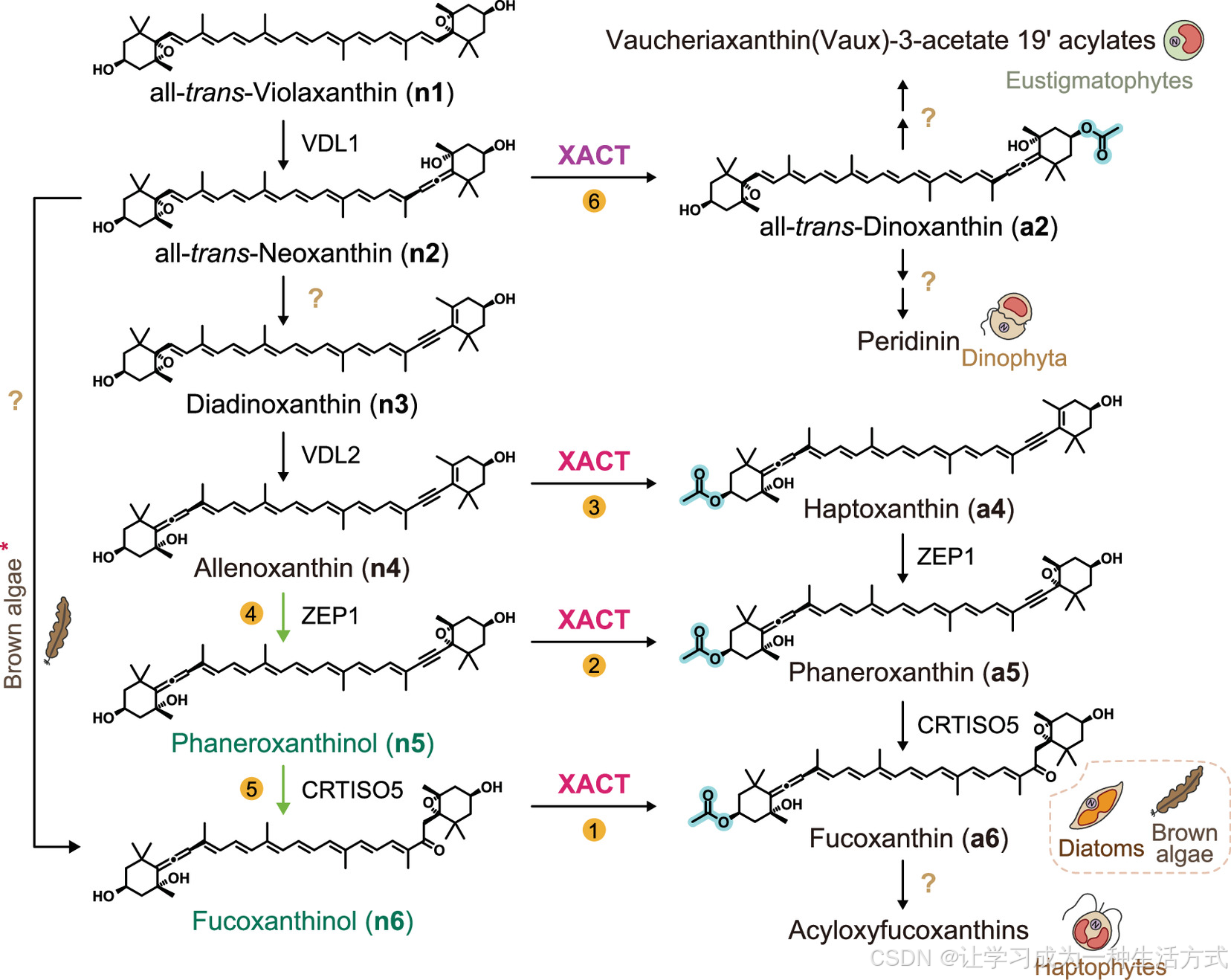
海洋藻类中经修订的类胡萝卜素生物合成途径示意图 。更新后的模型包含了从丙二烯叶黄素 到岩藻黄质 、以及从新黄质 到甲藻黄质 的新发现分支。新鉴定的中间体以绿色高亮标注,乙酰化步骤以蓝色阴影标示;未表征的酶以问号标记。由 ** 叶黄素乙酰转移酶(XACT)** 催化的步骤以品红色或紫色标注,目前仅在特定藻类谱系中得到实验验证。绿色箭头表示作用于新中间体的已知酶;红色星号代表褐藻(Phaeophyceae)中特有的合成途径。各分支旁标注了对应的藻类类群特异性标记;编号步骤为本研究阐明并验证的酶促反应(结果部分)。各编号对应的详细色素信息见补充附录表 S1。
从生物化学角度来看,这类类胡萝卜素同样具有高度多样性,并呈现出明显的谱系特异性特征。有色藻与定鞭藻主要合成岩藻黄质及其衍生物,而多数光合甲藻则合成多甲藻素(图 1)。尽管结构多样,这些类胡萝卜素大多具有一个共同的结构特征:两个末端环之一发生乙酰化修饰 ,如岩藻黄质、多甲藻素、甲藻黄质、无隔藻黄质酯及环甲藻素二酯。该修饰广泛存在于有色藻门、甲藻门和定鞭藻门等类群中,但与丙二烯键形成、羟基化等其他类胡萝卜素修饰相比,其分子机制仍研究甚少。
在海洋类胡萝卜素中,岩藻黄质因其重要的生态地位,成为研究海洋藻类类胡萝卜素修饰化学的核心模式物质。硅藻贡献了全球 20% 的固碳量并驱动硅质沉积至深海,而岩藻黄质作为硅藻主要的捕光类胡萝卜素,约占全球类胡萝卜素总量的 10%。近期在三角褐指藻中的研究已部分解析其从共同前体紫黄质开始的生物合成途径。该途径体现了类胡萝卜素代谢的进化创新,包括多个酶家族的扩张与新功能化:紫黄质脱环氧化酶家族的 PtVDL1/2、玉米黄质环氧化酶家族的 PtZEP1,以及类胡萝卜素异构酶家族的 PtCRTISO5。这些家族的部分成员最初发现于陆生植物,主要催化途径早期至番茄红素的步骤,或参与光保护性的叶黄素循环。然而,海洋类胡萝卜素生物合成仍存在一个关键空白:尚未发现任何已知的类胡萝卜素乙酰转移酶 ,使得基于同源序列的方法无法鉴定这一保守乙酰化步骤的催化酶。
本研究鉴定出一种叶黄素乙酰转移酶(XACT) ,填补了海洋类胡萝卜素生物合成领域这一长期存在的空白。我们首先在三角褐指藻中鉴定出 XACT,证实其为岩藻黄质合成所必需;随后对其他有色藻门藻类的 XACT 同源基因分析表明,该酶在有色藻门各类群的乙酰化色素合成中具有广泛功能。我们进一步证明,其底物特异性塑造了不同谱系中乙酰化类胡萝卜素的独特组成。该发现为在藻类、植物及微生物宿主中工程改造光合系统与高价值类胡萝卜素生产提供了重要进展。
结果与讨论
反向遗传学鉴定出岩藻黄质生物合成必需的乙酰转移酶候选基因
为鉴定三角褐指藻中缺失的类胡萝卜素乙酰转移酶,我们采用候选基因敲除 策略。候选基因筛选始于基于机器学习的注释工具 CLEAN,共获得 789 个归类于 EC 2.3.1 家族的基因(包含乙酰转移酶及其他酰基转移酶)。随后通过以下至少一项标准进行精简:1)在强光条件下显著下调 ------ 强光已知会抑制捕光色素合成,而已知途径基因VDL2 、ZEP1 和CRTISO5 均伴随下调(补充附录图 S1A);2)含有预测的叶绿体定位信号。经筛选最终得到 38 个候选基因(数据集 S1,补充附录图 S1B)。
我们进一步结合陆生植物的功能研究拓展筛选标准。小麦中 XAT 可催化叶黄素酯化,番茄中 PYP1 为叶黄素酯形成所必需。尽管这些酶催化长链酰基转移至类胡萝卜素,但其所属蛋白家族同样包含具有乙酰化功能的成员。本研究未找到小麦 XAT 的高置信度同源蛋白,但Phatr3_J43541 编码蛋白与番茄 PYP1 具有中等序列相似性;结合其 EC 2.3.1 注释,该基因也被纳入敲除候选列表(数据集 S1)。
为对候选基因进行功能验证,我们构建了 CRISPR/Cas9 敲除株系(数据集 S2)。鉴于转化株常出现嵌合体,我们采用两步鉴定策略:首先分离亚克隆以获得纯合(或双等位)突变体,多个候选基因均成功获得;随后验证 "基因敲除会导致岩藻黄质缺失并伴随前体积累" 的假说。尽管转化子菌落肉眼观察未见明显色素变化(可能由株系非克隆性所致),我们采用 ** 高效液相色谱(HPLC)- 二极管阵列检测器(PDA)** 以提高检测灵敏度。分析显示,Phatr3_J36932 突变体积累微量特征色素,其吸收光谱与岩藻黄质高度相似,但保留时间更短,表明极性更高(补充附录图 S2A,峰 n6);其他候选基因突变体均未检测到新色素峰。不过部分基因未能获得纯化的双等位突变体(数据集 S1),因此不能排除这些基因在色素代谢中具有功能。
基于三方面证据,Phatr3_J36932 被优先确定为关键候选基因:1)在 PhaeoNet 共表达网络中属于 "lightcyan1" 模块,该模块显著富集光合作用相关基因;2)其编码蛋白含有N 端乙酰转移酶结构域 与C 端类脂运载蛋白结构域 (图 2A);3)定位预测(数据集 S1)与叶绿体蛋白质组数据均提示其定位于叶绿体。综合以上证据,我们选取Phatr3_J36932 开展深入研究。
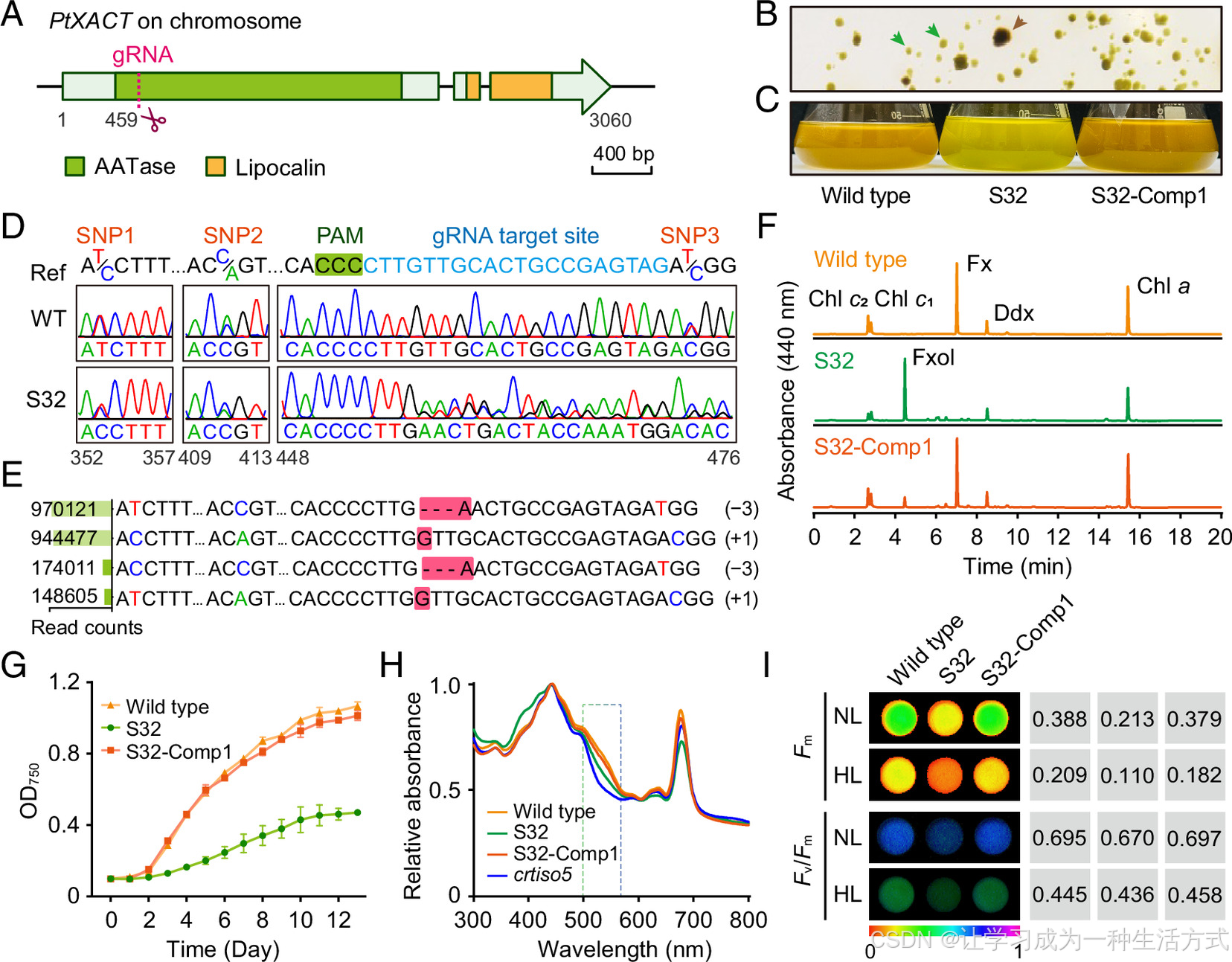
三角褐指藻 PtXACT 为岩藻黄质积累所必需。(A)PtXACT 基因位点(Phatr3_J36932 )结构示意图,其编码蛋白包含一个推定的醇乙酰转移酶(AATase)结构域 和一个可能参与疏水分子转运的脂运载蛋白结构域 。图中标示了用于 CRISPR/Cas9 基因编辑的向导 RNA(gRNA)靶位点。(B)PtXACT 敲除筛选中获得的代表性转化子;绿色箭头指示呈现绿色表型的突变株,棕色箭头指示具有野生型典型褐色的菌落。(C)野生型(WT)、PtXACT 突变体(S32)及回补株系(S32-Comp1)表型对比。(D)Sanger 测序验证野生型与 S32 突变体的基因型,数字表示 Phatr3_J36932 基因内的相对核苷酸位置。(E)通过深度测序获得的 S32 二倍体验证结果,证实 PtXACT 发生双等位杂合突变 。红色框标注 3 bp 缺失与 1 bp 插入事件;彩色碱基为单核苷酸多态性(SNP)。注:共观察到两种插入缺失类型,其与相邻 SNP 紧密连锁,证明为双等位基因编辑结果,排除了菌落为含不同插入缺失细胞混合物的可能。(F)野生型、S32 及 S32-Comp1 的色素 HPLC 色谱图。(G)正常光照条件(30 μmol photons m⁻² s⁻¹)下野生型、S32 与 S32-Comp1 的生长曲线。(H)室温下测定的全细胞吸收光谱,以 440 nm 最大吸收值进行归一化。(I)不同细胞株系经 40 分钟暗适应后的叶绿素荧光参数(每 200 μL 样品 1×10⁷ 个细胞)。NL 和 HL 为培养条件(非测量光):NL 正常光(30 μmol photons m⁻² s⁻¹),HL 强光(1000 μmol photons m⁻² s⁻¹),测量设置保持一致。
Phatr3_J36932 (XACT)为岩藻黄质积累与细胞正常生长所必需
在初步鉴定出 Phatr3_J36932 突变体后,对筛选得到的突变菌落进行两轮亚克隆。值得注意的是,在一块亚克隆平板上,部分菌落呈现明显的绿色表型 ,提示岩藻黄质生物合成可能受阻。选取代表性菌落命名为亚克隆 32(S32)并分离纯化。S32 在液体培养中仍维持绿色表型,因此被选作进一步研究材料。
色素谱分析显示,S32 突变体完全不积累岩藻黄质 ,但代偿性积累一种新色素。该色素保留时间更短,吸收光谱与岩藻黄质高度相似,符合缺失乙酰基的特征。对新色素的质谱分析验证了这一结论:高分辨质谱检测到 m/z 617.4204 [M+H]⁺ 和 599.4100 [M−H₂O+H]⁺ 正离子峰,对应分子式 C₄₀H₅₆O₅。观察到的 [M−2H₂O+H]⁺ 离子表明该新类胡萝卜素在 3 位与 3'位均含有羟基,其碎裂模式与岩藻黄质脱去乙酸和一分子水后的预期结果一致。综合以上数据,该新色素被鉴定为岩藻黄质的去乙酰化衍生物 ------岩藻黄质醇 。
随后对 S32 进行基因型鉴定。对 gRNA 靶标区域 PCR 扩增并 Sanger 测序,结果出现混合峰信号,提示 S32 为纯化的杂合突变体或仍为非克隆群体。对 S32 再次亚克隆获得的衍生株系测序结果均与原始 S32 一致,支持其为杂合突变体。进一步对靶标区域深度测序证实其杂合状态,发现两种独立的插入缺失突变:3 bp 缺失(−3 bp)和 1 bp 插入(+1 bp),且无野生型序列残留,证明 Phatr3_J36932 编辑成功。
−3 bp 变异通常不会改变阅读框,对蛋白翻译影响较小。但在 Phatr3_J36932 中,该突变导致第 153 位亮氨酸(L153)缺失,并使第 154 位组氨酸突变为天冬酰胺(H154N)。序列比对显示,L153 在不同物种同源蛋白及醇乙酰转移酶(AATase)家族中高度保守。后续功能实验证实该突变会导致酶活性完全丧失。基于以上结果,我们开展遗传回补实验,以验证 S32 突变体的表型改变是否特异性由该等位基因突变引起。
将 Phatr3_J36932 cDNA 转入 S32 菌株进行回补,获得多株色素恢复褐色的转化子,PCR 验证了回补载体的整合。选取 3 个代表性回补株系 S32-Comp1、S32-Comp2、S32-Comp3,其表型均得到恢复,HPLC 分析进一步证实岩藻黄质积累恢复。该遗传回补实验证明,S32 的表型缺陷特异性源于 Phatr3_J36932 功能丧失。因此,我们将该基因命名为叶黄素乙酰转移酶(XACT) ,其酶活后续经体外实验验证。
如上所述,PtXACT 包含两个独立结构域:N 端乙酰转移酶结构域与 C 端类脂运载蛋白结构域。为探究脂运载蛋白结构域是否为功能必需,我们在 S32 突变体中分别单独表达两个结构域。结果显示,乙酰转移酶结构域(结构域 1)可完全回补野生型表型,功能与全长蛋白相当;相反,即使通过转运肽将脂运载蛋白结构域(结构域 2)靶向叶绿体,也无法回补色素缺陷。上述结果表明,在岩藻黄质生物合成中,脂运载蛋白结构域对 PtXACT 功能并非必需 。
与岩藻黄质的捕光功能一致,xact 突变体(S32)生长速率下降,而回补株系可恢复至野生型水平。光谱数据显示,S32 在 550--580 nm 绿光区吸收能力降低,与同样缺失岩藻黄质的 crtiso5 突变体表型相似。叶绿素荧光检测显示,突变体最大荧光(Fm)下降,但 Fv/Fm 比值基本不变,表明其捕光天线尺寸减小,而非光化学效率受损。
XACT 可乙酰化岩藻黄质合成途径中的多个下游前体
xact 突变体缺失岩藻黄质并积累岩藻黄质醇,提示 PtXACT 可能催化岩藻黄质醇的乙酰化。为从生化上验证该功能,在大肠杆菌中表达并纯化 N 端带麦芽糖结合蛋白(MBP)标签的重组全长 PtXACT。体外酶活实验表明,在乙酰辅酶 A 存在下,PtXACT 可特异性将岩藻黄质醇转化为岩藻黄质;在缺失 PtXACT 或乙酰辅酶 A 的对照组中均未检测到产物生成。质谱分析显示,底物与产物之间 [M+H]⁺ 与 [M−H₂O+H]⁺ 离子峰均增加 42 Da,证实发生了羟基乙酰化修饰。
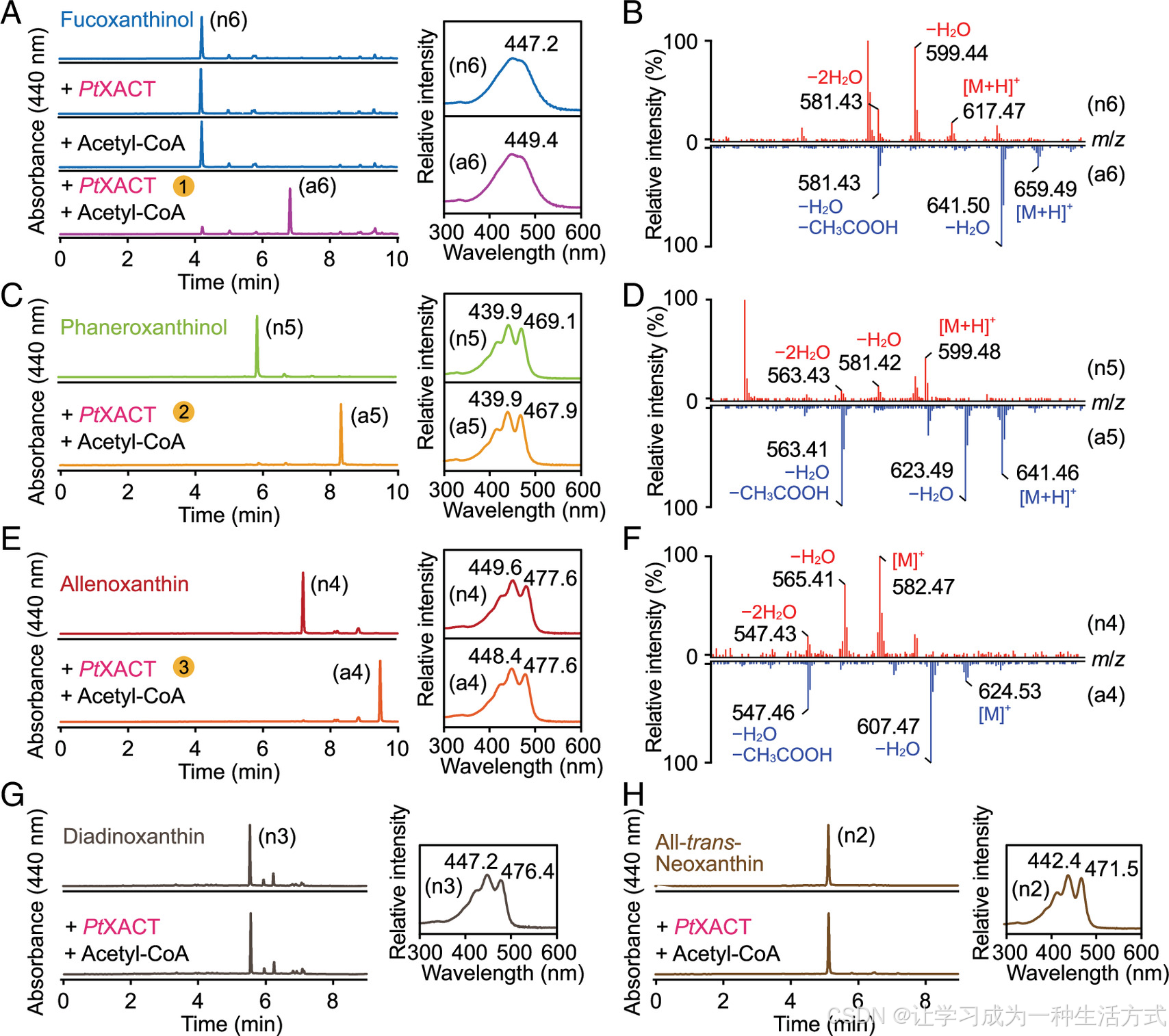
利用多种叶黄素底物对 PtXACT 进行体外酶学表征 。(A)PtXACT 催化岩藻黄质醇转化为岩藻黄质。右图为二极管阵列检测器(PDA)光谱,显示乙酰化后发色团特征保持不变,但色素极性发生改变。(B)单四极杆质谱(QDA)图谱对比:底物(红色)与对应乙酰化产物(蓝色)。(C)以显花黄质醇(n5)为底物的重组 PtXACT 酶促反应。(D)显花黄质醇(红色)与其乙酰化产物(蓝色)的 QDA 质谱对比。(E)以丙二烯叶黄素(n4)为底物的重组 PtXACT 酶促反应。(F)丙二烯叶黄素(红色)与其乙酰化产物(蓝色)的 QDA 质谱对比。此处观察到分子离子峰 [M]⁺而非质子化分子离子峰 [M+H]⁺,该现象在其他类胡萝卜素中已有报道。(G)以硅甲藻黄素(n3)为底物的重组 PtXACT 酶促反应。(H)以全反式新黄质(n2)为底物的重组 PtXACT 酶促反应。相应色素编号详见补充附录表 S1。图中所有酶促反应均孵育 2 小时。
XACT 属于醇乙酰转移酶(AATase)家族 (PANTHER 编号:PTHR28037;补充附录图 S3)。植物中存在另一类醇酰基转移酶,有时也缩写为 "AAT",但在功能与系统发育上均与 AATase 不同,归属于 PANTHER 家族 PTHR31623。该家族包含多种酶类,如 BAHD 酰基转移酶;尽管 PTHR28037 与 PTHR31623 家族均含有保守的 "HXXXD" 催化基序,但其底物特异性差异显著。植物醇酰基转移酶可识别多种辅酶 A 活化的酰基供体;相比之下,含 PTHR28037 结构域的酵母酶则严格偏好乙酰辅酶 A。我们对 PtXACT 的酰基供体偏好性进行了检测,发现其同样对乙酰辅酶 A 具有严格特异性,在所有测试酰基辅酶 A 底物中,仅对丙酰辅酶 A 表现出极微弱活性(补充附录图 S6)。这种狭窄的底物偏好性直接决定了类胡萝卜素产物仅发生乙酰化修饰。
我们进一步表达了仅含结构域 1 的截短型 PtXACT,其 N 端带有 MBP 标签。体外酶活实验证实,该结构域单独即可催化岩藻黄质醇转化为岩藻黄质,与体内回补实验结果一致(补充附录图 S7)。如前所述,−3 bp 突变导致保守位点 L153 缺失及 H154N 替换。为评估 L153 的功能重要性,我们分别纯化了缺失 L153 的全长蛋白与单独乙酰转移酶结构域。体外活性检测显示,两种变体均无法催化岩藻黄质醇的乙酰化(补充附录图 S7),表明 L153 对 PtXACT 的催化活性至关重要。
此前岩藻黄质生物合成途径模型认为,乙酰转移酶主要作用于丙二烯叶黄素;但本研究发现,xact 突变体(S32)中积累的是岩藻黄质醇而非丙二烯叶黄素。该结果提示,乙酰化步骤相对于其他下游修饰的顺序具有灵活性。因此我们提出假说:(1)XACT 对多种类胡萝卜素中间体具有更广的底物特异性;(2)后续酶促步骤可对未乙酰化的前体进行催化。
为验证上述假说,我们检测了 PtXACT 对一系列类胡萝卜素底物的活性。从已表征的突变体中分离从紫黄质到岩藻黄质的各类色素,经皂化去除乙酰基后,通过制备型 HPLC 纯化(补充附录图 S8)。体外实验表明,PtXACT 可将 7',8'- 二脱氢新黄质(本研究命名为显花黄质醇,Phxol)乙酰化生成显花黄质,质谱结果证实了该转化(图 3C)。定鞭藻黄质的去乙酰化形式(即丙二烯叶黄素)以及非天然的 9'- 顺式新黄质也可被 PtXACT 有效乙酰化(图 3E,补充附录图 S9A)。产物质谱分析显示出乙酰化特征性的质量偏移,同时存在与两端羟基去乙酰化及脱水相符的中性丢失峰(图 3B、D,补充附录图 S9B)。
我们进一步以全反式新黄质为候选底物进行检测。XACT 对其乙酰化理论上应生成甲藻黄质,而该类胡萝卜素及其衍生物在三角褐指藻中并不天然积累(图 1)。与此一致,体外实验显示 PtXACT 对全反式新黄质无催化活性。同样,硅甲藻黄素及上游前体紫黄质均不能作为乙酰化底物(图 3G,补充附录图 S9C)。综上结果表明,XACT 的底物特异性严格限定于岩藻黄质生物合成途径的后期中间体 。
岩藻黄质通过灵活的非线性途径合成
如前所述,xact 突变体积累岩藻黄质醇而非丙二烯叶黄素,提示在丙二烯叶黄素至岩藻黄质之间的生物合成途径中存在多个分支点。为探究未乙酰化的叶黄素(如丙二烯叶黄素、显花黄质醇)能否分别被 ZEP1 或 CRTISO5 催化生成岩藻黄质醇,我们通过对纯化色素进行皂化制备了去乙酰化类胡萝卜素底物。体外实验表明,添加辅因子后,PtZEP1 可将丙二烯叶黄素转化为显花黄质醇(图 4A);而在还原型黄素腺嘌呤二核苷酸(FADred)为辅因子的条件下,PtCRTISO5 可催化显花黄质醇转化为岩藻黄质醇(图 4A)。
尽管此前岩藻黄质生物合成途径被描述为从丙二烯叶黄素到岩藻黄质的线性过程,但本研究结果表明,CRTISO5 与 ZEP1 均可催化未乙酰化底物。这些发现支持对三角褐指藻岩藻黄质合成途径的修订模型,即存在三条潜在分支通路 ,乙酰化可发生在丙二烯叶黄素、显花黄质醇或岩藻黄质醇任一阶段(图 1、图 4B)。
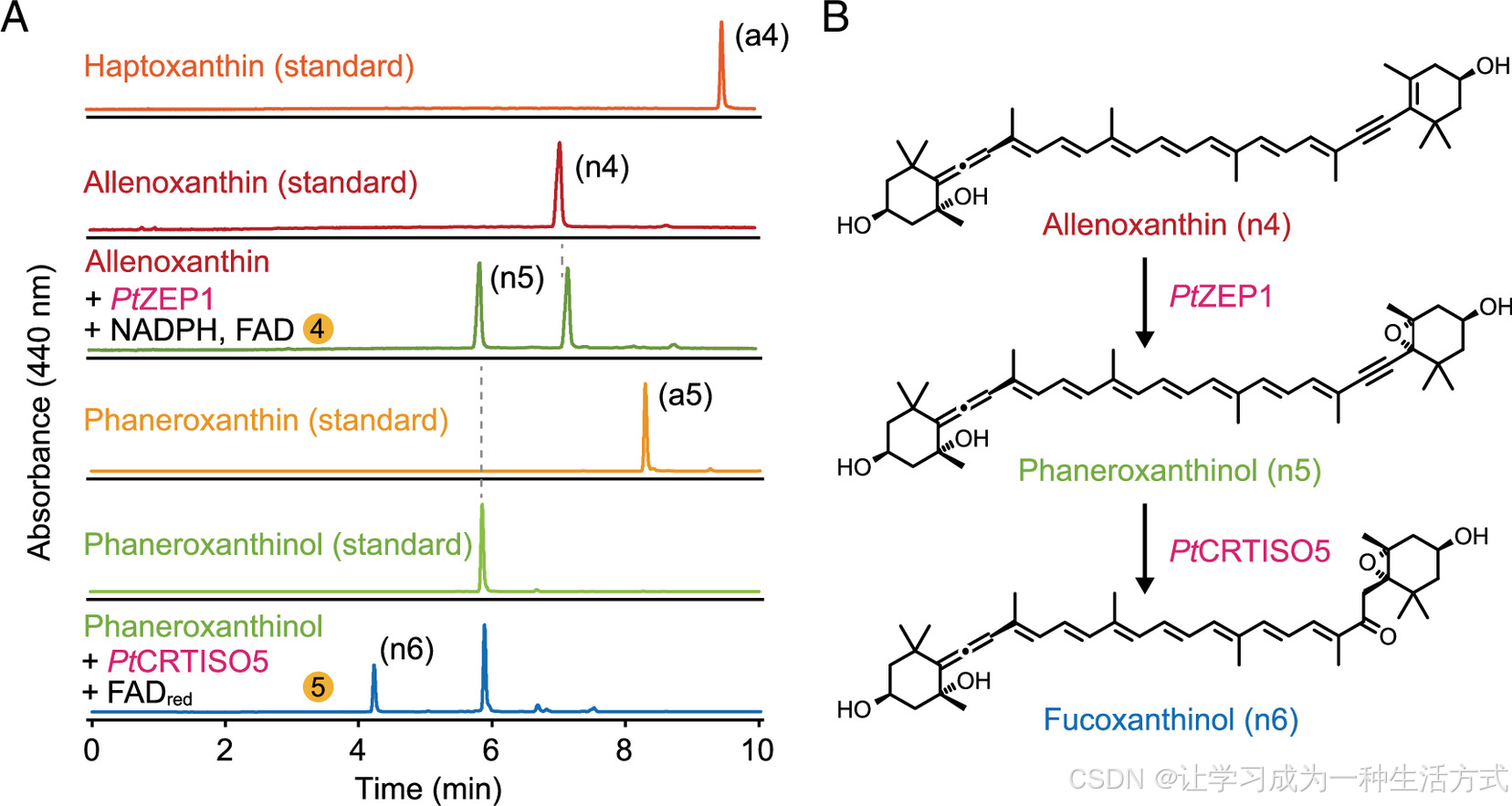
PtZEP1 与 PtCRTISO5 在体外催化未乙酰化类胡萝卜素的转化 (A)体外酶促实验证实:PtZEP1 催化丙二烯叶黄素(n4)转化为显花黄质醇(n5),而 PtCRTISO5 催化显花黄质醇(n5)转化为岩藻黄质醇(n6)。(B)PtZEP1 和 PtCRTISO5 在岩藻黄质生物合成中,对未乙酰化中间体催化作用的模式图。相应色素编号详见补充附录表 S1。本图中所有酶促反应均孵育 2 小时。
XACT 专一性保守于积累乙酰化类胡萝卜素的有色藻门类群中
鉴于乙酰化类胡萝卜素在有色藻门生物中广泛存在,我们探究其合成是否由一个保守的蛋白家族催化。以 PtXACT 的乙酰转移酶结构域(结构域 1)为查询序列,在 UniProt 等公共基因组与转录组数据库中进行 BLAST 搜索,E 值阈值设为 1e⁻⁵。
结果在硅藻及其他光合不等鞭毛类、定鞭藻和多种甲藻中鉴定到 PtXACT 的直系同源基因(E 值<1e⁻²⁰)。值得注意的是,在不合成乙酰化类胡萝卜素的类群中未发现 XACT 同源基因,包括陆生植物、绿藻、红藻和隐藻。此外,在非光合不等鞭毛类如卵菌中也未检测到 XACT 基因;卵菌虽是光合褐藻与硅藻的近缘类群,但不合成类胡萝卜素(数据集 S3)。蓝细菌是唯一检出同源序列的其他进化支,E 值介于 2e⁻¹¹ 至 3e⁻⁴之间。该蓝细菌蛋白大概率不参与类胡萝卜素合成,一方面其序列不普遍保守,另一方面在蓝细菌主要类群聚球藻目中几乎不存在。
以蓝细菌序列为外类群构建的系统发育树证实,藻类 XACT 家族构成一个单系支(图 5)。对代表性物种 XACT 蛋白的定位预测显示,其普遍定位于质体(数据集 S4)。在有色藻门藻类中,核编码的质体蛋白通过 N 端双组分前导肽 转运至质体基质,该结构由信号肽与叶绿体转运肽依次组成。利用 9 种不同定位预测工具分析显示,全部 18 条序列均含有信号肽;可进一步识别叶绿体转运肽的 HECTAR 与 MULocDeep 工具预测,18 条 XACT 序列中有 14 条含转运肽。对更大范围 XACT 蛋白的结构域分析进一步揭示出类群特异性差异:脂运载蛋白结构域 存在于甲藻及硅藻亚门(包括硅藻及其近缘类群)的 XACT 中,而定鞭藻与金藻亚门(如褐藻及其近缘类群)的 XACT 则缺失该结构域。
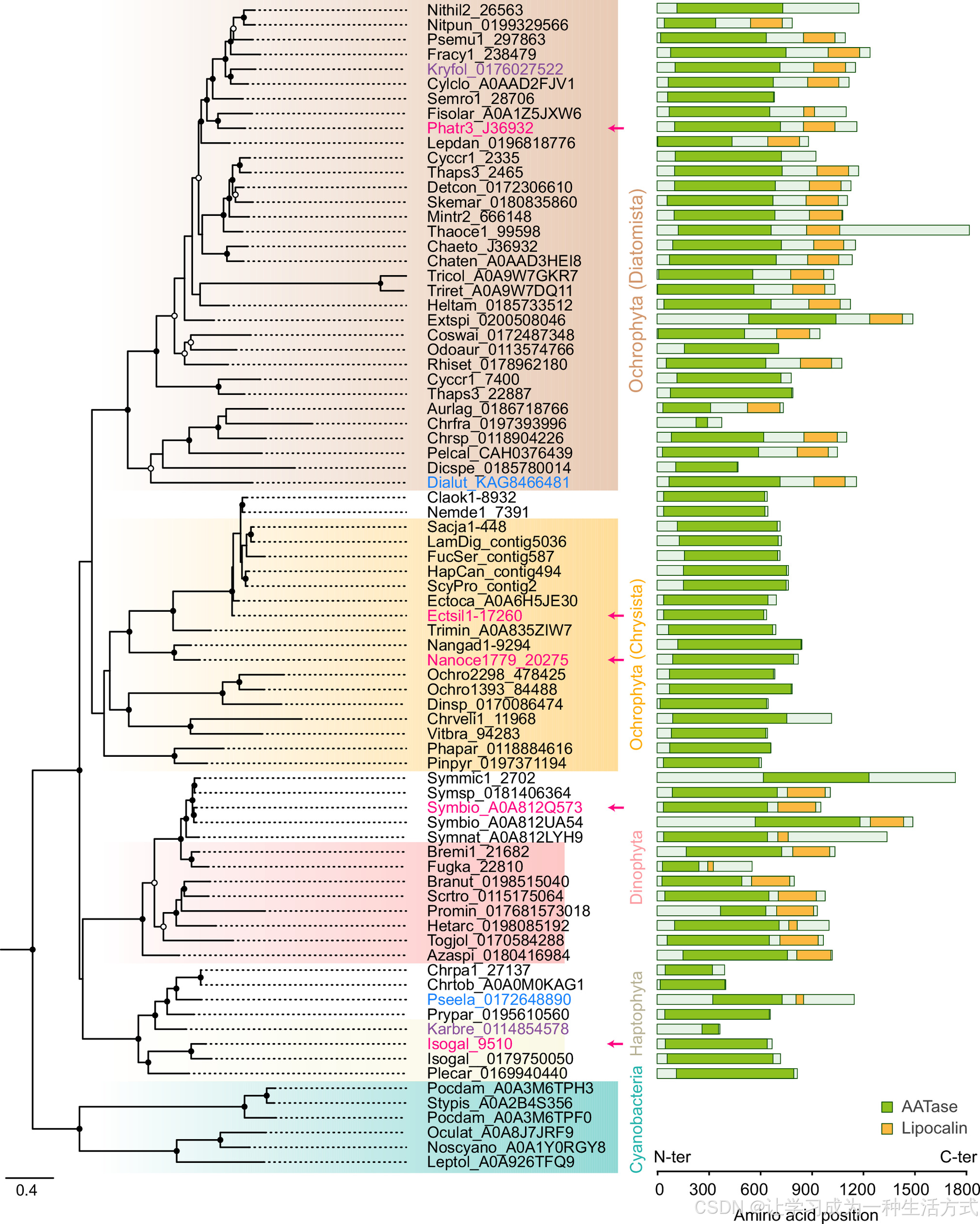
采用 LG + F + I + R5 替换模型,基于 74 个物种共 76 条 XACT 同源序列的比对结果(952 个比对氨基酸位点)构建最大似然树 。主要节点的自展检验值(100 次重复)以黑点(>90%)和白点(>75%)标示。利用 Interproscan 进行结构域预测,结构域注释来自 PANTHER(PTHR28037,醇乙酰转移酶)和 SUPERFAMILY(SSF50814,脂运载蛋白)数据库。品红色箭头 指示用于 XACT 同源基因功能验证的蛋白(图 7)。蓝色标注的登录号为不属于指定类群的序列。紫色标注的 ** 卡尔藻(Karenia )与 隐甲藻(Kryptoperidinium )** 序列位置与其三级质体起源一致。以蓝细菌支为外类群重新生根。物种名称与序列登录号见数据集 S3。
微拟球藻中敲除 XACT 会破坏类胡萝卜素合成并导致新黄质积累
XACT 在有色藻门藻类中的广泛保守性表明:(1)XACT 在多种有色藻门类群的乙酰化类胡萝卜素合成中普遍发挥作用;(2)底物特异性差异是这些类群捕光类胡萝卜素多样性的内在原因。为对金藻亚门 藻类的 XACT 同源基因进行功能解析,我们选取真眼点藻纲的有色藻类 ------** 微拟球藻(Nannochloropsis )开展进一步研究。值得注意的是,微拟球藻不合成岩藻黄质,而是积累其他乙酰化类胡萝卜素,主要为 无隔藻黄质 - 3 - 乙酸酯 - 19'- 酰基酯(Vaux)** 及紫黄质。已有研究表明,微拟球藻通过乙酰化步骤将新黄质转化为甲藻黄质,提示存在一个未鉴定的乙酰转移酶。成熟的遗传操作体系使微拟球藻成为研究 XACT 酶与其类胡萝卜素途径功能共进化的理想体系。
为直接解析微拟球藻 XACT 同源基因(NoXACT,No09G02500 )的功能,我们利用 CRISPR/Cas9 介导双链断裂,结合携带抗生素抗性基因的供体 DNA 片段同源定向整合,构建了多株海洋微拟球藻 XACT 突变株(补充附录,材料与方法)。基因型鉴定证实抗性盒与同源臂成功插入,NoXACT 被有效敲除(图 6A、B)。对NoXACT 敲除突变株的色素谱分析显示,Vaux 完全消失 ,同时大量积累一种特征化合物(图 6C);紫外 - 可见吸收与质谱分析鉴定该物质为全反式新黄质 (图 6C)。上述结果证实,NoXACT 是 Vaux 生物合成所必需 ,且全反式新黄质为该途径的前体。我们进一步推测,新黄质的乙酰化产物 ------ 甲藻黄质,可能是该途径的代谢中间体(图 1)。但不能排除 Vaux 合成途径同样存在非线性分支的可能,类似于硅藻中岩藻黄质的分支合成途径。
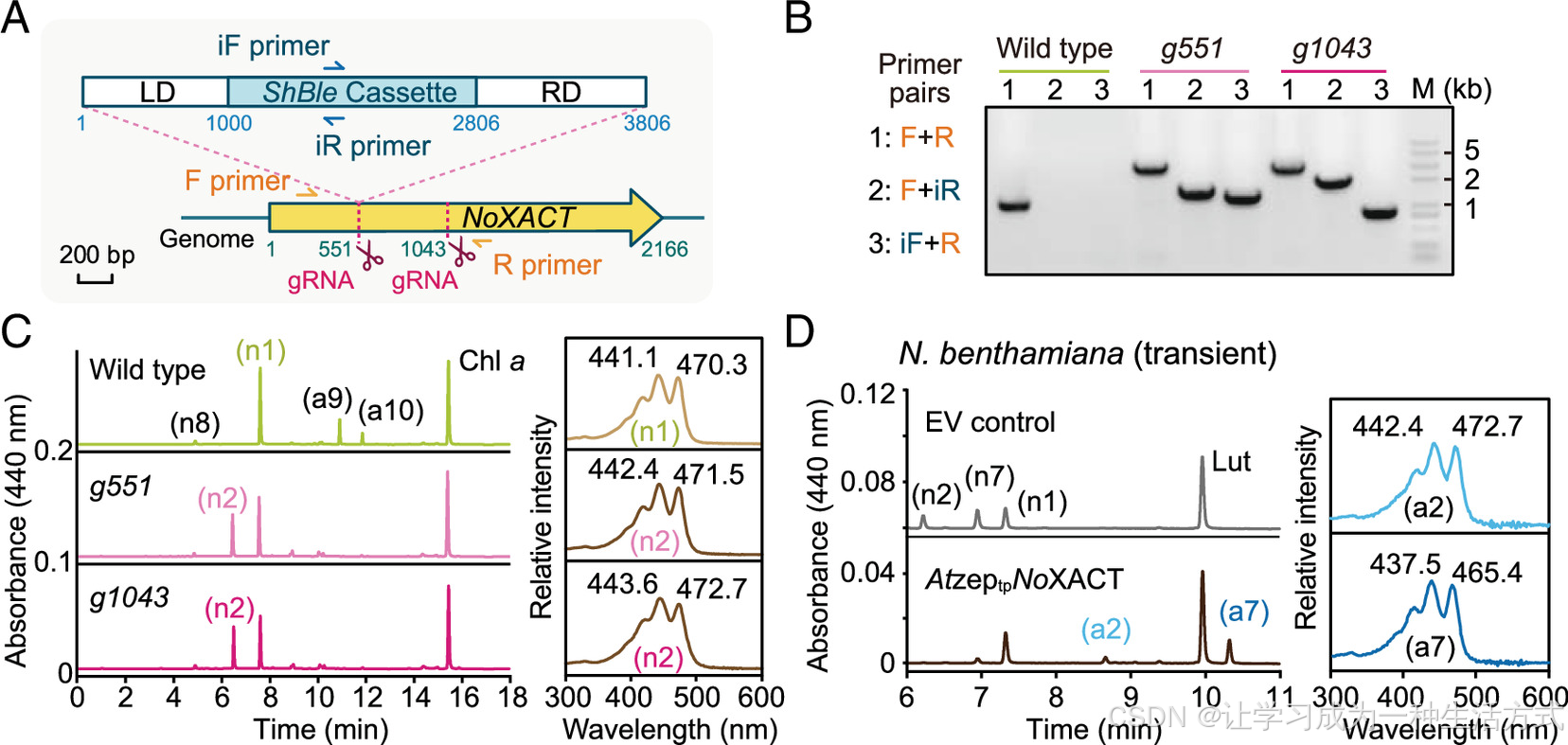
海洋微拟球藻 NoXACT 敲除突变体的构建与表征 (A)CRISPR-Cas9 介导 1.8 kb 腐草霉素抗性(ShBle )表达盒插入 NoXACT 基因外显子区域的示意图(突变体 g551);同时标注了突变体 g1043 的插入位点。LD:左侧同源臂(1 kb);RD:右侧同源臂(1 kb)。橙色与蓝色箭头表示用于野生型(WT)及突变体基因型鉴定的引物结合位置。(B)使用(A)中引物对扩增产物的琼脂糖凝胶电泳图。1.4 kb 条带为野生型 NoXACT 等位基因;更大条带为插入抗性盒的突变等位基因。引物对 2 和 3 跨基因组--抗性盒连接处,证实整合成功。(C)两个独立 NoXACT 敲除株系 g551、g1043 与野生型的色素谱对比。右图为特征色素的二极管阵列检测器(PDA)光谱。可见突变体中两种无隔藻黄质酯(a9、a10)完全消失,并出现全反式新黄质(n2)积累。(D)农杆菌介导 NoXACT 在本氏烟草叶片中瞬时表达的色素谱。为保证叶绿体定位,NoXACT 自身转运肽替换为拟南芥玉米黄质环氧化酶(AtZEP)的基质靶向信号。EV:空载体(阴性对照)。右图为特征色素的 PDA 光谱。未标注色素编号详见补充附录表 S1。
为进一步验证 NoXACT 的酶活性,我们采用两种独立策略:(1)在天然积累新黄质异构体的本氏烟草中进行异源表达;(2)重组蛋白体外酶活实验。NoXACT 在烟草叶片中瞬时表达后,出现两个新色素峰,结合光谱特征与保留时间鉴定为全反式甲藻黄质 与9′- 顺式甲藻黄质 。同时伴随内源新黄质含量下降,新黄质 / 紫黄质比值降低。尽管在植物体内的转化效率有限,上述结果仍证实 NoXACT 在异源系统中具有功能活性,并展现出将藻类类胡萝卜素合成途径改造至陆生植物以实现营养强化的潜力。
最后,为获得直接生化证据并与 PtXACT 进行比较,我们使用重组 NoXACT 蛋白完成了体外酶活分析,详见下文。
不同物种类胡萝卜素乙酰转移酶同源蛋白的底物特异性分化
为对 NoXACT 及其他难以遗传操作的有色藻门类群来源的 XACT 家族成员进行催化功能表征,我们利用重组蛋白开展一系列体外酶活实验。选取一系列丙二烯型类胡萝卜素底物 ,包括岩藻黄质醇、显花黄质醇、丙二烯叶黄素、全反式新黄质及 9'- 顺式新黄质,评估代表性 XACT 同源蛋白的底物偏好性。前四种色素均为海洋主要类胡萝卜素的已知前体。测试的酶包括:PtXACT(三角褐指藻)、NoXACT(微拟球藻)、IgXACT(定鞭藻球等鞭金藻)、StXACT(甲藻共生藻)及 EsXACT(褐藻长囊水云)。所有酶均在大肠杆菌中异源表达并纯化。
体外实验结果显示(图 7):PtXACT 优先催化丙二烯叶黄素(n4)和显花黄质醇(n5),也可微弱催化岩藻黄质醇(n6)生成岩藻黄质(a6);但未检测到 9'- 顺式新黄质乙酰化产物(9'- 顺式甲藻黄质,a7)或全反式新黄质乙酰化产物(甲藻黄质,a2),与此前单一底物实验结果一致。定鞭藻类(如球等鞭金藻)主要积累岩藻黄质衍生物,与硅藻相似,均不含甲藻黄质。与之相符,IgXACT 的底物谱与 PtXACT 高度相似,可催化岩藻黄质醇、显花黄质醇和丙二烯叶黄素,但不作用于全反式新黄质,反映了定鞭藻中天然不存在甲藻黄质的代谢特征。
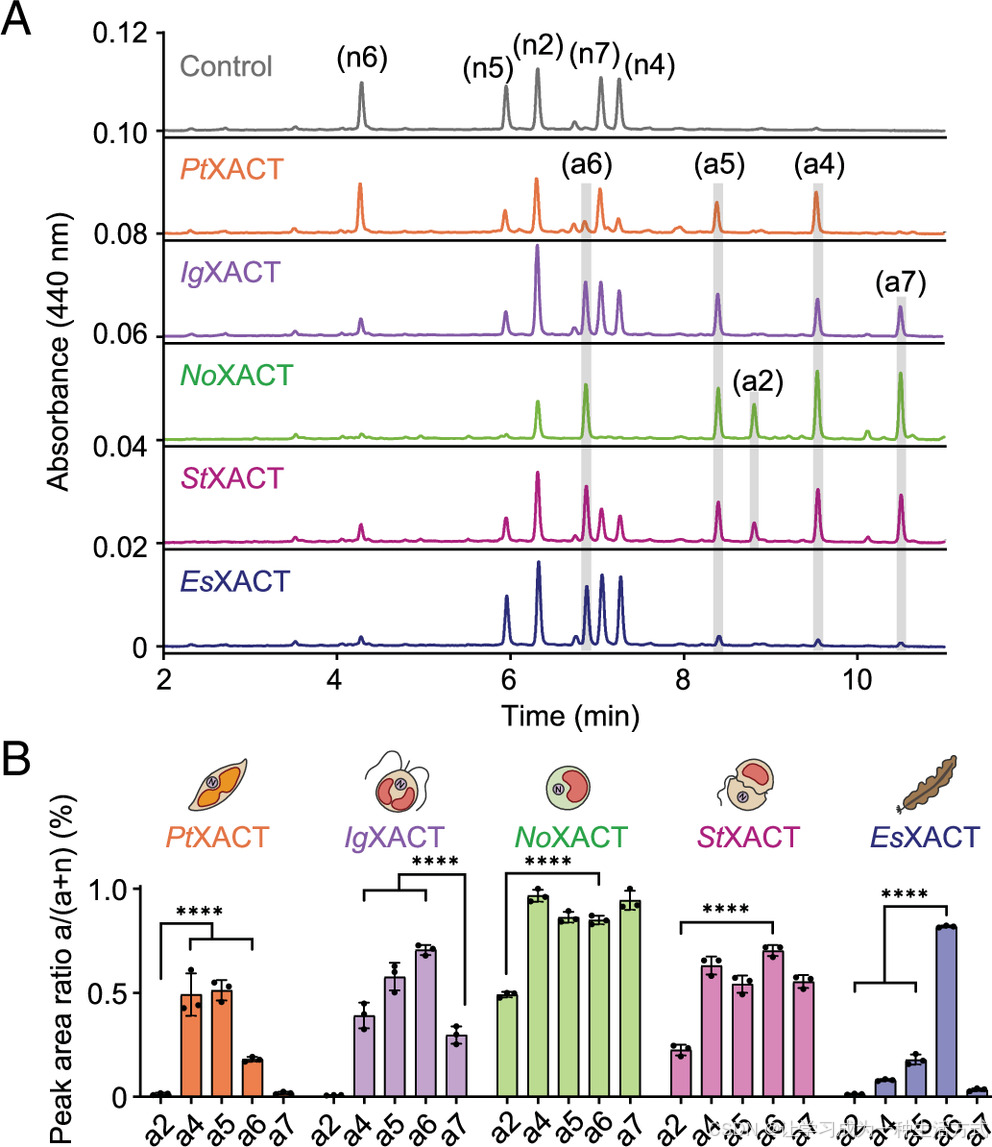
以5 种丙二烯型类胡萝卜素混合物 为底物,对 XACT 同源蛋白进行体外酶促分析(n - 峰)。(A)底物混合物与不同物种来源的 XACT 同源蛋白孵育 30 分钟后,反应产物的 HPLC 色谱图。产物峰(a - 峰)以阴影背景标出。(B)XACT 同源蛋白底物偏好性的定量分析。产物生成效率以产物峰面积占总峰面积(产物 + 剩余底物)的比值表示,基于 HPLC 定量计算。数据为平均值 ± 标准差(n=3)。n2:全反式新黄质;n4:丙二烯叶黄素;n5:显花黄质醇;n6:岩藻黄质醇;n7:9'- 顺式新黄质;a2:全反式甲藻黄质;a4:定鞭藻黄质;a5:显花黄质;a6:岩藻黄质;a7:9'- 顺式甲藻黄质。
如前所述,真眼点藻纲(如微拟球藻)不合成岩藻黄质,而是合成无隔藻黄质酯(Vaux),推测以全反式新黄质 为前体。同样,包括共生藻在内的许多甲藻合成多甲藻素而非岩藻黄质,研究认为其以全反式新黄质为前体,经全反式甲藻黄质中间体合成。与这些藻类各自的类胡萝卜素合成途径相符,NoXACT 和 StXACT 对全反式新黄质表现出强催化活性 ,而 PtXACT 和 IgXACT 对该底物无 detectable 活性(图 7)。
除对全反式新黄质的特异性差异外,XACT 酶还表现出一定的催化杂泛性。例如,多个成员对 9'- 顺式新黄质(n7)具有活性,该物质在陆生植物、绿藻及含绿藻起源次生质体的藻类中普遍存在,但在红藻和有色藻门生物中缺失。此外,NoXACT 和 StXACT 也可催化丙二烯叶黄素(n4)、显花黄质醇(n5)和岩藻黄质醇(n6)(图 7)。由于这些底物并非这些酶来源生物的天然代谢物,结果表明在真眼点藻和甲藻中,对这类次级催化活性缺乏明显的选择压力。但与 PtXACT 的结果一致,其他物种的 XACT 均不能以紫黄质或硅甲藻黄素为底物,说明 XACT 对底物具有严格特异性:仅识别在 3 - 羟基 -β- 紫罗酮环上具有C6--C8 丙二烯结构 、并可被乙酰化的叶黄素。
与硅藻类似,褐藻以岩藻黄质为主要捕光色素,但缺少硅藻特有的合成酶。目前提出了两条从新黄质合成岩藻黄质的可能途径:一条是先进行水合与烯丙位氧化,再发生乙酰化;另一条是先乙酰化生成甲藻黄质,再进行水合 / 烯丙位氧化。本研究发现,EsXACT 可高效乙酰化岩藻黄质醇(n6) (在所测底物中为其偏好底物),但对反式新黄质(n2)无活性(图 7),这一结果强烈支持第一条途径是长囊水云岩藻黄质合成的主要路线 。尽管不能完全排除长囊水云或其他褐藻中存在次要替代途径,但本研究指出了下一关键研究目标:鉴定负责将新黄质转化为岩藻黄质醇的未知氧化还原酶 (图 1)。
为验证上述结论,我们使用单一底物测定了全部 5 种 XACT 酶的表观米氏常数K ₘ与最大反应速率V ₘₐₓ,并通过饱和曲线双曲线拟合与 Lineweaver--Burk 双倒数图线性拟合进行数据分析(表 1,补充附录表 S3、图 S12)。偏好性底物通常表现为更高的结合亲和力(更低的K ₘ)或更快的催化速率(更高的V ₘₐₓ)。当多种底物竞争酶活性中心时,可通过比较专一性常数k cat/K ₘ评估相对转化效率,在酶浓度固定时,该值与V ₘₐₓ/K ₘ成正比。通过计算每种底物的V ₘₐₓ/K ₘ,并以最大值为基准进行归一化,我们估算了相对底物特异性(表 1,补充附录表 S3)。总体而言,这些结果与混合底物实验结果一致(图 7,补充附录图 S13)。具体而言,PtXACT 对丙二烯叶黄素和显花黄质醇的特异性高于岩藻黄质醇;相反,EsXACT 对岩藻黄质醇表现出极强的特异性。需要注意的是,对于类胡萝卜素这类亲脂性化合物,增溶方式会显著影响底物可及性,从而改变体外测定的表观K ₘ和V ₘₐₓ值。
Apparent kinetic parameters of recombinant XACTs under conditions tested
|---------------------|--------------------------------|--------------------------------------|------------------------------------------------------------------------------------------------|-----------------------------|-------------------------------------------------------------|--------------------------|
| Enzyme | Substrates | K m (μM) | V max (nmol min −1 mg protein −1 ) | R 2 | V max / K m | Rel. specificity |
| Pt XACT | all-trans- Neoxanthin (n2) | N.D. | N.D. | N.D. | N.D. | N.D. |
| Pt XACT | Allenoxanthin (n4) | 1.97 | 0.33 | 0.96 | 0.17 | 100% |
| Pt XACT | Phaneroxanthinol (n5) | 0.57 | 0.08 | 0.98 | 0.14 | 86% |
| Pt XACT | Fucoxanthinol (n6) | 4.38 | 0.10 | 0.96 | 0.02 | 14% |
| Pt XACT-Domain1 | all-trans -Neoxanthin (n2) | N.D. | N.D. | N.D. | N.D. | N.D. |
| Pt XACT-Domain1 | Allenoxanthin (n4) | 5.47 | 1.75 | 1.00 | 0.32 | 89% |
| Pt XACT-Domain1 | Phaneroxanthinol (n5) | 0.26 | 0.09 | 0.92 | 0.36 | 100% |
| Pt XACT-Domain1 | Fucoxanthinol (n6) | 0.69 | 0.06 | 0.88 | 0.09 | 25% |
| Ig XACT | all-trans -Neoxanthin (n2) | N.D. | N.D. | N.D. | N.D. | N.D. |
| Ig XACT | Allenoxanthin (n4) | 60.80 | 8.63 | 0.97 | 0.02 | 88% |
| Ig XACT | Phaneroxanthinol (n5) | 4.87 | 0.10 | 0.96 | 0.02 | 100% |
| Ig XACT | Fucoxanthinol (n6) | 4.29 | 0.08 | 0.96 | 0.02 | 81% |
| No XACT | all-trans -Neoxanthin (n2) | 0.17 | 1.29 | 0.63 | 7.73 | 100% |
| No XACT | Allenoxanthin (n4) | 2.01 | 8.44 | 0.94 | 4.20 | 54% |
| No XACT | Phaneroxanthinol (n5) | 1.45 | 5.10 | 0.93 | 3.53 | 46% |
| No XACT | Fucoxanthinol (n6) | 10.28 | 47.86 | 0.97 | 4.66 | 60% |
| St XACT | all-trans -Neoxanthin (n2) | 0.05 | 0.03 | 0.35 | 0.55 | 100% |
| St XACT | Allenoxanthin (n4) | 6.04 | 0.45 | 0.91 | 0.07 | 14% |
| St XACT | Phaneroxanthinol (n5) | 0.63 | 0.21 | 0.83 | 0.33 | 61% |
| St XACT | Fucoxanthinol (n6) | 1.29 | 0.61 | 0.90 | 0.47 | 86% |
| Es XACT | all-trans -Neoxanthin (n2) | N.D. | N.D. | N.D. | N.D. | N.D. |
| Es XACT | Allenoxanthin (n4) | 137.30 | 5.32 | 0.90 | 0.04 | 1% |
| Es XACT | Phaneroxanthinol (n5) | 15.77 | 1.58 | 0.87 | 0.10 | 3% |
| Es XACT | Fucoxanthinol (n6) | 3.73 | 13.21 | 0.91 | 3.54 | 100% |
为探究部分 XACT 酶中脂运载蛋白结构域 的功能意义,我们比较了全长 PtXACT 与仅保留醇乙酰转移酶结构域(结构域 1)的截短体的催化特性。尽管缺失脂运载蛋白结构域会使K ₘ值发生偏移,更有利于结合显花黄质醇与岩藻黄质醇,但同时丙二烯叶黄素的V ₘₐₓ也有所上升,使得 PtXACT 整体的底物偏好谱基本未发生改变 (表 1)。后续研究应进一步解析 AATase 结构域自身序列如何调控底物选择性。鉴于脂运载蛋白已知可结合小分子配体,我们强调该结构域在体内仍可能行使重要的调控功能 ;而在本研究的体外实验中,因缺乏天然配体,这类调控作用可能被掩盖。因此,未来工作需要鉴定 PtXACT 脂运载蛋白结构域的内源配体,并验证配体结合是否会调节其 AATase 活性。
综上,本研究结果表明,XACT 酶底物特异性的进化分化 塑造了不同藻类谱系类胡萝卜素合成途径的多样性。XACT 同源蛋白呈现出的谱系特异性底物偏好,决定了各类群捕光色素的组成特征,进而推动了这些生物对多样海洋环境的适应。
材料与方法
完整实验流程详见补充附录 "材料与方法"。简要说明如下:藻类菌株在特定培养条件下培养;利用 CRISPR/Cas9 技术构建三角褐指藻的靶向基因敲除株与回补株,以及海洋微拟球藻的敲除突变株。采用 HPLC 测定色素组成;重组蛋白在大肠杆菌中异源表达、纯化后,使用纯化底物进行体外酶活与动力学分析。功能验证包括在本氏烟草中进行瞬时表达。所有产物均通过二极管阵列检测器(PDA)或质谱进行鉴定。对突变体的生理表征包括生长测定与叶绿素荧光检测。采用最大似然法构建系统发育树以分析进化关系,并使用合理的重复数据集进行统计学显著性检验。
数据、材料与软件获取
S32 突变体与 S32-Comp 回补株可直接向通讯作者索取,无需材料转移协议。系统发育树文件及包含序列与序列比对的相关文件已上传至 Zenodo 平台(https://zenodo.org/records/17180345)。其余所有数据均在正文或支撑信息中提供。