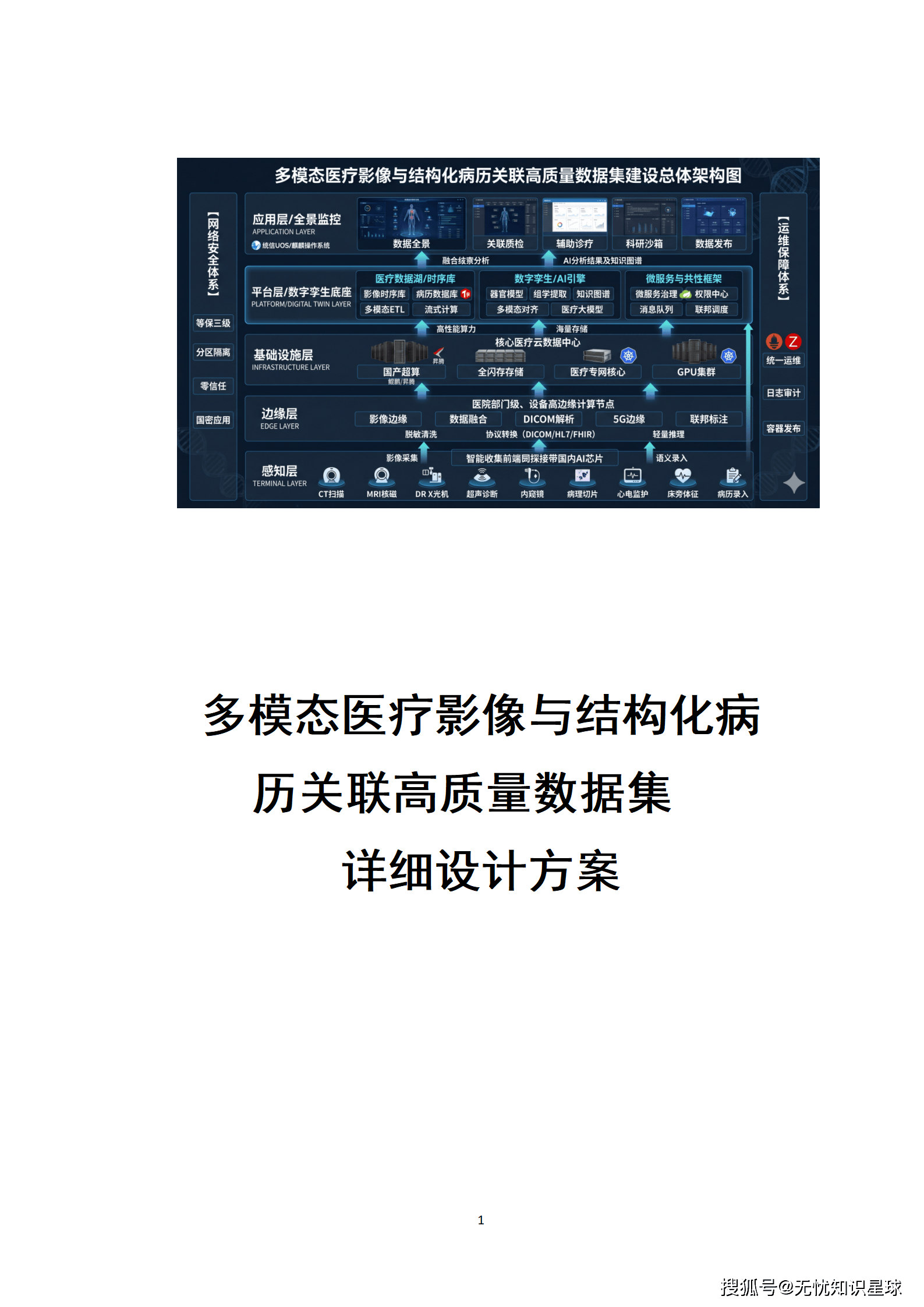
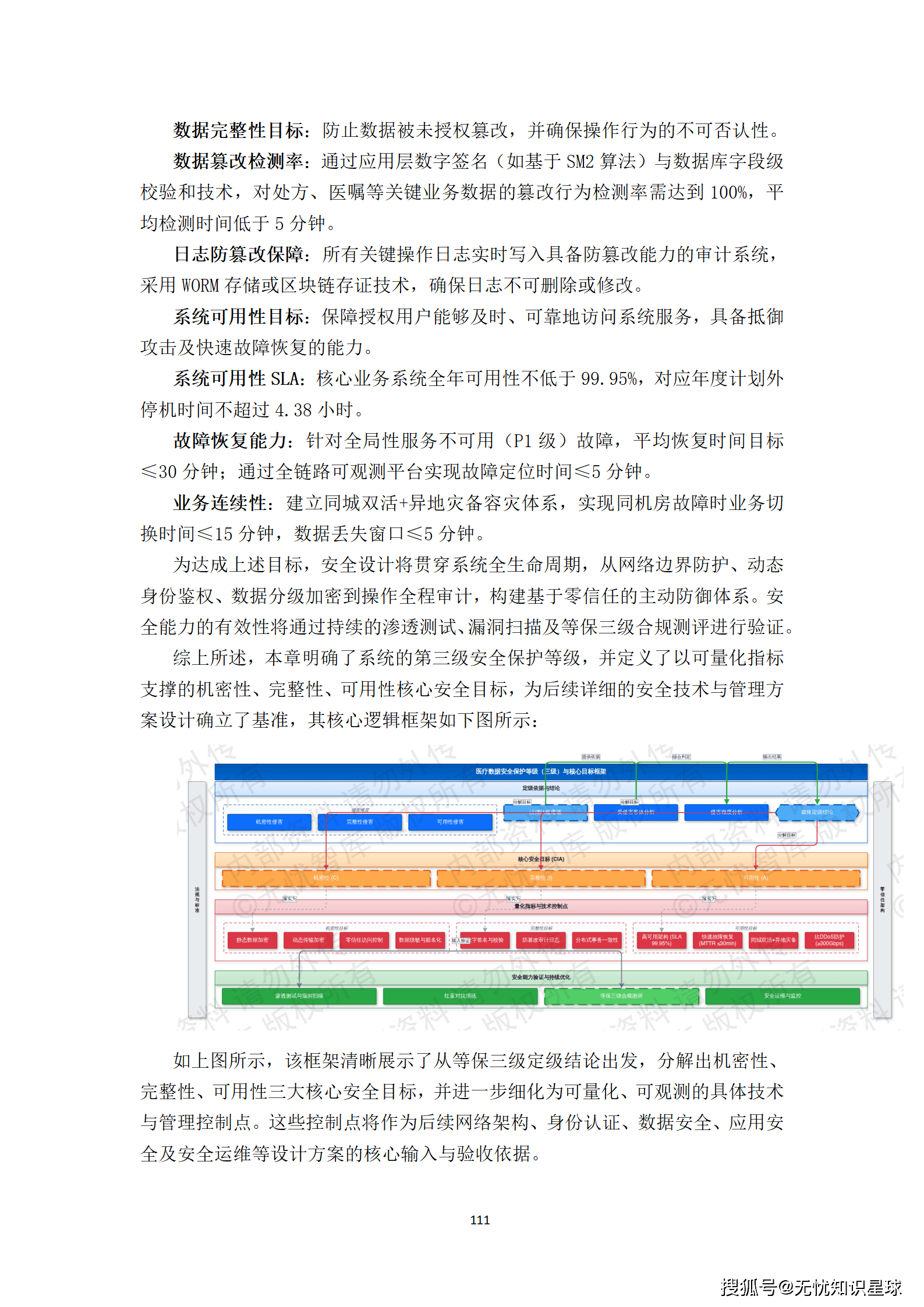
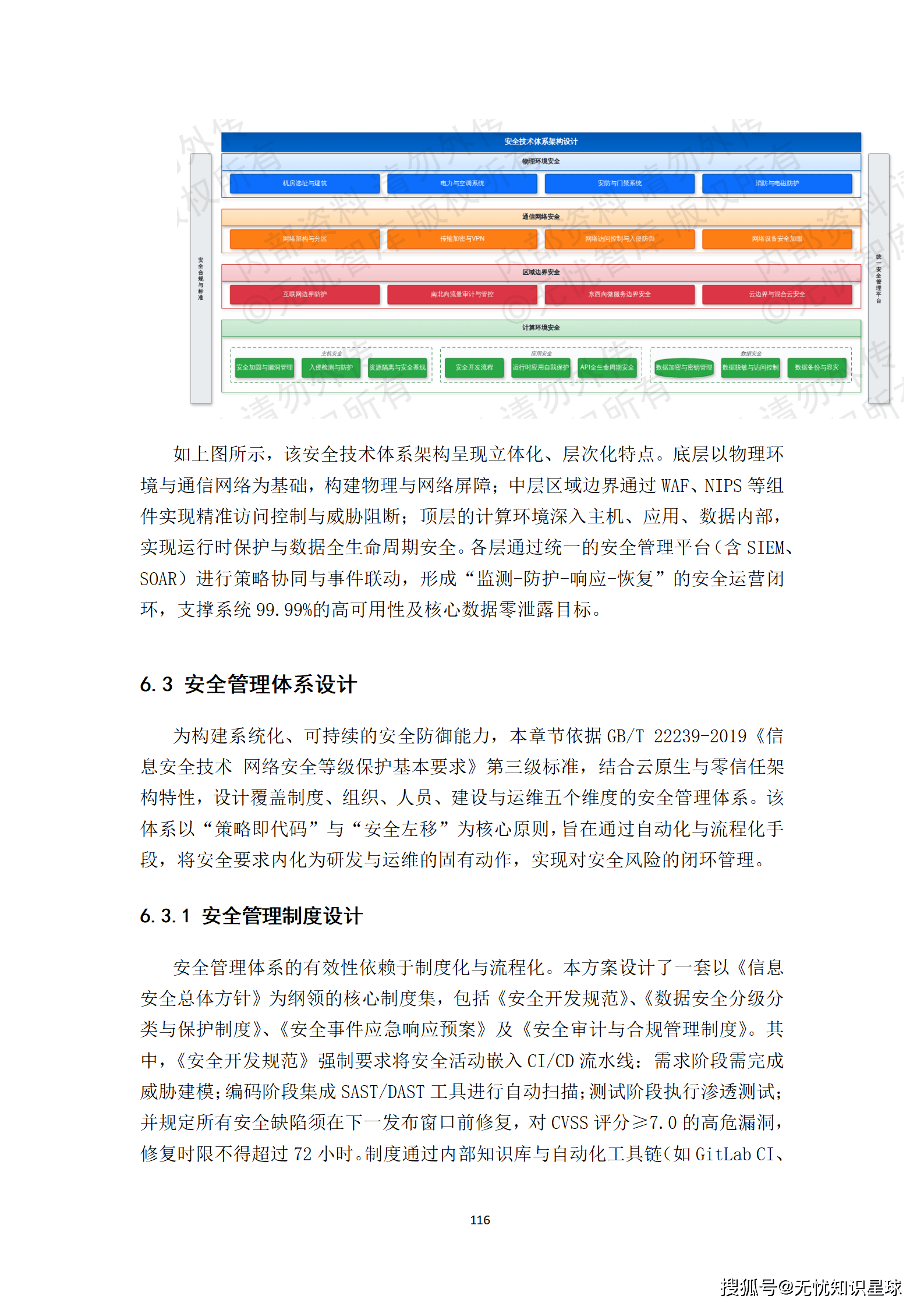
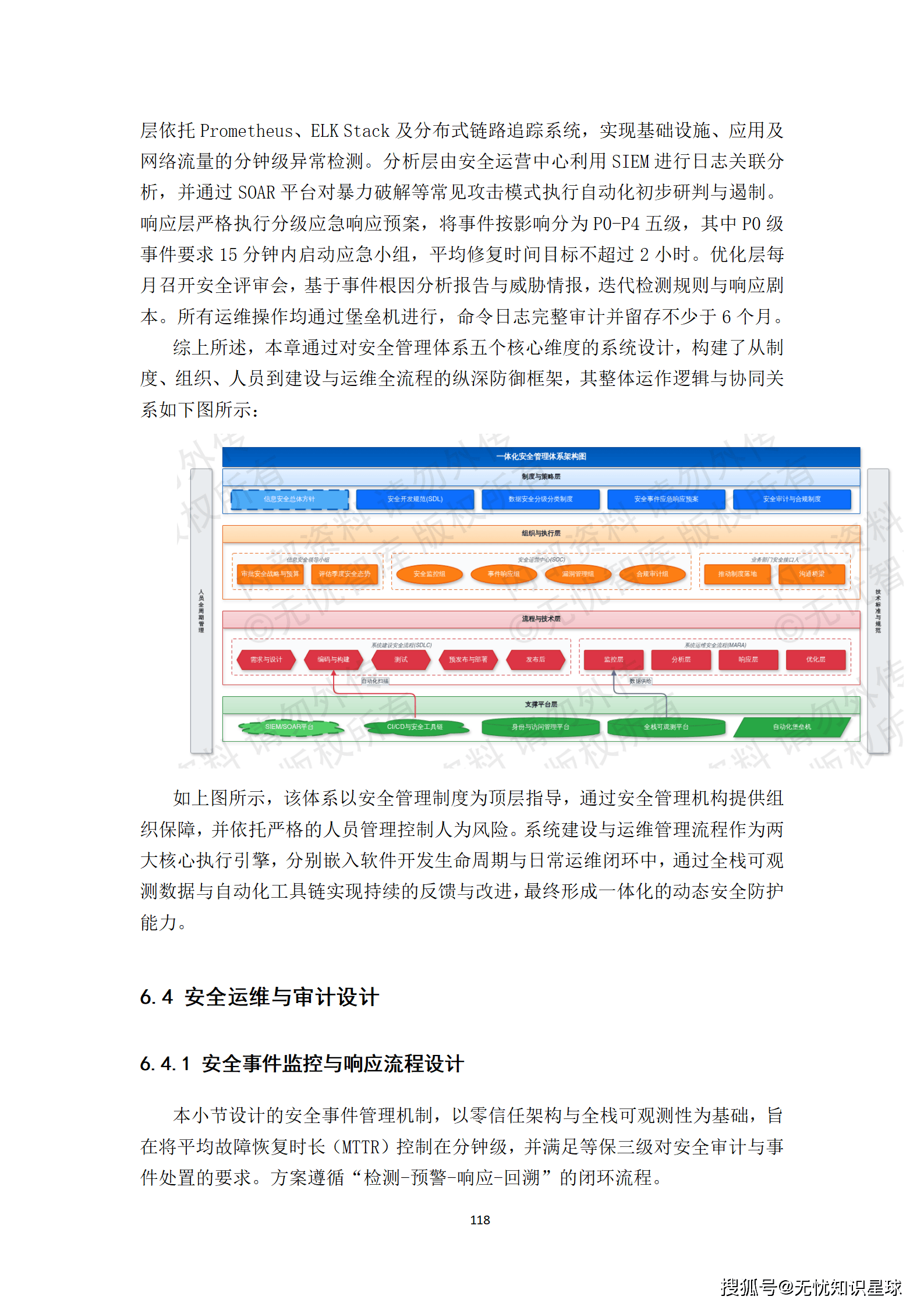
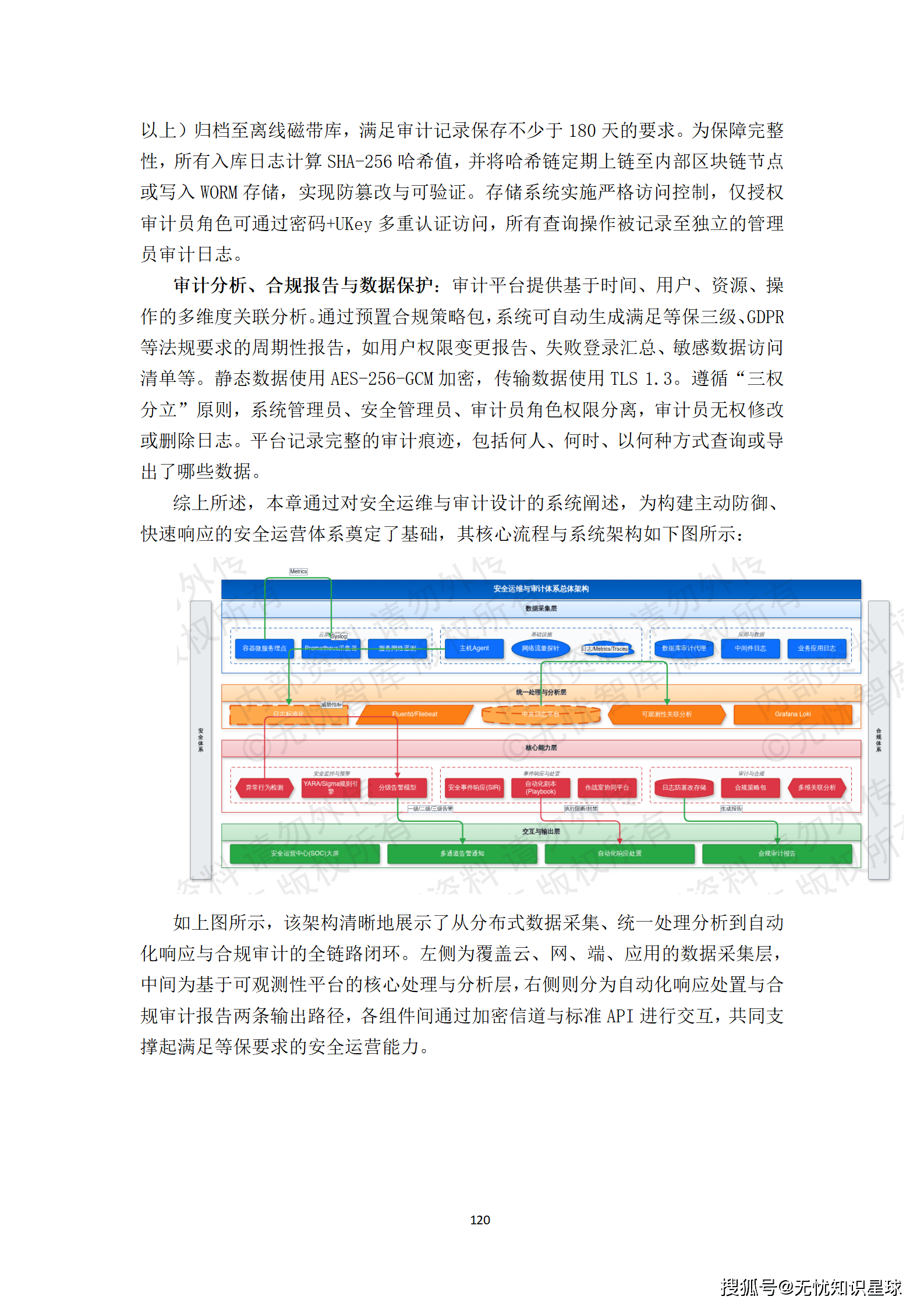
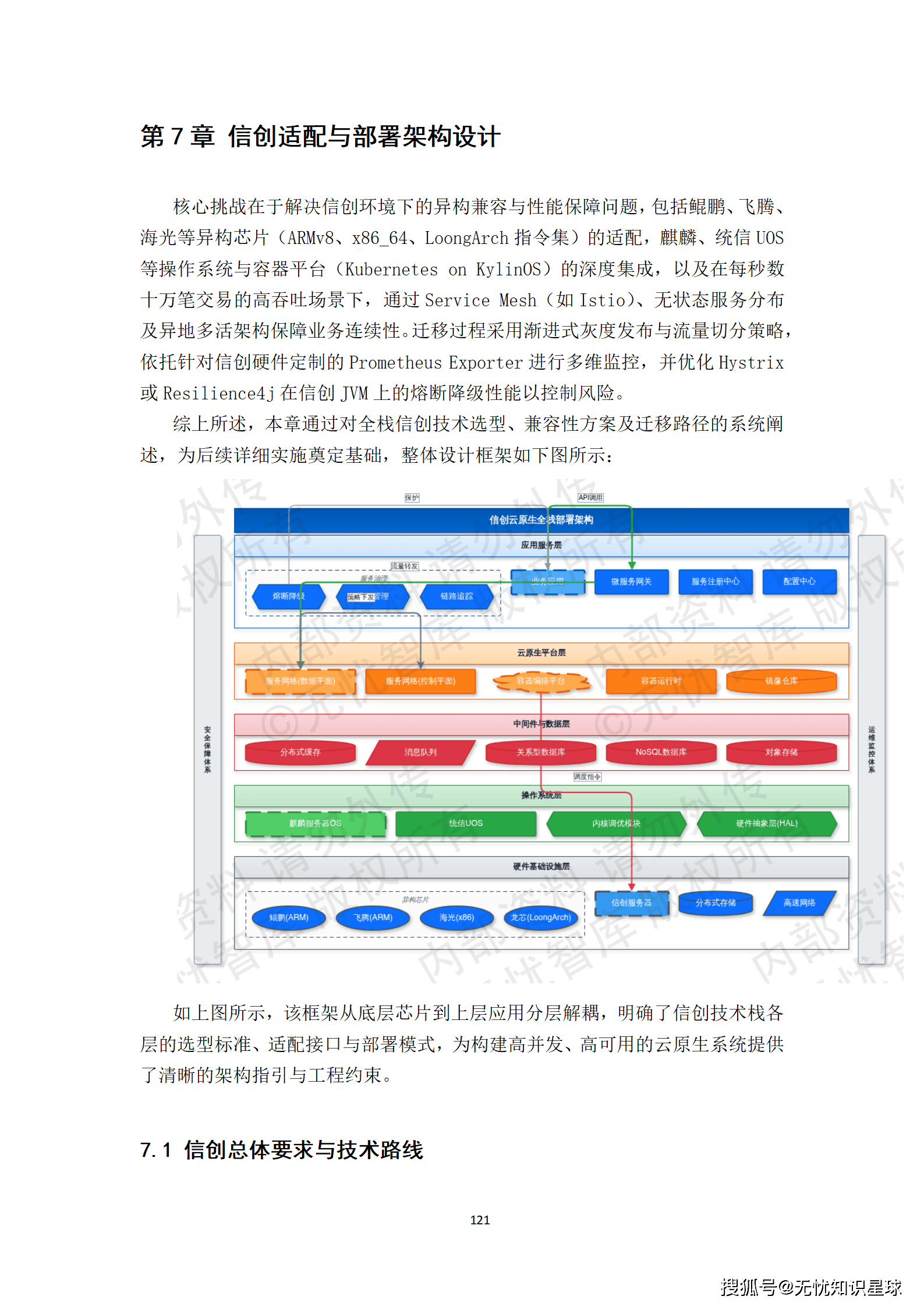
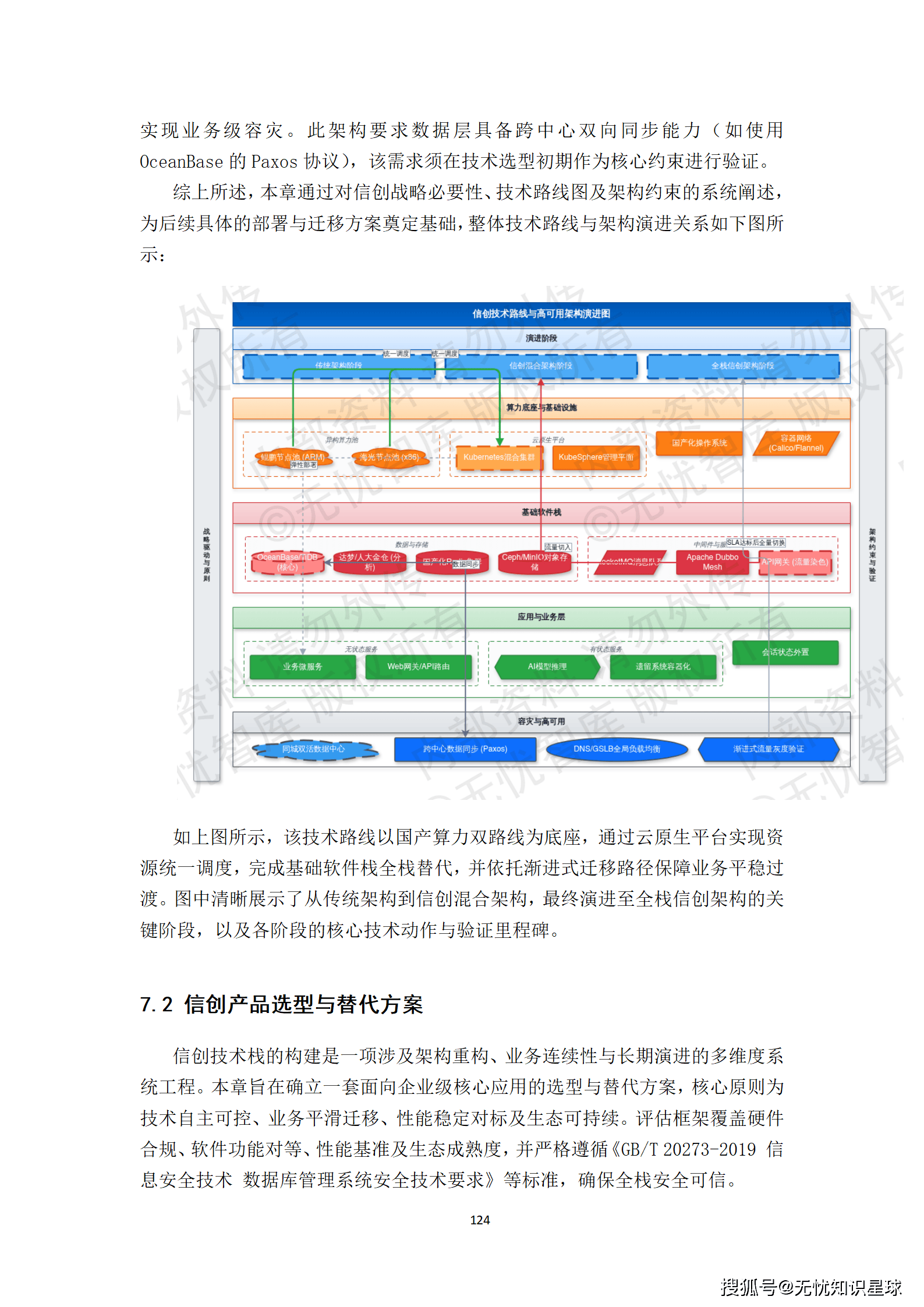
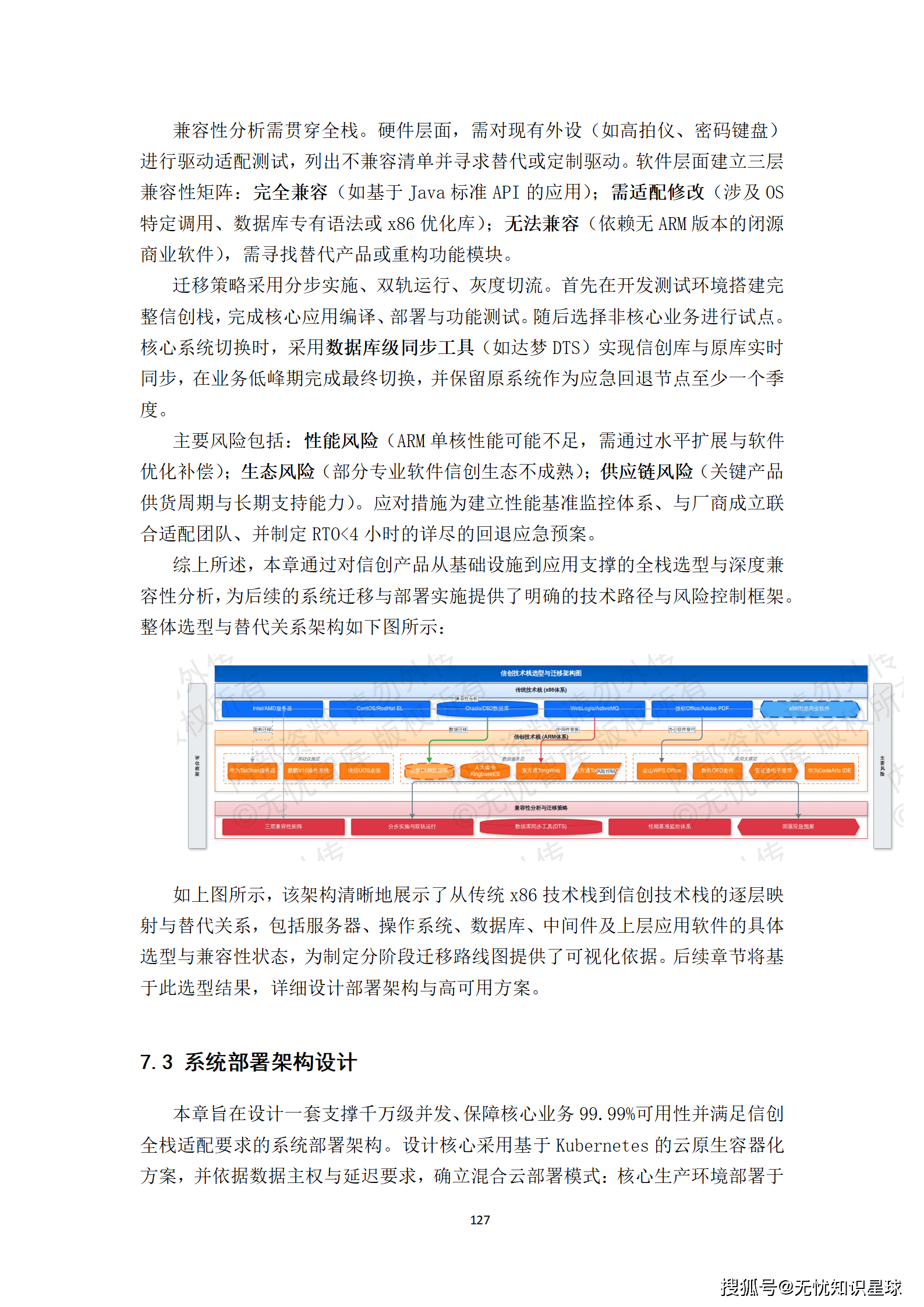
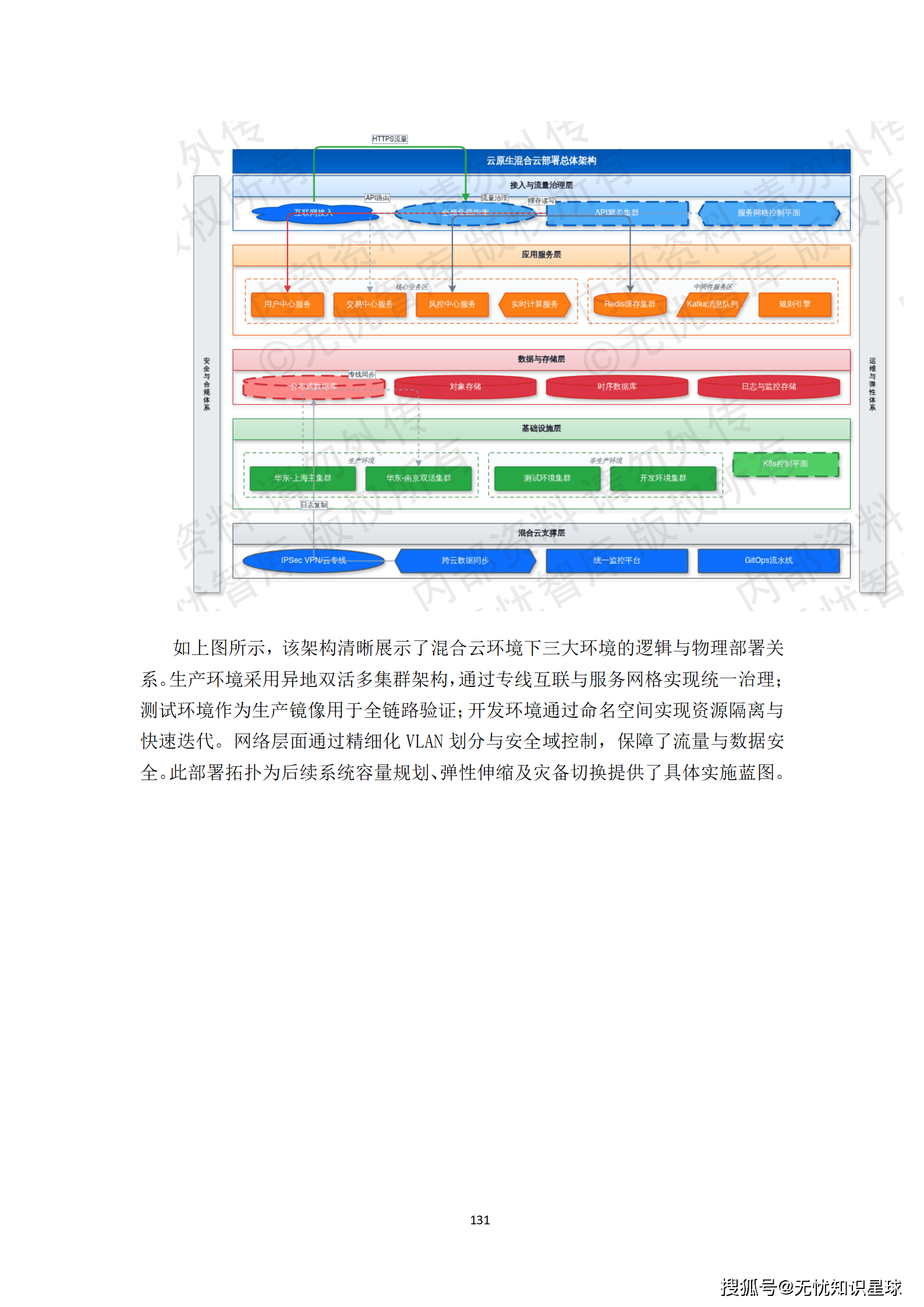
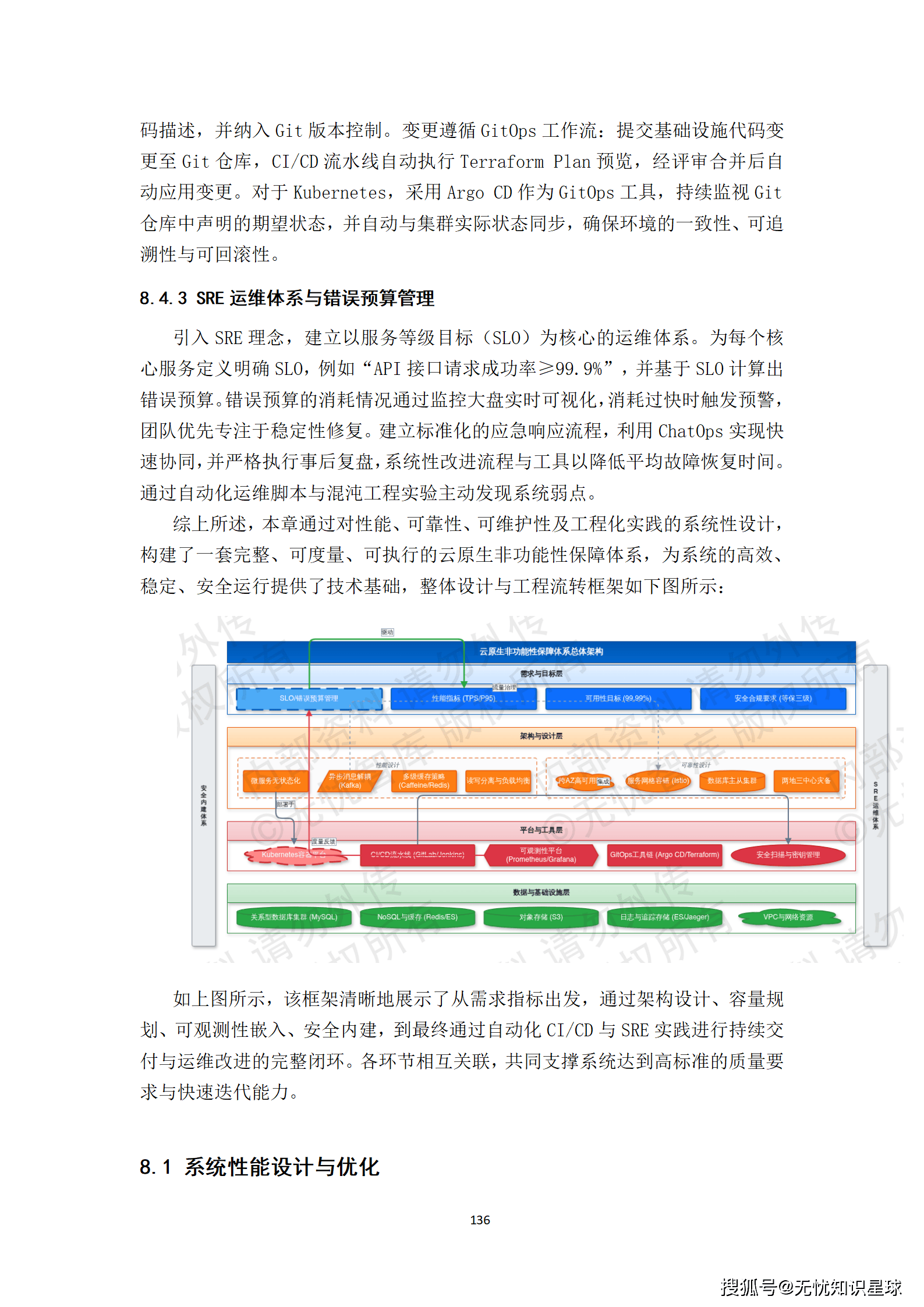
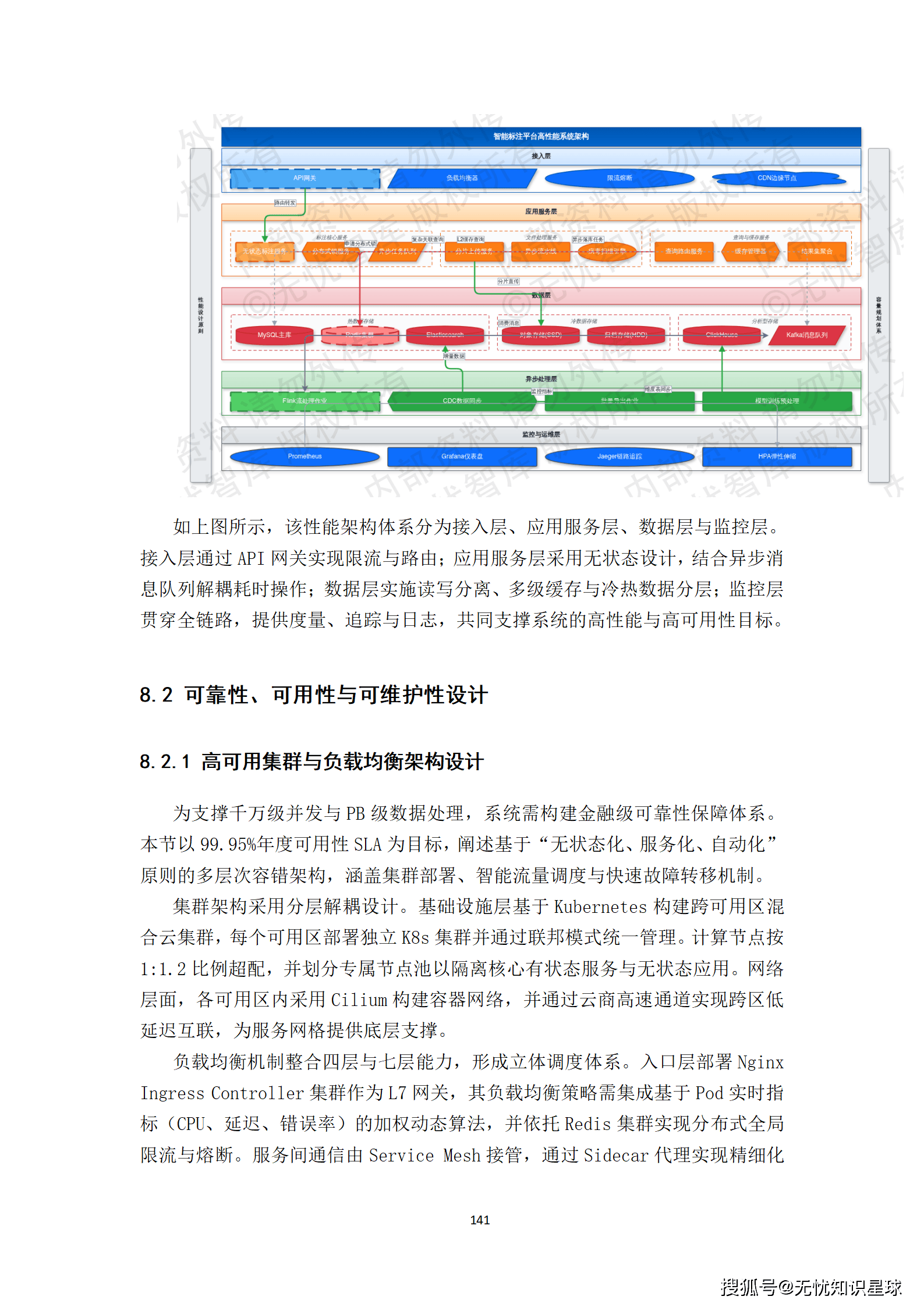
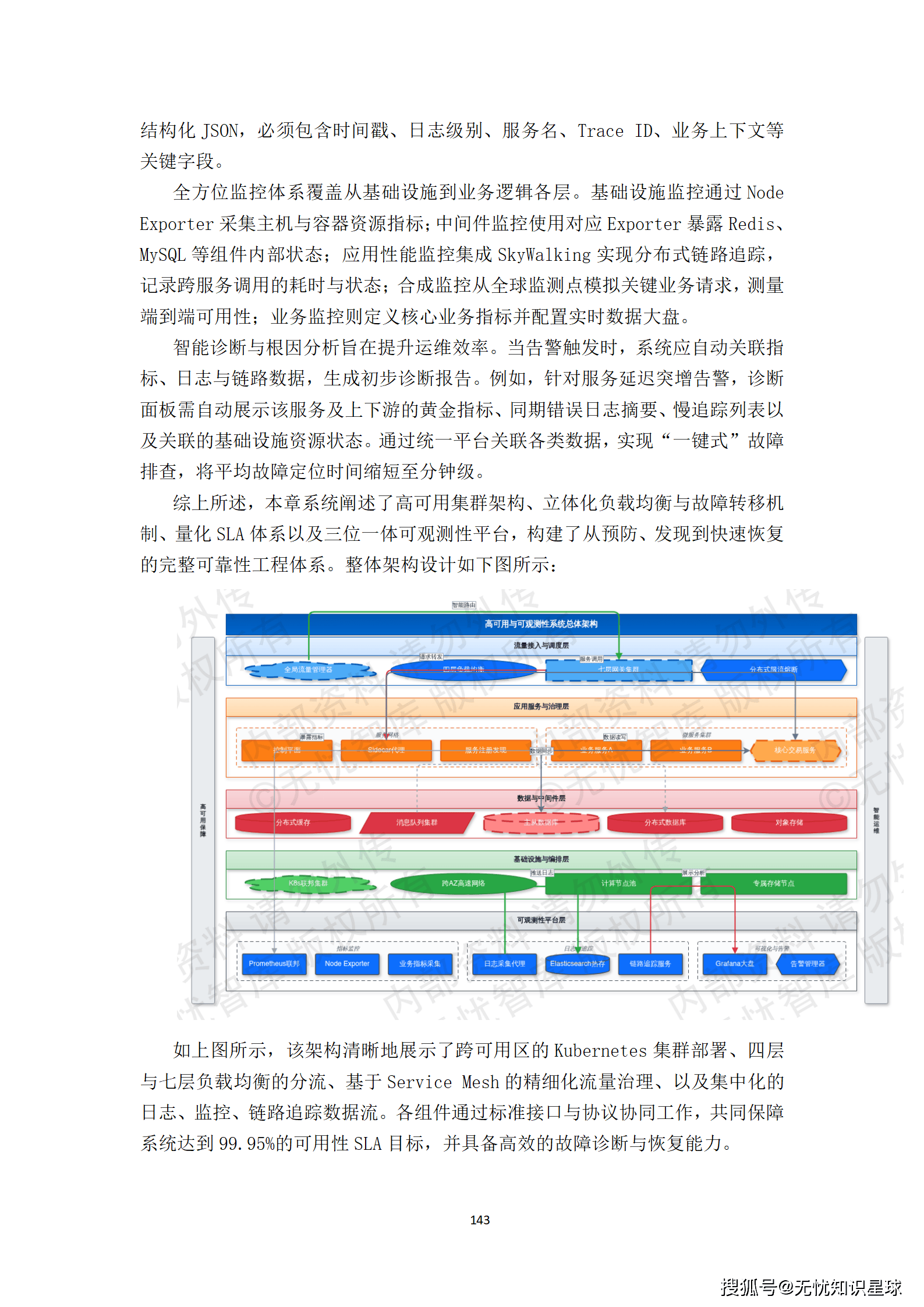
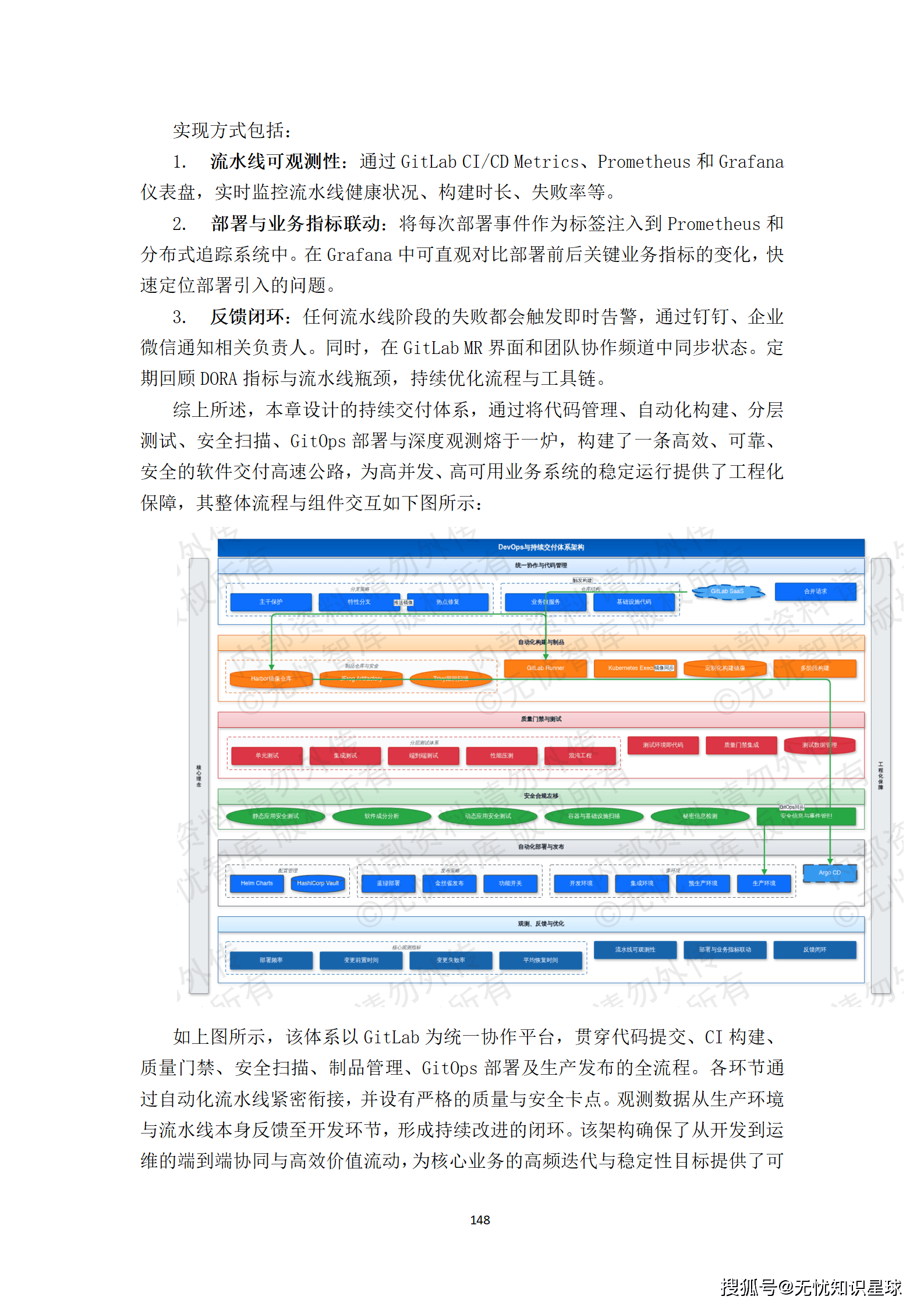
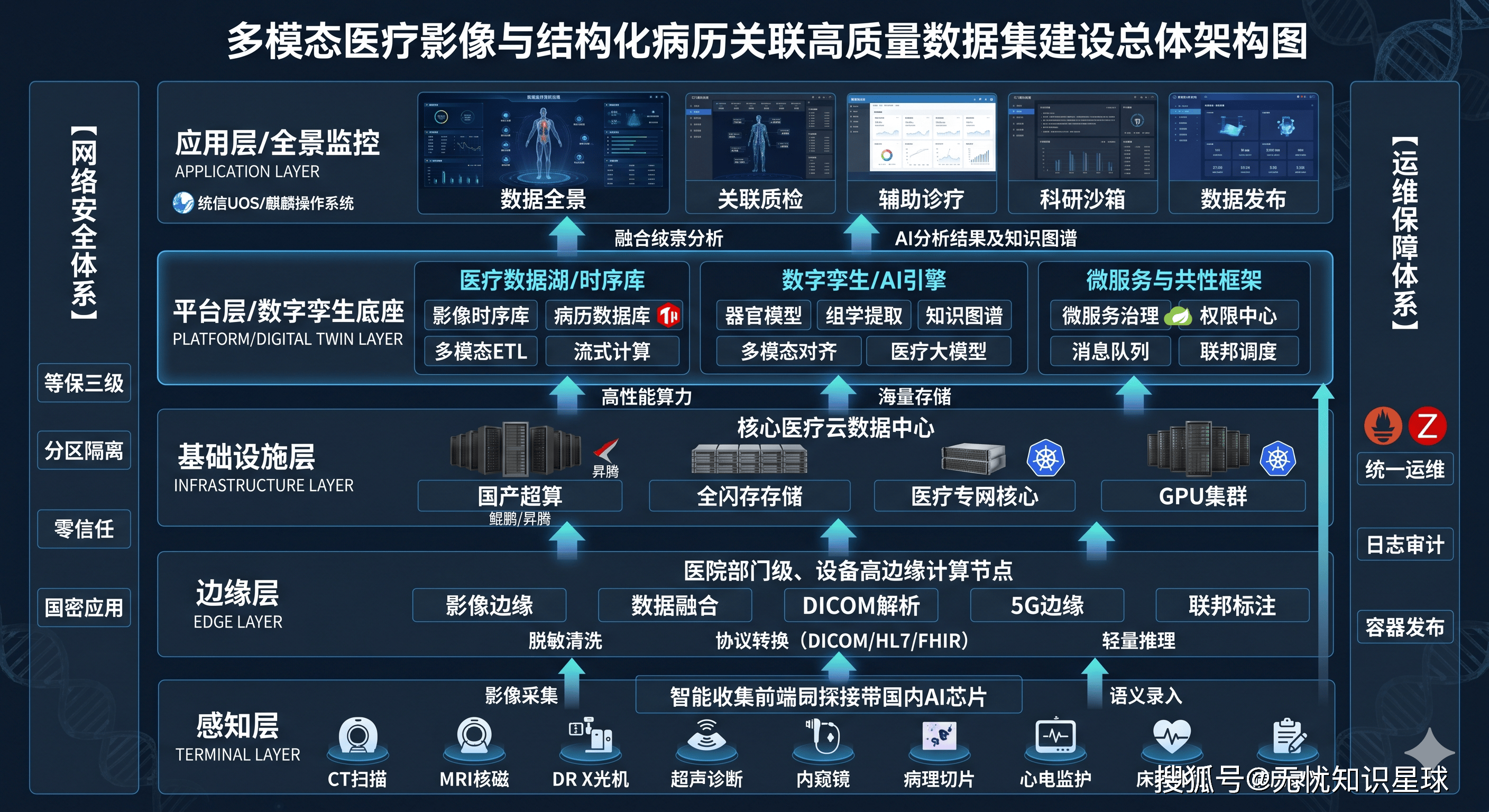
核心提示:本文系统梳理了构建医疗多模态高质量数据集的完整方法论,涵盖政策驱动、技术架构、工程实践与质量管控四大维度,是目前国内少有的、将医疗AI数据工程说透的系统性技术方案。
引言:数据是医疗AI真正的天花板
干了三十年咨询,见过太多医疗AI项目。有的项目,团队里顶级算法工程师,模型架构新颖,GPU算力充足,但最终落地惨淡。复盘下来,问题几乎都不出在算法上------出在数据上。
不是数据不够多,而是数据不够好。影像和病历各存各的,互不关联;标注标准因人而异,同一个病灶让五个医生看,画出五个轮廓;数据脱敏深度不一,有的中心留了残留标识符,合规风险一触即发。好的算法喂了烂数据,产出的模型在测试集上漂亮,一上临床就崩。
这不是技术问题,是数据工程问题。
本文要讲的,正是如何系统性地解决这个问题------从政策背景到工程架构,从DICOM解析到NLP结构化,从联邦标注到质量管控,一层一层把这件事说清楚。
一、战略背景:政策红利与现实鸿沟
1.1 政策层面的清晰信号
任何严肃的项目立项,必须先把政策逻辑搞清楚。医疗AI数据集项目的政策背景,比想象中更硬核。
《"十四五"数字经济发展规划》和《"十四五"全民健康信息化规划》,这两份文件叠加阅读,会发现一个共同指向:推动AI在医疗健康领域的规模化应用,同时强调健康医疗大数据的规范管理与互联互通。这两件事,表面上是一推一拉,本质上是同一件事的两面------要用数据,必须先治好数据。
《人工智能医疗器械注册审查指导原则》则更直接,它在监管层面明确了一件事:用于AI医疗器械注册的数据集,必须高质量、可追溯、具备临床相关性。这不是软约束,这是产品能否上市的硬门槛。
与此同时,《数据安全法》和《个人信息保护法》划定了数据处理活动的法律底线。医疗数据属于敏感个人信息,采集、处理、共享每一步都要满足"告知-同意"原则,且处理目的必须明确,不得超范围使用。
政策信号非常清晰:要做医疗AI,必须先建好数据基础设施,而且必须按规矩建。
1.2 现实层面的深层矛盾
政策指向了方向,但现实的起点在哪里?
坦率地说,起点比很多人想象的要低得多。
大多数医院的数据现状是这样的:HIS、EMR、PACS、RIS、LIS,各自成"烟囱",数据格式、标准、质量各异。一个患者的一次就诊,理论上应该形成影像、检验、病历、诊断的完整闭环,但实际上这些数据分散在五个不同的系统里,通过患者ID和就诊号这两根细线松散连接。一旦患者跨科室、跨院区,或者历史系统有过升级迁移,这两根细线就可能断掉。
更深的矛盾在于:临床医生的价值观和AI数据需求存在结构性冲突。 临床考核看的是业务量和诊疗质量,没有人因为数据录入不规范被扣钱。所以,非结构化病历里充斥着习惯用语和个人表达;DICOM头文件缺字段是常态;同一个检查在不同系统的状态记录,时间戳可能相差几小时。
这不是某一家医院的问题,这是行业性的系统问题。
二、核心痛点:数据瓶颈的四重困境
在详细分析了医院数据现状之后,可以把核心痛点凝练为四重困境。每一重都是独立的工程挑战,叠加在一起,就是为什么"有数据但没法用好"。
困境一:多模态数据割裂,图文对齐缺失
临床诊断本质上是多模态推理------影像给了形态学线索,病历给了病史背景,检验报告给了量化指标,三者合参才能给出有价值的判断。
但在数据层面,这三类数据是分离的。一份胸部CT影像,在PACS里有自己的Study Instance UID;对应的影像报告,在RIS系统里用检查号关联;而患者的病历记录,在EMR里用就诊号关联。这三个号码之间的映射关系,往往只存在于某个接口日志或中间表里,没有被系统性地管理。
结果是:AI模型无法自动学习"CT影像上的磨玻璃结节"和"影像报告中的疑似早期肺腺癌"之间的语义对应关系。多模态大模型最需要的"图文对齐"数据,在现有数据生态中几乎不存在。
困境二:标注标准不统一,数据质量噪声高
医疗标注的专业门槛极高。你不能随便找个人来标肺结节的边界,这需要经过专业训练的影像科医生。
但即使是经过训练的医生,在标注同一个病灶时,也会因为个人经验、理解偏差或使用工具的差异,产生边界上的差异。这种差异看起来只有几个像素,但对模型来说就是标注噪声。研究表明,标注噪声过高会导致模型在训练集上过拟合,但在跨中心验证时泛化性能骤降------临床不可信。
更麻烦的是,多中心协作标注时,"中心效应"会被放大。不同机构对同一标注规范的理解存在偏差,即使有《标注指南》,也会在实操中产生系统性的标注差异。
困境三:数据孤岛与合规压力并存
医疗数据跨机构流通面临双重压力:一方面是法律约束,个人信息保护法对数据处理和共享设定了严格要求;另一方面是行政壁垒,各科室、各机构把数据视为自己的资产,跨部门共享需要繁琐的审批流程。
这导致一个尴尬局面:想训练一个有临床价值的AI模型,需要来自多家医院、多个科室的多样化数据;但每一步数据流动都需要合规论证。传统的"数据集中汇聚"模式,合规风险大,落地周期长,往往在数据还没汇聚完就已经耗尽项目预算。
困境四:数据治理体系缺失,质量管控无法闭环
大多数机构内部没有数据资产目录,没有标准化的数据质量评估流程,没有跨系统的数据血缘追踪工具。
这意味着,当一个模型在某个医院的验证数据集上表现不理想时,没有人能快速定位问题------是训练数据本身有偏差?还是某一批次的标注质量有问题?还是源数据的采集时期和验证数据差异太大?
这种"无法溯源、无法归因"的状态,是医疗AI工程化的最大障碍之一。
三、总体设计:从蓝图到工程的转化
3.1 建设目标的三层分解
清醒的工程项目必须把目标说清楚,而不是停留在"构建高质量数据集"这种虚化表述。
业务层面:建立标准化、可追溯的数据生产流水线。目标是把非结构化原始数据转化为符合行业标准(DICOM、HL7 FHIR)的结构化标注数据,将数据准备周期从原来的数周缩短至数天,将因数据问题导致的模型返工率大幅压降。
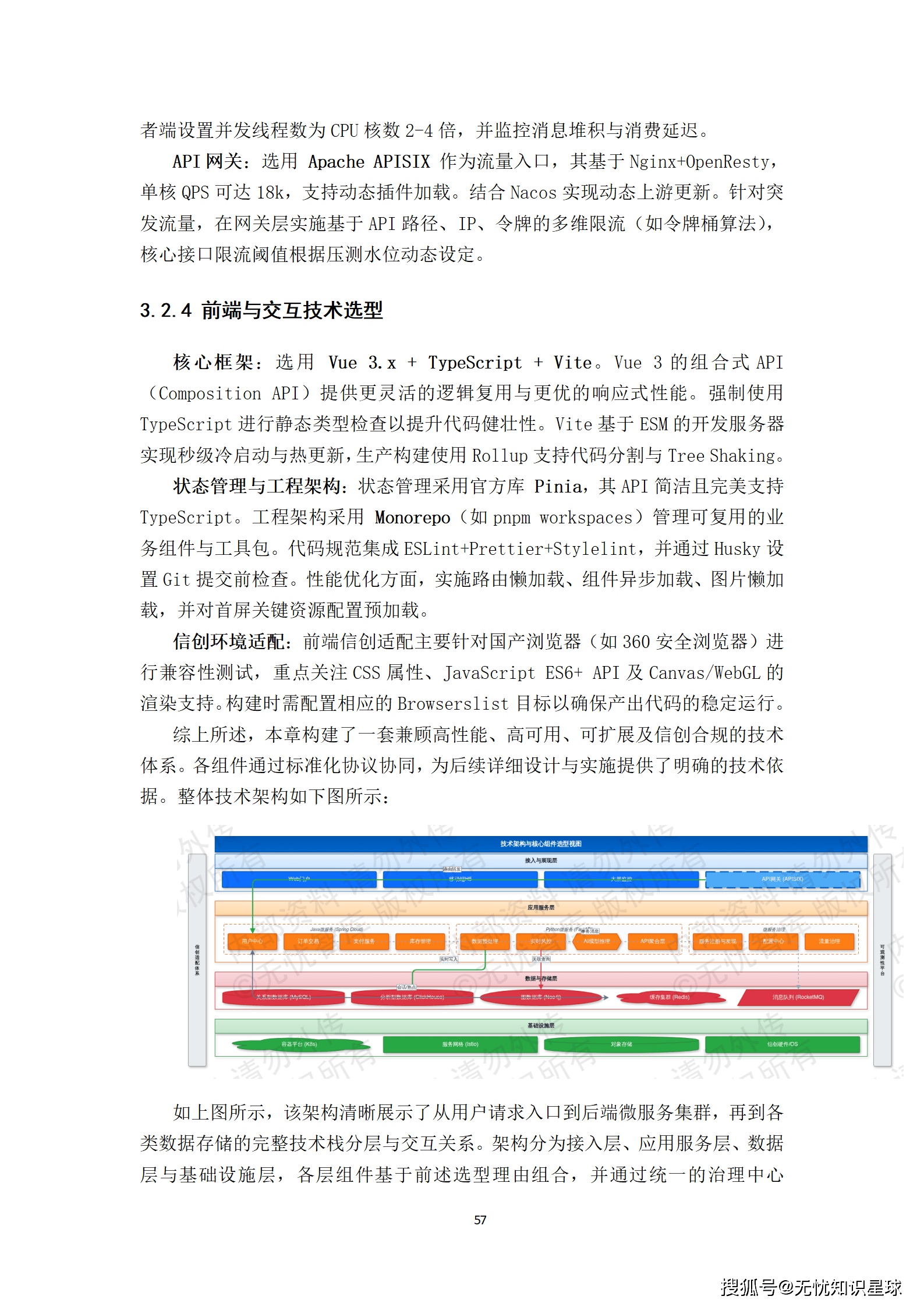
技术层面:搭建高可用、弹性伸缩的企业级数据平台。平台基于微服务与容器化架构,核心服务SLA不低于99.9%,核心API接口P95响应时间低于200毫秒,支持并发标注任务数不低于1000个。
数据层面:构建覆盖数据全生命周期的治理框架。核心产出是规模不低于N万条、标注质量合格率达99.5%以上的高质量数据集,并配套完整的数据标准规范与元数据目录。
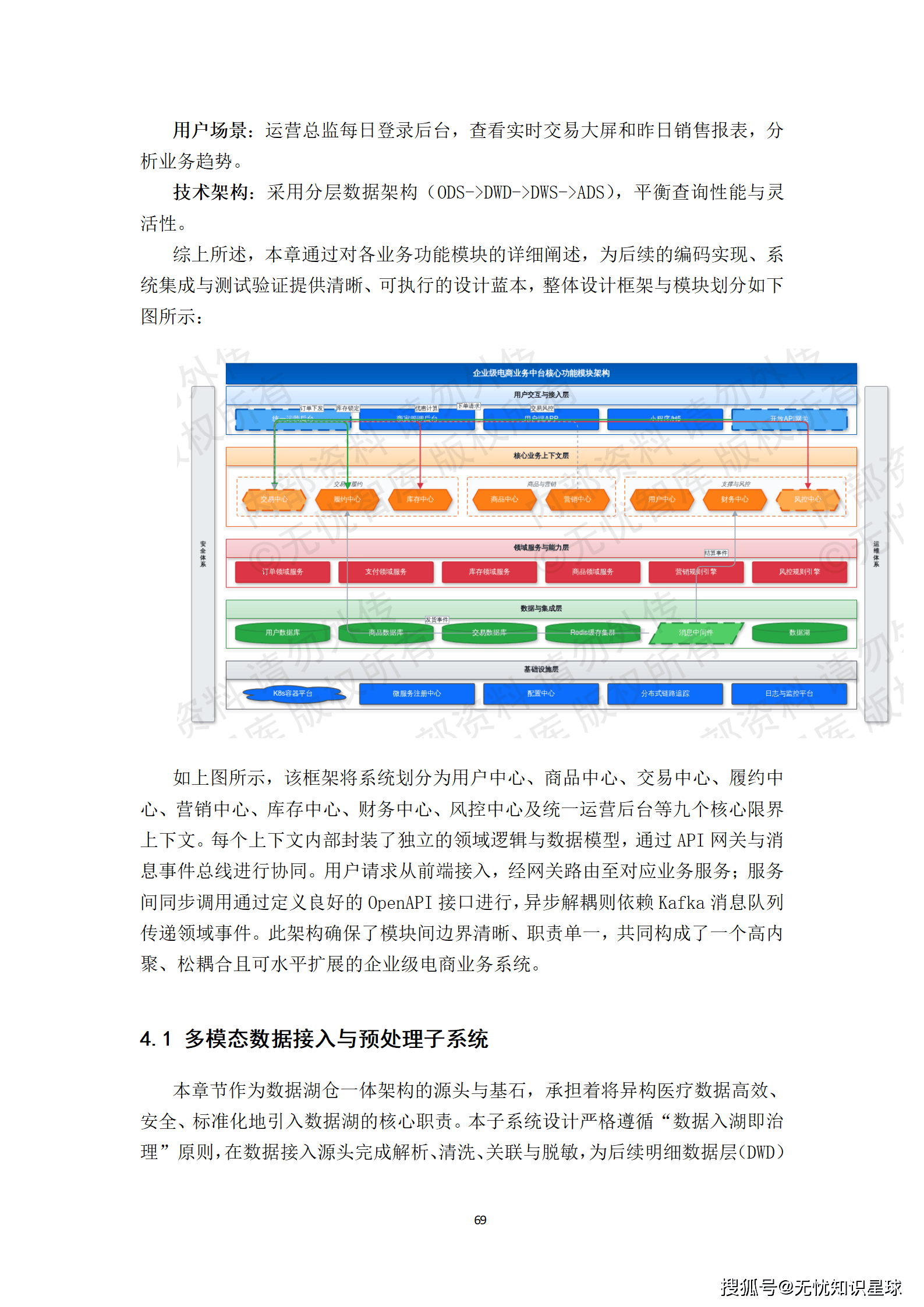
3.2 建设内容的五大模块
整个项目拆解为五大核心建设内容,每一块有明确的边界和验收标准:
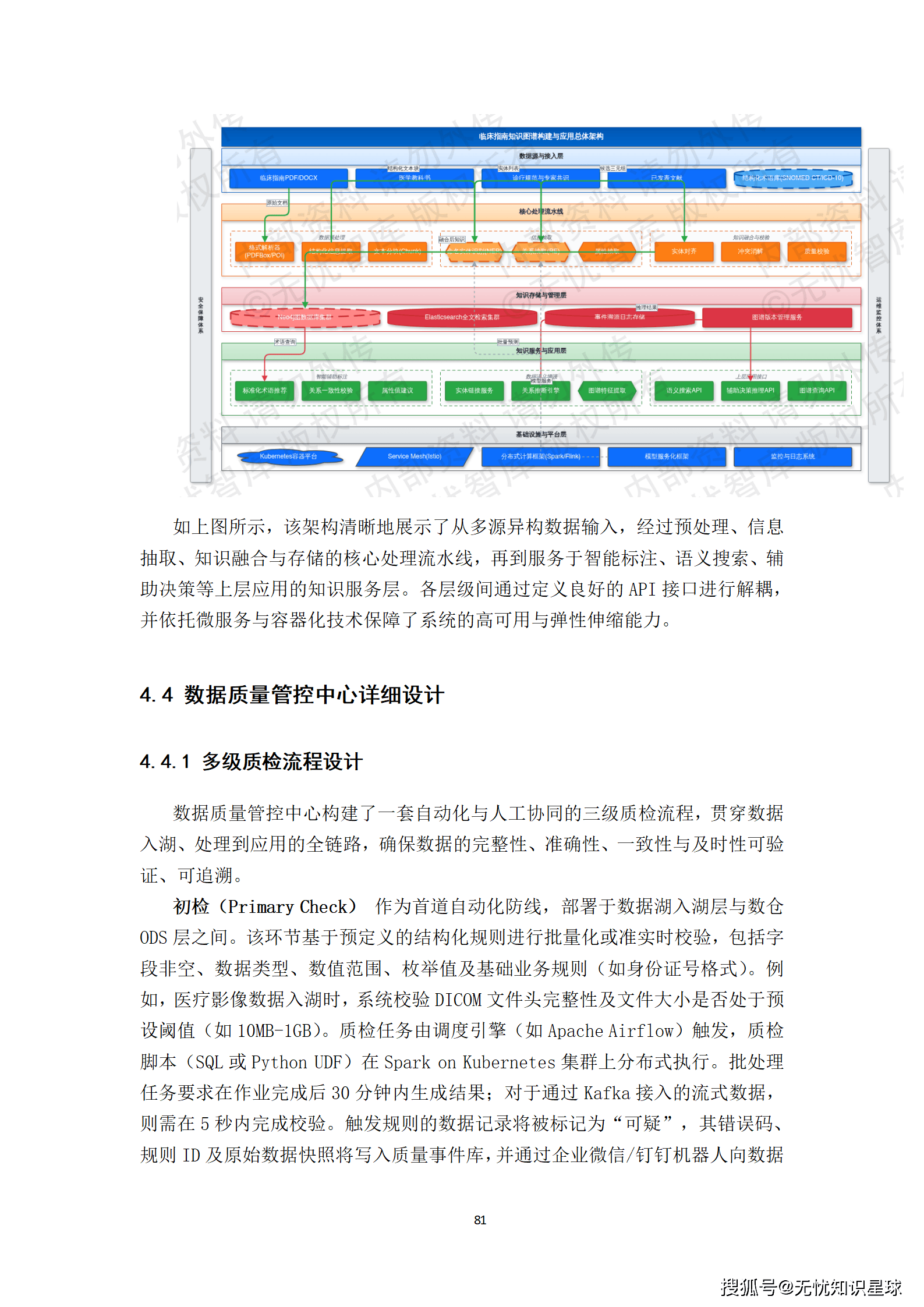
一是多模态数据智能处理底座:实现DICOM影像的自动化解析、非结构化病历的NLP结构化处理,以及跨模态数据的精准关联对齐。这是整个数据生产体系的源头,没有这一层,后续一切免谈。
二是联邦化协同标注平台:支持分布式、安全合规的多中心标注任务管理,集成智能预标注与质控工具。这是解决数据孤岛问题的核心手段------数据不出域,但标注协作可以跨域。
三是临床知识增强系统:构建融合诊疗指南的医学知识图谱,用于辅助标注决策与数据质量校验。这一层是提升数据语义丰富度的关键,也是让AI模型具备可解释性的基础。
四是全链路数据质量管理体系:覆盖从数据接入、标注、质检到版本发布的全过程质量度量与管控。这不是一个孤立的模块,而是贯穿整个数据生产流水线的横切关注点。
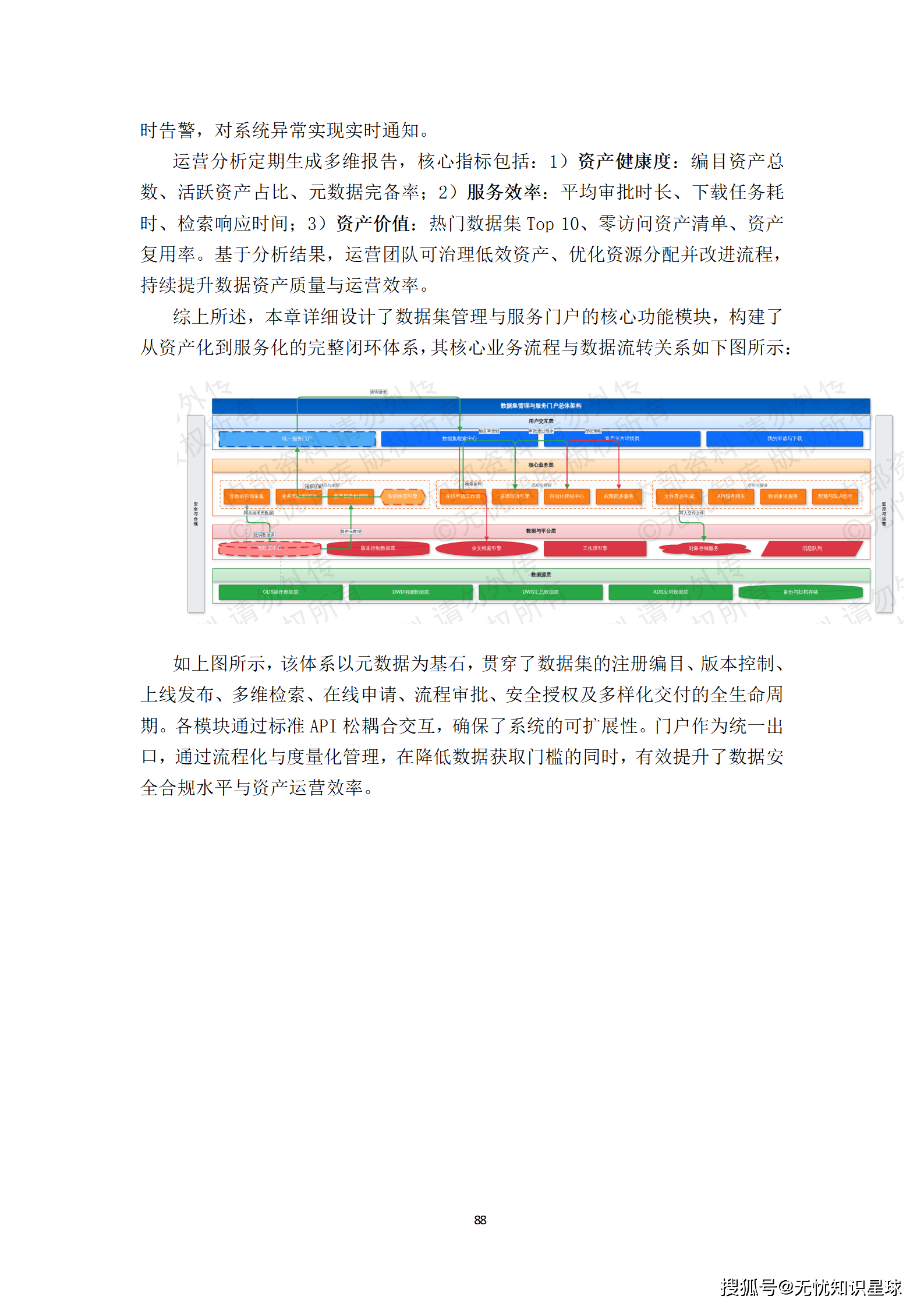
五是标准化数据集服务门户:提供数据集的编目、检索、申请与安全交付功能。这是面向用户(算法研究员、模型训练团队)的最终交付界面。
3.3 明确不做什么同样重要
工程项目常见的失败模式是范围蔓延。必须清楚地界定:这个项目不承担AI模型的研发与部署;不负责原始数据的采集获取;不包含标注员团队的招募管理;不做与未开放接口专有系统的深度定制集成。
边界清晰,才能把资源集中在真正有价值的事情上。
四、技术架构:系统设计的核心逻辑
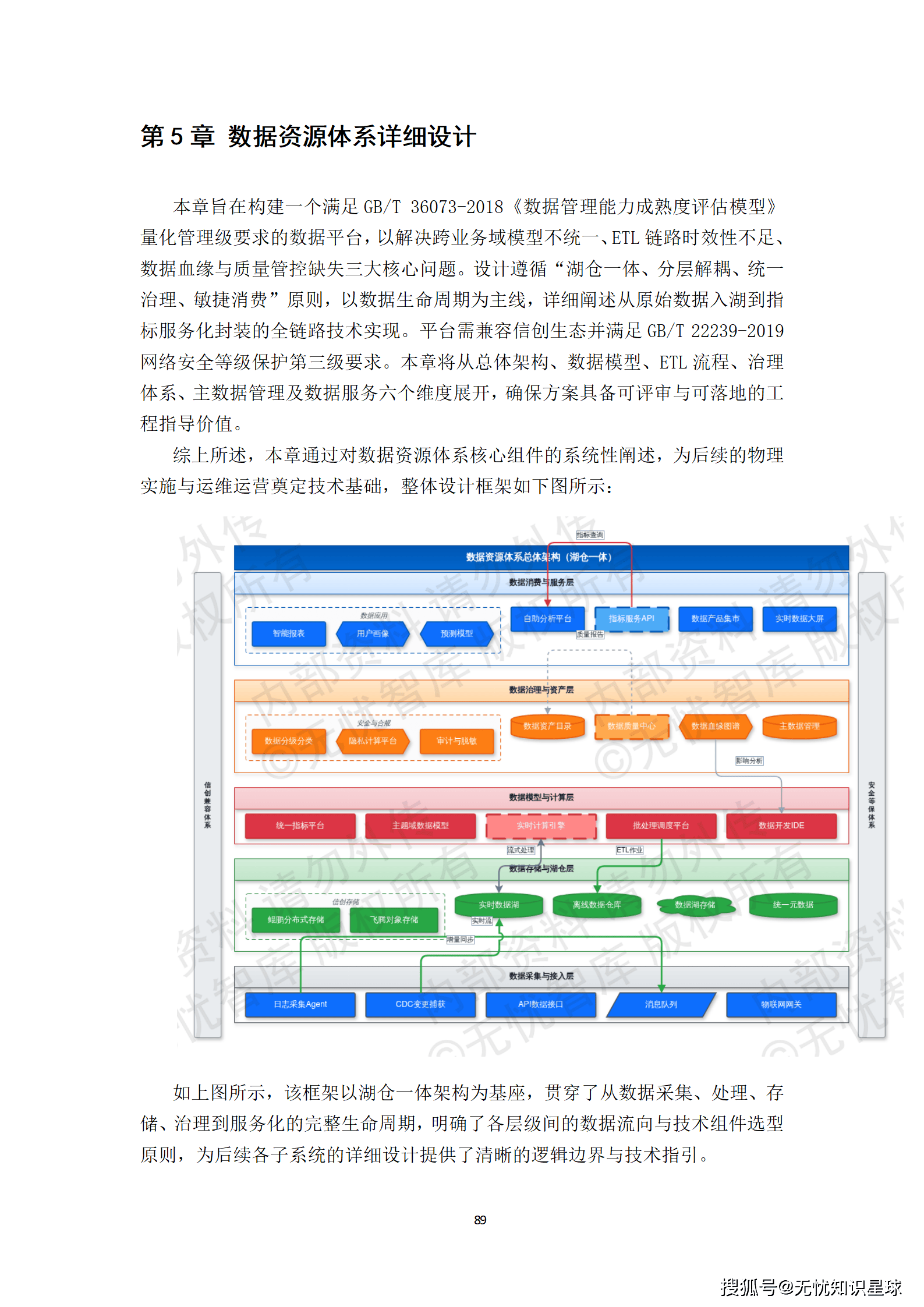
4.1 数据分层:湖仓一体的架构选择
为什么选择湖仓一体架构?这个问题值得认真回答。
医疗AI的数据有个显著特点:原始数据体量巨大(DICOM序列,单个检查就可能达到数GB),但真正用于模型训练的加工数据,在结构、规模、查询模式上和传统数仓完全不同。传统数仓的强Schema约束,在面对非结构化影像数据时基本失效;纯数据湖又缺乏ACID事务保证,数据质量难以管控。
湖仓一体架构,把数据湖的灵活性和数据仓库的治理能力结合起来,是目前处理这类"大体量+强治理"需求的最优解。
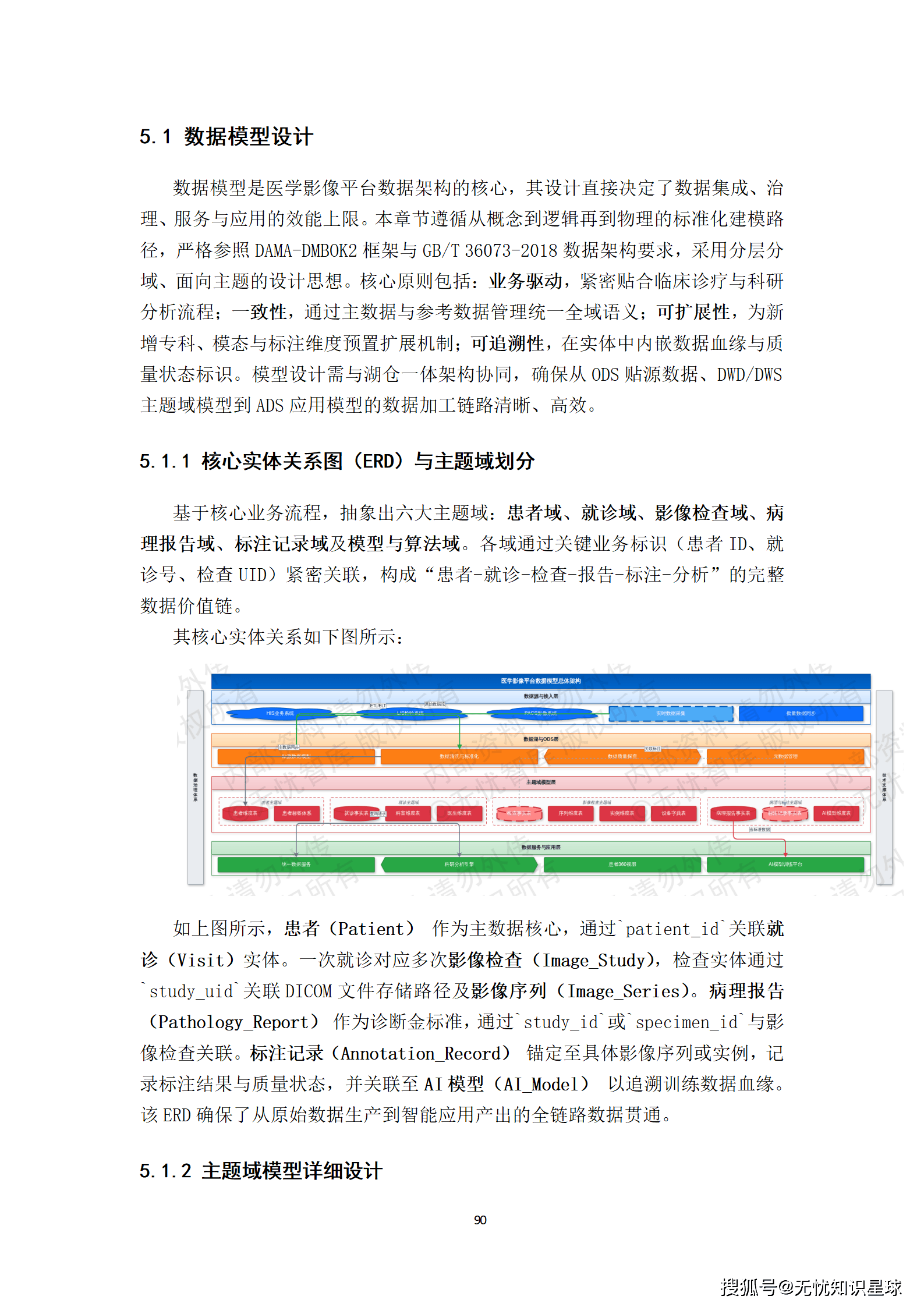
数据分层采用经典的ODS-DWD-DWS-ADS四层架构:
- ODS层(原始数据层):存储从各医院接入的原始数据,保持原始格式,仅做脱敏处理,不做任何业务转换。这一层的数据不可变更,是所有后续处理的源头锚点。
- DWD层(明细数据层):完成格式标准化、模态关联和基础质检,形成以"患者-就诊-检查"为核心的统一数据模型。这一层是多模态关联对齐发生的地方。
- DWS层(汇总数据层):按疾病、影像模态、标注状态等维度聚合,形成可供快速检索和统计的宽表。
- ADS层(应用数据层):面向具体AI模型训练需求,输出标准格式(COCO、TFRecord等)的数据集版本。
4.2 技术选型的核心原则
技术选型不是比较哪个框架更先进,而是看哪个选型在约束条件下最能解决问题。
对于数据流编排,选择Apache NiFi,原因是它对DICOM C-STORE协议有较好的原生支持,且可视化的数据流配置降低了运维门槛。对于分布式计算,选择Apache Spark,因为DICOM影像的批量解析和NLP处理都是典型的大数据批处理场景。对于任务调度,使用Airflow,它的DAG管理和依赖追踪能力,非常契合数据流水线的编排需求。
在安全合规层面,所有涉及患者信息的数据,传输采用TLS 1.3,存储采用国密SM4加密,并基于RBAC实现细粒度权限控制。这不是可选的,是合规要求。
五、DICOM解析引擎:影像数据入湖的硬骨头
很多人低估了DICOM解析的工程复杂度。DICOM 3.0标准本身就有几千页文档,而且各厂商的设备实现都有私有扩展。一台西门子的CT和一台GE的CT,输出的DICOM文件在私有标签、压缩算法上可能有显著差异。这不是bug,这是DICOM标准允许的厂商扩展。
5.1 解析流水线的设计
DICOM解析流水线基于dcm4che3开源库构建,接入方式采用DICOM C-STORE SCP服务,在104端口监听来自医院PACS的主动推送。
解析过程分三步:
第一步,传输语法识别:DICOM文件头里记录了传输语法UID,这决定了像素数据的编码和压缩方式。必须先正确识别传输语法,才能用对应的解码器处理像素数据。常见的传输语法包括:隐式VR小端序(医院内网传输最常见)、JPEG Lossless无损压缩(胸片、乳腺钼靶常用)、JPEG 2000无损(病理图像常用)。
第二步,元数据提取与标准化:按照DICOM数据字典,强制解析患者信息组、检查序列信息组、图像属性组中的关键Tag。提取的元数据以JSON格式写入ODS层,同时记录完整的数据血缘(源系统IP、接收时间戳、文件大小、MD5校验值)。这个MD5校验值不是摆设------当数据下游出现问题时,可以用它验证数据完整性,快速排查是传输问题还是解析问题。
第三步,像素数据预处理:CT影像的原始像素值是Hounsfield单位(HU值),直接给模型用没有意义。需要根据窗宽窗位将HU值映射到的显示灰度区间,同时记录原始像素间距和切片厚度(这两个参数对后续的三维分析至关重要)。预处理后的影像以无损PNG格式或NIfTI格式存储于对象存储,元数据中记录存储路径和访问URL。
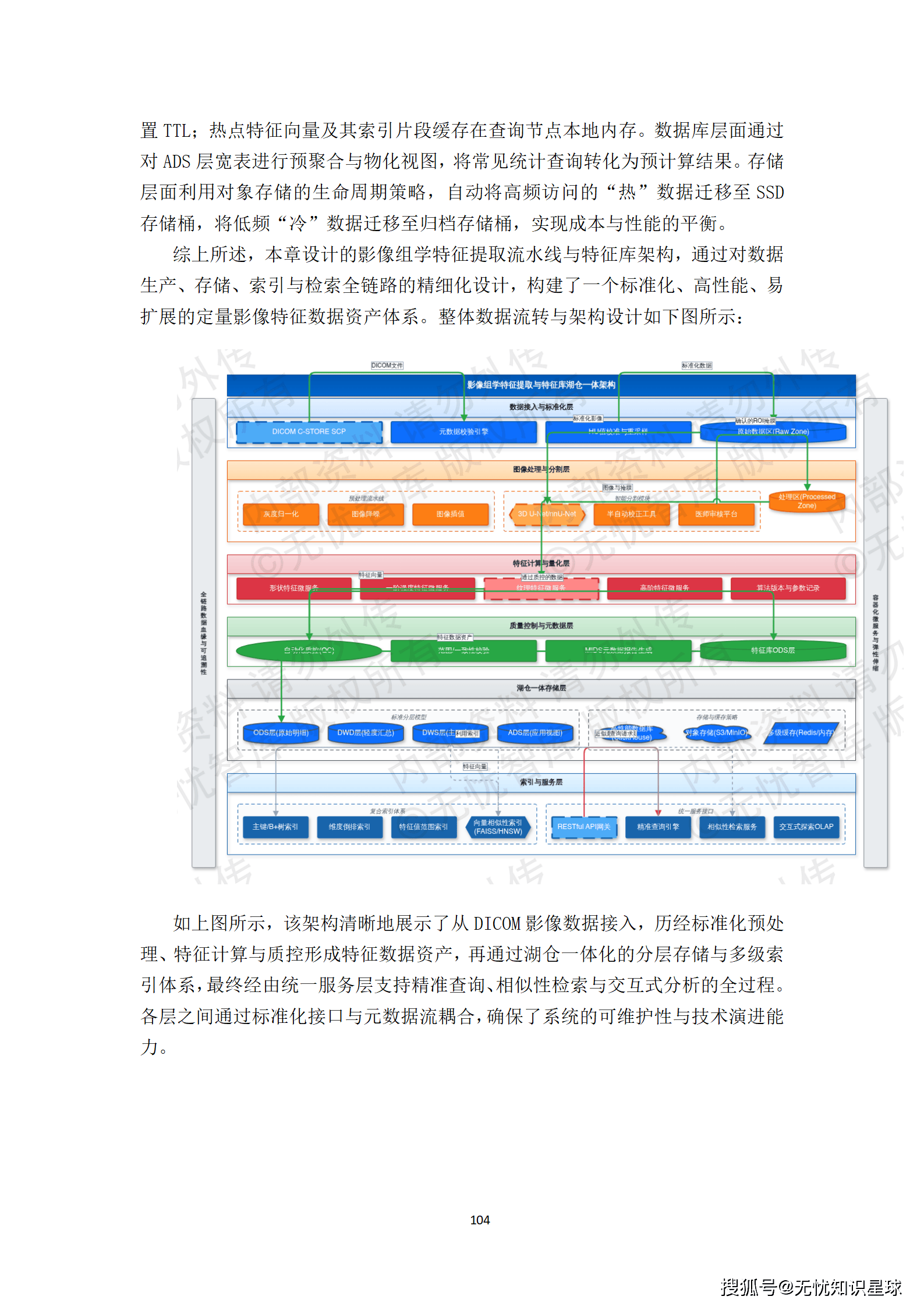
5.2 影像特征提取:三类特征的工程价值
影像数据入湖后,还需要做特征提取,供后续数据检索和模型辅助标注使用。特征分三类:
深度学习特征:使用在大型医学影像数据集上预训练的卷积神经网络,截取全连接层前的特征向量。这类特征维度高(通常1024维或更高),语义丰富,适合做相似影像检索,也可以作为迁移学习的起点。
影像组学特征:遵循IBSI(影像组学标准倡议)标准,对影像感兴趣区域提取一阶统计特征(均值、方差、峰度等)、形状特征(体积、表面积、球形度等)、纹理特征(GLCM、GLRLM矩阵等)。这类特征数量多(通常上百个),可解释性强,是影像组学研究的核心。
统计特征:全图像素值的直方图统计量、信噪比、对比度等基础特征。这类特征计算快,可以用于快速的图像质量评估和异常检测。
六、NLP结构化引擎:从自由文本到机器语言
病历文本的NLP处理,是整个数据工程中挑战最高的环节之一。原因不复杂:自由文本是人类语言,充满歧义、省略、个人习惯和隐喻。把它转化成机器可靠理解的结构化信息,本身就是一个未完全解决的科学问题。
6.1 为什么病历NLP格外难
中文病历文本有几个特别棘手的特点:
专业术语密集且多样化。同一个诊断,可以表达为"急性心肌梗死"、"AMI"、"心梗"、"冠状动脉闭塞导致的心肌坏死",这些表达在临床上等价,但对NLP模型来说是完全不同的字符序列。
时序信息隐晦。病程记录里的时序关系往往通过"前日"、"次晨"、"术后第三天"这类相对时间表达,没有绝对时间戳,需要结合上下文推断。
否定和不确定性表达复杂。"排除肺栓塞"和"诊断肺栓塞"在字面上只差一个词,但医学含义相反。"不除外恶性"比"良性"的风险高出一个数量级。这类否定和不确定表达,是NLP标注数据中污染最严重的来源。
6.2 处理流程:规则+深度学习的混合架构
文本处理流水线采用"规则引擎+深度学习模型"的混合架构,原因是两者有互补性:规则引擎在高准确率要求的固定格式实体(如药品名、ICD编码)上表现稳定,深度学习模型在复杂语境的实体识别上更有优势。
预处理阶段:字符编码检测与转换、段落切分与句子分割。分句规则需要针对中文病历定制------"如:"、"即:"等引导词后的内容不能被错误切分;换行符在病历里有时代表段落结束,有时只是格式换行,需要根据上下文判断。
实体识别阶段:核心模型采用在中文医学文本上微调的BERT-BiLSTM-CRF架构,识别疾病与诊断、手术与操作、药品、检查检验、身体部位与症状等实体类型。识别后,实体被映射至ICD-10(疾病)、LOINC(检验)、SNOMED CT(临床概念)等标准编码体系。
关系抽取阶段:基于依存句法分析与注意力机制的关系分类模型,从识别出的实体中抽取语义关系,形成"主语-谓语-宾语"三元组。例如,从"患者因急性阑尾炎行腹腔镜阑尾切除术"中,提取出(患者)-因病-(急性阑尾炎)和(患者)-接受-(腹腔镜阑尾切除术)两个三元组。
所有结构化结果以JSON-LD格式输出,并关联至原始文本的字符偏移位置,确保可追溯------当结构化结果有误时,可以直接定位到原文的具体位置进行核查和修正。
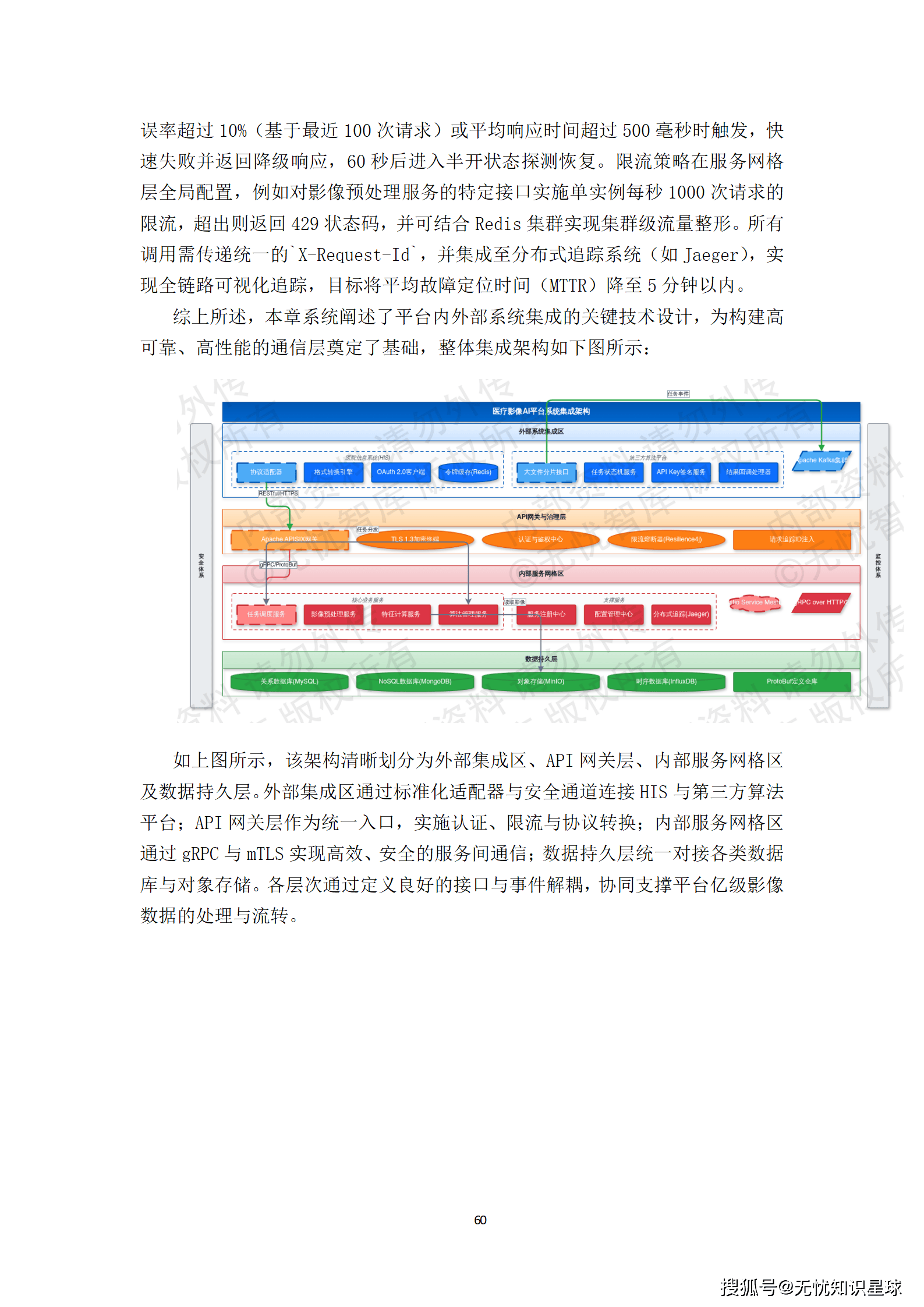
七、多模态关联对齐:数据价值的关键跃升
DICOM解析做好了,NLP结构化做好了,但这两件事是独立完成的。把同一个患者的影像、文本、检验报告关联起来,形成完整的临床视图,才是多模态数据真正有价值的地方。
7.1 患者主索引:关联的基础
多模态关联的核心挑战是患者身份的确认。一个患者在不同系统里可能有不同的标识符------HIS里有住院号,PACS里有检查号,医保系统里有医保号。这些标识符之间的映射关系,往往只存在于业务接口日志里,没有被系统性管理。
解决方案是建立独立的EMPI(企业主患者索引)服务,采用"确定性匹配+概率性匹配"的双阶段策略:
确定性匹配:当两条记录的身份证号完全一致,或"姓名+出生日期+性别"三者完全匹配时,直接判定为同一患者。这一步覆盖了大多数正常情况。
概率性匹配:对于缺乏强标识符的记录,使用Jaro-Winkler距离计算姓名相似度,结合出生日期差异、性别一致性等字段,通过Fellegi-Sunter模型计算整体匹配概率。概率高于0.93的记录自动关联,0.75至0.93之间的进入人工复核队列。
7.2 检查-报告-影像时序对齐
确认患者身份后,还需要把同一医疗事件产生的多模态数据在时间线上对齐。关键在于以"患者-就诊-时间点"为维度,构建时序事件链。
DICOM文件里的Accession Number字段(检查号)是连接影像数据和RIS报告的桥梁;就诊号是连接影像、报告和EMR病历的更上层关联键。对齐算法以就诊时间为锚点,将同一就诊下所有检查申请按照申请时间排序,将DICOM检查、检验报告、病历文书的记录时间,映射到对应的检查申请时间点上。
所有关联关系以图数据库的形式存储,支持高效的跨模态查询。这意味着:给定任意一个病例,可以快速查出它关联的所有影像序列、报告、病历记录和标注数据,以及每一条数据的来源和处理历史。
八、联邦化标注平台:打破数据孤岛的核心路径
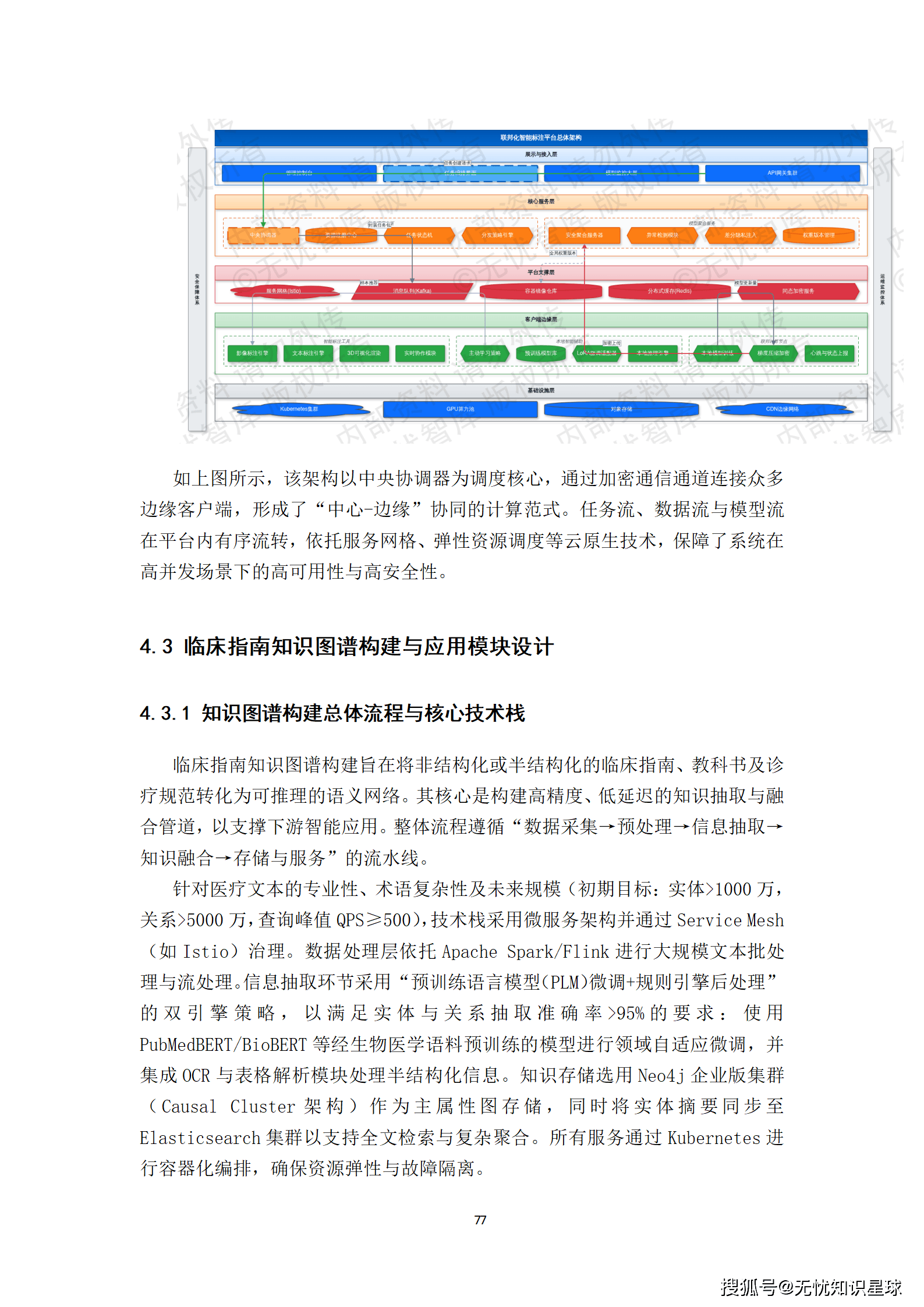
联邦学习在医疗领域的讨论已经很多,但真正落地的实践案例还不多。这里不讲概念,讲工程实现层面的关键设计。
8.1 为什么联邦标注是必要的
"数据不出院"是很多医院的底线要求,这不仅是政策压力,也有现实的IT安全考量。但如果数据不出院,怎么做多中心协同标注?
联邦化标注的核心思路是:标注工具和标注任务下发到各个节点(各医院),标注医生在本地环境里完成标注,标注结果以加密形式参与联邦聚合,原始数据永不离开本地网络。
这需要解决几个工程难题:标注界面和工具必须与中心平台保持同步,标签体系、标注规范要完全一致;跨节点的质控和仲裁需要在不暴露原始数据的前提下实现;任务分发、进度追踪、绩效统计需要在分布式环境下正常运作。
8.2 标注平台的核心功能设计
多模态标注工具集:针对不同数据类型定制工具。DICOM序列标注支持多平面重建(MPR)视图联动浏览,可以同时看轴位、矢状位、冠状位三个切面;提供3D分割刷、体积测量工具,支持窗宽窗位动态调整。病理WSI标注支持快速缩放导航,可以在几十倍放大下做细胞级别的标注。EMR文本标注支持实体和关系的同步标注,并能实时调用NLP模型提供标签建议。
混合标注模式:支持自然语言描述性标注(口述病灶特征)和结构化标签标注(从预定义标签树选择)的结合。系统通过集成NLP模型,将描述性文本自动解析并建议可能的结构化标签,辅助医生提升效率。
主动学习集成:标注过程中可实时调用联邦模型对未标注区域进行推理,将预测结果(如分割掩膜)作为预标注供医生审核修正。修正后的结果作为高质量样本反馈至联邦训练循环。这个"预标注-审核-反馈"的闭环,是提升标注效率最有效的工程手段------有研究显示,在质量合格前提下,预标注可以将专家审核时间压缩60%至80%。
8.3 标注任务的生命周期管理
标注任务从创建到验收,经历一个完整的状态机:
待分配 → 标注中 → 待质检 → 质检中 → 质检通过/驳回 → 已仲裁
每个状态转换都有对应的事件记录和通知机制。标注医生完成标注后提交,触发质检流程;质检驳回后,带着质检意见自动反馈至标注医生工作台,形成学习闭环;对于争议较大的样本(如IoU<0.8),触发专家仲裁,仲裁结果作为黄金标准版本入库。
九、质量管理体系:数据的生命线
好数据不是自然产生的,是质量管理体系生产出来的。这一点在医疗AI领域格外重要,因为数据质量的上限,就是模型临床可信度的上限。
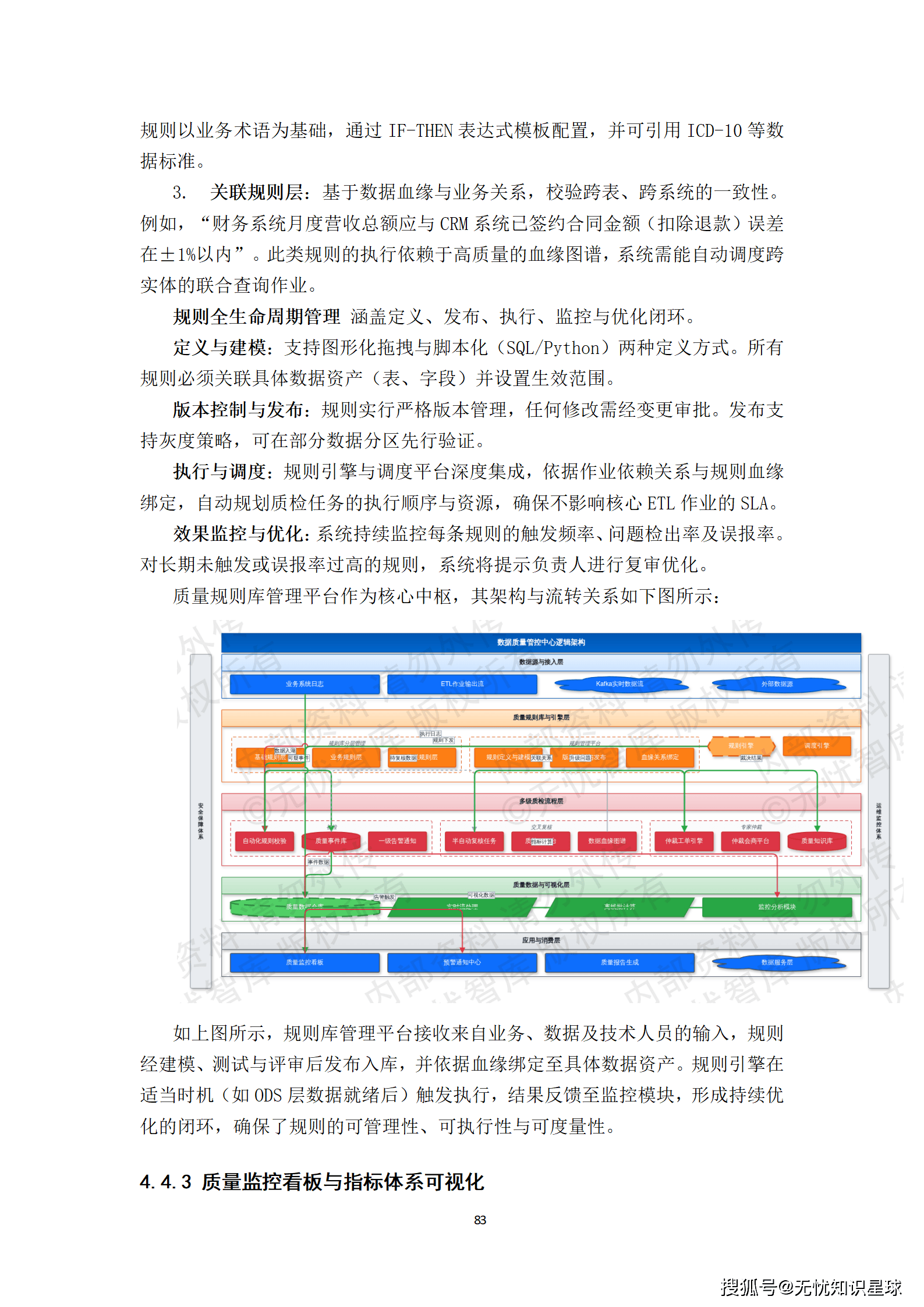
9.1 三级质检机制
质检体系设计为三级,每一级有不同的侧重:
一级:自动化规则质检。入湖前强制通过四个自动质检器:
- 格式校验器:检查DICOM头文件完整性、编码规范性;
- 内容质检器:利用预训练模型评估影像质量(是否有严重伪影、分辨率是否达标)并检测统计异常值;
- 关联校验器:校验影像、报告、标注通过主数据ID正确关联,不允许出现"有影像无报告"或"有标注无影像"的孤儿数据;
- 隐私合规校验器:验证PHI脱敏准确率,生成审计日志。
二级:交叉审核质检。对于关键标注(如恶性肿瘤边界),强制要求至少两名医生独立标注后进行交叉审核。系统自动计算标注者间一致性指标(Cohen's Kappa或Fleiss' Kappa),高亮显示差异区域,供质检专家仲裁。
三级:专家抽样终审。按不低于5%的比例随机抽样,由资深医师终审。终审结果和评语记录在数据集质量报告中,作为数据集版本发布的重要依据。
9.2 量化质量标准
建立量化标准是质量管理的基础。拍脑袋说"质量很高"没有意义,必须有可测量的指标:

这些指标不是摆设,而是每一批数据入库的通行证。未达标的数据不能进入训练集,需要回溯问题根源,修正后重新提交质检。
9.3 质量闭环的关键:反馈机制
质量管理不能是单向的"检查-拒绝",必须有反馈闭环。质检仲裁后,结果和评语自动反馈至原标注医生工作台,医生可以看到自己的标注哪里出了问题、为什么被驳回、正确标注应该是什么样的。这个反馈机制既是质量改进的手段,也是标注团队能力建设的路径。
对质量持续不达标的标注员,系统可以自动触发再培训流程或限制任务领取权限。这不是惩罚,而是在保证数据质量的前提下对人员能力的负责。
十、数据集版本管理与生命周期治理
很多工程团队在数据集版本管理上投入不够,结果是:模型迭代了,但不知道第几个版本用的哪批数据;某个模型性能突然下降,无法判断是代码变了还是数据变了;论文发表后,审稿人要求提供原始实验数据,发现已经无法精确复现。
10.1 版本控制设计
数据集版本采用"数据集名称_YYYYMMDD_Vx"的命名格式(如Lung_Nodule_CT_20251001_V2),区分主要版本和次要版本:
- 主要版本(V1→V2):标注标准重大变更、疾病分类体系调整、大规模数据增补。主要版本升级需经数据治理委员会审批。
- 次要版本(V1.0→V1.1):少量数据纠错、标注边界微调、格式修正。次要版本由数据管理员审核即可。
每次版本升级,在数据湖保留旧版本不可变快照,并通过血缘工具记录演变关系。所有模型训练任务必须明确指定所用数据版本号,确保实验可复现。
10.2 数据-模型双向溯源
当某数据集版本产出的模型出现性能下降时,需要快速判断是数据问题还是代码问题。这要求建立数据版本、模型版本与实验记录之间的强关联图谱:
- 给定一个模型版本,可以查出它训练用的数据集版本;
- 给定一批数据(包括其中有质量问题的子集),可以查出哪些模型使用了这批数据,评估影响范围;
- 给定一个实验运行记录,可以完整复现它的数据输入和代码版本。
这个双向溯源能力,是数据治理成熟度的重要标志,也是通过医疗AI监管审查的重要基础。
十一、非功能性需求的工程约束
优秀的系统设计,非功能性需求(性能、可用性、安全、扩展性)和功能性需求同等重要。
性能约束:核心交易接口(如数据集检索、标注任务分发)P95响应时间≤1秒,P99.9≤3秒。DICOM解析目标TPS≥500,支持并发标注任务数≥1000。
可用性约束:核心服务年度可用性≥99.95%(全年计划外停机≤4.38小时),采用高可用集群部署,单节点故障30秒内自动切换。容灾设计采用同城双活+异地灾备,RPO≤5分钟,RTO≤30分钟。
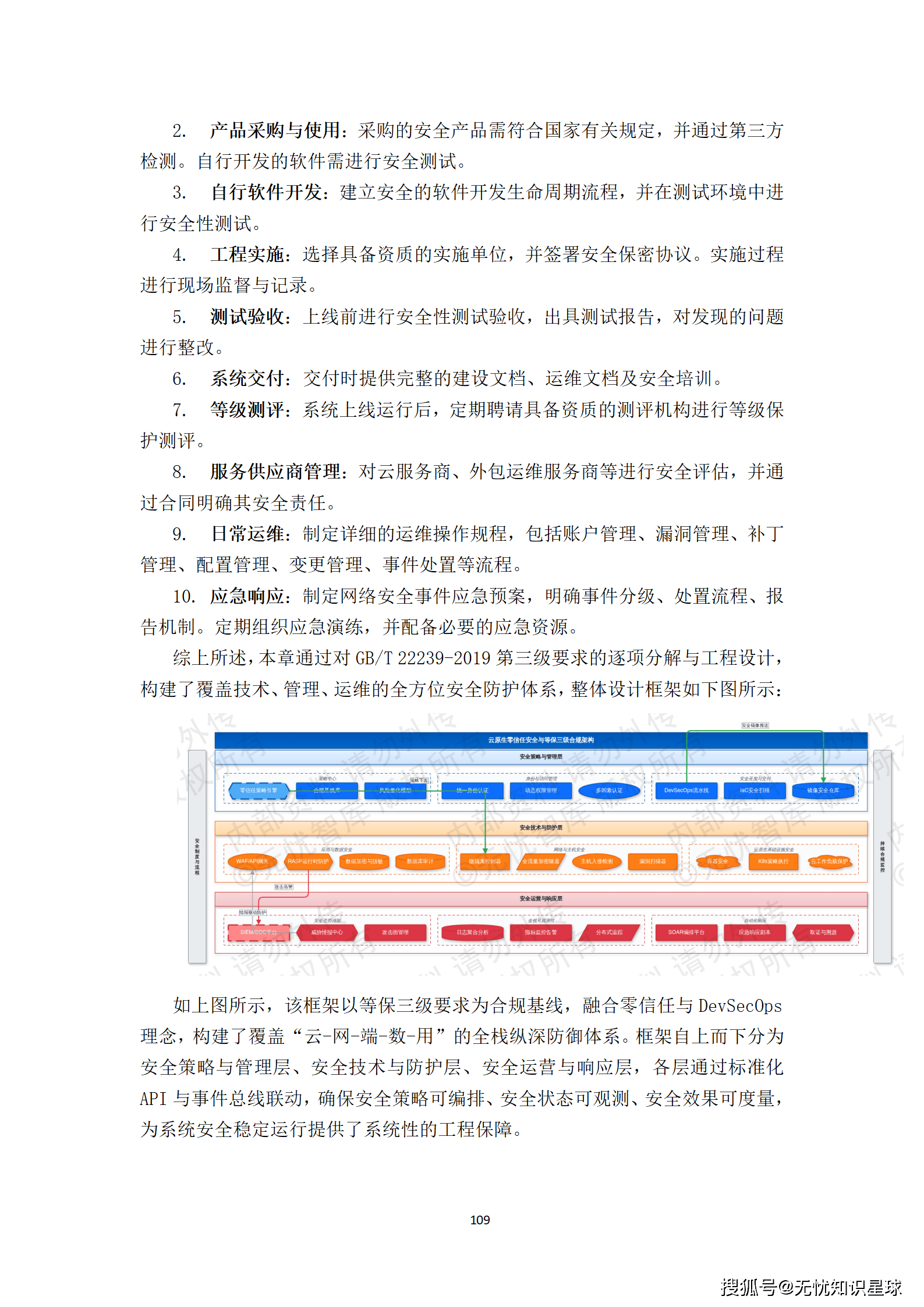
安全约束:满足网络安全等级保护三级要求。所有数据传输使用TLS 1.3加密,存储使用国密SM4加密。敏感操作(如主数据删除)需双因素认证,并留存完整操作日志。安全能力需内生于架构,而非事后叠加的补丁。
扩展性约束:采用微服务架构和容器化部署,支持水平弹性扩缩容。新的数据模态接入、标注工具扩展、质检规则调整,应能通过管理后台配置或插件机制实现,不需要改动核心代码。
十二、数据标准与合规:不可绕开的红线
12.1 核心标准遵循
数据标准不是锦上添花,是互操作性的基础:
- DICOM 3.0:医学影像数据的存储和传输标准,必须严格遵循,不允许破坏DICOM标准格式;
- HL7 FHIR R4:医疗信息交互的现代标准,核心业务接口(如患者信息、检查申请)优先采用FHIR定义;
- ICD-10:疾病分类编码标准,所有疾病诊断实体必须映射至ICD-10编码;
- LOINC:实验室检验和临床测量的标准编码体系;
- GB/T 39725-2020:个人信息去标识化的国家标准,脱敏处理必须满足此标准要求。
12.2 合规框架
合规不是一次性审查,而是贯穿整个数据生命周期的持续活动:
数据采集合规:每家合作医院的数据使用,必须有经过伦理委员会审批的数据使用协议,明确数据范围、使用目的、安全措施和数据销毁要求。
数据处理合规:脱敏处理要有标准化规则模板和审计日志,可以证明哪些PHI字段被如何处理。
数据流转合规:数据的每一次访问、查询、下载都要记录,形成不可篡改的审计追踪链条。这不仅是合规要求,也是事故发生后快速溯源的能力基础。
合规审计:平台需要支持第三方安全审计,并能生成可追溯至具体项目、算法和操作人员的完整数据流转日志。
十三、数据集规划:规模、模态与疾病覆盖
13.1 规模目标
首期数据集目标不少于10万例,数据需源自至少5家三级甲等医院,以确保来源多样性和代表性。单一机构数据会带来系统性偏差------那家医院的设备特点、医生习惯、病患人群特征,都会被模型"学进去",导致在其他医院部署时泛化性能骤降。
13.2 模态构成

13.3 疾病覆盖
疾病覆盖需聚焦高诊疗需求领域,一期涵盖八个核心谱系:肺癌(含不同亚型与分期)、乳腺癌(钼靶与病理)、结直肠癌(CT与病理)、脑卒中(CT与MRI)、冠状动脉疾病(冠脉CTA)、阿尔茨海默病(结构MRI与PET)、糖尿病视网膜病变(眼底彩照)、骨折(X光与CT)。
每个疾病谱系需包含不同分期(早、中、晚期)及治疗前后状态样本。对于罕见病例,需要制定专项采集和数据增强策略,防止类别不均衡导致的模型偏差。
结语:数据基础设施是医疗AI的真正护城河
聊到这里,我想说一句可能让一些人不舒服的话:在医疗AI领域,算法层面的竞争壁垒远没有数据层面的竞争壁垒高。
算法可以复现,论文是公开的,开源框架降低了一切高级算法的使用门槛。但一个高质量的、多模态关联的、覆盖中国人群疾病谱的医疗数据集,需要多家医院多年的数据积累、专业医生的大量标注投入、完善的数据治理体系,以及解决数不清的合规和工程问题。这些东西没有捷径,也无法用钱快速买来。
谁先建立起这个数据基础设施,谁就在中国医疗AI的长期竞争中占据了最难被攻破的阵地。
这就是为什么本文描述的这套数据工程体系,看起来工程量巨大、细节繁琐,但每一个设计决策都值得认真对待。DICOM解析的MD5校验、NLP实体识别的置信度阈值、EMPI的概率匹配参数、Kappa系数的分层标准------这些细节,就是高质量数据集和普通数据堆砌之间的分水岭。
做好数据,是医疗AI从"技术演示"走向"临床实用"的必经之路。没有别的方法。
关于本文:本文系统梳理了多模态医疗影像与结构化病历关联高质量数据集的设计方案,涵盖政策背景分析、技术架构设计、DICOM解析工程、NLP结构化处理、联邦化标注平台、全链路质量管理、数据集版本治理等核心主题,适合医疗AI产品经理、数据工程师、技术架构师及医疗健康领域数字化从业者阅读参考。