核心看点
- AAVLINK利用Cre/loxP介导的分子间DNA重组,实现双/三载体系统对"大基因(>5 kb)"的高效、精准递送与全长蛋白重构,是AAV递送领域的新一代技术路径。
- 在细胞与多种动物模型中,AAVLINK对荧光素酶等报告基因的重构效率显著优于内含肽(intein)蛋白反式剪接与mRNA反式连接等技术,且全长蛋白占比高、截短副产物极少。
- 在Shank3相关Phelan‑McDermid综合征与SCN1A相关Dravet综合征小鼠模型中,AAVLINK介导的基因替换可恢复关键蛋白表达、改善行为表型并显著延长存活,显示出明确的治疗潜力。
- AAVLINK2.0通过弱启动子(SCP1)与蛋白降解标签(UDeg3a)显著降低Cre残留表达,提升安全性;同时研究团队构建了198个大基因/编辑工具的资源库,载体信息已在Addgene等平台共享,加速方法推广与临床转化
腺相关病毒(AAV)是基因治疗领域的理想载体,它具有非致病性、可感染分裂与非分裂细胞、能介导基因长期稳定表达且插入突变风险低等优势,已在视网膜病变、血友病等多种遗传病的临床治疗中获批应用。但AAV存在一个关键技术瓶颈------包装容量通常小于5kb,这使得超过该长度的大基因无法被有效递送。为解决这一问题,科研人员开发出DNA反式剪接、RNA 反式剪接、蛋白反式剪接等策略,但这些方法普遍存在基因重构效率低、易产生截短蛋白副产物、依赖特定切割位点等缺陷,难以满足临床治疗的需求。
2026年1月27日,中国科学院深圳先进技术研究院路中华研究员 、刘太安副研究员 团队与北京大学第一医院姜玉武教授 团队联合在Cell 发表题为"AAVLINK: A potent DNA-recombination method for large cargo delivery in gene therapy "的研究论文。研究团队开发出基于Cre/loxP介导的分子间DNA重组技术的AAVLINK系统,旨在实现大基因的高效、精准递送。

·研究结果 ·
一、AAVLINK系统的设计与优化
AAVLINK采用双载体设计突破容量限制,核心依赖Cre/loxP位点特异性重组机制。其中一个载体携带目的基因(GOI)的5'端序列和剪接供体(SD),另一个载体携带Cre重组酶序列、lox位点、目的基因3'端序列及poly(A) 信号。
该系统的重组过程分为三步:第一步是Cre重组酶表达;第二步是Cre介导两个载体的lox位点重组,将目的基因的5'端与3'端连接,同时使Cre编码序列与表达元件分离,实现其表达自抑制;第三步是重组后的基因经RNA剪接,最终表达出全长目的蛋白。
为降低重组的可逆性,研究团队采用了不对称突变的lox位点(loxJT15和loxJTZ17),重组后产生的双突变lox位点无法被Cre识别,使重组过程不可逆。实验验证显示,该系统在HEK293T细胞、小鼠皮层及食蟹猴脑组织中均能高效重构增强型黄色荧光蛋白(EYFP),且几乎不产生截短蛋白,Cre重组酶的表达也会在重组完成后快速降至基线水平。
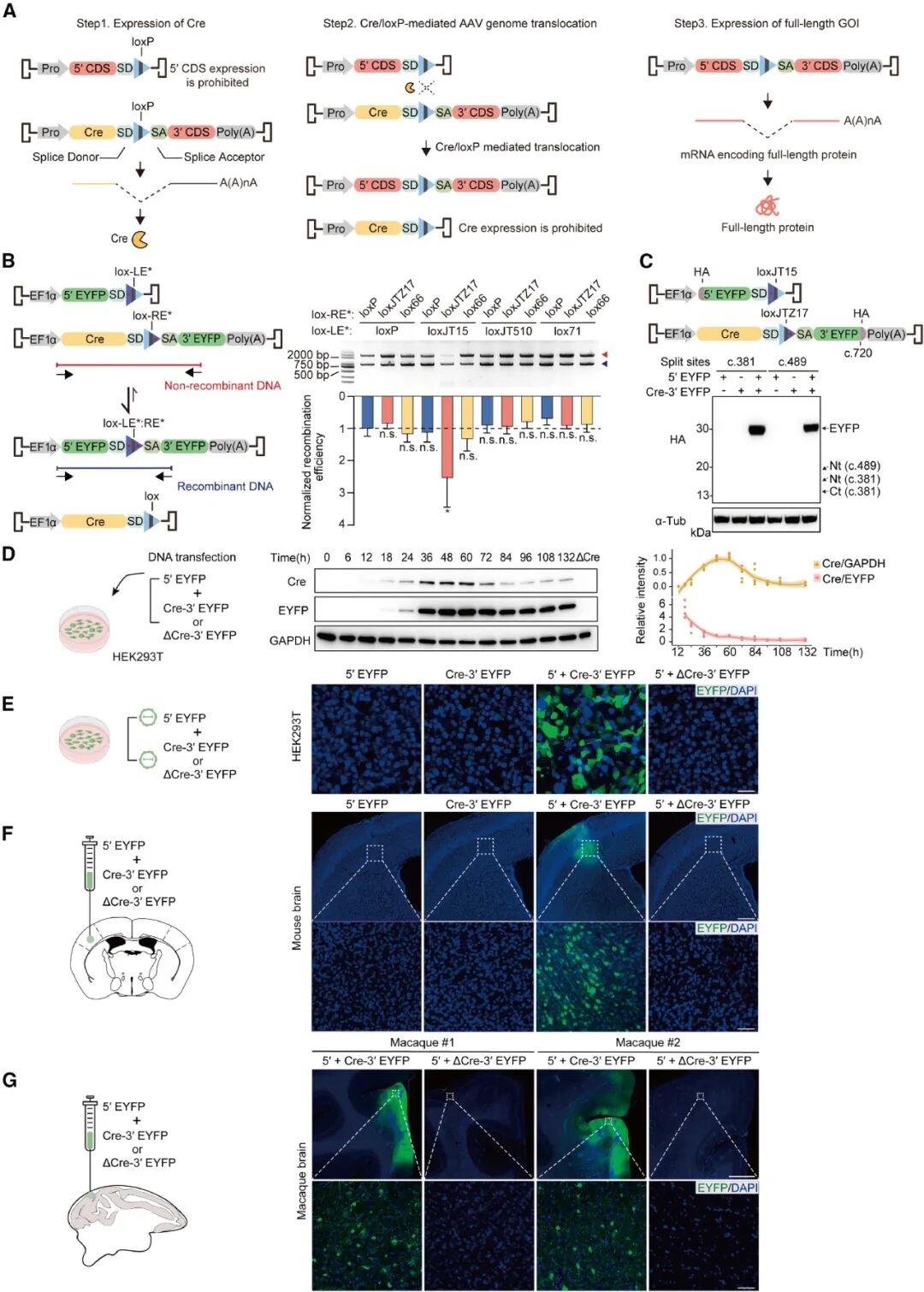
图1. AAVLINK的设计与优化
二、三载体系统拓展超大基因递送能力
为进一步承载更大的基因片段,研究团队开发了三载体AAVLINK系统。该系统引入两组互不干扰的lox位点,第一组负责连接目的基因的5'端与中间片段,第二组利用带有spacer突变的lox2272位点连接中间片段与3'端,避免不同lox位点之间的交叉反应。
实验中,研究人员将红色荧光蛋白(TagRFP)基因拆分为三段并分别装入三个载体,在HEK293T细胞、小鼠及食蟹猴脑组织中均实现了高效的全长蛋白表达,且无截短副产物。经测算,三载体AAVLINK系统的有效递送容量可达11kb,足以覆盖绝大多数人类遗传病相关的大基因。
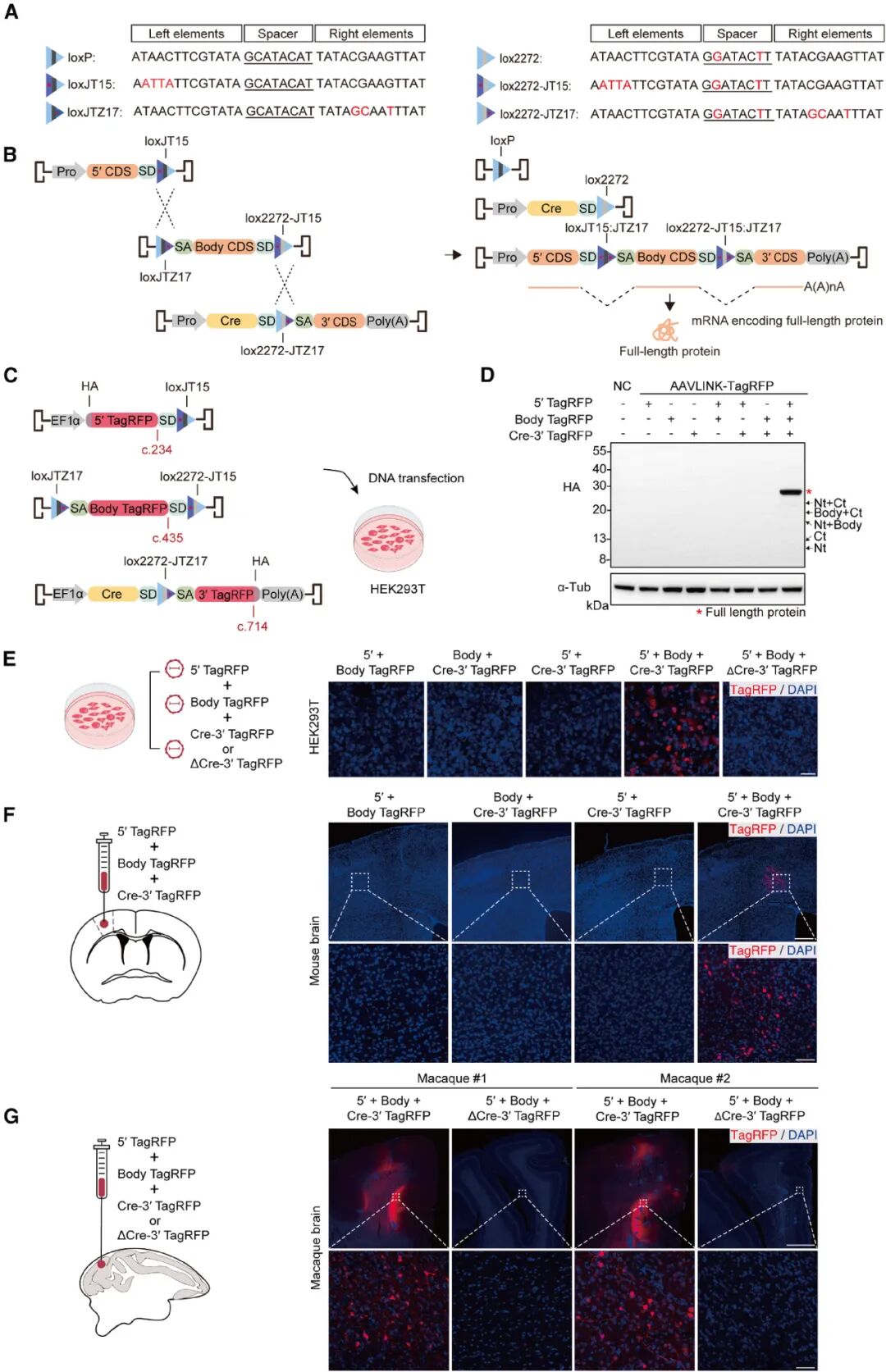
图2. AAVLINK三载体系统递送基因
三、相比传统方法,AAVLINK具有显著效率优势
研究团队将AAVLINK与主流的内含肽(Intein)介导蛋白重组、StitchR mRNA反式连接技术进行了全面对比。在荧光素酶报告基因实验中,双载体AAVLINK的重构效率最高是内含肽方法的23.3±1.3倍,三载体系统的效率更是达到后者的245.5±156.7倍。
在体内实验中,通过小鼠眼眶后注射递送荧光素酶基因,AAVLINK的发光强度是内含肽方法的4.5±1.4倍。针对Shank3(5.4kb)、CEP290(7.4kb)等大基因的重构实验显示,AAVLINK的蛋白表达量远超内含肽方法,且全长蛋白占比高达83.4%±2.4%,而内含肽方法的全长蛋白占比仅为0.2%。与StitchR技术相比,AAVLINK在细胞和小鼠脑组织中的基因重构效率也具有明显优势。
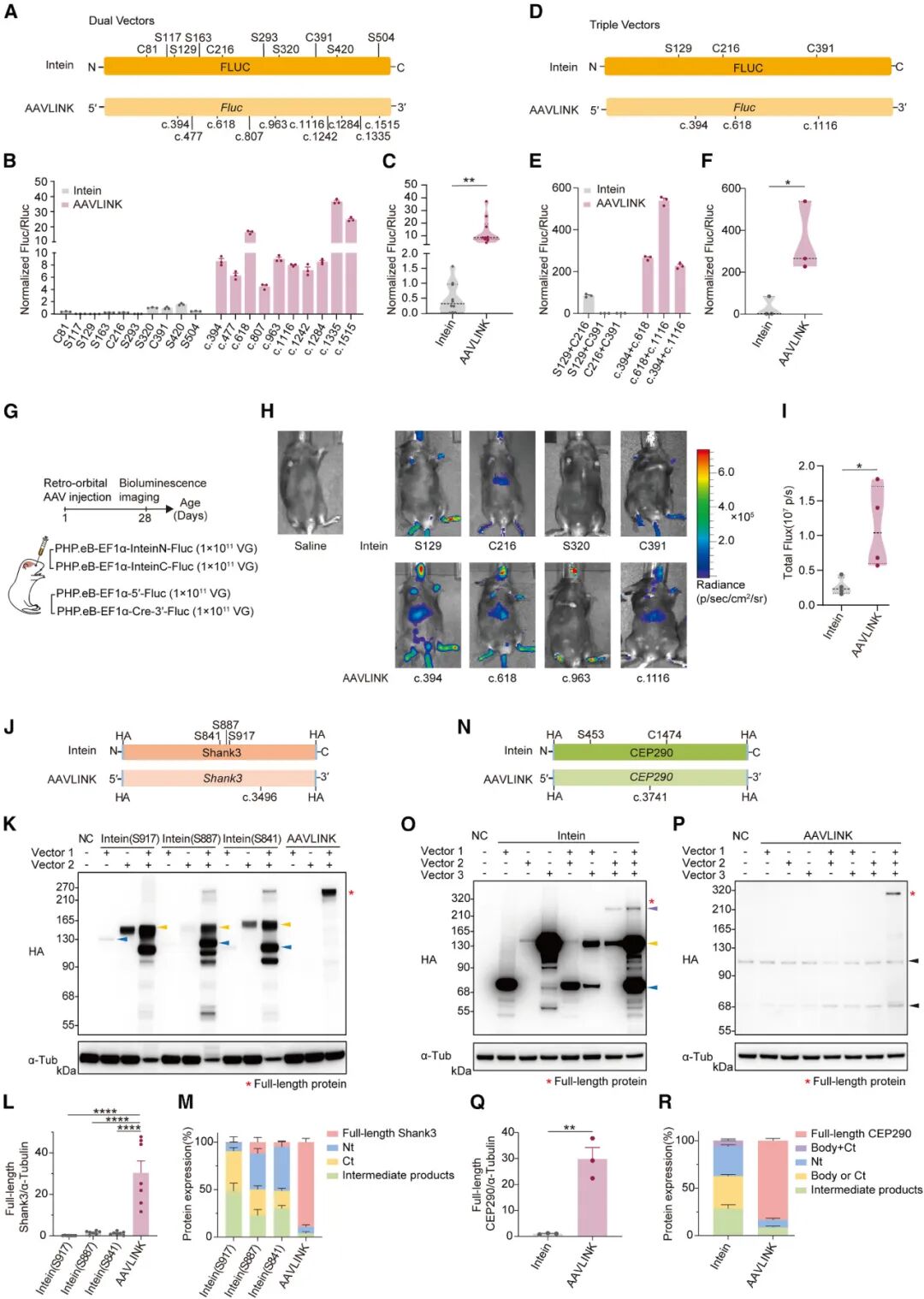
图3. AAVLINK与内含肽方法的比较
四、AAVLINK在疾病模型中验证治疗潜力
研究团队在两种遗传病小鼠模型中验证AAVLIN的治疗效果。在Shank3基因敲入突变的Phelan-McDermid综合征模型中,向小鼠纹状体注射携带Shank3基因的AAVLINK载体后,脑组织中检测到大量全长Shank3蛋白表达,小鼠的刻板行为和运动能力缺陷得到显著改善。
在SCN1A基因缺失的Dravet综合征(一种难治性癫痫)模型中,新生小鼠经眶后静脉注射 AAVLINK-SCN1A载体后,脑内成功表达Nav1.1蛋白,小鼠的高热诱导癫痫发生率显著降低,存活时间大幅延长。电生理实验证实,治疗后的小鼠海马锥体神经元兴奋性恢复正常,快放电中间神经元的功能也得到修复,癫痫相关的皮层脑电异常活动明显减少。
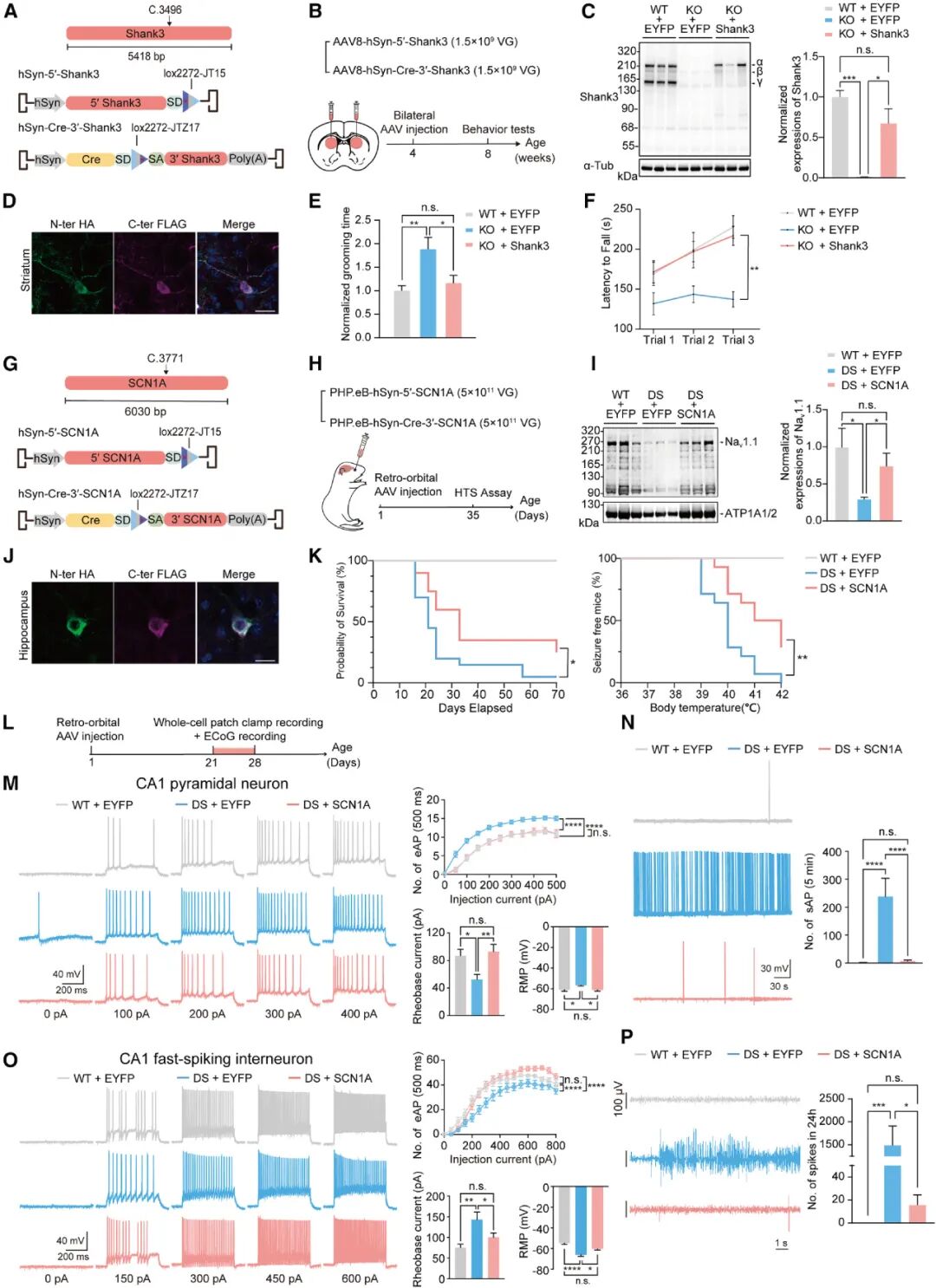
图4. AAVLINK介导的基因替换疗法在PMS和Dravet综合征小鼠模型中的应用
五、高效递送CRISPR工具,拓展基因编辑应用场景
AAVLINK还可用于递送体积庞大的CRISPR基因编辑工具。研究人员将SpCas9、腺苷碱基编辑器ABE8e、胞嘧啶碱基编辑器YE1-BE4max、转录激活因子dSpCas9-VPH等工具拆分为两段,通过双载体AAVLINK递送,在细胞中实现了高效的蛋白重构与功能验证。
在体内实验中,AAVLINK递送的SpCas9可在小鼠肝脏中实现Rosa26位点的精准切割;递送的ABE8e可编辑Pcsk9基因,有效降低小鼠体内的Pcsk9蛋白水平;递送的dSpCas9-VPH则能在小鼠海马中特异性激活SCN1A基因的表达,为基因编辑疗法的体内应用提供了新方案。
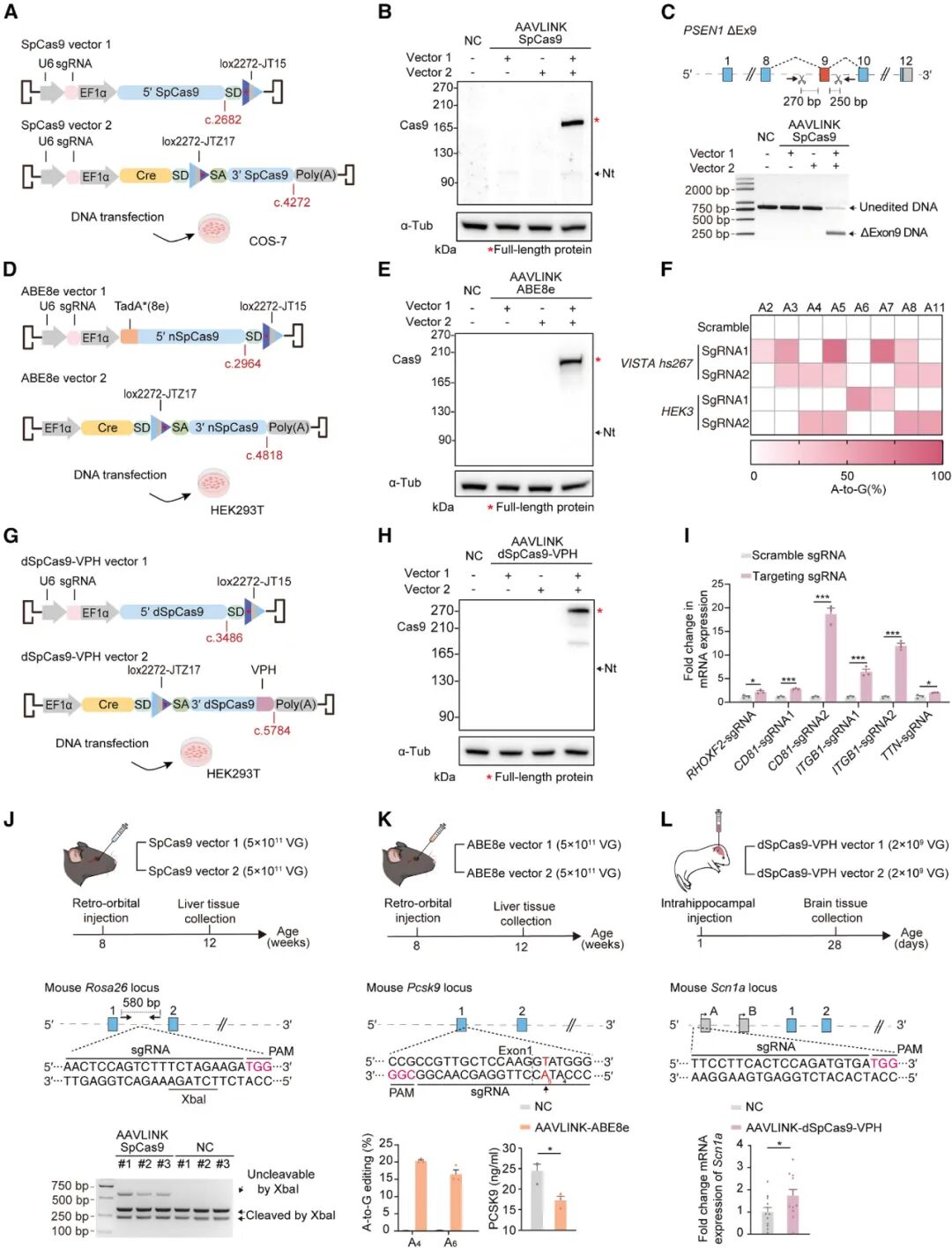
图5. 通过AAVLINK递送CRISPR工具
六、AAVLINK2.0升级,提升生物安全性
为解决Cre重组酶长期表达可能带来的生物安全隐患,研究团队开发了升级版的 AAVLINK2.0系统。该系统通过两步优化降低Cre的残留表达:一是选用弱启动子SCP1驱动Cre表达,减少其初始表达量;二是在Cre蛋白C端融合降解标签UDeg3a,加速Cre的蛋白降解。
实验结果显示,AAVLINK2.0在维持高效基因重构能力的同时,Cre蛋白的表达水平降至Western blot检测下限,在小鼠和食蟹猴脑组织中均未检测到Cre的残留信号,极大提升了该系统的临床转化潜力。
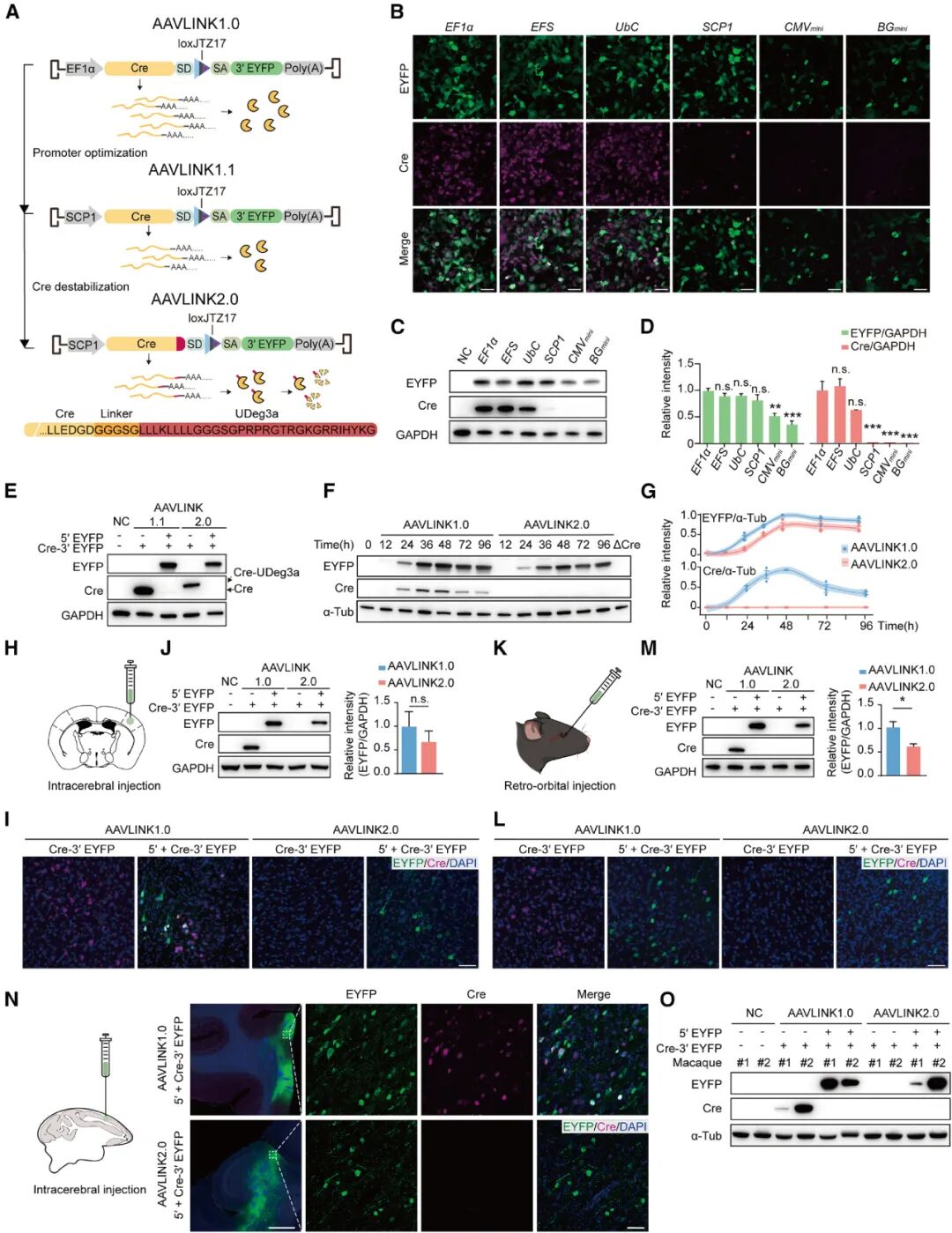
图6. AAVLINK2.0系统中Cre表达最小化
七、构建198个大基因资源库,开放共享科研工具
研究团队基于AAVLINK系统构建了一个大基因递送资源库,涵盖193个与遗传病相关的大基因(包括166个自闭症风险基因和27个其他遗传病基因)和5个CRISPR工具。所有基因均在细胞水平验证了DNA重组和蛋白表达的有效性,相关载体信息已上传至Addgene等质粒库,并搭建了专用网站(http://AAVLINK.com/)供科研人员查询和获取。
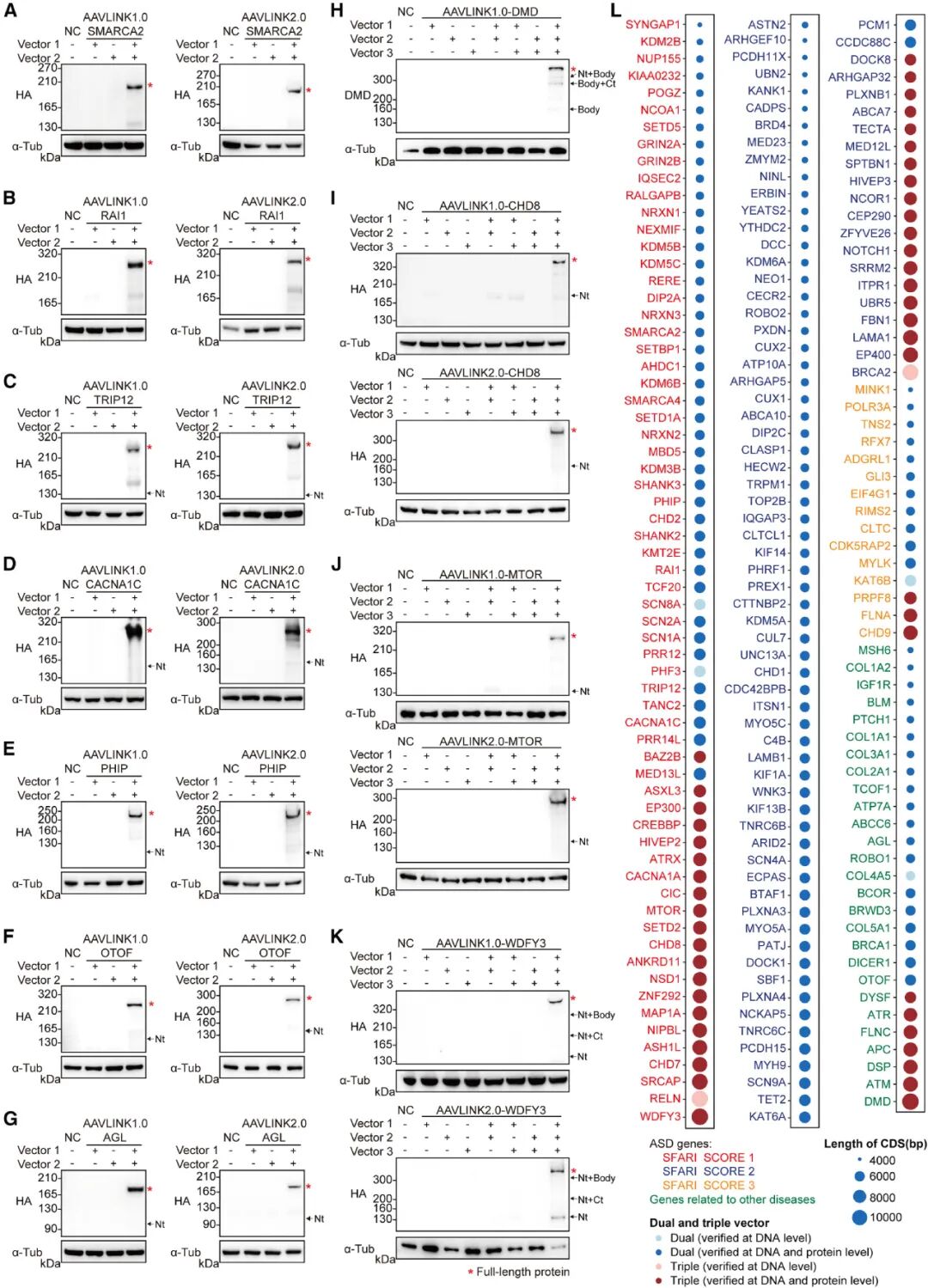
图7. 用于遗传疾病相关大基因递送的AAVLINK资源库
·总结 ·
AAVLINK系统的研发与应用,为基因治疗领域长期存在的大基因递送难题提供了突破性解决方案。从基础研究到临床前开发,稳定的AAV载体与精准的组织靶向又是实现AAVLINK优势的重要保障。本研究中运用和元的AAVLINK载体,靶向精准,质量稳定,作者通过Cre/loxP介导的精准重组机制,结合双载体与三载体的灵活设计,该系统不仅突破了传统AAV载体的容量限制,更在效率、特异性和生物安全性上实现了多重优化,其2.0版本对Cre表达的精准调控进一步降低了临床应用风险。从疾病模型的成功救治到CRISPR工具的高效递送,再到198个大基因资源库的构建,AAVLINK展现出横跨基础研究与临床转化的广泛价值,为自闭症、难治性癫痫等因大基因缺陷导致的遗传病提供了全新治疗路径。
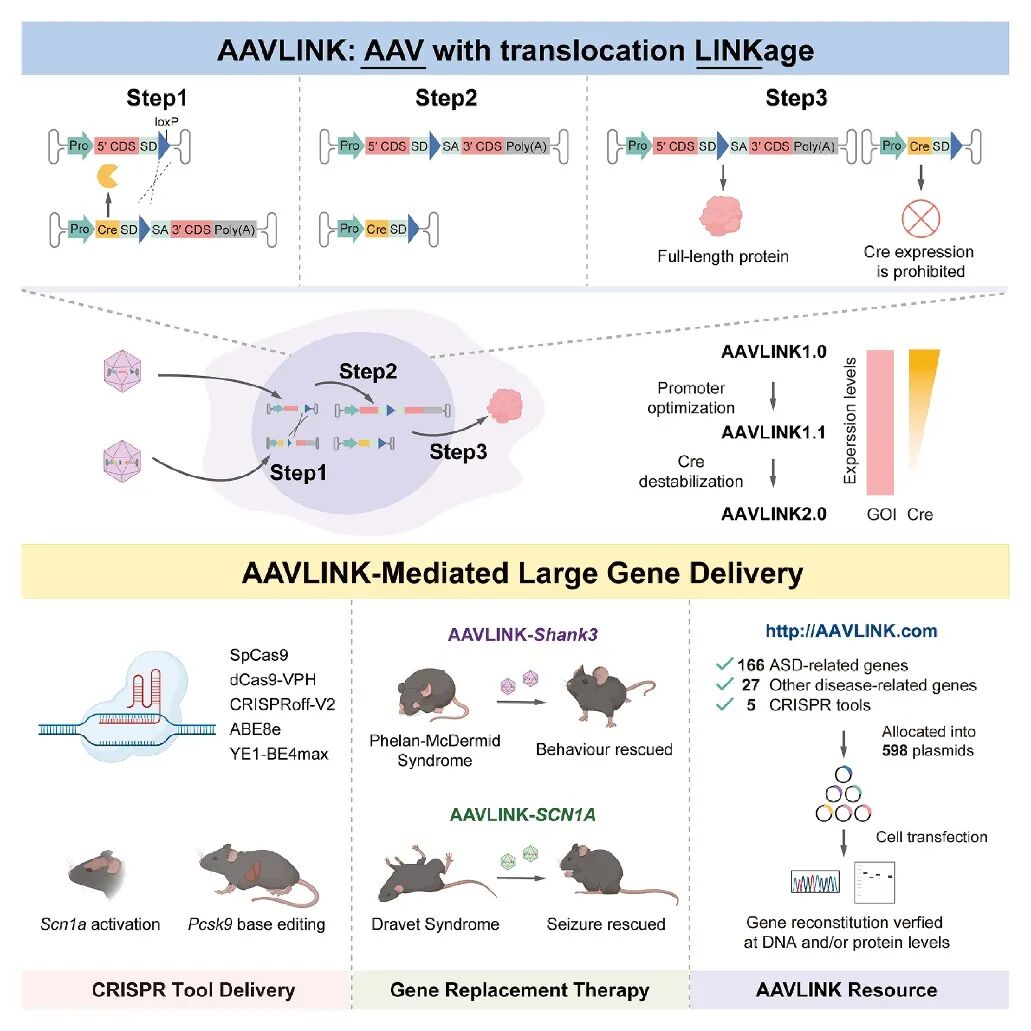
图8. AAVLINK系统模式图
FAQ
Q1:AAVLINK适合哪些基因/场景?
AAVLINK主要面向超出单AAV包装上限(通常>4.7--5 kb)的较大基因,如神经精神疾病相关基因(Shank3、SCN1A、CEP290等)和大型CRISPR编辑工具(SpCas9、碱基编辑器、转录激活因子等)。通过双载体或三载体设计,AAVLINK可在细胞及多种组织(如脑、肝、眼等)中实现全长基因重构与功能表达。
Q2:双载体与三载体AAVLINK如何选择?
一般而言,对于编码区(CDS)长度适中的基因,优先考虑双载体AAVLINK;当CDS进一步增大,超出双载体系统的安全/效率窗口时,可选用三载体AAVLINK进行分段递送。