01
文献学习

今天分享的文献是由空军军医大学西京医院赵丽娜教授等团队于2026年3月在《Radiotherapy and Oncology》(中科院2区,IF=5.3)上发表的研究"A longitudinal CT-based subregional radiomics nomogram for predicting local recurrence-free survival in esophageal squamous cell carcinoma after definitive chemoradiotherapy: a multicenter study "即基于纵向CT的亚区域放射组学列线图预测食管鳞状细胞癌根治性放化疗后局部无复发生存期:一项多中心研究,该研究开发并验证了一种基于纵向CT影像的亚区域放射组学列线图(Clrad),用于预测食管鳞状细胞癌患者接受根治性放化疗后的局部无复发生存期。研究通过构建肿瘤内亚区域与肿瘤周围区域的放射组学特征,结合临床因素,显著提升了预后预测性能,并通过SHAP解释与RNA测序揭示了模型背后的生物学机制。
创新点:①首次整合纵向CT与亚区放射组学 ,同时捕捉肿瘤时空异质性 ,突破传统单一时点全肿瘤分析的局限。②构建融合模型 ,结合瘤内亚区与瘤周特征,经多模型比较优选GBM,预测性能显著优于传统方法 。③引入SHAP与转录组学双重解释 ,揭示影像特征与B细胞活化、氧化应激的关联,提升模型可解释性与生物学可信度。
临床价值:①构建Clrad列线图 ,精准分层局部复发风险,指导个体化辅助治疗与随访策略 ,优化临床决策。②基于多中心数据验证 ,模型在外部队列中表现稳健,具备良好泛化能力 ,利于临床推广。③影像与转录组关联分析 ,为靶向肿瘤微环境与氧化应激的干预策略提供潜在生物标志物与理论依据。
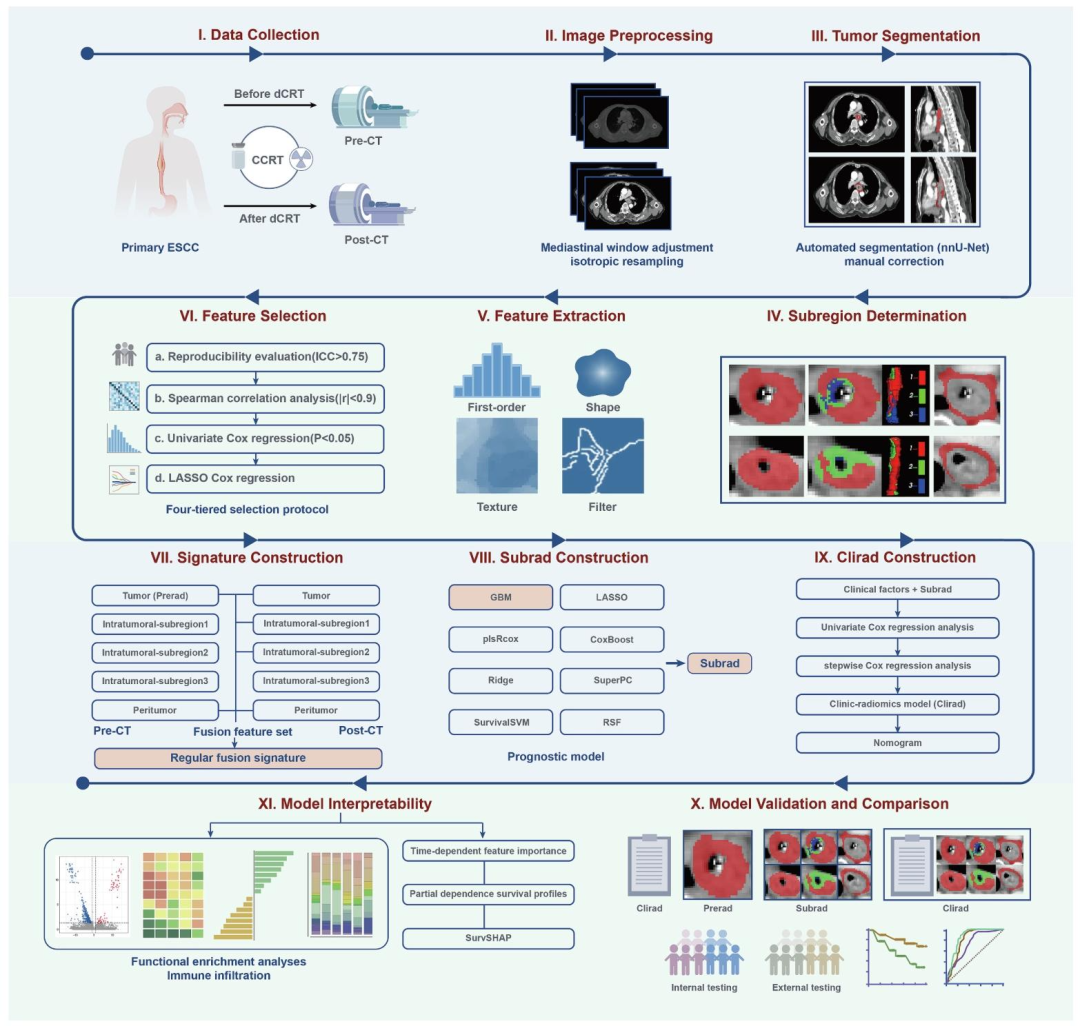
图 1:研究整体工作流程图
影像与数据预处理模块(I-IV步)
I. 数据收集:纳入ESCC患者dCRT治疗前(Pre-CT)、治疗后(Post-CT)的纵向增强CT影像,同步收集临床基线、治疗参数、随访数据,以及用于影像基因组学的配对肿瘤组织样本。
II. 影像预处理:对CT影像行标准化处理,包括纵隔窗调整(窗宽400HU、窗位40HU)、各向同性重采样(1.0×1.0×1.0mm³),消除设备与扫描参数带来的系统偏差。
III. 肿瘤分割:采用nnU-Net自动分割算法勾画肿瘤靶区、瘤周区域,再由高年资放射科医师人工校正,确保ROI精准性。
IV. 肿瘤亚区判定:研究核心创新步骤,通过「局部熵图生成→初级k-means聚类为40个超体素→次级k-means聚类→最大化CH指数确定最优3个瘤内亚区」,完成肿瘤空间异质性的定量分区。
特征筛选与模型构建模块(V-IX步)
V. 特征提取:基于PyRadiomics从全肿瘤、3个瘤内亚区、瘤周区域,分别提取符合IBSI标准的1316个影像组学特征,涵盖一阶、形状、纹理、滤波后特征4大类。
VI. 特征筛选:四阶严格筛选流程避免过拟合与冗余:①可重复性评估(ICC>0.75);②Spearman相关性分析(去除r>0.9的冗余特征);③单因素Cox回归(保留P<0.05的LRFS相关特征);④LASSO-Cox回归筛选非零系数核心特征。
VII. 区域特异性特征构建 :基于LASSO-Cox系数,为治疗前/后全肿瘤、瘤内亚区、瘤周区分别构建区域特异性签名,其中治疗前全肿瘤签名定义为Prerad(传统对照模型)。
VIII. Subrad签名构建 :①合并3个数据集C-index>0.6的区域特征为融合特征集;②对比8种主流生存模型;③基于内部验证集最优性能选择GBM算法,构建纵向亚区融合影像组学签名Subrad。
IX. Clirad模型构建 :①通过单因素+多因素Cox回归筛选临床独立预后因素;②与Subrad签名行逐步多因素Cox回归,构建临床-影像组学融合模型Clirad,并可视化为列线图。
模型验证与可解释性模块(X-XI步)
X. 模型验证与对比:通过C-index、时间依赖性AUC评估预测性能;KM生存分析+log-rank检验验证风险分层能力;校准曲线、亚组分析验证模型一致性与稳健性。
XI. 模型可解释性分析:通过时间依赖性特征重要性、SurvSHAP解析模型决策机制;通过功能富集、免疫浸润分析等影像基因组学方法,挖掘Subrad签名的生物学机制。
02
研究背景和目的
研究背景
食管鳞状细胞癌(ESCC)是食管癌最常见的病理类型,根治性放化疗(dCRT)是局部晚期不可切除患者的标准治疗方案 。然而,即使接受规范治疗,仍有超过50% 的患者面临局部复发风险,五年生存率不足 25%,凸显了精准预后评估的临床紧迫性。传统影像组学模型多基于治疗前全肿瘤区域提取特征,这种方法往往平均化了肿瘤内部的空间异质性 ,难以捕捉肿瘤微环境的关键信息。近年来,亚区域(habitat)影像组学 通过划分瘤内不同功能亚区、结合瘤周区域,能够更精细地反映肿瘤的生物学异质性。此外,肿瘤在治疗过程中会经历结构和功能的动态演变,仅依靠治疗前图像无法完整刻画其时间维度的变化。因此,将治疗前后纵向CT图像与亚区域分析相结合 ,有望更全面地捕获肿瘤的时空异质性,从而提升预后预测的准确性。尽管深度学习模型在预测性能上表现优越,但其"黑箱"特性限制了临床可解释性,而可解释性机器学习方法(如SHAP)与放射基因组学分析的结合,可在提供预测结果的同时揭示其背后的生物学基础,增强临床医生的信任与采纳意愿。
研究目的
本研究旨在开发并验证一种基于纵向CT图像的亚区域影像组学列线图(Clirad),用于预测接受根治性放化疗的ESCC患者的局部无复发生存期(LRFS) 。研究通过整合治疗前后增强CT图像中的瘤内亚区与瘤周区域 影像组学特征,构建反映肿瘤时空异质性的融合特征集,并借助广义提升回归模型(GBM)建立亚区域影像组学标签(Subrad)。在此基础上,将Subrad与具有独立预后价值的临床因素(如同步化疗)相结合,形成临床-影像组学联合模型 ,并以列线图形式呈现,以提供个体化的复发风险预测。研究进一步采用SHAP方法 对模型进行解释,揭示关键特征对预测结果的影响,同时通过RNA测序与功能富集分析 探索影像组学标签背后的生物学机制,特别是其与肿瘤微环境中B细胞活化、氧化应激响应 等通路的相关性。通过多中心、多队列的严格验证,本研究旨在构建一个兼具高预测性能与临床可解释性的预后工具,为ESCC患者在接受dCRT后的个体化治疗决策(如是否加强辅助治疗或避免过度治疗)提供影像学支持。
03
数据和方法
研究数据
总样本量:306例ESCC患者
数据来源:西京医院(227例,训练+内部验证)、四川省肿瘤医院(79例,外部验证)
数据内容:dCRT前后CECT影像、临床资料、随访数据、14对组织样本用于RNA测序
技术方法
影像处理与分割:CECT预处理后,采用自动分割+手动校正勾画肿瘤与肿瘤周围区域。
亚区域聚类:基于HU值与局部熵,通过K-means聚类将肿瘤划分为3个亚区域。
特征提取与筛选:提取1316个放射组学特征,经ComBat校正、可重复性、相关性、Cox回归、LASSO等筛选。
模型构建:比较8种生存模型,选择GBM构建Subrad融合特征;结合临床因素构建Clrad列线图。
模型评估:C-index、AUC、Kaplan-Meier、校准曲线、亚组分析。
解释性分析:SHAP、SurvSHAP(t)等。
生物学探索:RNA-seq、GSEA、GSVA、CIBERSORTx免疫浸润分析。
04
实验结果
Subrad模型在外部测试集中C-index为0.706,显著优于临床模型(0.629)与传统全肿瘤放射组学(0.598)。
Clrad模型结合Subrad与同步化疗,C-index在训练集为0.896,内部测试集0.725,外部测试集0.708。
风险分层:高风险组LRFS显著更差(P<0.05)。
生物学机制:高风险组富集B细胞活化、氧化应激相关通路,且naive B细胞浸润更高。
解释性:Subrad是模型中最强预测因子,SHAP分析展示了个体化风险解释。
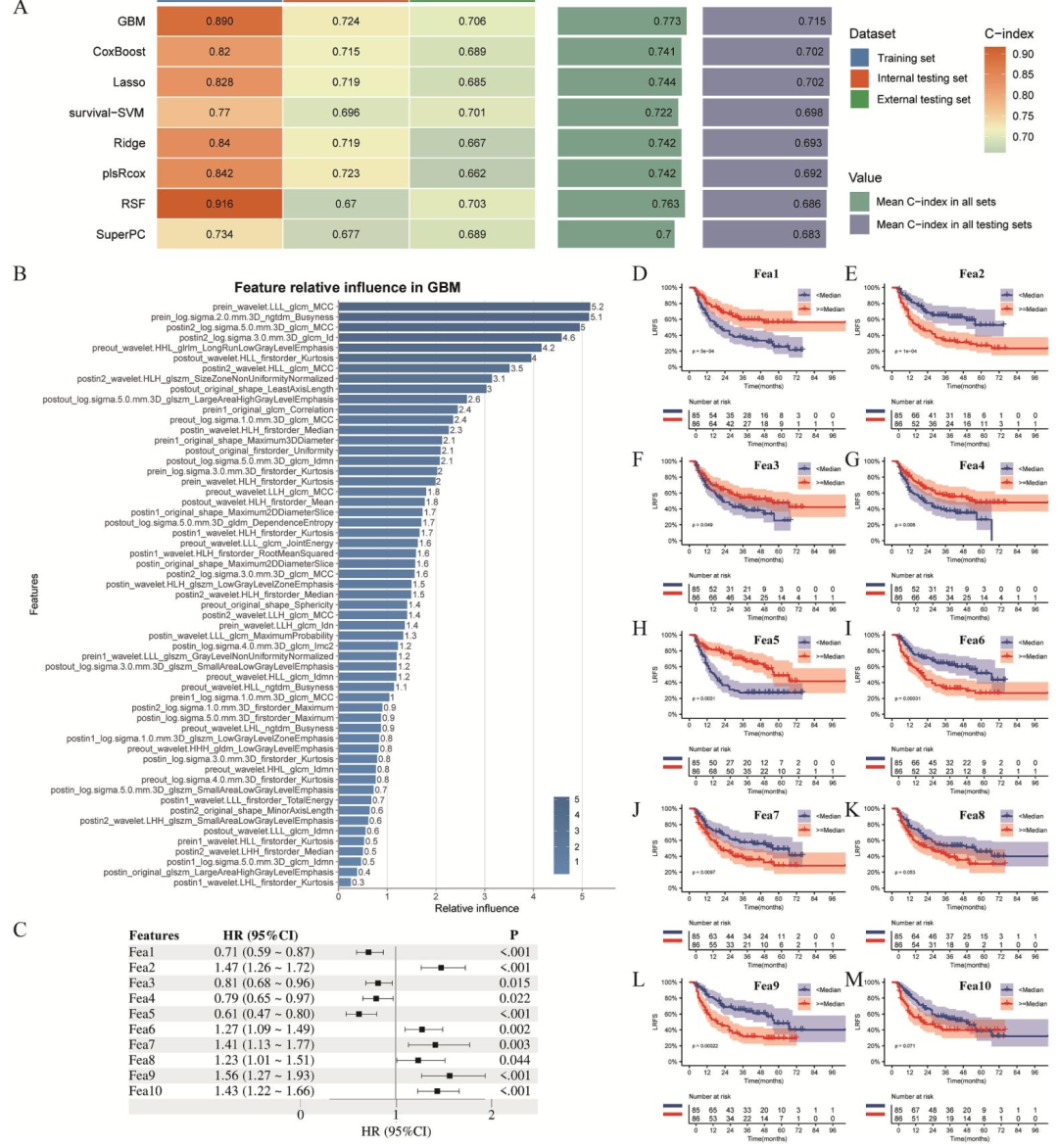
图 2:Subrad签名的模型选择与关键特征评估
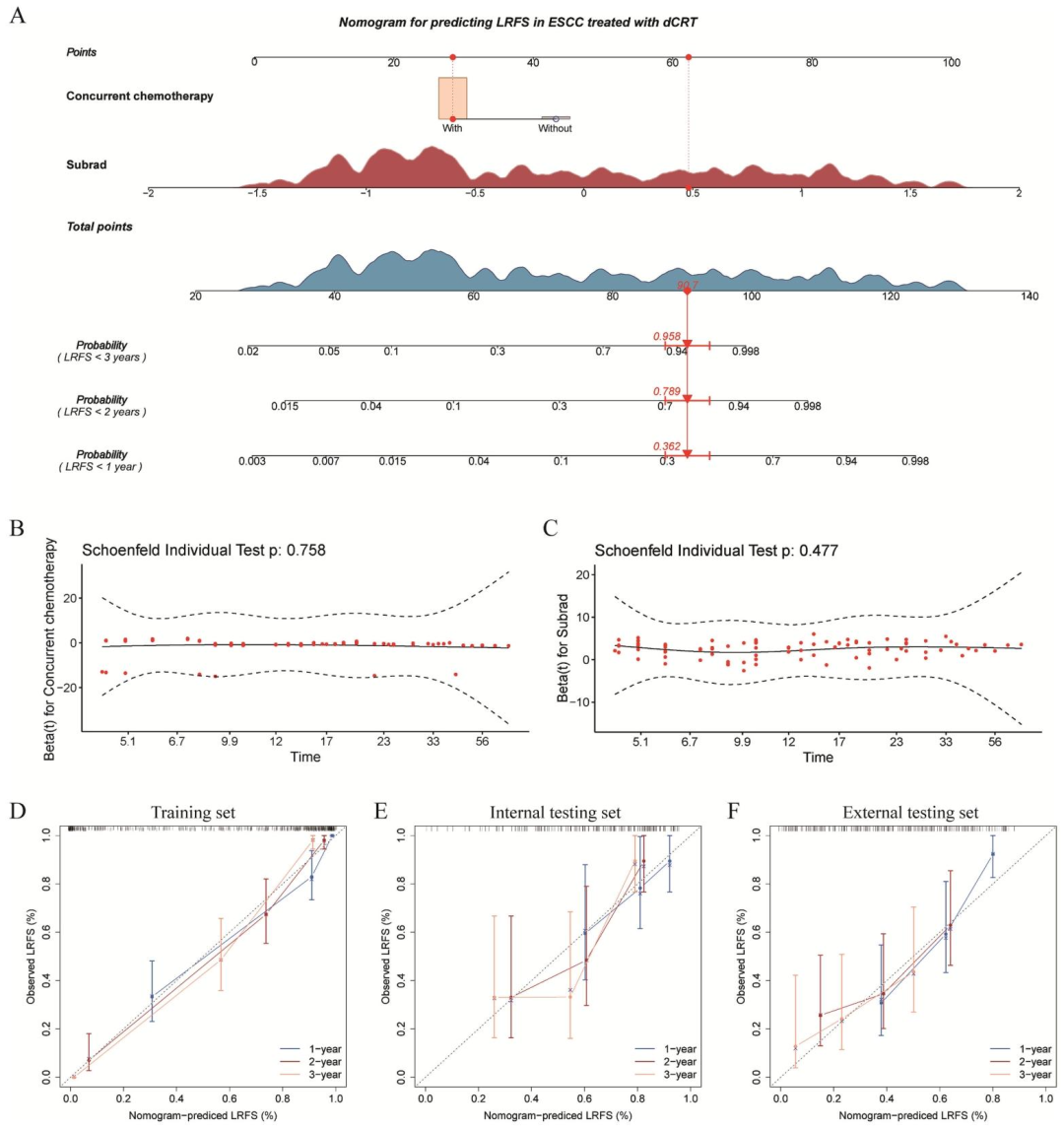
图 3:预测ESCC患者dCRT后LRFS的Clirad模型
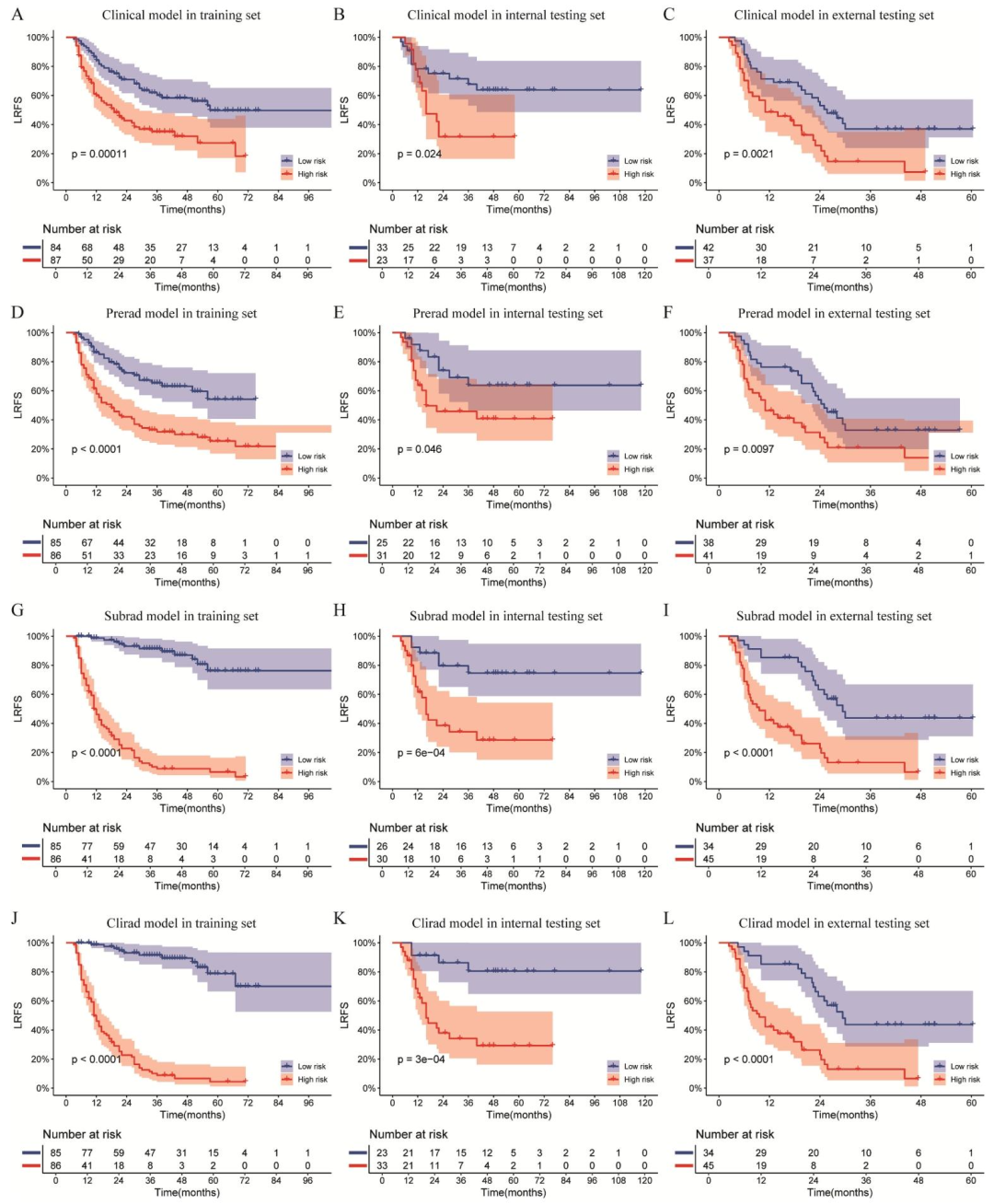
图 4:LRFS的Kaplan-Meier生存分析
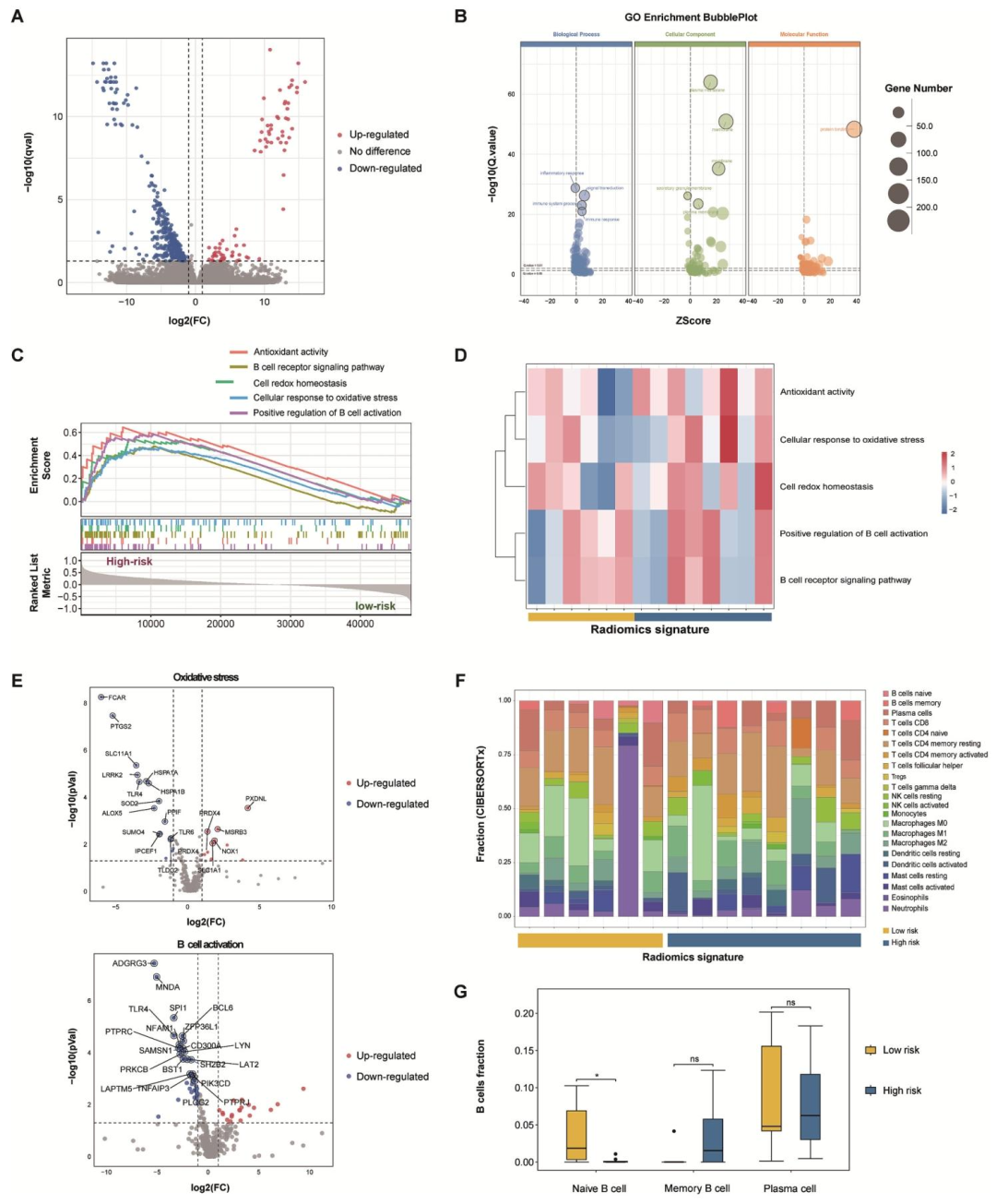
图 5:基于RNA测序的高低风险组生物学过程探索
05
研究结论
该研究构建并验证了一个基于纵向CT亚区域影像组学 的临床-影像组学列线图(Clirad),用于预测食管鳞癌患者接受根治性放化疗后的局部无复发生存期 。通过整合肿瘤内亚区域与肿瘤周围区域的动态影像特征,并结合临床因素(如同步化疗),该模型在多个独立队列中均表现出优于传统全肿瘤影像组学模型和单纯临床模型的预测性能 ,其C-index在外部测试集中达到0.708。研究进一步利用SHAP可解释性方法 和转录组分析 揭示了模型背后的生物学基础,发现高风险组患者富集了与B细胞活化、氧化应激反应 相关的通路,提示这些生物学过程可能影响复发风险。该模型能够有效将患者划分为高、低复发风险亚组,为个体化治疗策略(如强化辅助治疗或避免过度治疗)提供了具有可解释性的影像学工具,但其推广仍需前瞻性、多中心、大样本研究的验证。
参考文献:Gong J, Yang Z, Li J, Wang Q, Meng F, Liu M, Sun H, Zhao L. A longitudinal CT-based subregional radiomics nomogram for predicting local recurrence-free survival in esophageal squamous cell carcinoma after definitive chemoradiotherapy: a multicenter study. Radiother Oncol. 2026 Mar 3;218:111471. doi: 10.1016/j.radonc.2026.111471.