01
文献学习

今天分享的文献是由四川大学华西医院田蓉、李康等团队 于2026年3月23日在**《** European Journal of Nuclear Medicine and Molecular Imaging 》(中科院1区top,IF=7.6) 上发表的研究"A deep learning PET-CT biomarker for early progression (POD24) and survival stratification in follicular lymphoma: a multicenter study"即基于深度学习PET/CT的生物标志物用于滤泡性淋巴瘤早期进展(POD24)及生存分层:一项多中心研究,该研究开发并验证了一种基于基线¹⁸FFDG PET/CT的深度学习影像生物标志物(DLS),用于预测滤泡性淋巴瘤患者24个月内疾病进展(POD24)及生存风险分层。通过提取PET/CT图像的影像组学特征,结合多种机器学习与深度学习方法,构建并验证了GAMformer模型,最终形成多参数模型,显著优于传统临床风险评分。
创新点:①首次将表格深度学习应用于FL的POD24预测 ,利用GAMformer模型融合PET/CT影像特征,显著提升预测性能。②构建多参数模型整合DLS、MTV与LDH ,实现优于FLIPI等传统评分工具的精准风险分层 。③验证DLS在不同组织学分级中的一致预测能力 ,实现分级无关的个体化预后评估。
临床价值:①实现POD24高危患者的早期识别 ,为治疗强化或降级策略 提供可靠影像学依据。②提升滤泡性淋巴瘤预后评估的精准度 ,通过AI驱动的影像标志物优化个体化治疗决策 。③方法具备多中心验证与良好泛化能力 ,有望融入临床工作流,推动精准肿瘤学实践。
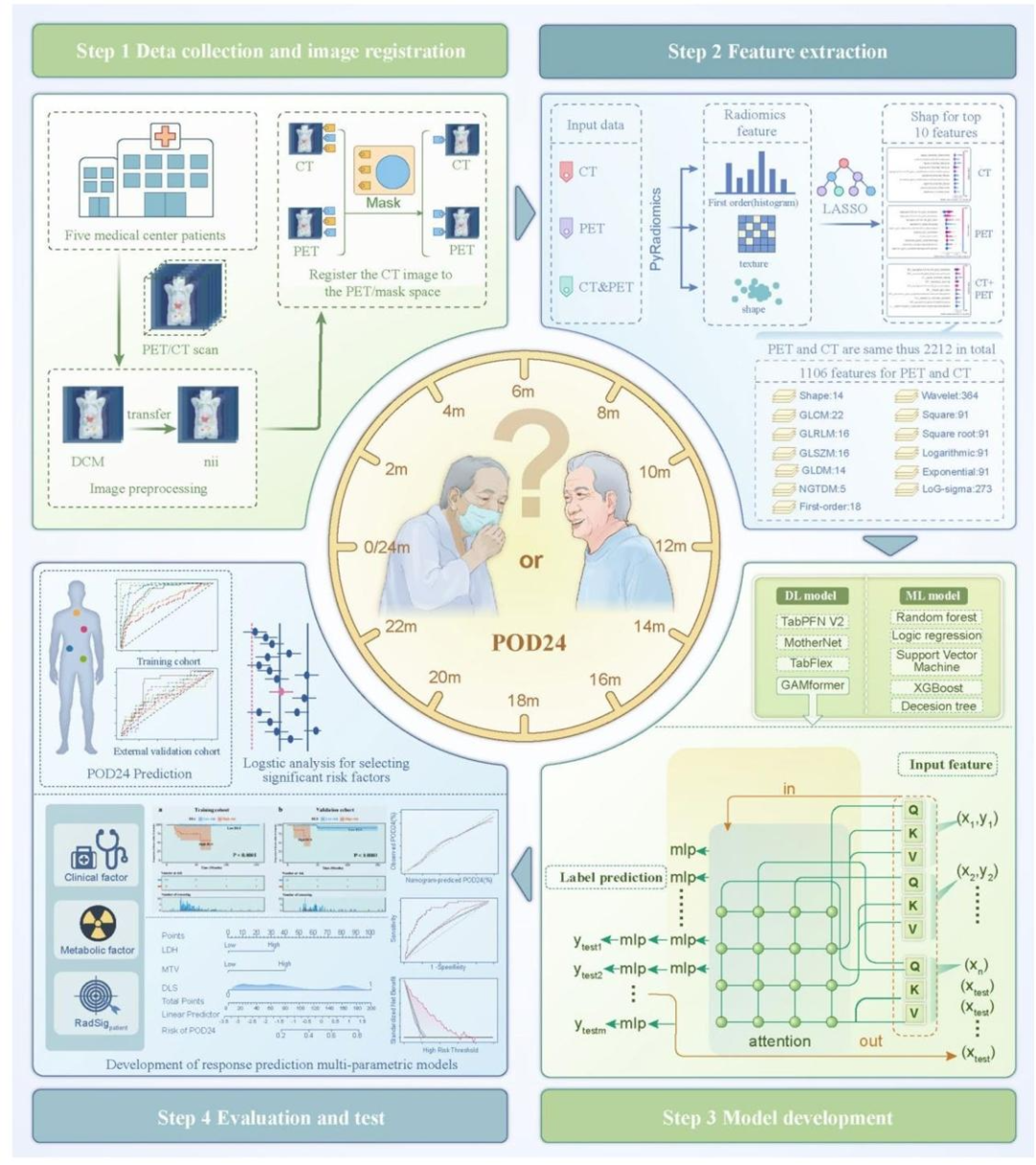
图 2 : 研究整体工作流程图
Step1:数据收集与影像配准
收集基线¹⁸F-FDG PET/CT数据,完成PET与CT影像的三维空间配准,保证肿瘤靶区对齐。
Step2:影像组学特征提取
分割肿瘤体积(VOI),提取1106个高维组学特征(形态、一阶统计、纹理、小波/LoG高阶特征)。
Step3:模型构建
LASSO算法筛选关键特征;对比5种传统机器学习+4种表格深度学习模型;选定GAMformer输出深度学习评分(DLS);融合DLS+临床/影像参数构建多参数模型。
Step4:模型评估与验证
用AUC、校准曲线、决策曲线分析(DCA)评估效能;Kaplan-Meier生存分析验证风险 分层能力。
02
研究背景和目的
研究背景
滤泡性淋巴瘤(FL)是最常见的惰性非霍奇金淋巴瘤亚型,具有显著的临床和生物学异质性。尽管多数患者对初始治疗反应良好,但仍有相当比例的患者在治疗后24个月内出现疾病进展(POD24),这一早期终点事件与极差的长期生存预后密切相关,已成为评估FL患者风险的关键临床指标。然而,现有的临床预后工具如FLIPI、FLIPI-2及PRIMA-PI等在个体化风险预测中表现欠佳,其阳性预测值和区分度有限,难以精准识别高危患者18F FDG PET/CT作为FL分期和疗效评估的标准影像学手段,可提供代谢肿瘤体积(MTV)、总病变糖酵解(TLG)等定量参数,但这些传统指标难以全面捕捉肿瘤内部复杂的空间与代谢异质性,而后者正是导致复发与治疗抵抗的关键因素。近年来,深度学习特别是表格型基础模型的发展,为从PET/CT影像中提取高维、亚视觉特征提供了新途径,但其在FL中用于POD24预测的研究尚属空白。因此,亟需开发一种基于基线PET/CT的可靠影像生物标志物,以实现对POD24的精准预测和生存风险分层。
研究目的
本研究旨在开发并验证一种基于基线18F FDG PET/CT影像的深度学习评分(DLS) ,用于预测滤泡性淋巴瘤患者确诊后24个月内疾病进展的风险,并实现个体化的生存预后分层。研究首先从多中心队列中收集患者的PET/CT影像数据,通过肿瘤分割提取高维影像组学特征,随后比较五种传统机器学习算法与四种先进表格型深度学习模型的预测效能,筛选出最优模型并将其输出定义为DLS。在此基础上,研究进一步将DLS与临床变量及PET代谢参数相结合,构建多参数预测模型 ,以提升对POD24的预测能力。通过在独立验证队列中对模型的区分度、校准度及临床净获益进行全面评估,并与现有临床风险评分(如FLIPI、FLIPI-2、PRIMA-PI)进行对比,研究旨在验证该深度学习生物标志物的优越性、稳定性及其在不同组织学分级中的适用性,最终为FL的精准治疗决策和风险适应性管理提供一种新型、非侵入性的影像学工具。
03
数据和方法
研究数据
共纳入309例初诊FL患者(1--3a级),来自5家医学中心
随机分为训练组(n=210)与验证组(n=99)
中位随访时间:训练组43.4个月,验证组45.4个月
POD24事件:训练组38例,验证组17例
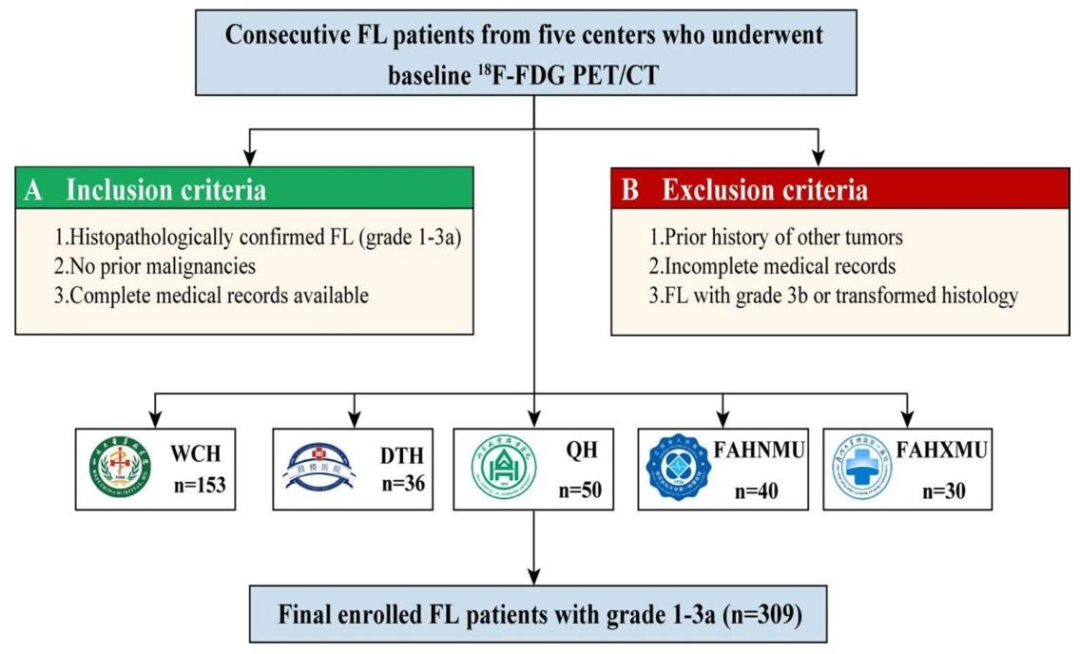
图 1 :患者筛选流程图
技术方法
图像处理:PET/CT图像配准,半自动肿瘤分割(41% SUVmax阈值)
特征提取:使用PyRadiomics提取1,106个影像组学特征(PET、CT及融合模态)
模型构建:
传统机器学习:LR、DT、RF、SVM、XGBoost
表格型深度学习:GAMformer、MotherNet、TabPFN、TabFlex
特征选择:LASSO + SMOTE处理类别不平衡
多参数模型:将DLS与MTV、LDH结合,构建联合模型
评价指标:AUC、校准曲线、决策曲线分析、Kaplan-Meier生存分析
04
实验结果
DLS表现:GAMformer模型在验证集中AUC为0.753,优于其他模型
多参数模型:AUC在训练组为0.882,验证组为0.797,优于FLIPI、FLIPI-2、PRIMA-PI
生存分层:DLS可显著区分高、低风险患者(P < 0.0001)
组织学分级:DLS在高、低分级中均具显著预后分层能力(P < 0.0001)
独立预测因子:LDH(OR=0.509)与MTV(OR=1.290)在多元分析中独立预测POD24
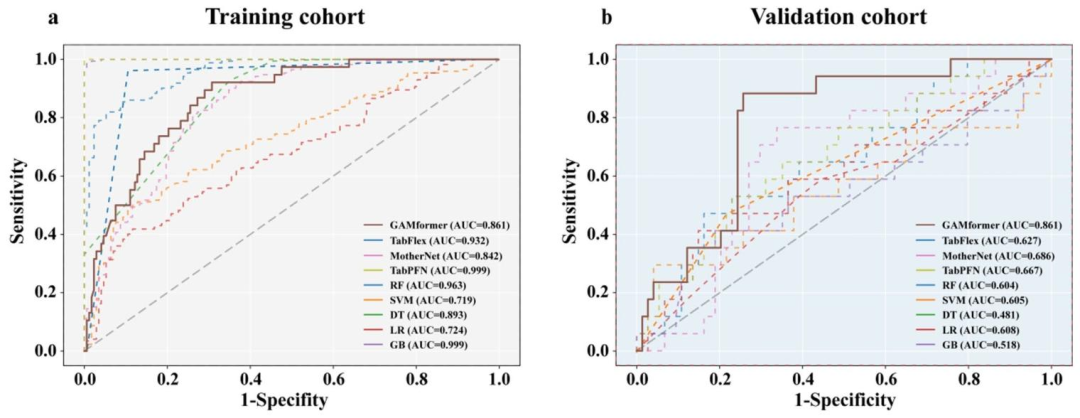
图 3:不同模型预测POD24的ROC曲线分析结果
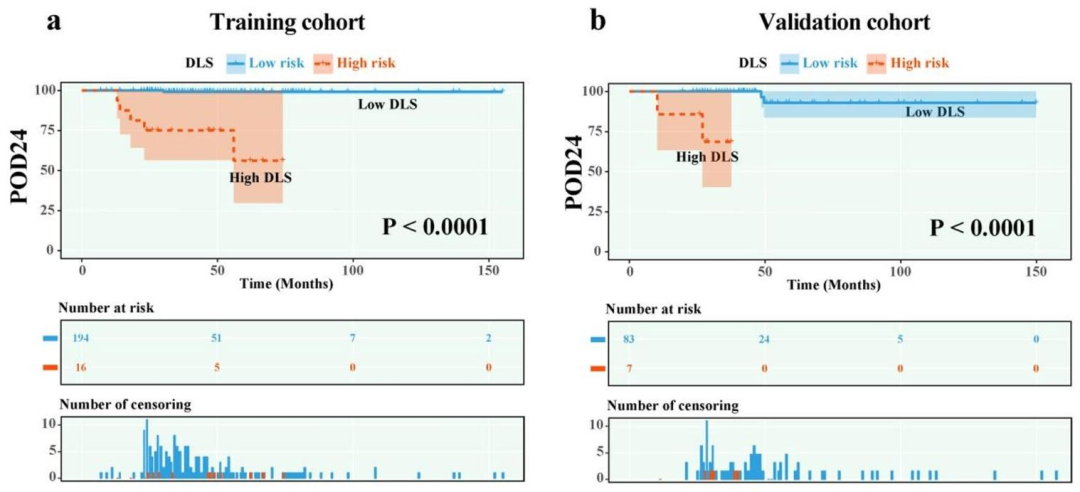
图 4:基于深度学习评分(DLS)的总生存Kaplan-Meier分析
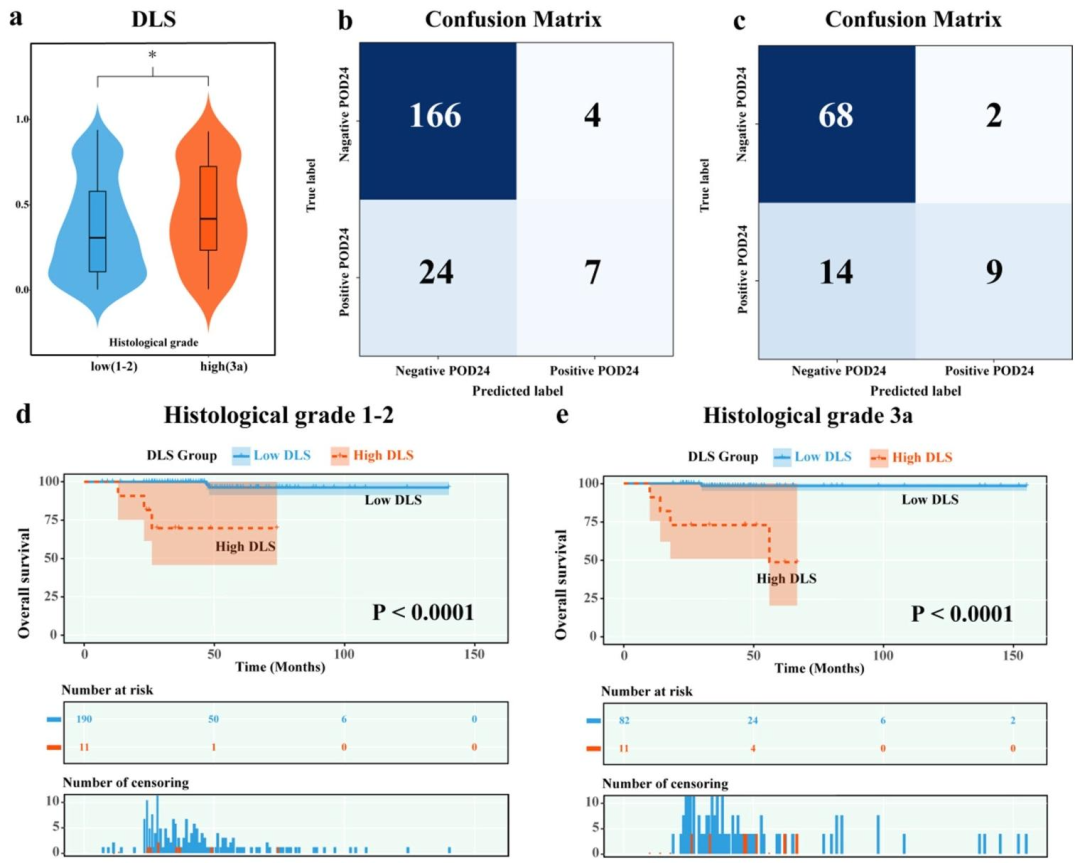
图 5:滤泡淋巴瘤不同病理分级的DLS分布、混淆矩阵及生存分析
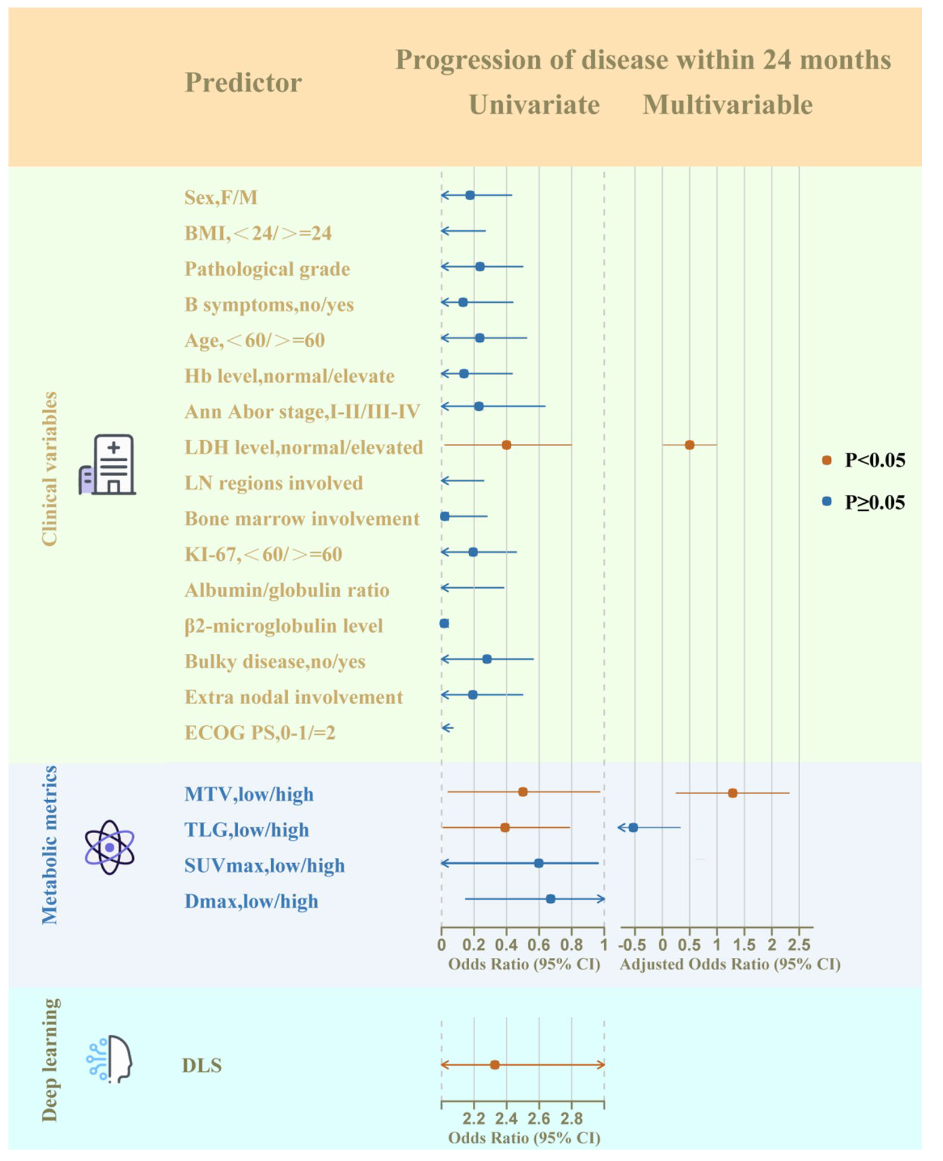
图 6:POD24单因素与多因素分析森林图
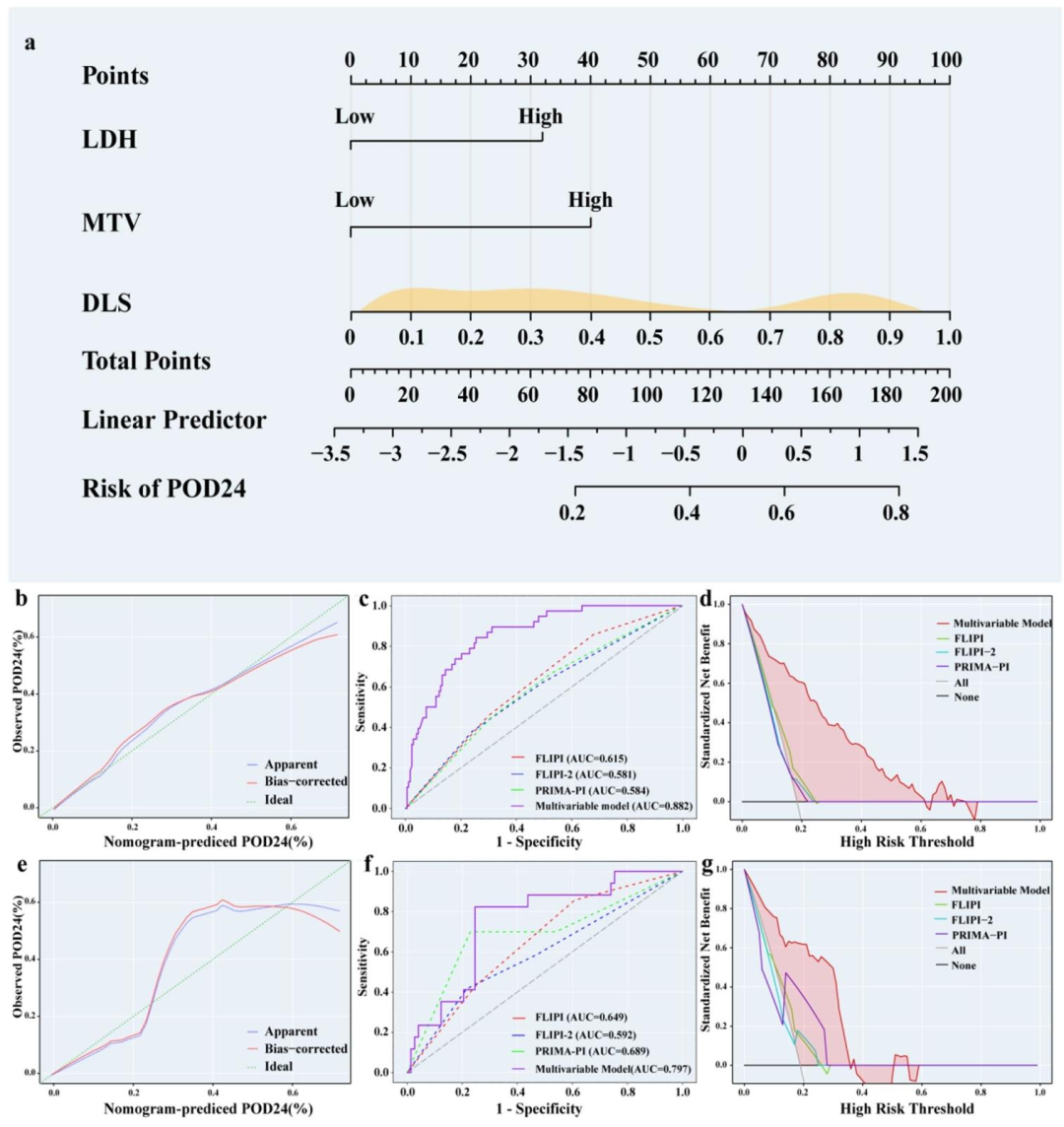
图 7:多参数模型预测POD24的综合验证
05
研究结论
该研究通过多中心数据证实,基于基线¹⁸FFDG PET/CT的深度学习评分(DLS) 能够有效预测滤泡性淋巴瘤(FL)患者的24个月内疾病进展(POD24) 并实现精准生存风险分层 。其中,GAMformer模型 在多种算法中表现最优,训练集与验证集的AUC分别达到0.857和0.753。将DLS与乳酸脱氢酶(LDH) 及代谢肿瘤体积(MTV) 整合构建的多参数模型,进一步将预测性能提升至AUC 0.882(训练集)和0.797(验证集),显著优于传统临床评分如FLIPI、FLIPI-2及PRIMA-PI。该DLS在不同组织学分级(包括低级别1--2级与3a级)中均展现出一致且稳健的风险分层能力 ,并与患者总生存期显著相关(P < 0.0001)。研究提示,该影像生物标志物有望在初诊阶段精准识别高危患者,为实施风险适应性治疗策略提供重要依据,推动FL个体化诊疗进程。
参考文献:Huang H, Zhang T, Jiang Z, Zhang Z, Jiang Q, Teng Y, Zhou H, Ding C, Xu J, Jiang M, Xu B, Jiang C, Tian R, Li K. A deep learning PET/CT biomarker for early progression (POD24) and survival stratification in follicular lymphoma: a multicenter study. Eur J Nucl Med Mol Imaging. 2026 Mar 23. doi: 10.1007/s00259-026-07838-x. Epub ahead of print. PMID: 41870550.