作者,Evil Genius
今天我们首先分享一个思路,就是怎么分析不同条件下的空间重塑。
首先提出问题
与许多其他组织一样,乳腺组织会随年龄增长不断积累体细胞突变。这些基因变化解释了为何乳腺癌的发病率在晚年升高。值得注意的是,年轻患者(40岁以下)中发生的肿瘤与晚年发生的肿瘤有所不同,但局部组织微环境在肿瘤早期发展中的作用仍不清楚。例如,肿瘤发生的空间背景可能在限制、塑造或促进肿瘤形成方面发挥重要作用。然而,无论是这种局部空间背景的特征,还是其随年龄变化的演变方式,目前都尚未被充分理解。对衰老乳腺组织更清晰的认识,可能会为肿瘤的早期发展提供线索,并提示预防或降低风险的方法。
问题提出以后,针对课题收集数据,当然我们这里是空间转录组数据
旨在探索乳腺组织中的细胞及其相互关系如何随年龄变化,以及整个器官结构如何改变。通过空间转录组数据得以将细胞分类为上皮型或组织微环境型,并确定其活化状态及多细胞结构。
分析发现,老年女性(≥50岁)的乳腺组织比年轻女性(<50岁)的组织含有更少的细胞,并且在这些细胞中,增殖的细胞也更少。这一观察结果几乎适用于我们识别的所有细胞类型(包括上皮细胞------即可能发生癌变的细胞)。
通过追踪乳腺细胞组成随年龄的变化,发现年轻女性的组织中B细胞相对更丰富,而年长组织中则含有更高比例的炎症细胞,如M2型巨噬细胞。还发现,年长组织经历了结构重塑:组织微环境细胞(包括免疫细胞)位于离上皮细胞更远的位置,并且组织中含有更少的乳腺小叶(产乳腺体)以及更多的脂肪。一项无偏倚的分析(统计了整个年龄范围内组织特征差异的数量)表明,这些变化并非随年龄稳步成比例地发生,而是主要发生在绝经期前后。
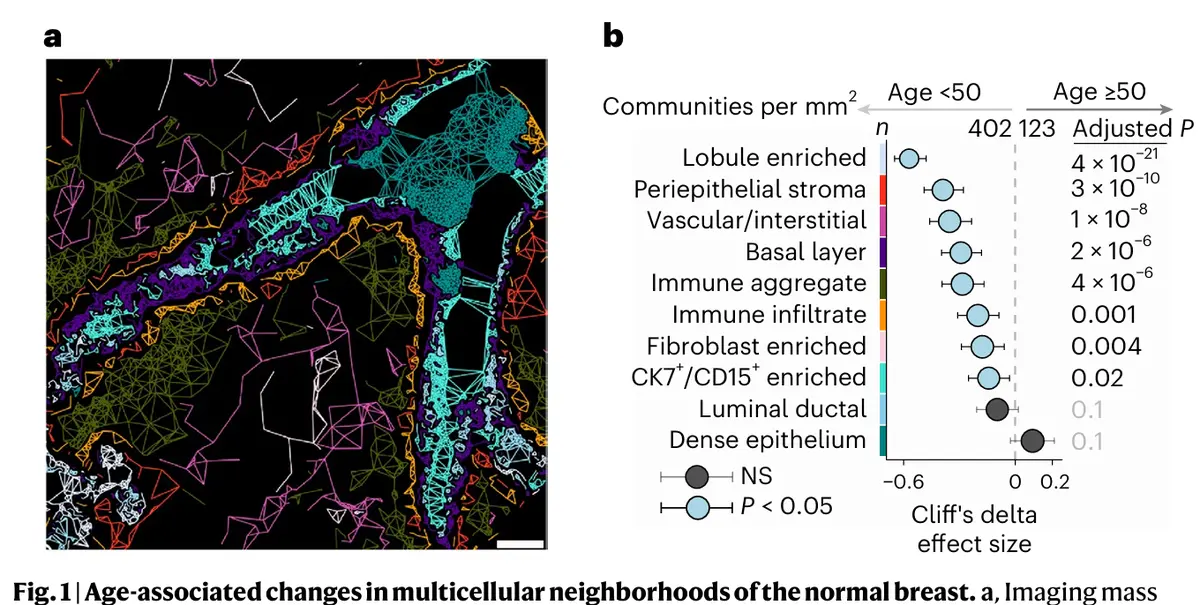
第三步:依据数据分析推断其中的生物学意义
微环境对细胞的约束作用会随着年龄增长而减弱。
今天分享的文献

知识积累
炎症是癌症的主要风险因素,无论是源于自身免疫性疾病、长期感染还是环境暴露,且风险通常随疾病的持续时间和严重程度而增加。
炎症可能导致持久的表观遗传改变,从而降低肿瘤发生的阈值。
表观基因组作为癌症的因果驱动因素的作用已变得明确。当细胞应对环境挑战时,表观基因组受到动态调控,使DNA的新区域变得可接近和活跃,将转录因子(TF)蛋白引导至这些位点,并激活新基因和细胞功能的表达。在再生和免疫过程中,表观基因组的改变在反复暴露后可以持续存在并累积,从而增强对后续刺激的反应。尽管这种表观遗传"记忆"主要被描述为适应性的,但有证据表明它也可能带来适应不良的后果,并增加未来的疾病风险。
结果1、干细胞保留结肠炎的记忆
炎症记忆的存在:在小鼠慢性结肠炎模型中,即使组织在形态和功能上已恢复(超过100天),结肠干细胞的表观基因组仍与健康对照显著不同。这种记忆在分化细胞中减弱或消失。
核心分子特征:记忆表现为AP-1转录因子结合基序的染色质可及性累积性增加,同时ETS家族基序可及性也增加,而CTCF位点可及性下降。
细胞异质性:约10%的干细胞在结肠炎恢复后表现出极高的AP-1基序可及性,且存在FOS蛋白水平升高的细胞亚群。
记忆的动态维持:虽然FOS蛋白水平在炎症消退后迅速下降,但AP-1位点的染色质可及性下降缓慢,在恢复102天后仍可检测到,表明记忆是独立于TF蛋白水平而长期维持的表观遗传改变。
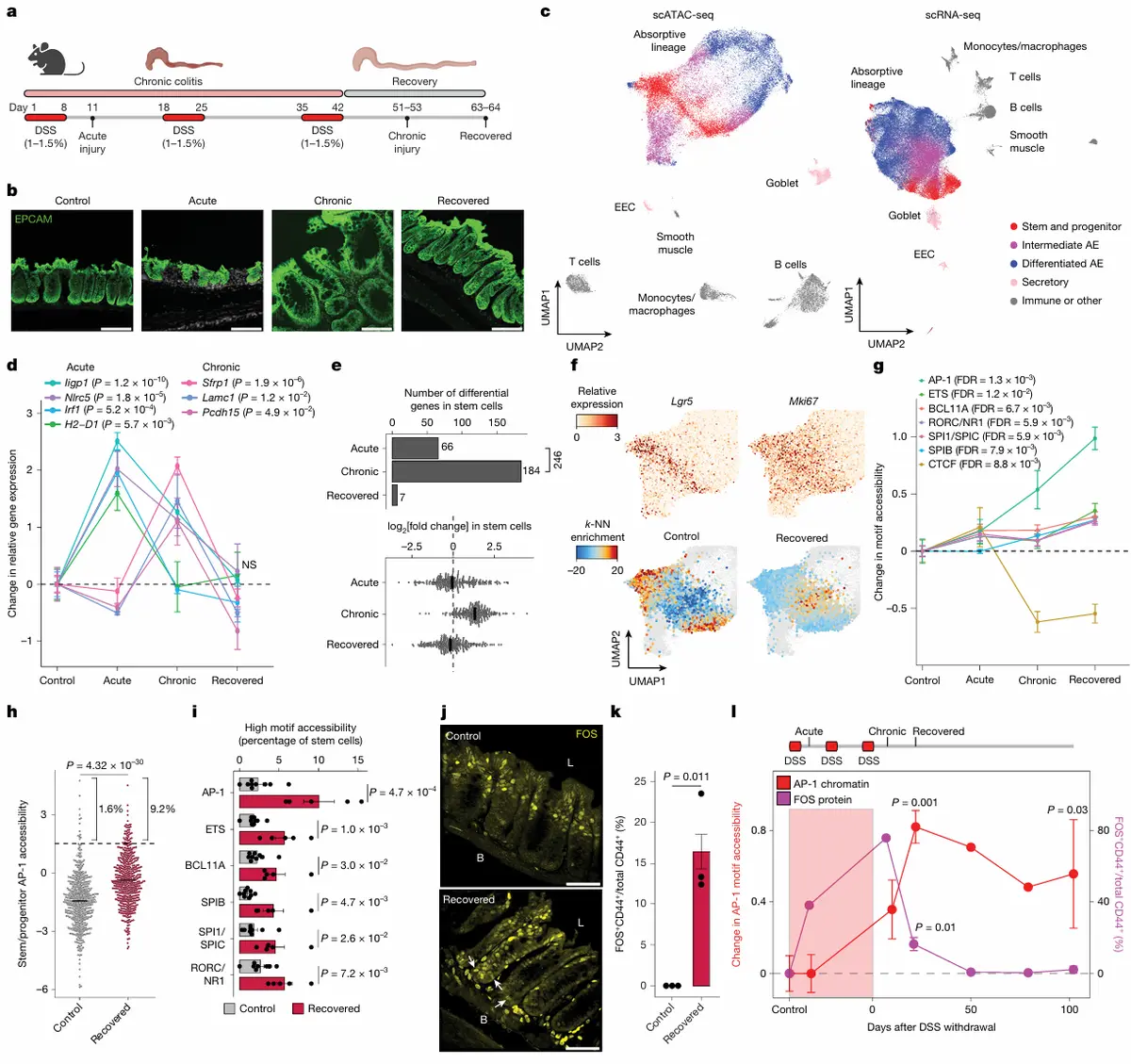
结果2、表观遗传状态是克隆性遗传的
记忆是细胞内在的:将从结肠炎小鼠分离的干细胞在体外培养成类器官后,即使脱离了体内的炎症微环境,这些类器官仍然表现出更强的增殖能力和再生形态,证明记忆是干细胞固有的。
记忆具有克隆遗传性:利用新开发的SHARE-TRACE技术(可同时检测单细胞的克隆谱系、基因表达和染色质可及性),发现AP-1基序的可及性状态能在克隆(源自同一祖先的细胞群)内稳定遗传。而ETS、CTCF等因子的记忆则可能依赖外部信号。
AP-1驱动的再生程序:AP-1的激活与一个与伤口愈合、细胞骨架重塑、干细胞增殖相关的基因程序(P20)高度相关。在结肠炎类器官中抑制AP-1活性,会优先阻断其增殖能力。
记忆的长期维持机制:
短期功能依赖:AP-1的活性对于维持记忆表型(如过度增殖)是必需的。但长时间抑制AP-1并不能永久擦除记忆,停药后异常表型会恢复。
长期稳定储存:记忆最终由染色质可及性和DNA甲基化的持久改变来编码。结肠炎导致的AP-1位点DNA去甲基化,在AP-1被抑制后仍无法恢复。
潜在生物学意义:这种可遗传的表观状态可能赋予携带记忆的干细胞克隆适应性优势,使其在组织内形成一片具有"癌前状态"的表观遗传场,从而影响未来的疾病发生。
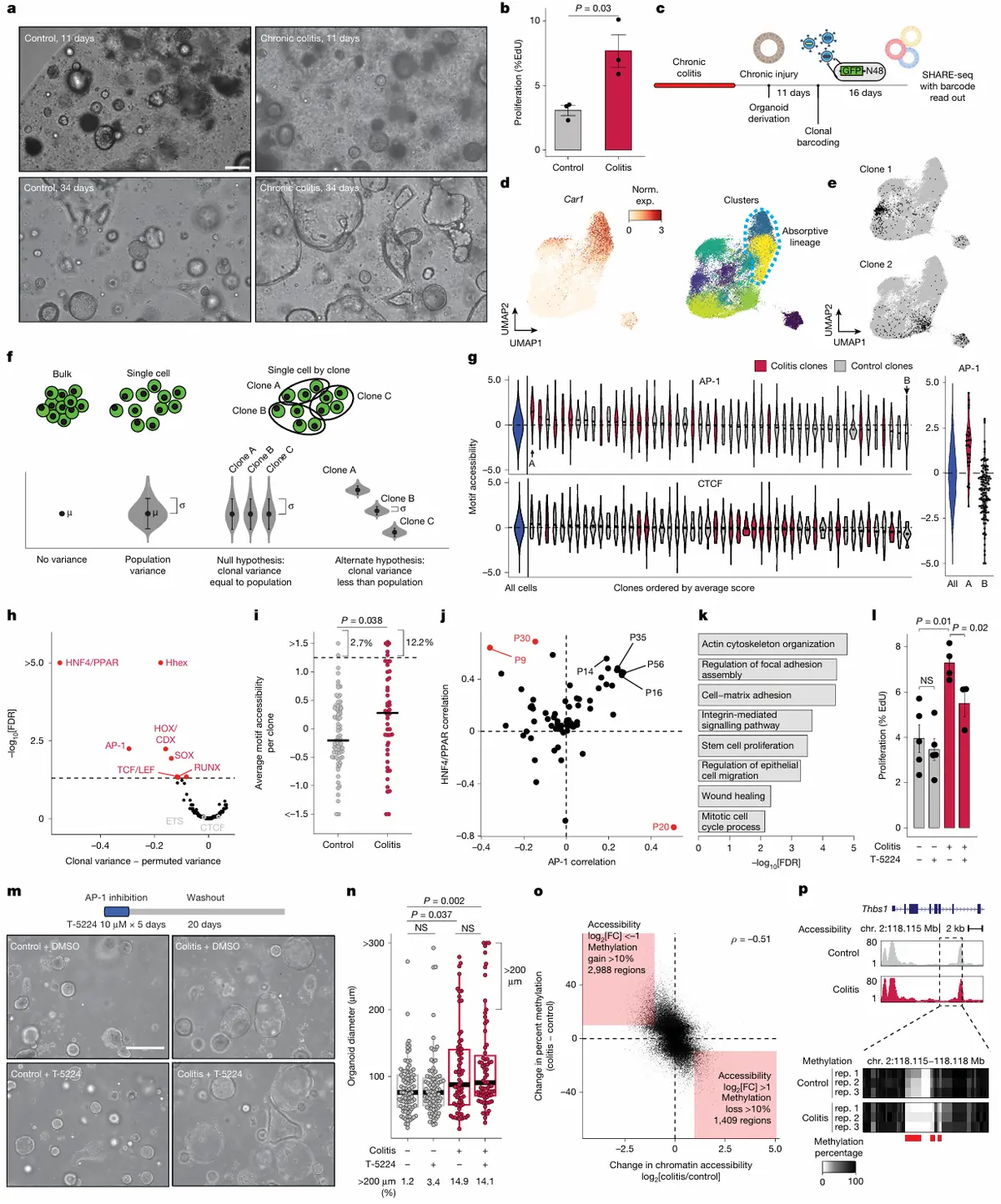
结果3、FOX因子稳定AP-1结合
发现关键复合motif:利用seq2PRINT技术,在结肠炎进展过程中鉴定出一个AP-1/FOX复合基序,其可及性随炎症记忆而增加,并能通过置换核小体来增强DNA可及性。
FOX依赖AP-1结合:抑制AP-1活性后,FOX在DNA上的结合足迹也随之丢失,且两者丢失程度高度相关,表明FOX在这些位点的结合依赖于AP-1。这一现象在人类炎症性肠病(IBD) 患者来源的类器官中也得到验证。
生化验证协同作用:体外结合实验证实,FOXA1和FOXP1均可增强AP-1与DNA的结合。其中FOXP1的作用尤为显著,它不仅增强复合基序的结合,还能通过蛋白-蛋白相互作用增强AP-1单独基序的结合。
FOXP1的特殊机制:FOXP1能显著增强JUN(无需FOS) 与DNA的结合,为表观遗传记忆中组织特异性因子与AP-1家族特定成员(如JUN)协同作用的机制提供了生化基础。
生物学意义:FOX因子已知在肠道伤口愈合和结直肠癌(CRC)中发挥作用,本研究揭示其核心功能之一是稳定AP-1在结肠炎记忆相关区域的结合,从而连接了炎症记忆与疾病进程。
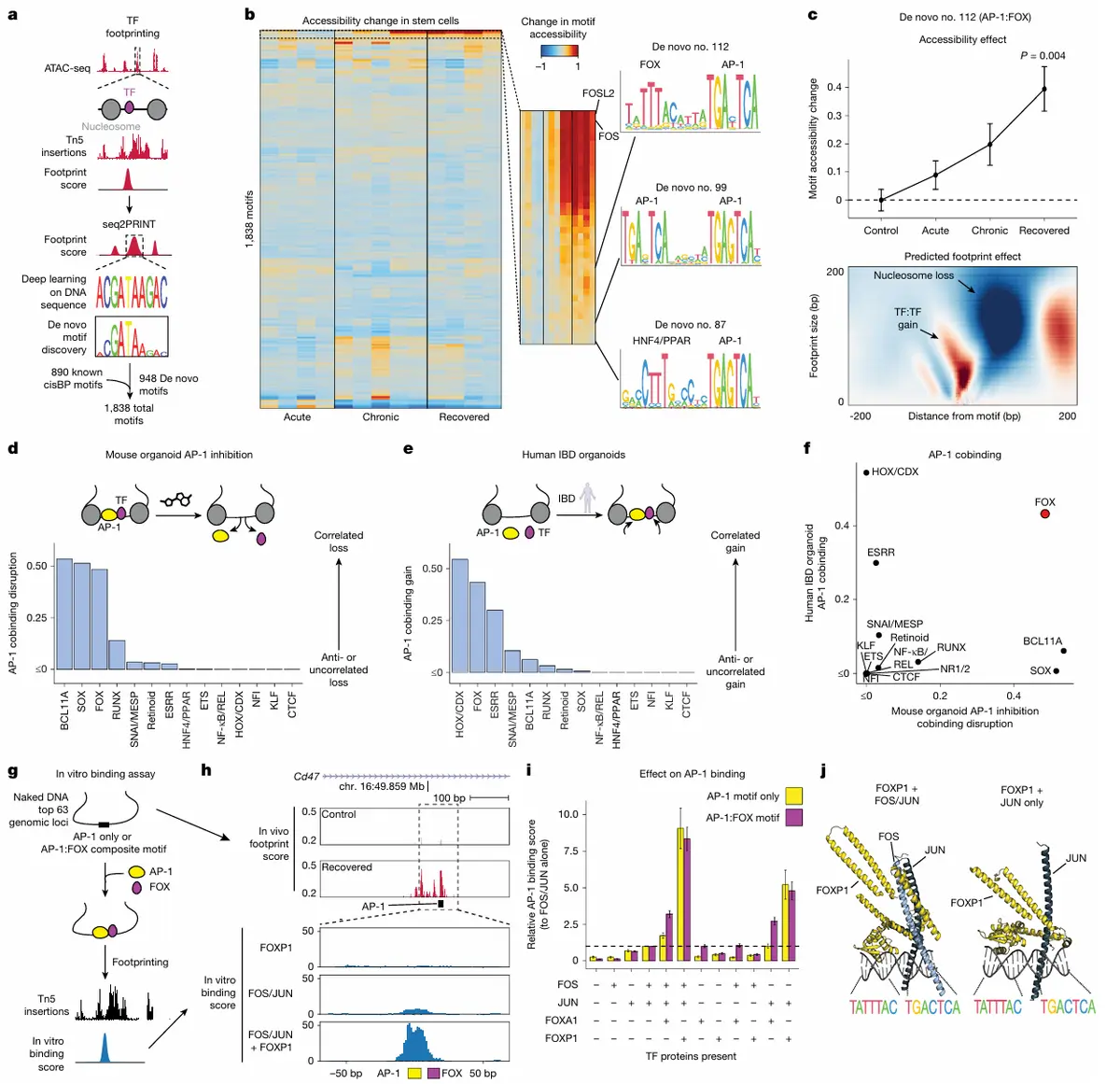
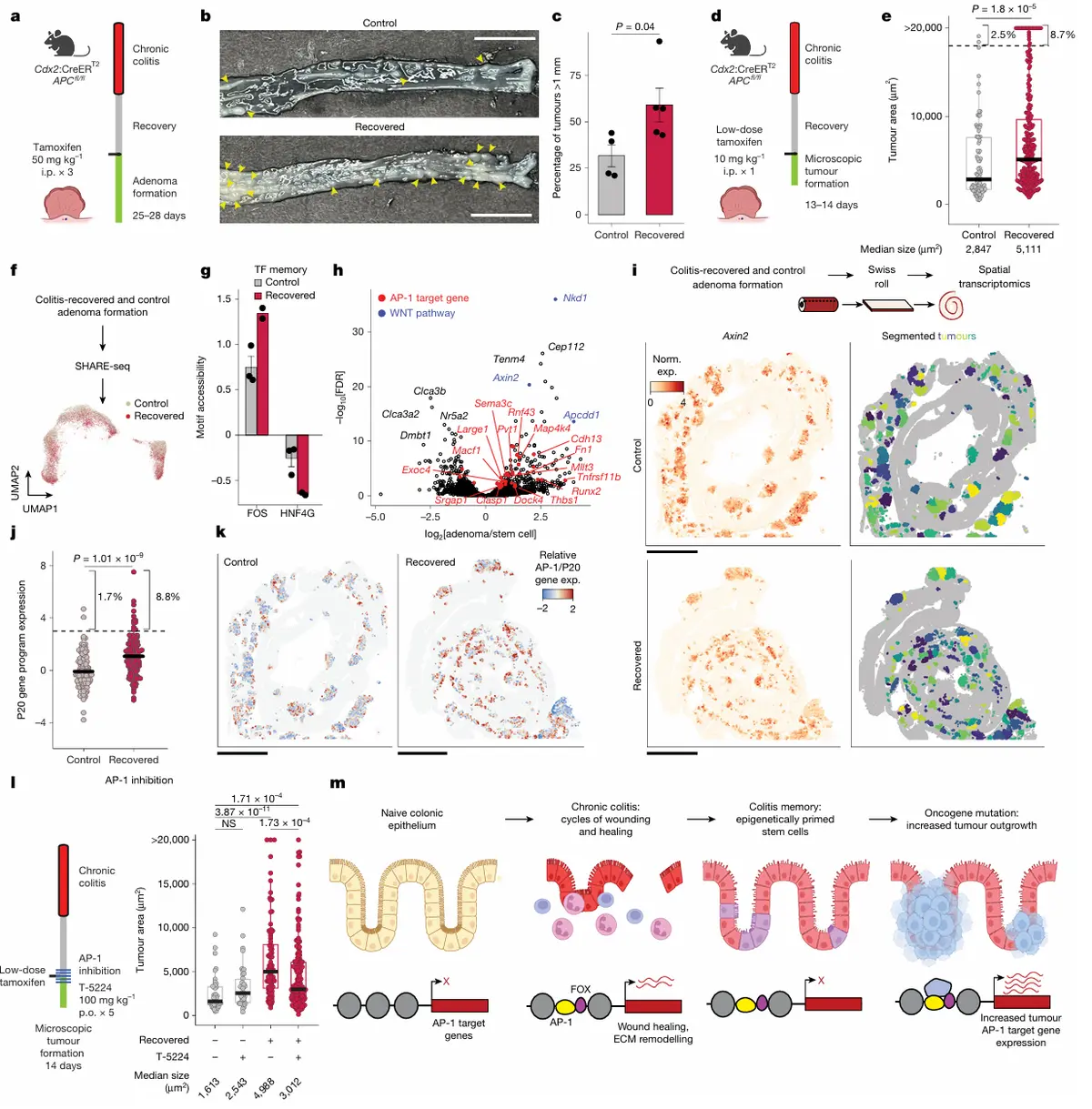
结果4、结肠炎的记忆促进肿瘤生长
记忆促进肿瘤生长:在结肠炎恢复后的小鼠中诱导APC基因缺失(模拟结直肠癌的常见起始事件),其形成的腺瘤(早期肿瘤)比对照组体积更大。这种促进作用并非源于肿瘤数量增多,而是源于单个微观肿瘤在早期生长更快。
肿瘤异质性重现:与干细胞中AP-1记忆的异质性一致,结肠炎背景下的肿瘤中也存在一个高表达AP-1相关基因的亚群(8.8%),该亚群还额外激活了促癌程序(如PDGF信号、增殖、血管生成)。
AP-1是关键驱动者:在肿瘤起始阶段抑制AP-1活性,可使结肠炎恢复小鼠的肿瘤体积中位数缩小近40%,但对对照组无影响,证明AP-1活性是介导这种促癌效应的核心。
机制模型:慢性炎症在结肠干细胞中编码了一种以"修复"为特征的表观遗传记忆(AP-1及组织特异性TF结合位点的可及性累积增加)。当这些携带记忆的干细胞获得致癌突变后,记忆会通过持续激活促增殖基因程序,加速恶性进展,从而解释了慢性炎症为何会增加癌症风险。
最后来看看方法

visium HD

