论文总结
该研究基于UK Biobank中51,904名参与者的数据,分析了2,923种血浆蛋白与9种衰老相关表型(如生物学年龄、健康寿命、虚弱等)的关联。共鉴定出227个与衰老显著相关的蛋白,主要富集于炎症和再生通路。血浆蛋白在生物学年龄41岁、60岁和67岁出现三次显著变化高峰,且不同器官的蛋白变化模式各异。孟德尔随机化分析支持CXCL13、DPY30、FURIN、IGFBP4、SHISA5与衰老存在因果关系。这些蛋白与多种疾病(尤其是心血管病)及全因死亡率密切相关,并可介导生活方式对衰老的影响。研究为衰老的生物标志物识别和干预靶点提供了重要依据。
摘要
**引言:**血浆蛋白质组学检测了成千上万种蛋白质的水平,具有鉴定健康衰老临床生物标志物的潜力。
**目标:**这项大型蛋白质组学研究旨在确定健康衰老的临床生物标志物,并进一步探索参与衰老的潜在机制。
**方法:**本研究分析了51,904名英国生物库参与者的数据,以探讨2,923种血浆蛋白与9种衰老相关表型的关联,包括Pheno Age、KDM Bio Age、健康寿命、父母寿命、衰弱和寿命。使用蛋白质组学测量蛋白质水平,并以P < 1.90E-06的显著性阈值评估相关性。我们利用DE - SWAN方法检测和测量了生物衰老过程中血浆蛋白质组的非线性变化。孟德尔随机化用于评估因果关系,PheWAS探讨了这些蛋白质的更广泛的健康影响。
结果:我们鉴定了227个与衰老( P < 1。90E-06)显著相关的蛋白,其中炎症和再生通路被显著涉及。我们的研究结果揭示了中年人生物衰老过程中血浆蛋白质组的波动模式,在41岁、60岁和67岁时发现了生物年龄相关变化的特定峰值,以及不同器官中与年龄相关的蛋白质变化模式。 此外,孟德尔随机化进一步支持了血浆CXCL13、DPY30、FURIN、IGFBP4、SHISA5水平与衰老之间的因果关联,强调了这些药物靶点的重要性。这5个蛋白具有广泛的作用。对衰老相关蛋白的PheWAS分析强调了它们在重要生物学过程中的重要作用,特别是在总死亡率、健康维持和心血管健康方面。此外,蛋白质还可以作为健康生活方式和衰老过程的中介。
**结论:**这些重要发现强调了在关键期监测和干预衰老过程的重要性,同时在血浆蛋白质组图谱中发现了与年龄相关疾病的潜在生物标志物和治疗靶点,从而为健康老龄化提供了有价值的见解。
引言
健康和寿命之间的差距表明了积极寻求治疗方法的潜力。老人学假说认为,衰老是所有慢性疾病的首要危险因素 1 。因此,与单独治疗每种慢性疾病相比,靶向与衰老相关的因素可能在改善健康寿命方面具有更大的优势。然而,目前针对衰老的治疗干预措施并不理想。获得持续缓解的有限成功与我们对其发病机制的不完全了解密切相关。解开这些难以捉摸的机制对于为更有效的治疗干预奠定基础至关重要。 在这种情况下,蛋白质作为基因表达的最终产物,在细胞功能中发挥着关键作用,并为疾病的病理生理学提供了直接的见解 2 。因此,分析年龄相关表型中的蛋白质失调可能揭示衰老前的内部过程。这提供了对潜在机制的见解,并为个性化治疗策略铺平了道路 3 。先前在衰老研究中对单个蛋白质的强调,确实产生了几种与衰老相关的蛋白质的发现。例如,细胞周期蛋白依赖性激酶抑制剂P16INK4A参与细胞衰老 4 ,促炎细胞因子IL - 6与炎症有关 5 ,胰岛素样生长因子IGF - 1与长寿途径有关 6 。 此外,APOE 7 和FOXO3 8 已被确定为影响寿命和寿命的因素。通过全面的蛋白质组学分析,可以更透彻地了解衰老过程,并有可能发现与之相关的其他生物标志物。然而,关于衰老的蛋白质组学研究仍然存在一些悬而未决的问题。先前的一些研究集中在血浆中与年龄相关的蛋白质特征,但受限于小样本和对衰老表型 9、10 的年龄相关蛋白质的偏见。虽然按时间顺序衰老是匀速进展的,由于生理和疾病相关的变化,个体之间的生物老化是不同的,从而导致不同的健康结果 11 。因此,生物年龄反映了个体的整体生理状态,具有更全面的评估作用 12 。研究衰老过程中血浆蛋白质组的动态变化对于揭示衰老相关疾病的分子机制至关重要。此外,通过对各种表型进行蛋白质组学研究,增强了我们对与人类衰老相关的生物学机制和分子标志物的理解 13 。蛋白质组学可以通过单表型方法鉴定衰老相关蛋白,如极度寿命、健康寿命和家族寿命等。 目前,全基因组关联研究( genome-wide association studies,GWAS )主要针对单一表型来探索蛋白质组学 14、15 的干预靶点。然而,这些方法忽略了这些性状和其他衰老相关因子之间的共享生物学,例如衰老和生理衰弱的蛋白质组学标记。研究多种表型可以更全面地探索人类衰老的潜在生物学机制,并有助于确定促进健康衰老的更精确的生物标志物 16 。弥合这种知识鸿沟也为年龄相关性疾病的早期识别和后续干预提供了可能。因此,在英国生物库( UKB )的前瞻性队列中,我们在超过50000名参与者的样本中调查了2923个基线血浆蛋白水平与健康老龄化之间的关系。首先,我们使用线性、逻辑回归和cox回归分析来检测与衰老相关的蛋白质组浓度,以确定与生物年龄相关的血浆蛋白。此外,我们对它们在衰老过程中的生物学功能和细胞表达进行了表征,并在生物衰老过程中的血浆蛋白质组轨迹分析中确定了生物衰老的3个重要的血浆蛋白质组峰。为了强调其临床意义,我们进行了孟德尔随机化。通过分析建立因果联系,发现潜在的治疗靶点,并发现与这些蛋白质相关的健康临床意义。
方法
研究对象
UKB是一项正在进行的队列研究,于2007年4月开始,在英国不同地区招募了50万名40 - 69岁的人 17 。参与者访问了评估中心,他们完成了问卷调查,进行了体格检查,并提供了生物样本 18 。本研究获得伦理批准,受试者均签署书面同意书。本研究根据批准的申请号19542的条款,利用了UKB资源。
蛋白质组学测定
从超过50万的UKB参与者中,选择了超过5万人在基线评估期间收集的血浆样本。其中,46,673人被随机挑选,1,268人因参与COVID - 19重复成像研究而被挑选,6,365人由13个参与联盟成员根据特定的研究兴趣挑选。这些选取的样本总体上具有UKB人群的代表性。对于详细的参与者选择方法和样本处理,参考Sun等人的补充信息 19 。血样采集于EDTA抗凝管中,4℃2500g离心10min,分离血浆,- 80℃保存。 然后将样品送往瑞典使用Olink ExploreTM Proximity Extension Assay进行分析,在不同的面板中对2,923个蛋白质分析物进行定量,对应2,941个蛋白质。严格的质量控制保证了组间和组内变异系数分别小于20 %和10 %。关于样本选择、处理和质量控制的进一步细节可在先前的出版物中获得 20 。蛋白水平被报告为标准化蛋白表达( NPX )值,对扩增对照进行标准化,并进行对数转换,以尽量减少变化,而不需要UKB进行额外处理。
结果定义
与人类衰老相关的选定方面包括一系列因素,包括生物年龄、端粒长度、健康寿命、父母寿命、特殊长寿和衰弱。详情见附表2。我们应用Klemera - Doubal方法( KDM )和PhenoAge方法( PA ) 21 ,从血液化学和临床数据中使用综合方法量化生物年龄( BA )。先前的研究已经详细地计算和解释了这些措施的 22、23 。KDM涉及生物标志物对实际年龄( CA )的回归,这表明个体的生理年龄与美国国家健康和营养检查调查( NHANES )Ⅲ数据集中观察到的平均生理年龄相匹配。 Pheno Age是基于生物标志物和CA得出的死亡率预测评分,反映NHANESⅢ中平均死亡风险与预测风险相等的年龄。我们使用BioAge软件包进行计算 23 。为了测量BA和CA之间的差异,对KDM - BA和PA的CA进行了回归,并将结果作为"年龄加速"。UKB采用聚合酶链式反应( PCR )方法测量端粒长度( LTL ),结果对表型数据盲法。比较端粒长度PCR产物( T )和内参基因PCR产物( S )的扩增情况,得到T/S比值。t和s值。
在每次运行中都对校准品样品( DNA由20个个体混合而成)进行了校准。本研究采用经对数转换、z - score调整的T/S比值精确代表相对LTL,同时考虑技术因素 24 。健康寿命定义为8个预定义的健康寿命结束事件中任何一个事件首次出现的时间,参照已发表的UKB健康寿命研究的方法 25 。这些事件包括7种与年龄相关的疾病- -充血性心力衰竭( CHF )、心肌梗死( MI )、慢性阻塞性肺疾病( COPD )、中风、痴呆、糖尿病和癌症以及死亡。健康寿命定义为研究样本中不存在这些疾病。 被试者被认为在这些条件中的任何一个条件的最早诊断或死亡时已经达到了健康寿命的终点。父母寿命是根据参与者在死亡时对父母年龄的自我报告来计算的 26 。在父母一方的预期寿命数据不可得的情况下,另一方的预期寿命被替代。在缺少父母一方预期寿命信息的情况下,计算父母双方的平均预期寿命。如果父母双方均健在或年龄小于40岁,则个体被排除在分析之外,因为这些病例可能预示着意外死亡。 被试的特殊寿命由父母中是否至少有一人活到85岁或以上,或者父母中是否没有一人活到85岁来决定 27 。此外,参与者根据母亲和父亲的年龄进行分类,不论是死者还是活着。"母亲长寿"一词被用来表示母亲已经达到85岁或以上,而不管父亲的身份如何。类似地,父亲长寿被定义为父亲年龄达到85岁或以上,而不论母亲的状况如何。为了评估衰弱状态,我们使用了Fried表型,该表型包括5个自我报告或客观测量的成分:体重下降,力竭,低握力,身体活动不足和步行速度缓慢 28 。
衰老相关蛋白的鉴定
Cox回归模型用于评估蛋白质水平与健康跨度之间的关系。使用线性回归模型检验蛋白质水平与Pheno Age、Pheno Age加速、KDM - BA、KDM - BA加速、端粒长度和父母寿命之间的关系。采用Logistic回归模型检验蛋白质水平与衰弱和长寿之间的关联。调整潜在的混杂因素,包括基线年龄、性别、种族、汤森剥夺指数( TDI )、教育水平、吸烟状况、饮酒状况。我们应用严格的Bonferroni校正( P < 0 . 05 / 2,923 / 9 )来评估每个结果的显著相关性。
功能富集分析
后续分析中包含的蛋白质(n = 227)符合以下标准:它们与所有九种表型相关,并且在不同表型间表现出一致的关联。利用FUMA的GENE2FUNC功能进行了组织富集分析。DEG组最初通过对GTEx数据库中54种组织类型的双侧t检验对每种组织进行检测。随后使用超几何测试探索这些DEG集中的衰老相关蛋白。为探索已识别重要蛋白的功能富集,我们使用了Enrichr平台(https://maayanlab.cloud/Enrichr/),使用Olink面板的完整蛋白作为背景基因集\[30\]。富集分析基于基因本体(GO)术语和京都基因与基因组百科全书(KEGG)途径进行。为控制多重检测,采用了Benjamini-Hochberg方法,假发现率(FDR)低于0.05的结果被认为具有统计学显著性。我们使用TRRUST数据库,该数据库包含8444个TF靶向关系,涉及800个人类转录因子,研究了衰老相关蛋白的上游调控因子\[31\]。该分析结合Metaspace,帮助识别了调节这些蛋白表达和活性的潜在转录因子。随后,利用R包ggplot2可视化了最具代表性的生物过程、通路和变形因子。
生物老化期间蛋白质的轨迹
我们选择了227种名义上与衰老相关的蛋白质,以估算它们在生物衰老过程中的轨迹。最初,我们对蛋白质水平进行了z标准化。随后,我们采用了局部估计的散点图平滑(LOESS)回归32,跨度为300,以拟合每种血浆蛋白与生物年龄,考虑了关联分析中使用的所有协变量。随后,我们利用欧几里得距离计算了LOESS估计值之间的两两差异。最后,我们采用完整方法进行分层聚类,将不同轨迹模式分类为衰老过程中的四个集群。
差分表达式 − 滑动窗口分析(DE-SWAN)
我们采用了通过R软件包DEswan实现的DE-SWAN方法,检测和测量了生物衰老过程中等离子体蛋白质组的非线性变化33。最初,我们大致估算了健康参与者的生物年龄,仅根据生物年龄分布纳入40至70岁之间的人群。这导致共使用了30个中心,每个中心有±一年的窗口。在差异表达分析中,我们采用了以下模型:蛋白质水平 ∼ a + b1 生物年龄 低/高 + b2 性别 + b3 族裔 + + e。显著水平由每波生物年龄的q值表示,采用Benjamini-Hochberg修正确定。此外,在R包车内使用方差分析函数计算了II型平方和。β值<0.05的蛋白质被认为具有统计学显著性。如前所述,通过KEGG数据库进一步推断了每个簇的对应生物通路34。只有p值<0.05的生物过程被认为具有显著性。基于GTEx的组织富集结果,我们鉴定出与多个器官相关的蛋白质。我们的分析重点是特定组织,包括脂肪组织、动脉、泌尿系统(包括肾脏和膀胱)、大脑、上消化道(包括食管和胃)、免疫组织、肠道和肺部。这些样本因其在年龄相关疾病中的作用已被充分理解,并且在我们考察的队列中存在相关表型数据。采用DE-SWAN方法进行识别和量化在生物衰老过程中,每个器官血浆蛋白质组的非线性变化。
孟德尔随机化与药物能力评估
我们采用双样本磁共振分析蛋白质对健康衰老的因果影响,以蛋白质为暴露变量,并以其对健康衰老的影响作为结果评估。基于UKB数据内部计算了9个健康衰老相关表型的GWAS总结数据,排除了具有蛋白质数据的参与者。我们重点选用英国的欧洲参与者进行pQTL映射。蛋白质遗传工具通过显著的SNP(p < 5E-08)被鉴定,这些SNP经历了聚团(1000 kb距离,LD r2 ≤ 0.01),这是1000基因组项目的欧洲LD参考面板。我们采用了Steiger滤波,排除具有回文特征和中间等位基因频率的SNP,并在主要分析中采用反方差加权(IVW)方法进行因果估计。使用R2和F统计量评估工具变量(IV)与风险因素之间的关联。数值越高,MR分析中的仪器强度和统计能力越高。统计分析使用R软件"TwoSampleMR"35进行。每个优先目标的可药性均根据Finan的标准进行检查36。
Phewas
我们进行了广泛的分析,探讨关键健康衰老相关蛋白(n=5)与多种表型之间的联系。基于通路富集和组织表达分析结果,选定了六类表型进行进一步研究:体成分指标、血脂、肾功能、脑功能、免疫和肺功能指标。本研究主要关注动脉疾病、泌尿系统疾病、脑部相关疾病、上消化道疾病、肠道疾病、肺部疾病、癌症和死亡。诊断采用ICD-10编码系统,基线时已有既往疾病的个体被排除在分析之外。随访终点定义为疾病最早发生、死亡日期或随访期结束(2023年6月30日)。Cox比例模型评估了衰老相关蛋白与发作疾病之间的关联,而线性回归模型则识别了衰老相关蛋白与表型之间的关联。模型调整了可能的混杂因素,如年龄、性别、族裔、TDI、教育水平、吸烟状况和酒精状况,并对多项修正应用了Bonferroni修正。我们构建了三角形图,将可调节的风险因素、蛋白质和健康衰老特征联系起来,所有这些特征都表现出如假设中一致的关联方向。仅包含五种被鉴定为MR阳性的蛋白质,用于介导分析,以探讨蛋白质在风险因素与健康衰老之间的潜在介导作用。更多细节可见补充方法和补充表17。
结果
人口特征
共有51,904名英国人(UKB)参与者,年龄在39至70岁之间,其中46%为男性(补充表1)。血浆样本使用Olink Explore 3072处理,产生了2923个独特蛋白质(补充表3)。提供健康寿命、端粒长度(LTL)、父母寿命等数据的参与者子集分析中包括寿命、生物年龄和虚弱情况(补充表2)。整体研究设计见图示摘要。
蛋白质组范围内的衰老关联
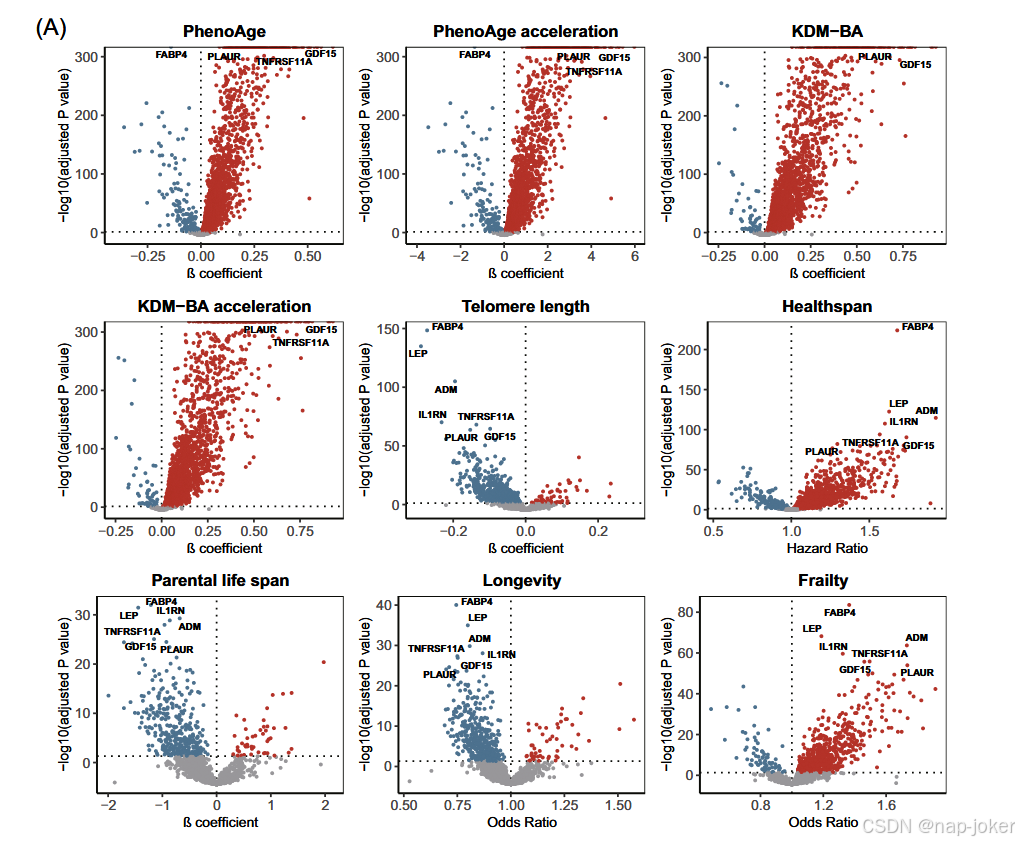
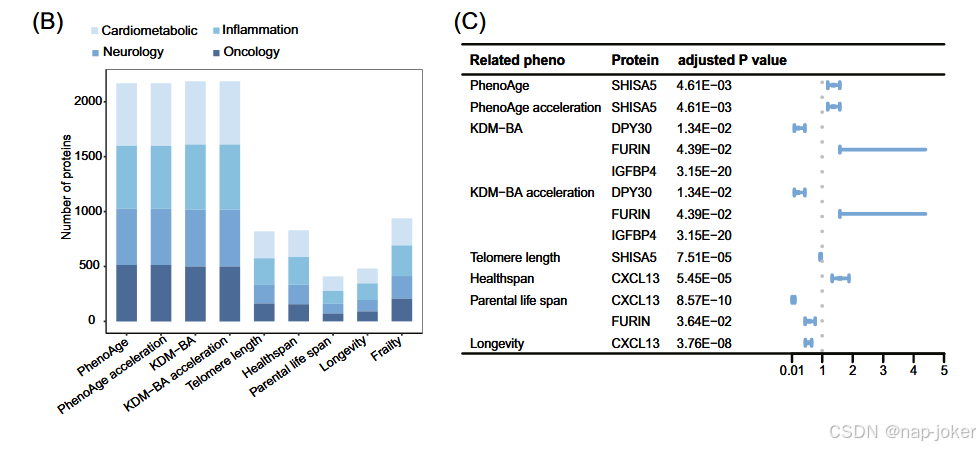
图1。健康衰老与血浆蛋白的关系。A:散点图显示了9个与衰老相关的性状与2923个蛋白质之间的关联。Cox回归模型被用于考察蛋白质水平与健康寿命之间的关联。采用线性回归模型研究蛋白质水平与表龄、表龄加速、KDM-BA、KDM-BA加速、端粒长度及亲本寿命之间的关联。应用逻辑回归模型研究蛋白质水平与虚弱和寿命之间的关联。显示的p值为双侧,并经过多次比较调整。水平虚线以上的蛋白质与Bonferroni修正后与衰老相关性状显著相关(P < 1.90 × 10--6)。B. 图显示与衰老相关性状显著相关的各类蛋白质数量,包括四类:心血管代谢、炎症、神经和肿瘤。C. 关于血浆蛋白与健康衰老关联的孟德尔随机化分析结果。森林图显示5种磁共振识别蛋白对健康衰老的因果效应。方框代表比值(OR),横线表示95%置信区间。
共测试了26,307个关联,涵盖2,923个蛋白质和9个结局。在整个数据集中,共有12,193个显著关联超过了Bonferroni修正的多重对比检验(P < 1.90E-06≈0.05/2,923/9)。研究发现,KDM-BA拥有最多的相关蛋白(n = 2,188,74.85%),其次是表龄(n = 2,168,74.17%)、虚弱(n = 939,32.12%)、健康寿命(n = 830,28.40%)、LTL(n = 820,28.05%)、寿命(n = 482,16.49%)和父母寿命(n = 410,14.03%)。我们评估了与9种健康相关衰老表型显著相关的蛋白质数量和比例。蛋白质含量最高的与炎症相关,端粒长度和父母寿命除外(表龄,n = 573;表龄加速,n = 573;KDM − BA,n = 596;KDM-BA加速度,n = 596;健康寿命,n = 253;寿命,n = 151;虚弱度,n = 279)。心脏代谢蛋白数量紧随其后,而神经学和肿瘤学相关的蛋白质在多种表型中表现出相似的数量(见图1B)。结果的更多细节见图1和补充表4。我们发现227种蛋白质与所有表型一致相关。其中2种具有抗衰老保护作用(PON3和UMOD),225种促进衰老。我们发现PON3和UMOD在所有九种与衰老相关的表型中都表现出显著的保护性关联(补充表4)。PON3是一种对外氧松酶家族成员,能结合循环中的高密度脂蛋白(HDL),并通过其抗氧化活性抑制低密度脂蛋白(LDL)的氧化,从而减轻氧化应激和动脉粥样硬化进展------这些是心血管衰老的关键驱动因素37,38。UMOD作为主要尿蛋白,对肾脏管完整性、防尿路感染及系统性炎症调节至关重要39,40。UMOD中的遗传变异与肾脏衰老轨迹和健康寿命相关41。这两种蛋白在多种衰老相关表型中的保护作用表明,它们可能通过调节氧化应激和炎症通路,系统性地延缓衰老过程,使其成为潜在的跨表型生物标志物或衰老干预的治疗靶点。EGFR和NTRK3表现出情境依赖效应:两蛋白均与表观遗传年龄指标(KDM--BA和KDM--BA加速)正相关,但在临床衰老表型中表现出保护性关联。EGFR信号传导被认为与细胞衰老及相关分泌表型的诱导有关,表明长期EGFR激活可能加速表观遗传衰老,尽管在组织修复方面可能带来潜在益处42。NTRK3编码TrkC受体,该受体激活MAPK信号以支持神经元分化和存活。它在本体感觉神经元的发展中起着关键作用,这些神经元对运动协调和认知至关重要,暗示其在健康衰老中具有神经保护作用43。然而,NTRK3的改变也与肿瘤发生有关44,表明其具有情境和年龄依赖的功能。这些双重作用可能有助于解释其在某些表型中的衰老预防关联以及KDM-BA和KDM-BA加速中的促进衰老效应,这可能反映了不同的表观遗传衰老过程。这些多效性作用很可能是观察到的表型特异性关联的基础,因此需要进一步的机制性研究来澄清它们对不同年龄维度的贡献。
为评估空腹时长的潜在混杂效应,我们通过调整空腹时间进行了敏感性分析,并对完全调整后的模型。在最初识别的227种蛋白质中,有222种在所有衰老表型中仍保持显著性(补充表5)。在空腹调整分析中,仅出现了五种蛋白(ANGPT2、EDA2R、EGFR、FOLR2、NTRK3),而五种蛋白(CCN3、CCN5、CXCL9、SULT2A1、THY1)已不再显著。为评估性别特异性差异中年龄相关蛋白质变化的潜在差异,我们分别对男性和女性进行了分层分析。女性共有94种蛋白显示出显著的年龄关联,而男性则鉴定出80种蛋白。其中,49种蛋白质与性别年龄一致相关,45种蛋白在女性中显著,31种蛋白仅有男性(补充表6--7)。值得注意的是,若干免疫和炎症相关蛋白,如CHI3L1、CD83和HAVCR2,在男女中均与年龄持续相关,表明免疫衰老存在共同的途径。另一方面,某些蛋白质表现出性别特异性相关性:例如,TGFA和LGALS9仅在女性中与年龄显著相关,而TREM2和LEP则仅为男性特有。这些性别特异性模式可能反映了激素调节、免疫系统衰老或其他生物学过程(如更年期)的潜在差异。综合来看,这些结果强调了在研究年龄相关蛋白质组变化时,将性别视为生物学变量的重要性。
衰老相关蛋白的生物功能
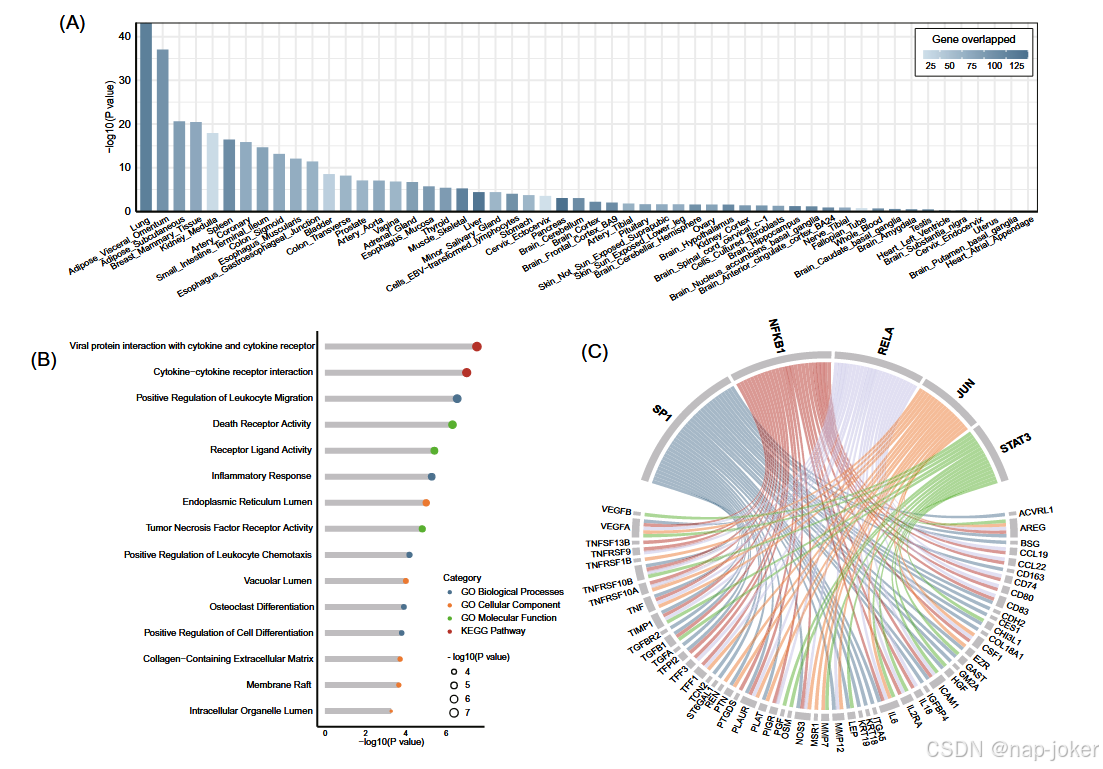
图2。健康衰老相关蛋白质的生物学功能。A:图示了健康衰老相关蛋白的组织特异表达模式。分析基于包含54种组织类型的GTEx v8数据库,使用功能映射与注释(FUMA)中的GENE2FUNC进行。B. 通路富集分析结果。x轴表示每个项P值的−对数10,表示FDR校正后的统计显著性。不同术语在纵轴上列出,其来源用不同颜色区分。C. 转录因子富集分析结果。图示了在FDR校正后显著富集排名前五的转录因子。缩写:KEGG,京都基因与基因组通路百科全书。
我们仅纳入那些结果阳性、与所有九种表型相关且在后续分析中表现出一致关联的蛋白质(n=227)。随后,利用GTEx v8数据库在54个组织中检测了这些已识别蛋白的差异表达。我们的蛋白质在肺部、脂肪组织、动脉、上消化道(包括食管和胃)、免疫组织以及泌尿系统(包括肾脏和膀胱)表现出显著的差异表达(图2A)。我们的研究重点是脑组织中蛋白质的表达。值得注意的是,蛋白质在脑组织中表现出明显差异(补充表8)。这些区域包括我们分析中的大脑皮层和额叶皮层(图2A)。衰老相关蛋白的功能分析显示,炎症相关通路和细胞成分在丰富方面显著丰富(补充表9,图2B)。细胞因子-细胞因子受体相互作用通路表现出强烈的统计显著性,同时"病毒蛋白与细胞因子及细胞因子受体"通路的富集,表明年龄相关蛋白参与关键炎症信号过程。分子功能如TNF受体活性和死亡受体活性,以及炎症反应、白细胞迁移的正向调控和白细胞趋化性等生物过程均显著高估。这些发现表明,炎症调节构成了与衰老相关蛋白质的主要生物学特征,可能促成慢性炎症和随着年龄增长而产生的免疫失调。在细胞定位方面,衰老相关蛋白显著富含内质网腔、液泡腔、膜筏以及含胶原蛋白的细胞外基质等成分。这些区室对蛋白质合成、运输、分泌以及细胞与环境的相互作用至关重要。观察者变化表明,衰老改变了体内细胞环境和细胞器功能,可能损害细胞的新陈代谢、分泌和废物清除能力,从而在衰老相关功能衰退和疾病的启动和进展中起作用
接着,我们利用TRRUST数据库识别了衰老相关蛋白的潜在转录因子靶点31。我们确定了调控这些基因生物效应的前五大转录因子(图2C,补充表10)。前五大转录因子包括转录因子sp1(SP1)、核因子(NF)-jB亚基1(NFKB1)、核因子(NF)-jB p65(RELA)、信号换导剂和transcrip激活剂STAT3 和原癌基因 AP-1 转录因子亚基(JUN)。SP1在衰老过程中起着关键作用,调节核细胞质运输基因,影响细胞信号通路,并受到氧化应激影响45。这最终影响细胞对外部信号的响应能力及其功能稳定性46。NFKB1在慢性炎症导致年龄相关认知能力下降中起着关键作用47。在NF-jB活性和炎症增强的小鼠中,研究人员观察到早期记忆丧失、神经炎症增加以及特定脑区的衰老细胞增多。对认知障碍小鼠使用布洛芬显著改善了认知功能,从而证实了NFKB1在炎症相关认知衰退中的作用47。TRRUST衍生的转录因子共同支持免疫和炎症通路在衰老机制中的核心地位。
生物老化过程中血浆蛋白的轨迹
我们研究的后续阶段是确定与血浆蛋白和生物衰老相关的轨迹模式。我们对227种显示与生物衰老名义相关的蛋白质轨迹进行了剖析,此外还分析了5种特别重要的蛋白质(图3A3C)。为降低蛋白质组的复杂性,采用了无监督的层级聚类技术,将轨迹相似的蛋白质分组。结果发现了4个随年龄变化的蛋白质轨迹簇(Fig. 3D,补充图1)。每个簇中的蛋白质数量范围为2至107(补充表11)。第2、3和4簇的蛋白质呈对数轨迹。一般来说,等离子体蛋白质组在整个生命周期中观察到的大多数变化都呈现非线性模式。在分析的4个簇中,有3个富含特定的生物通路(P < 0.05),表明生命周期中生物过程存在明显但有序的变化(补充表12)。与细胞因子介导信号通路相关的蛋白质水平在60岁之前持续上升,之后出现指数增长(群2)。与白细胞迁移正向调控相关的蛋白质在衰老过程中增长最快(群4)。
生物衰老相关蛋白的浪潮
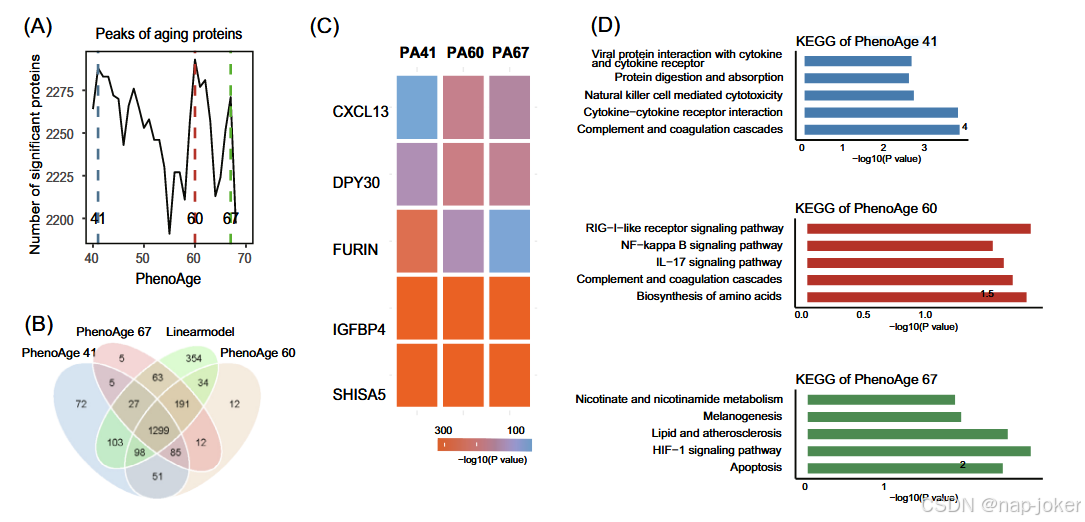
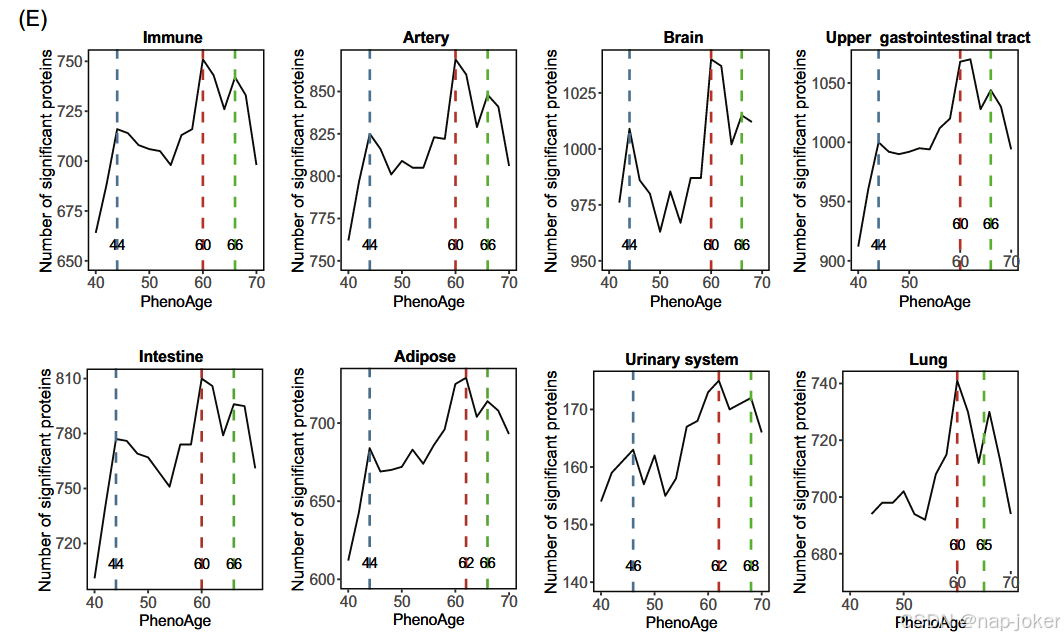
图4。生物老化过程中的等离子体蛋白波。A.上半部分展示了衰老过程中血浆蛋白数量的差异表达。值得注意的是,在生物年龄41、60和67岁时观察到三个峰值,表明不同的衰老阶段或阶段。B. 生物年龄蛋白波段之间的重叠。C. 热图展示了5种与衰老相关的蛋白质在41、60和67岁生物年龄的重要性。D. 识别KEGG生成的每个蛋白波相关的关键生物过程。E.衰老过程中血浆蛋白表达的差异在不同器官组织中存在差异。除肺部外,其他器官在生物年龄时观察到三个峰值,表明不同的衰老阶段或阶段。值得注意的是,肺部的第一个高峰最晚出现,年龄为60岁。
本研究旨在探讨等离子体蛋白质组在生物衰老过程中变化的动态模式。为量化这些变化,我们采用了DE-SWAN分析,重点关注两年一期区间,并比较一年区块内的群体。滑动窗口方法允许追踪蛋白质组从年轻到年长生物年龄的转变。值得注意的是,在41岁、60岁和67岁时,发现了三个显著的蛋白质变化峰值(见图4A-B)。即使调整了q值阈值,这些峰值依然可检测,凸显了这些生物年龄相关波的稳健性(补充表13)。有关这些峰相关蛋白质的详细信息,请参阅补充表14。被鉴定为与衰老相关的5种生物重要蛋白在三个生物年龄波段均产生显著效果(图4C)。分析再次使用KDM-BA作为生物年龄测量,结果一致。更多细节可见补充材料(补充表15)。我们识别出几条潜在的特征通路(图4D,补充表16)。我们在不同生物年龄发现了具有特征性的通路。41岁时,这些通路包括免疫相关、代谢通路和细胞信号通路。60岁时,这些疾病涉及免疫调节、代谢和与衰老相关的通路。67岁时,炎症、代谢调控和细胞周期调节相关的通路具有显著特征。这表明生物年龄在不同阶段展现出不同的通路特征,凸显了生物过程的复杂性和多样性。
研究发现了生物衰老过程中不同器官蛋白质变化的明显模式(见图4E,补充表13,补充表15)。每个器官在不同年龄段观察到显著的蛋白质变化峰值,如免疫蛋白、动脉蛋白、大脑蛋白、上消化道蛋白和肠道蛋白分别为44、699、60和67。脂肪组织在62时出现了第二个峰值,尿路系统的第一个峰值出现在46。肺部衰老相对较晚,峰值分别在60岁和65岁。这些发现不仅如此揭示了一种独特的蛋白质变化模式,反映了器官衰老相关的早期蛋白质变化,同时也暗示了不同器官间共享的衰老机制。这种对蛋白质相关生物过程的共同敏感性,使得器官衰老过程及相关生理变化能够同步监测。
性别特异性老化相关血浆蛋白波
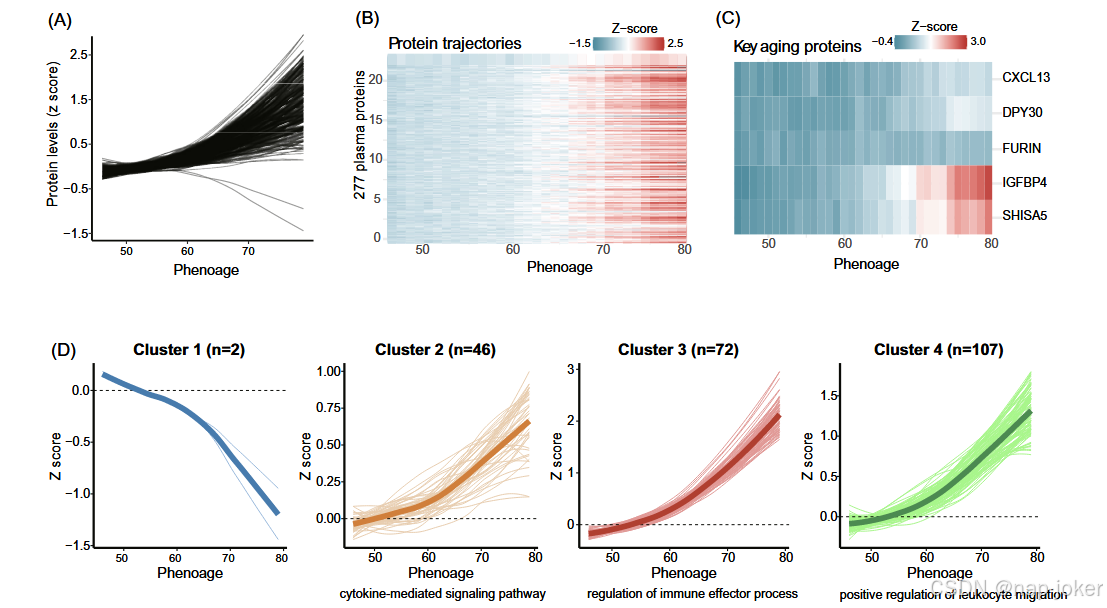
图3。等离子体蛋白质组在生物衰老过程中改变轨迹。A.该研究考察了血浆蛋白在衰老过程中的轨迹。利用z分数归一化,利用LOESS方法估算了227种血浆蛋白的轨迹。B.热图直观地展示了血浆蛋白在衰老过程中的轨迹。C. 热图特别突出显示了5种与衰老相关的蛋白质在衰老过程中的轨迹。D. 聚类分析确定了四类不同血浆蛋白在衰老过程中的轨迹。每个簇的平均轨迹用更粗的线条直观强调,并标注了每个簇内的蛋白质数量以供参考。
为探索性别特异性蛋白质组衰老轨迹,我们进行了按性别分层的DE-SWAN分析(补充表17)。在女性中,我们观察到3个明显的衰老相关蛋白变化峰值,分别发生在49岁和64岁(补充图3)。值得注意的是,49岁以后的趋势显示出显著蛋白质数量的急剧且持续下降,暗示系统性衰老的潜在转折点。这种下降可能反映了围绝经期和更年期相关的突发生理变化,包括激素戒断、免疫调节改变以及炎症负担增加。虽然在64度出现了进一步峰值,但较为不明显,且发生在下降的背景趋势上,凸显了女性衰老可能呈"悬崖式"的轨迹。相比之下,雄性表现出不同的模式,蛋白质组衰老呈更为振荡的轨迹。在生物年龄46、56和67岁时观察到三个峰值(补充图4),且未见女性那样的峰后衰退。这些波动可能反映了与年龄相关的分子变化更为渐进的积累,可能受性别特异性激素下降、代谢过程和免疫衰老差异的调节。第三个高峰为67岁,与总人口重叠,表明晚年衰老在性别间存在共同特征。这些发现强调了男女生物衰老轨迹的不同,并强调了衰老研究中性别分层分析的必要性。
药物靶点影响
进行了两样本孟德尔随机化(MR)分析,以探讨227种衰老蛋白与9种相关表型之间的潜在因果关系。共有6,278个血液cispQTLs可供分析,涵盖225种蛋白质(补充表18)。我们的初级分析显示血浆中存在5种与衰老风险相关的蛋白质(图1C,补充表19)。遗传上,血浆DPY30、FURIN和IGFBP4水平较高与KDM-BA及其加速风险增加相关,而SHISA5水平升高则与PhenoAge及其加速风险增加相关。结果显示,遗传预测的血浆CXCL13水平与生命寿命终结风险增加相关(b = 0.458,P = 2.42E-07)、寿命缩短(b = −0.610,P = 1.67E-10)以及父母寿命缩短(b = −3.171,P = 3.81E-12)。未发现其他衰老蛋白与衰老之间存在关联(均为P > 0.05)。所有仪器的F统计量范围为13至20,740(补充表18)。我们进行了斯泰格滤波,以确认所有因果方向均来自蛋白质水平到与衰老相关的性状(补充表20),支持了我们MR发现的稳健性。此外,研究发现有十种蛋白质是可药物治疗的。每种蛋白质的可拖拽层详见补充表21。
全表型关联分析结果
我们考察了衰老蛋白与器官相关表型之间的关系(补充表22)。Bonferroni校正后,发现了103个显著关联(图5A及补充表23)。DPY30与表现型数量最多,特别是与炎症相关的。最常见的关联与炎症(如CRP、嗜酸性粒细胞、淋巴细胞、单核细胞、白细胞、中性粒细胞)、脂肪组织(躯干脂肪量和全身脂肪量)以及血液成分(如LDL胆固醇和甘油三酯)相关,这些成分与5种蛋白质相关。并非每种蛋白质在这些认知方面都扮演重要角色。IGFBP4、CXCL13和SHISA5与认知密切相关,尤其是在数字记忆和反应时间方面。衰老相关蛋白与器官表型之间的相关性强调了它们在生物过程中的重要作用。这些蛋白质很可能调节整体健康,反映了器官间的相互作用和通讯网络。这一广泛影响表明它们在维持多个器官平衡与健康方面发挥着关键作用。 我们进一步表征了已识别蛋白的疾病相关性和临床意义。Bonferroni校正后,发现了82个显著关联(图5B及补充表23)。这五种蛋白质(CXCL13、DPY30、FURIN、IGFBP4、SHISA5)与多种疾病和死亡率密切相关。它们与心血管疾病、神经系统疾病、癌症、消化和泌尿系统疾病、呼吸系统疾病以及死亡率有显著相关性。心血管疾病,尤其是心肌梗死、充血性心力衰竭、高血压和心绞痛,这些蛋白质之间关联频率最高,且与5个蛋白质有关联。关于5种蛋白质对死亡率影响的研究揭示了重要发现。SHISA5风险最高(HR = 2.454),其次是IGFBP4(HR = 2.031)、FURIN(HR = 1.346)、DPY30(HR = 1.314)和CXCL13(HR = 1.312)。这些数据表明,特定蛋白质的年龄相关变化影响多个器官和疾病风险,尤其是心血管代谢。这凸显了进一步老龄化研究的重要性,暗示了有前景的调查方向。
风险因素对衰老过程的影响由血浆蛋白介导
我们关注心血管代谢因子是否能通过调节与衰老相关的关键蛋白质来影响衰老过程,特别是鉴于综合心血管代谢评分LE8与衰老之间的相关性48(图5C)。在45个潜在三角形中,包含与健康衰老相关的临床因子-蛋白质关联中具有显著且一致的方向性联系,共有17个三角形表现出显著的介导效应(补充表25)。我们鉴定出五种与衰老呈磁共振阳性关联的蛋白质,作为LE8与健康衰老关系的中介(见图5D)。所有显著三角形中,中位数中介率为41.99%。我们观察到SHISA5是多种生物过程中的重要介质,在多种结局中表现出最显著的积极介导效应。具体而言,SHISA5在虚弱(48.5%)、KDM-BA(10.0%)、KDM-BA加速(10.0%)、表龄(46.1%)、表龄加速(45.7%)和健康寿命(21.2%)方面表现出显著的积极介导作用。
讨论
血浆蛋白质组学是一种有前景的方法,用于识别与衰老相关的临床生物标志物。本研究分析了UKB中的2,923种蛋白质,以探讨它们与9个与衰老相关的性状:表龄、表龄加速、KDM-BA、KDM-BA加速、健康寿命、LTL、父母寿命、寿命和虚弱。共有227个蛋白质和所有表型都有持续的关联。进一步研究了这些蛋白质的生物功能及其对衰老的影响。此外,我们的研究揭示了生物衰老过程中的动态变化,蛋白质组变化在41、60和67年代末的生物衰老阶段达到顶峰。这些发现凸显了这些时期对于干预生物衰老过程至关重要。此外,我们测试了它们与衰老的因果关系,发现CXCL13、DPY30、FURIN、IGFBP4和SHISA5为有前景的衰老生物标志物候选。PheWAS对衰老相关蛋白的分析结果表明,这些蛋白质在生物过程中发挥着关键作用,包括调节整体健康和维持多个器官之间的平衡。 L.-Z. 马,W.-S.刘,Y。他等人。《高级研究杂志》80 (2026) 691--704 我们的研究强调炎症在衰老中的关键作用。与衰老相关的关键蛋白主要富含与炎症相关的通路。此外,在这些蛋白质聚集后,观察到若干蛋白簇的关键病理也与炎症相关。最新研究发现,针对促炎细胞因子网络作为抗衰老策略的潜力。抗炎药物,包括二甲双胍、阿司匹林、雷帕霉素和布洛芬,目前正在研究其潜在的抗衰老效果。例如,二甲双胍已证明通过调节IKK/NFjB等通路,在2型糖尿病患者中有效减少慢性炎症并促进健康衰老49,以及GPX7/NRF250和新近确定的靶点PEN251。阿司匹林已被证明能通过减少氧化应激来延缓复制衰老。此外,研究已确认CD36是SASP相关机制的关键介质。CD36特异性短干扰RNA已被证明能有效减少衰老肌组织细胞中的SASP分泌52。我们的研究表明,衰老相关蛋白在多个器官中表现出组织特异性的表达模式,在某些区域如大脑皮层和额叶皮层中表现尤为显著。这支持了越来越多的证据表明,器官特异性衰老轨迹背后有不同的分子过程。在大脑中,特别易受衰老影响的区域------如前额叶皮层------在突触可塑性和离子通道稳态上发生显著变化。例如,SYNPR是一种与突触囊泡相关的蛋白,参与调节化学突触传递,已被研究与AD中乙酰胆碱(ACh)释放的Ab诱导障碍相关53。同样,调节神经元兴奋性和长期增强的N-甲基天冬氨酸(NMDA)受体GRIN2A在衰老皮层中表现出异常剪接模式54。GRIN2A的失调与钙介导的老年神经元兴奋毒性有关,从而加剧帕金森病模型中的氧化应激和神经退行性疾病55。这些发现强调了组织特异性蛋白质改变------尤其是在大脑中------在介导衰老过程中结构和功能衰退的相关性。值得注意的是,尽管大脑因易受年龄相关认知退化影响仍是核心关注点,但我们发现多个器官蛋白质富集的发现表明,独特的分子特征可能支撑着器官特异性衰老轨迹。研究这些组织富集蛋白不仅可能推动我们对多器官的理解,还能为不同器官的衰老过程提供新的生物标志物和机制性见解。我们研究的另一个关键发现是生物衰老过程中发生的等离子体蛋白质组变化。识别出三波与41岁、60岁和67岁生物年龄相关的必需蛋白质波,伴随着剧烈的生理变化。这些峰上的蛋白质在组成和功能上存在部分重叠富集。与一般的生物衰老过程不同,我们的发现表明41可能代表生物衰老的潜在起始时间点,其特征是免疫相关、代谢和细胞信号通路,这也是该时期衰老的一个潜在机制。这个已有60年历史的国家正值更年期过渡期。这一时期发生的变化比生命其他阶段更为明显56。这些变化不仅体现在激素水平上,还体现在免疫力和组织功能中。此外,我们发现与HIF-1信号通路相关的蛋白质在67岁时表达差异。研究表明,HIF-1信号通路以及p53和TNF-a等因子,在动脉夹层、动脉粥样硬化等心血管疾病中至关重要57,58。HIF1A参与HIF-1信号通路和p53信号通路,导致缺氧条件下通过HIF-1a上调p5359。总体来看,这些发现表明生物衰老的节奏在不同生命周期中不均匀,因此需要进一步研究以阐明不同生物衰老阶段某些蛋白质的潜在机制。 702 在我们的分析中,我们识别出若干生物衰老的潜在生物标志物。CXCL13、DPY30、FURIN、IGFBP4和SHISA5成为MR显示重要性最高的潜在关键药物靶点。CXCL13在衰老中的作用主要体现在神经炎症和免疫反应中。研究表明,随着年龄增长,小胶质细胞的再生导致CXCL13的表达增加,而CXCL13与AD中tau蛋白的变化相关60。此外,在免疫检查点抑制剂治疗中,CXCL13通过吸引B细胞到受损器官,促进免疫相关不良事件61。这些发现表明CXCL13在调节与衰老相关的神经炎症和免疫反应中至关重要。DPY30是H3K4组蛋白甲基转移酶复合体的核心成分,已被确认是细胞增殖和衰老的关键调控因子62。DPY30的丧失会引发一种衰老表型,表现为ROS升高、CDK抑制剂如p16INK4a的激活,以及通过ID蛋白途径对细胞周期基因的转录失调,表明其在调节衰老相关细胞应激反应中起着核心作用62。FURIN在衰老中的作用主要体现在其表达和定位的变化上。在糖尿病条件下,肾小球细胞中的FURIN表达减少,但它会在内质网和高基氏体内积累,导致细胞外基质重塑失调。这种失调加速了GBM物质的沉积,损害肾小球过滤功能,从而加速衰老过程63。IGFBP4由衰老细胞作为衰老相关分泌表型的一部分释放,并作为应激介质。低剂量照射等基因毒性压力源可能触发其释放到血液中,与衰老效应相关。向小鼠注射IGFBP4可增加其肺部、心脏和新肾的衰老细胞64。SHISA5,也称为SCOTIN,是一种可诱导p53的跨膜蛋白,定位于内质网和核膜,已知在细胞应激条件下介导凋亡。p53在衰老过程中起着关键作用,其功能衰退与老年人癌症发病率增加相关65。此外,不同的p53同构体已被证明能调控细胞衰老和与年龄相关的疾病66。这些发现表明,SHISA5可能通过p53信号通路参与衰老,通过调节细胞存活率和应激反应。了解这五种蛋白质对衰老和代谢疾病(如糖尿病和阿尔茨海默病)的影响,为针对性的干预和治疗提供了机会。这些蛋白质显著影响多个器官的功能,强调客观评估的重要性,避免带有偏见的语言。研究参与者是年轻的印第安人来自英国的维二尔,代表衰老的早期阶段。在这些年轻群体中,研究揭示了一种明显的蛋白质变化模式,更准确地反映了早期衰老相关的蛋白质变化。研究鉴定出与肺功能、炎症和脑功能相关的多种蛋白质。这些发现支持衰老在不同器官中同时发生,且可能共享蛋白质相关生物过程的共同易感性。这种共享机制使得能够同时监测多个器官的衰老过程及相关生理变化。
本研究结合了高通量蛋白质组学剖析与大型社区队列中健康衰老的深入评估,并辅以广泛的长期临床随访。英国生物样本库此前的蛋白质组学研究主要聚焦于个体衰老表型。例如,薛等人在43,895名参与者中检测了2,920种血浆蛋白,发现了102和90种与虚弱和虚弱相关的蛋白质67。同样,赵等人对2923个蛋白质和端粒长度的全球信息(GWAS)数据进行了蛋白质组范围的随机化,识别出22种与白细胞端粒长度有因果关系的蛋白质68。虽然这些研究提供了关于特定衰老相关性状的宝贵见解,但其单一表型方法可能忽视了跨年龄维度的共享生物学机制。相比之下,我们的研究利用经过验证的生物年龄测量方法(KDM-BA和表龄),系统性地考察了超过5万人中9923种不同衰老表型中的蛋白质。这一多维方法揭示了12,193个Bonferroni显著关联,远超以往单一性状分析的范围。值得注意的是,227种蛋白质在所有结局中显示出一致关联,凸显了其作为系统衰老生物标志物的潜力。通过整合分子、临床和功能老化维度,我们不仅复制了先前报道的关联(如炎症和氧化应激通路),还发现了如PON3和UMOD等新型交叉表型调控因子。这些发现使我们的研究成为理解共享衰老机制和识别健康衰老干预高优先治疗目标的综合资源。然而,解读结果时需要注意一些局限性。首先,Olink目前使用的平台可能无法完全覆盖人类蛋白质组,尽管它提供了循环血浆蛋白的全面测量,但由于蛋白质测量偏好存在偏差。然而,我们的研究通过使用超过5万个体的数据和2923种蛋白质,成功解决了我们设定的科学问题。需要注意的是,我们的大多数研究参与者都是白人。尽管我们进行了内部和外部交叉验证并观察到校准良好的模型,但在更大、种族多样化的人群中验证我们的研究成果至关重要。第三,参与UKB的个体可能比不参与者更注重健康,这可能导致对健康持续时间的患病率和发病率低估。然而,以往的研究显示,慢性病病例的确诊与初级保健记录之间存在高度相关性。
总结
我们的研究揭示了生物衰老过程中血浆中蛋白质组的变化。值得注意的是,我们确定了生物年龄41、60和67为关键过渡点,并识别GDF15、CXCL13、DPY30、FURIN、IGFBP4和SHISA5为有前景的生物衰老标志物。这些发现对我们理解生物衰老的分子机制有重要贡献,并对系统性衰老的发展具有重要意义未来针对年龄相关疾病的生物标志物和个性化治疗靶点。
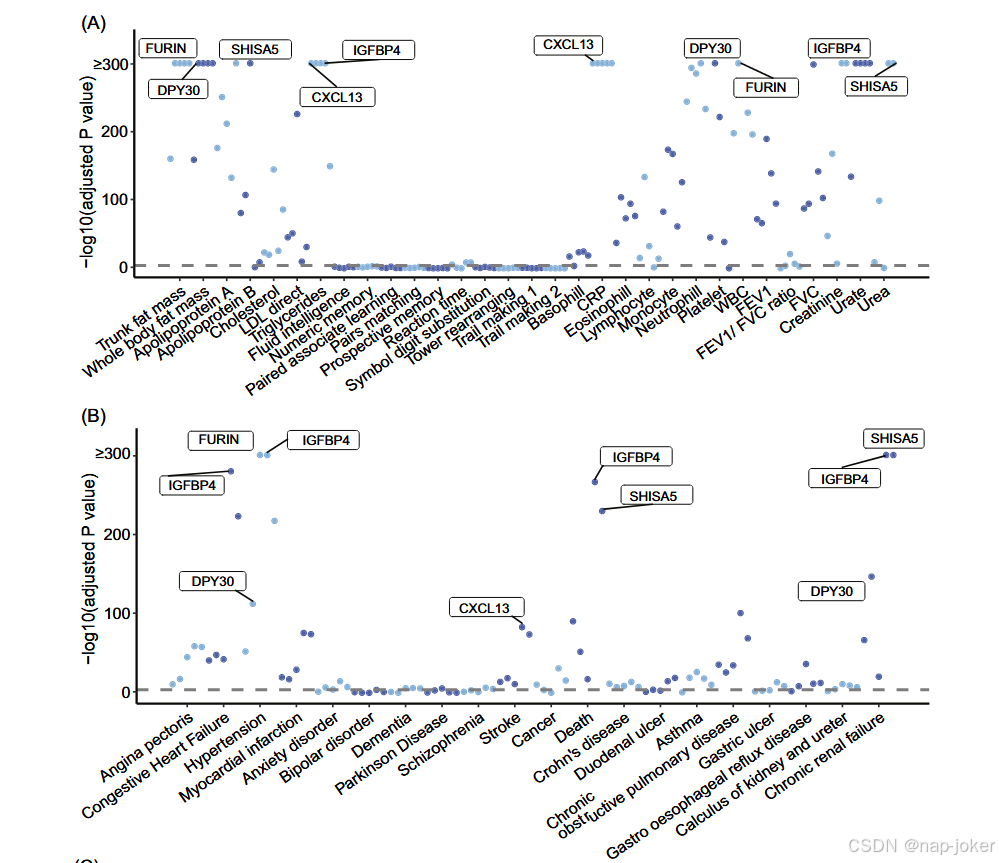
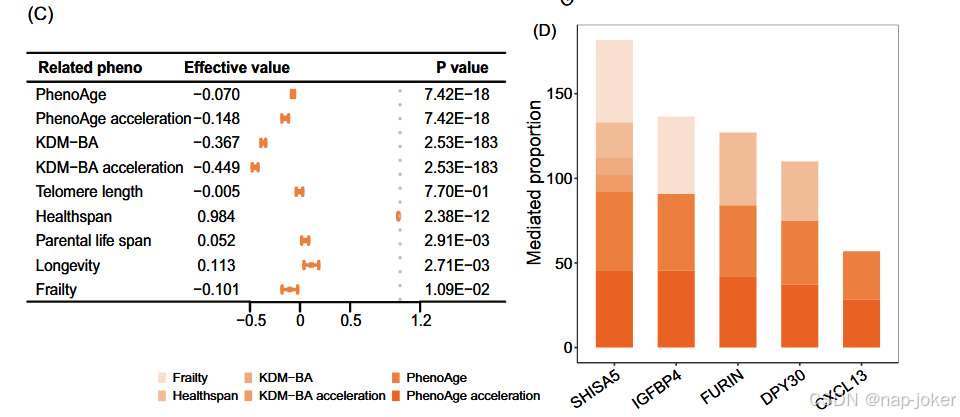
图5,衰老相关蛋白的现象组关联分析。A-B。五种关键衰老相关蛋白与器官表型、疾病及死亡率之间的表型全范围关联分析。纵轴表示每个关联的P值的− log10,横轴代表不同的表型类别。显示的P值为双侧,经过多次测试调整。每个图中的灰线是Bonferroni 0.05修正阈值。C. LE8与衰老之间的关联。D. 条形图显示了每次暴露中介导蛋白的比例及发生结果。这表明可调节风险因素在通过蛋白质中间体介导的衰老影响中占比。提供了健康衰老中各蛋白质显著介导的详细中位数比例。