本笔记基于杨荣武教授主编的《生物化学》第四版,配图也来自教材
糖原的存在有利于维持血糖的浓度,也提供了一种容易被快速动员的短期能源储备。实际上,不仅仅是动物可以合成糖原,一些细菌、古菌和真菌也可以合成,比如大肠杆菌、农杆菌和酵母
糖原的分解
细胞质基质内的糖原的分解主要是磷酸解,只有在分支点上的葡萄糖残基是被水解下来的
糖原的磷酸解
糖原的磷酸解是由糖原磷酸化酶催化的,被磷酸解的葡萄糖残基总是位于非还原端,糖原磷酸化反应在胞内是自发的(因为磷酸的浓度很高)总的来说,磷酸解和水解的差别其实就在于用磷酸基团代替了水分子,离去的葡萄糖残基结合脱质子的磷酸(类比氢氧根),糖原链新的非还原端连接质子
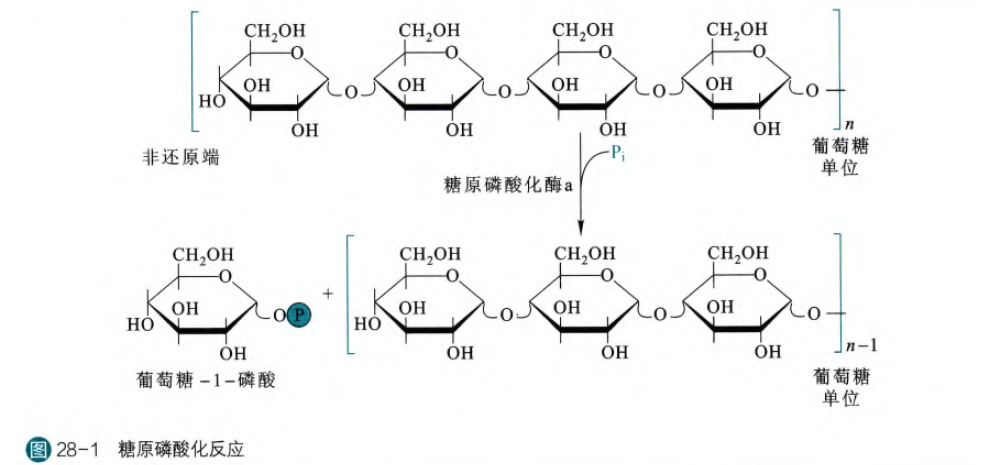
糖原磷酸化酶是由两个完全相同的亚基组成,每一个亚基通过席夫碱各共价结合一个磷酸吡哆醛。但是其实磷酸吡哆醛真正起到活性作用的是磷酸基团,而非吡哆醛
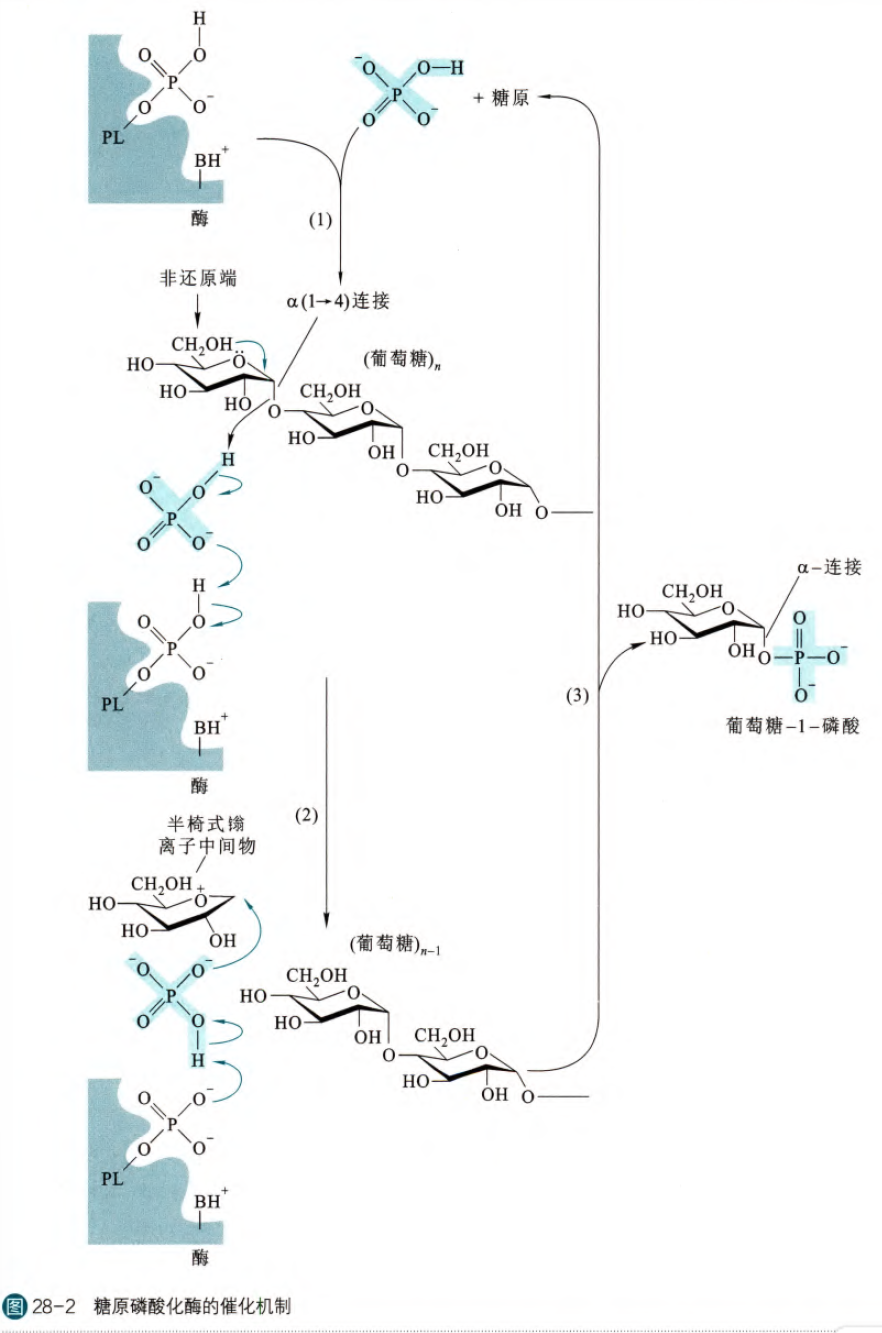
整个反应可以分为两步,一步是磷酸基团介导的葡萄糖残基的脱落并形成半椅式鎓离子中间物,第二步是磷酸基团与中间物的结合形成G-1-P,同时酶上的磷酸基团也恢复与原态,这里的酶实际上发挥的是广义的酸催化,与亲电进攻无关。这整个反应的发生水分子都被完全排除在活性中心之外,有效地防止水解反应的发生。
然后磷酸解产生的G-1-P可以通过磷酸葡萄糖变位酶来转变为G-6-P(这一步是可逆反应),生成的G-6-P可以进入糖酵解,如果细胞当中存在葡萄糖-6-磷酸酶的话(比如肝细胞),那么就可以通过糖异生途径释放到血液中来调节血糖,但是对于肌糖原而言,因为肌细胞不表达葡萄糖-6-磷酸酶,所以肌糖原仅可以用于肌细胞,而不参与血糖的调节
分支点葡萄糖残基的水解
糖原磷酸化酶的作用有限,一方面仅仅可以磷酸解α(1->4)糖苷键,而不可以磷酸解α(1->6)糖苷键,另外,如果糖原磷酸化酶不可以作用所有的α(1->4)糖苷键,当遇到与分支点相距4个葡萄糖残基的糖苷键时变无法水解,这个时候需要脱支酶的作用
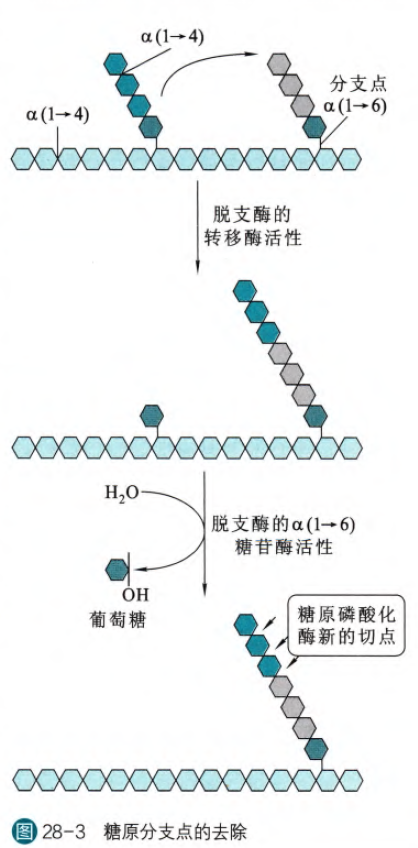
脱支酶是一种双功能酶,一个功能是具有α(1->4)葡萄糖基转移酶活性,此活性可以使得与分支点葡萄糖残基相连的不能被磷酸解的3个葡萄糖单位转移到邻近的寡糖链的非还原端,并且维持α(1->4)糖苷键连接。
遗留在分支点的葡萄糖残基在脱支酶的第二个功能即α(1->6)糖苷酶的活性作用下,被水解成游离的葡萄糖分子(在这个意义上,肌糖原是可以通过脱支酶产生微量的游离葡萄糖分子)
因为一个糖原同时存在很多非还原端,所以这些非还原端同时可以作为磷酸化酶的作用目标,使得糖原在较短时间内就可以释放出较多的葡萄糖分子
(淀粉酶是具备糖原水解的活性的,淀粉酶分为两种,一种是α-淀粉酶,这种淀粉酶是内切淀粉酶,不同于糖原磷酸化酶一般一个一个从非还原端脱离,而是可以直接作用于所有的α(1->4)糖苷键,但是最后剪切的结果一般不是单个葡萄糖分子,而是寡聚糖链;一种是β-淀粉酶,这种淀粉酶是外切淀粉酶,这种酶的作用机理基本上就是糖原磷酸化酶作用机理(差别在于是水解),也是从非还原端进行剪切的,遇到分支点距离几个残基的时候就会受到阻碍)
溶酶体内糖原的分解
溶酶体内的糖原被认为是通过细胞自噬进入的,其降解是由单一的水解酶即酸性α-糖苷酶催化的,这种酶也叫做酸性麦芽糖酶,对于α(1->4)糖苷键和α(1->6)糖苷键都具有水解活性,从而可以使得糖原分子当中的所有葡萄糖单位都直接以游离的形式释放出来
(星形胶质细胞也存在糖原,此糖原对于低血糖时神经元的功能以及长期记忆的形成密切相关,在收到信号激发之后,星形胶质细胞的糖原就会分解并且进一步降解为乳酸,然后乳酸运输到附近的神经元,神经元细胞可以吸收乳酸并通过乳酸脱氢酶将其转化为丙酮酸,丙酮酸即可进一步参加线TCA循环分解功能)
糖原的合成:
糖原合成的一般特征
-
葡萄糖需要活化,葡萄糖分子不可以直接缩合在一起,而是需要活化为UDP-葡萄糖(UDPGlc)才可以发生合成
-
需要引物,催化糖原合成的酶不可以直接从头开始催化,只能将UDPGlc转移到事先已经合成好的引物分子上。能够充当糖原合成引物的分子有两种,一种是还没有完全降解的糖原分子,其非还原端就可以作为引物,一种是蛋白质,对于酵母和动物而言,我们把充当引物的蛋白质称为糖原素。
-
糖链延伸具有方向性,这一点非常容易理解,因为我们糖苷键连接的时候便具备着严格的方向性,包括我们前面介绍的糖原的水解上也是从非还原端向还原端水解的
-
分支点的引入需要专门的分支酶
糖原合成的详细步骤
葡萄糖的活化分为三步:
(1)在己糖激酶或者是葡萄糖激酶的作用下,葡萄糖被磷酸化为G-6-P
(2)在磷酸葡萄糖变位酶的崔海霞,G-6-P转变味G-1-P
(3)在UDPGlc的焦磷酸化酶的催化下,G-1-P代替UTP的焦磷酸活化为UDPGlc(这是在动物体和酵母当中发生的),而在细菌体内,G-1-P最终活化为ADPGlc
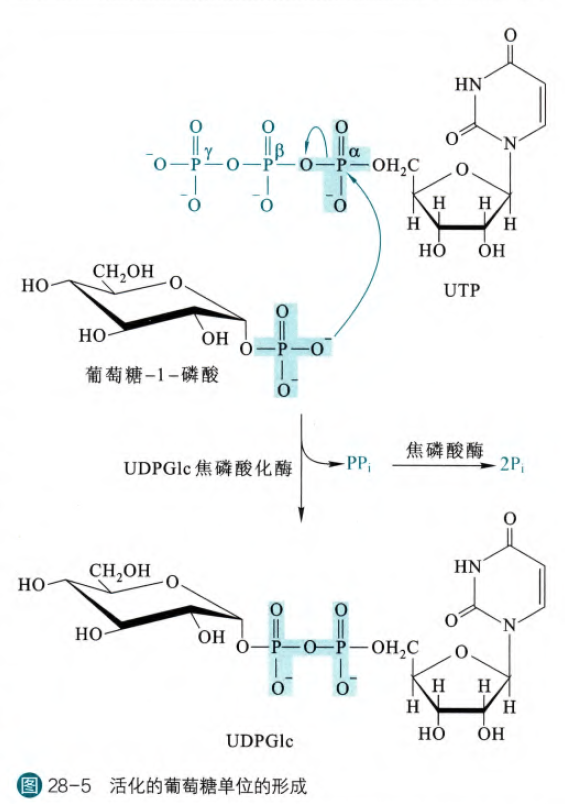
其实在第三步过程当中,仅仅是替换焦磷酸的过程是可逆的,但是焦磷酸的水解过程是一个自由能很大的自发过程,所以可以驱动着UDPGlc的转变
所以从游离的葡萄糖合成活化的UDPGlc一共需要消耗两分子的NTP
糖原合成的启动
糖原合成的启动是由糖原素引发的,糖原素具有自催化的活性,即糖原素自带的酪氨酸葡萄糖糖基转移酶的催化下,第一个葡萄糖单位从UDPGlc上转移到糖原素Tyr194残基的羟基上,同时生成一个UDP,此时的糖苷键称为O型糖苷键,后面糖原素会继续催化8~12个UDPGlc的连接,接着糖原合酶便会接手
糖原合酶需要与糖原素结合才可以催化糖原链的延伸,当合成到一定长度之后,糖原合酶和糖原素脱离,此时糖原的合成也完毕了。所以糖原的长度是受到限制的,这样也显示了分支点多不仅有利于糖原的迅速动员,同时也有利于一个糖原分子尽可能聚合多的葡萄糖分子
那么支链的形成需要分支酶的作用,分支酶可以将一个六糖或者是七糖单位,从一段长于11个葡萄糖残基的糖链的非还原端转移到邻近的糖链上,并且以α(1->6)糖苷键相连,新的分支点至少距离老的分支点4个葡萄糖残基
(这里对于转移数目严格的把控有两点意义,一是确保转移后的两条链可以正常延伸,转移的单位要大于6是和被转移的链不少于11都是为了转移之后这两链都可以继续延伸;二是,保证分支点适当的距离有助于糖原的正常分解,如果距离过近一方面会给糖原磷酸化酶造成较大的空间位阻,另一方面也会使得脱支酶存在较大的空间位阻)
(另外有两点比较细节:一是糖原素是两个相同的亚基组成的同源二聚体,所以一个糖原素可以同时引发两条糖原主链的延伸(细胞内可以合成多少糖原实际上是取决于细胞当中有多少糖原素);二是分支酶转移的分支不一定要来自于主链,也可以是来自于已经延长一段距离的支链,这样由此形成多级分支结构)
糖原代谢的调控
因为糖原的合成是要付出代价的,也就是同一个葡萄糖先由糖原释放,然后再重新合成糖原,实际上是要多付出1个NTP的,那么为了防止能量的浪费,细胞当然会这种空转。所以机体对于糖原的分解和合成也是交互调控的。
糖原分解的限速酶是糖原磷酸化酶,糖原合成的限速酶是糖原合酶,那么这两种酶就是糖原代谢的主要调节目标。这两种酶的调节方式有两种,一是别构调节,二是受激素控制的可逆磷酸化调节
别构调节
肝糖原和肌糖原的糖原磷酸化酶是同工酶,在结构和调节机制上存在差别
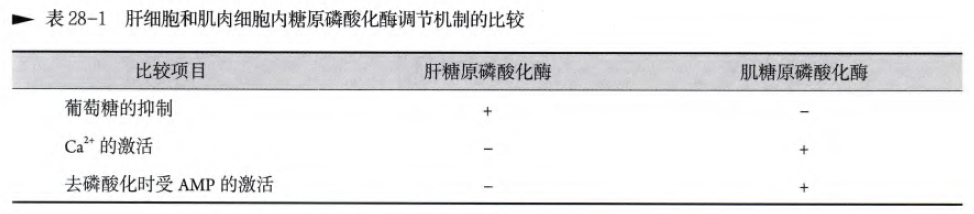
肌糖原磷酸化酶的别构调节
首先我们需要明确肌糖原磷酸化酶可以分为四种状态,实际上是两种和两种状态的组合。我们把没有磷酸化的肌糖原磷酸化酶(在这一小节中简称为酶)称为b型,被磷酸化的酶称为a型,那么同时在这两型酶当中,都存在着R态和T态。但是区别在于两点,一点是a型中R态的比例显著高于b型中R态的比例;第二点是a型中无论R态还是T态都不受到G-6-P、AMP和ATP的别构效应。而b型中的T态会因为AMP而别构激活转变为T态,R态会因为ATP和G-6-P的别构抑制转变为T态(T态之所以活性较低是因为其酶活性中心被自身一段肽链形成的环遮掩了)
至于a态和b态之间的转变是由肾上腺素的调控的,当肾上腺素作用在肌肉细胞时,会促进b型转变为a型,那么a型也会因为磷蛋白磷酸酶的作用转变为b型(因为磷蛋白磷酸酶是组成型酶,所以a型会自发的转变为b型)也就因此,在静息状态下,酶的基本形式都是b型
那么我们如何理解这多种状态呢?从b型T态出发,这是肌细胞的能量充足的时候,当肌纤维开始收缩,细胞能量水平降低的时候,此时ATP和G-6-P的抑制作用下降,AMP的激活作用上升,所以b型有更多的T态转变为了R态,这是一般情况下的调控(主要的调控机制就是细胞的能量水平);但是肌细胞也可以听从更高水平的指示,当肾上腺素作用在肌细胞的时候,即激活肌糖原磷酸化酶b激酶活性,从而促进b型转变为a型,这一转变相当于直接再添一把火,但是等到激素作用结束(激素水平下降之后),a型也会变回b型,回到静息状态。
肝糖原磷酸化酶的别构调节
肝糖原磷酸化酶在调控机制上与肌糖原磷酸化酶存在着较大的差异。
首先,会对别构效应物产生反应的是磷酸化的a型而非去磷酸化的b型
其次,别构效应物也非上述提到的三种物质,而是葡萄糖,葡萄糖会促进a型转变为b型
糖原合酶的别构调节
糖原合酶也有a型和b型,但是a型主要是去磷酸化形式,而b型主要是磷酸化形式
G-6-P是糖原合酶的别构效应物,能够降低b型合酶对UDPGlc的Km值,从而使磷酸化的合酶合成糖原。
(这里做一个简单的总结,可能a型和b型,R态和T态有点晕,但是这里注意它们的本质定义就好,a型是高活性状态,也就是R态的比例高于T态,b型反之,所以不要用是否磷酸化定义ab型也不要用是否会被别构效应物调节来定义;可以以肌糖原磷酸化酶的a型和b型为基准,肝糖原磷酸化酶不同的点是受到别构效应物(Glc)的调节,同时Glc可以直接介导a型转变为b型,糖原合酶差别在于磷酸化的不同,a型是去磷酸化的,而b型是磷酸化的。关于磷酸化也是比较简单判断的,我们可以用胰高血糖素作为参考(代表细胞低能态),胰高血糖素会促进磷酸化,那么为了保证能量的供应,自然糖原磷酸化酶要有活性,所以磷酸化的是高活性态的a型,那么反之拮抗的就应该是糖原合酶,磷酸化的是低活性的b型)
受激素控制的"可逆磷酸化"调节
这一部分可以说是所有部分当中最绕的,但是核心请记住,在低能状态要磷酸化,这样激活糖原磷酸化酶抑制糖原合酶;在高能状态要去磷酸化,这样抑制糖原磷酸化酶激活糖原合酶
好了接下来我们先从直接作用的酶开始说起,这里隆重登场的酶有两种一种是糖原磷酸化酶b激酶(之后简称激酶)一种是磷蛋白磷酸酶,因为其主要在这里发挥作用的是蛋白质磷酸酶1(PP-1)。
那么激酶可以促进糖原磷酸化酶磷酸化,从而促进b态向a态的转变,激活活性,同时磷酸化糖原合酶,从而促进其由a态向b态转变,抑制活性。
但是PP-1总体来说和激酶的作用相反,但是调节机制会更复杂,关键在于PP-1对于肝糖原磷酸化酶的作用是有条件的。
我们再来关注这两种酶在什么情况下可以被激活。
激酶被激活的条件有两个,一个是其β亚基上被磷酸化修饰,这样其的活性可以部分激活(磷酸化的重要signal对于肝细胞是胰高血糖素,对于肌细胞是肾上腺素);而是其sita亚基是钙调蛋白,需要与钙离子结合才可以部分激活酶活性(钙离子释放对于肝细胞是肾上腺素的作用,而对于肌细胞是神经冲动的作用),那么当两个条件同时满足的时候,激酶活性达到最大
PP-1活性调节的机制相对来说更加复杂,在肌细胞和肝细胞普遍存在的调节机制是,在胰岛素的作用下细胞中某种激酶的活性上调,PP-1中与糖原结合的G亚基被磷酸化作用,这时候PP-1处于高活性状态;但是在胰高血糖素和肾上腺素的作用下,PKA会被激活,从而磷酸化G亚基的另外一个位点,从而使得G亚基与糖原分离,一旦分离之后PP-1便失去活性
在肌细胞当中,主要通过PPI-1(PP-1的抑制剂)(也是一种蛋白)与PP-1的结合从而抑制PP-1的活性。这种抑制蛋白比较有意思,一方面其在没有磷酸化的条件是没有活性的,在磷酸化的条件下是活性的,这个也正好和我们之前的分析对上了,在低能状态,PPI-1被磷酸化激活,然后从而抑制PP-1的活性;另一方面是PP-1本身就具备去磷酸化PPI-1的活性,也就是PPI-1抑制时间是有限的
在肝细胞当中,PP-1发挥作用还受限于肝糖原磷酸化酶给不给它这个机会。PP-1可以结合a型的R态和T态,但是只有T态才会把Ser14位暴露出来(这是糖原磷酸化酶调控的位点,对于糖原合酶存在多个磷酸化位点)。所以PP-1仅仅可以对T态发挥作用,对于R态束手无策。那么这个时候就回扣我们在上面讲到的为什么Glc可以促进肝糖原磷酸化酶从a向b的转变呢?实际上Glc促进的是a态的R向T态转变,这样就给了PP-1发挥作用的机会,从而促进a态向b态转变
另外,PP-1的底物之一还有b激酶,从而进一步调控糖原合成和降解。但是除了我们介绍的两种调控酶,其实PKA可以促进糖原磷酸化酶和糖原合酶的磷酸化,同时糖原合酶同时也受到PKC、AMPK、糖原合酶激酶和酪蛋白激酶的磷酸化,这些激酶都可以抑制糖原合酶的活性
以上总结的内容大家也可以看出复杂性,但是不论如何,糖原的合成与分解始终都是拮抗的,所以调控它们的机制也是如此