 ANGPT2(血管生成素2)作为血管生成素家族的核心分泌型糖蛋白,由496个氨基酸组成,是调控血管稳态与病理性血管重塑的关键靶点。该蛋白特异性表达于血管内皮细胞,通过靶向TIE2酪氨酸激酶受体,深度参与机体血管发育、屏障维持及多种病理进程,已成为当前生物制药领域备受关注的研究热点。#卡梅德生物 #生物实验 #实验室日常 #科研干货
ANGPT2(血管生成素2)作为血管生成素家族的核心分泌型糖蛋白,由496个氨基酸组成,是调控血管稳态与病理性血管重塑的关键靶点。该蛋白特异性表达于血管内皮细胞,通过靶向TIE2酪氨酸激酶受体,深度参与机体血管发育、屏障维持及多种病理进程,已成为当前生物制药领域备受关注的研究热点。#卡梅德生物 #生物实验 #实验室日常 #科研干货
核心作用机制
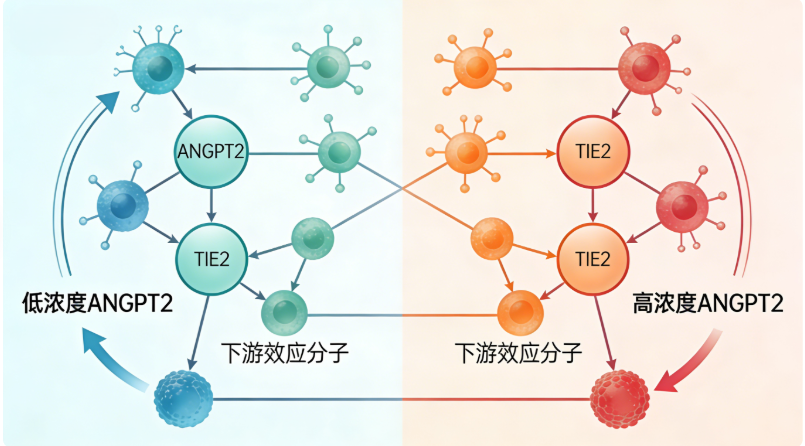
ANGPT2的生物学功能高度依赖ANGPT2-TIE2信号通路,并与同家族的ANGPT1形成动态调控网络。两者虽共享TIE2受体,但效应截然不同:生理状态下,ANGPT1持续激活受体磷酸化,维持血管内皮紧密连接与周细胞覆盖,稳固血管屏障;而在病理状态下,ANGPT2表达上调,作为竞争性拮抗剂阻断ANGPT1介导的信号传导,导致血管通透性升高并诱发炎症。此外,ANGPT2可与VEGFA协同放大病理性血管生成信号。值得注意的是,其功能具有浓度依赖性,低浓度辅助血管生成,高浓度则破坏稳定性,这一特性为药物干预提供了明确的分子基础。
药物研发现状
目前全球范围内,靶向ANGPT2的上市药物以双特异性抗体为主,代表性产品为罗氏研发的法瑞西单抗(Faricimab)。作为首款获批的VEGFA/ANGPT2双抗,该药通过同时阻断两条通路,既抑制异常新生血管生成,又恢复血管屏障稳定性,显著延长了眼底血管病变患者的给药间隔。尽管暂无单纯靶向ANGPT2的单克隆抗体上市,但相关单靶点药物正处于临床前或早期临床研究阶段,致力于优化亲和力与降低脱靶效应,为未来单一适应症治疗储备管线。
未来发展趋势
未来该靶点的研发将聚焦于双抗迭代升级、适应症拓展及药物形式多元化。一方面,新一代双抗旨在进一步延长给药周期至半年一次;另一方面,研究正从眼底疾病向颅内血管异常、慢性炎症及糖尿病并发症等领域延伸。此外,纳米抗体、基因治疗等新型形式的出现,以及与抗炎药物的联合疗法,将为提升治疗应答率提供新路径。针对科研人员在靶点验证与药物筛选中的需求,卡梅德生物可以提供ANGPT2重组蛋白、抗体定制及相关检测试剂盒等技术服务,助力科研项目高效推进。