在制药企业的QA/QC或RA,经常会发生这样一幕"标准接力赛":
当一个品种准备申报出口或进行一致性评价对标时,团队需要同时开启数个网页:一个是需要付费订阅且复杂的USP(美国药典)官网,一个是界面极其不友好的EP(欧洲药典)在线库,还有一个是全日文的JP(日本药典)PDF......
"这个杂质限度在USP新版里是不是又收紧了?"
"为什么EP的最新增补版还没更新到我们的本地库?"
"客户要查十年前的老标准,去哪里翻旧PDF?"
这种"标准孤岛"与"版本断层",不仅是研发效率的杀手,更是药企合规体系中一颗随时可能引爆的雷。在全球监管趋严的今天,靠手动翻PDF、靠碎片化下载来对标国际标准,其风险成本已无法估算。
对于志在出海的药企而言,药典标准不是一张静态的纸,而是一条动态的流。
很多企业在研发初期,仅参考了当时的"现行版"。然而,药典的增补与修订速度往往超过研发周期。如果在申报前夕忽略了最新一版的微小变更,可能导致整个批次的稳定性试验需要重做,甚至直接触发注册审评的退回。
更棘手的挑战在于**"追溯"**。在进行专利无效分析或处理产品质量诉讼时,往往需要精准查阅十年前甚至更久之前的标准。这种历史版本的稀缺性,常让企业陷入"有据难查"的困境。
药智数据国外药典数据库是解决方案之一,它建立了横跨8国/地区的"标准全景图"。它不仅实时同步USP、EP、JP等主流药典的最新数据,更将历史版本进行了系统化整合。
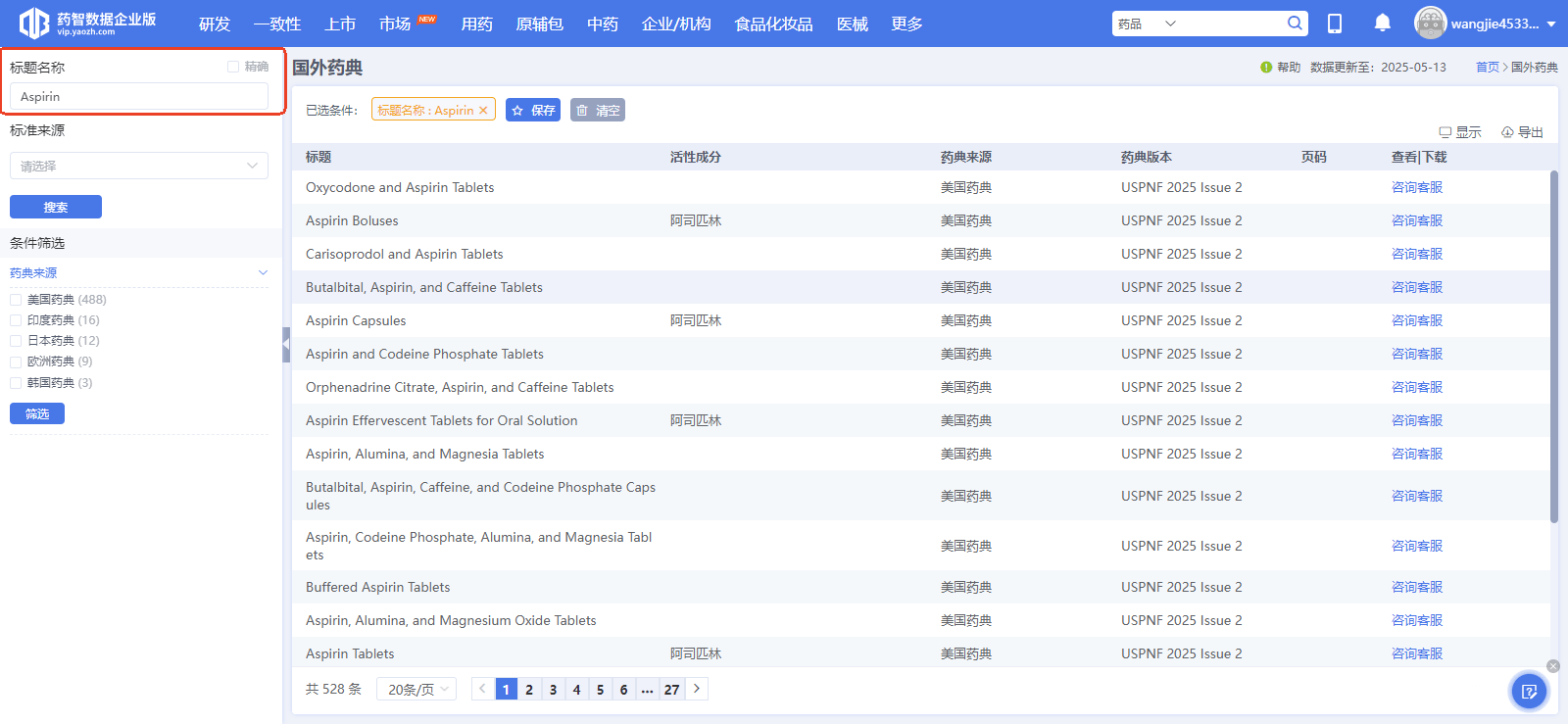
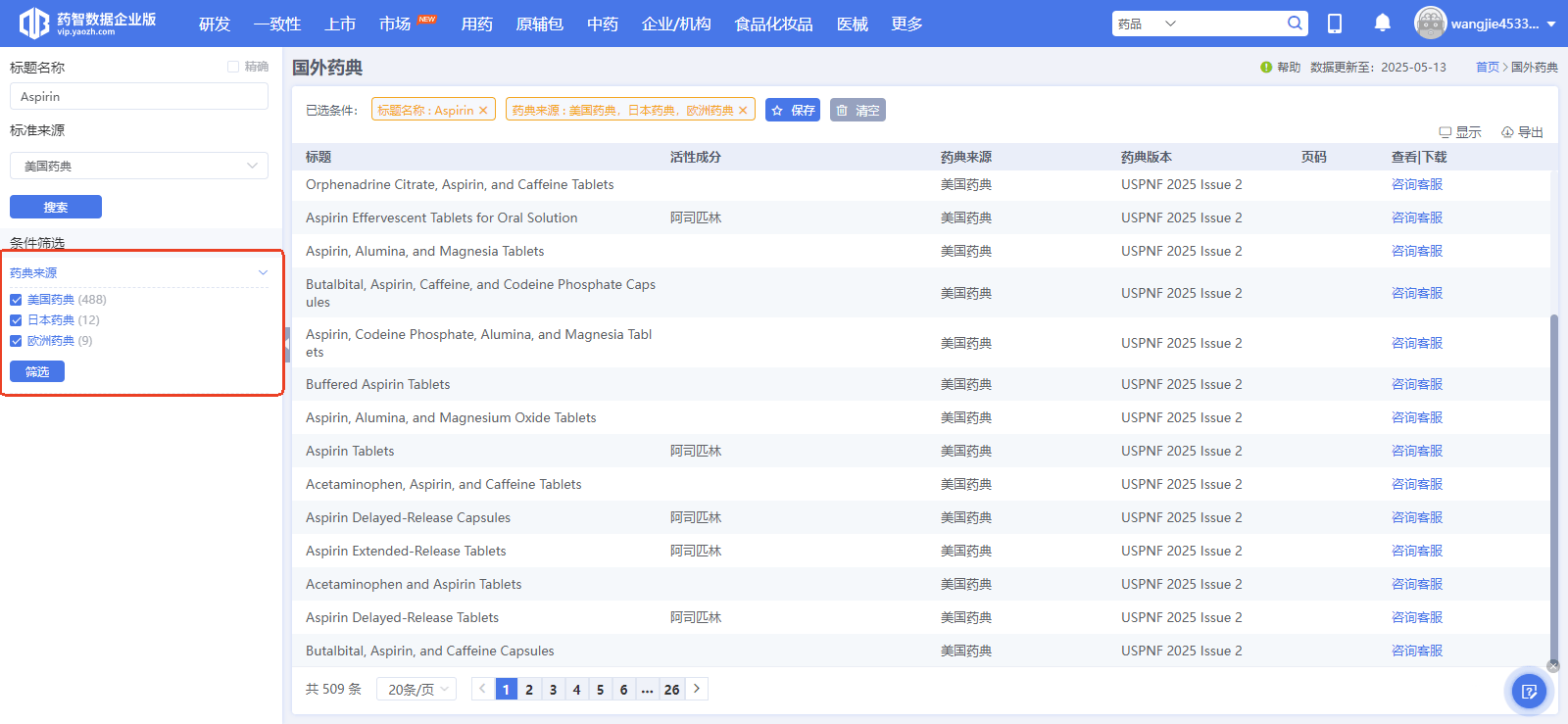
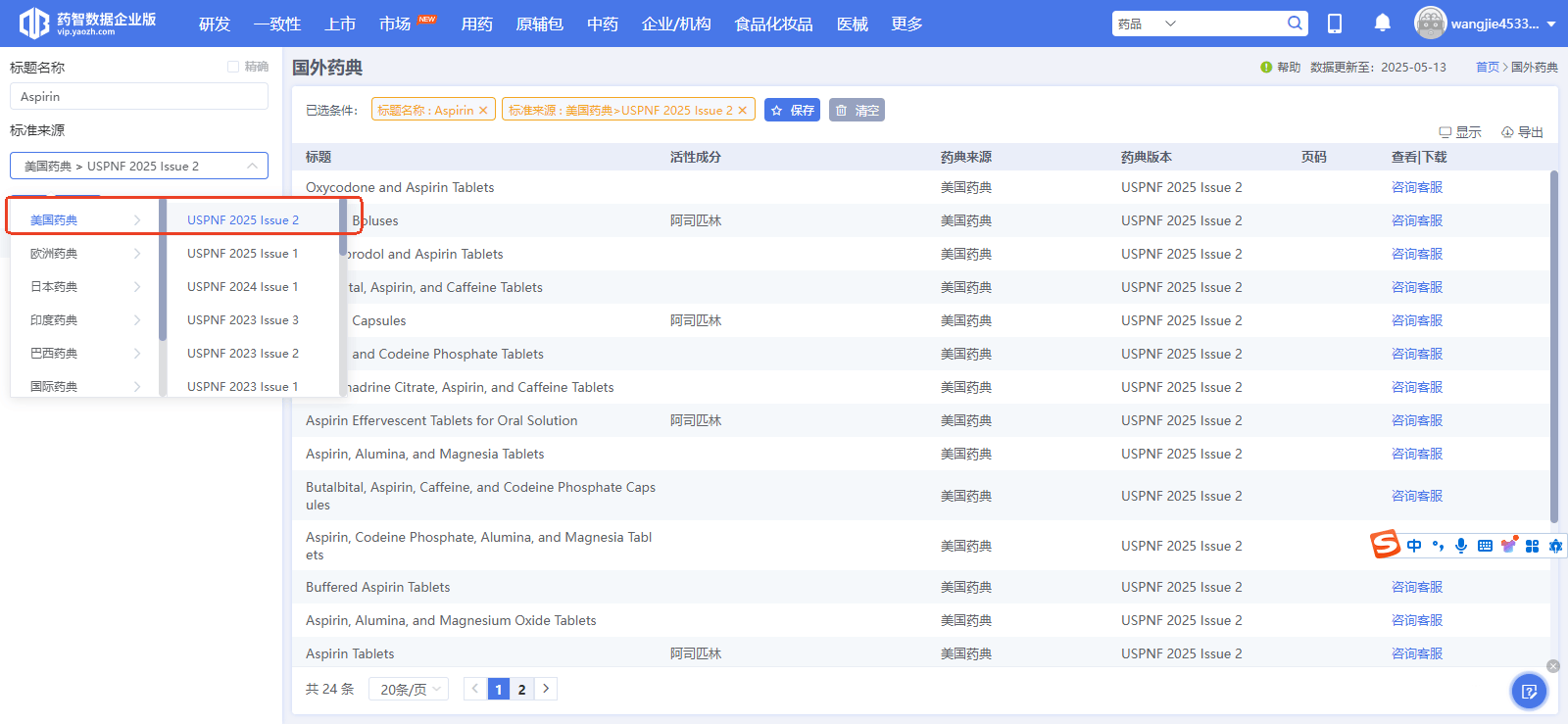
当QA不再需要为了一个标准变迁而翻箱倒柜,而是能在一分钟内完成"跨版本、跨国别"的对标时,企业构建的是一种**"确定性"的合规能力**。这种能力,是应对全球飞行检查最坚实的底气。
在医药出海的大潮中,数据不是负累,而是指南针。
国外药典数据库背后代表的,不仅是一个工具,而是一套**"对标全球,实时风控"**的质量管理理念。它帮助中国药企打破与国际标准之间的数字鸿沟,让合规不再是被动的应对,而是主动的战略布局。