在药品关联审评审批制度下,原料药、药用辅料和药包材(简称"原辅包")与制剂已深度绑定,其质量与可及性直接关系到药品研发的成败与上市速度,对于药企而言,如何高效、精准地筛选出合规、优质且稳定的原辅包供应商,并洞察其技术审评状态,成为优化研发布局、保障供应链安全的核心环节。
药智数据原料药、药用辅料和药包材数据库已解决这些痛点。
以某仿制药企业计划寻找质量稳定且价格合适的辅料------微晶纤维素为例。
可通过原辅包数据库直接检索"品种名称=微晶纤维素""登记类型=辅料"的数据再来进行二次分析,已获批准(A状态)的原料药是更稳妥、更主流的选择,通常也意味着更低的直接议价空间;而采购尚在审评中(I状态)的原料药,虽然理论上采购方可能获得更大的议价主动权,但其背后隐藏的风险和后续成本可能更高。可再额外通过单独检索企业名称,查看该企业登记的原辅包登记情况来分析该企业实力,或者用企业筛选系统、药品补充申请备案、美国DMF等其他数据库交叉检索企业、辅料供应商的变更等信息。
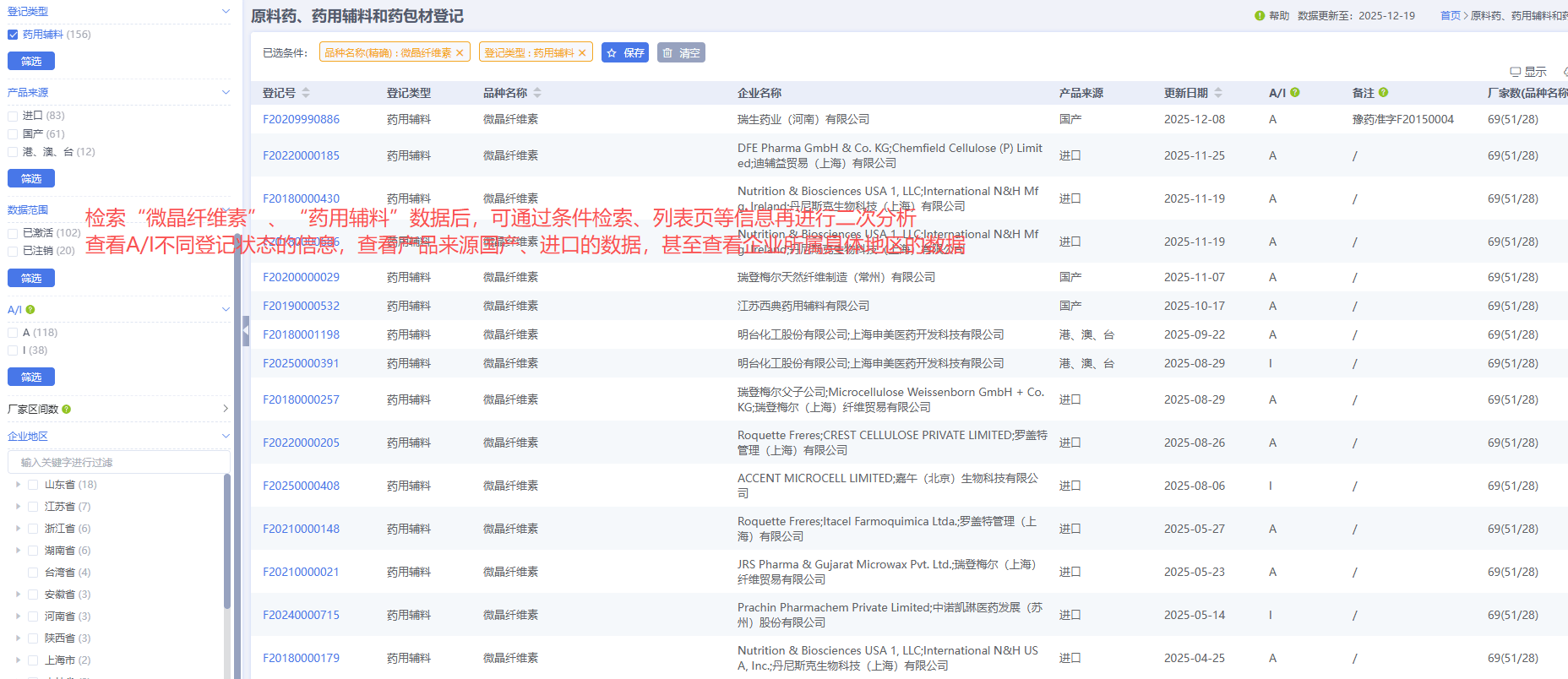
以原料药厂家自身为例,通过原料药、药用辅料和药包材数据库监控自身及竞争对手产品的官方登记状态变化,了解同类产品中哪些竞争对手已获得"A"状态,明确自身市场定位和竞争策略,识别市场空白或竞争红海,制定定价与生产策略。
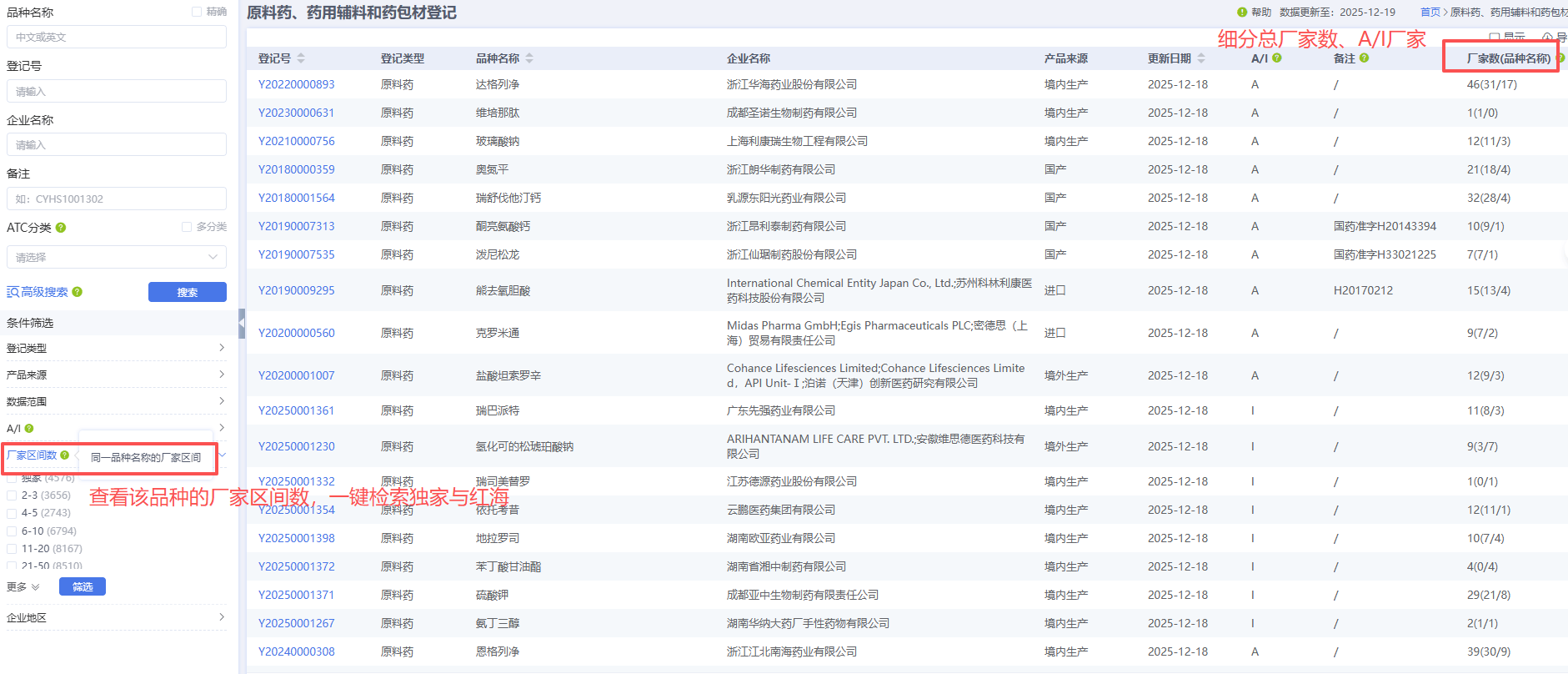
该数据库将散乱的官方登记信息转化为结构化、可分析的战略情报。它帮助药企与研发机构在药品开发早期就做出明智的供应链决策,有效管控质量与供应风险,最终为加快药品研发上市、优化成本结构、构建韧性供应链提供坚实的数据基石。