在免疫学与生物药研发领域,CD274(又称PD-L1)作为B7家族的关键成员,因其在调控免疫稳态中的核心作用而备受关注。作为免疫细胞表面的关键抑制性配体,CD274通过与受体PD-1结合,传递抑制信号,防止免疫系统过度激活。本文将从技术角度,对CD274靶点的分子机制、下游信号通路验证以及抗体药物研发方向进行系统解析。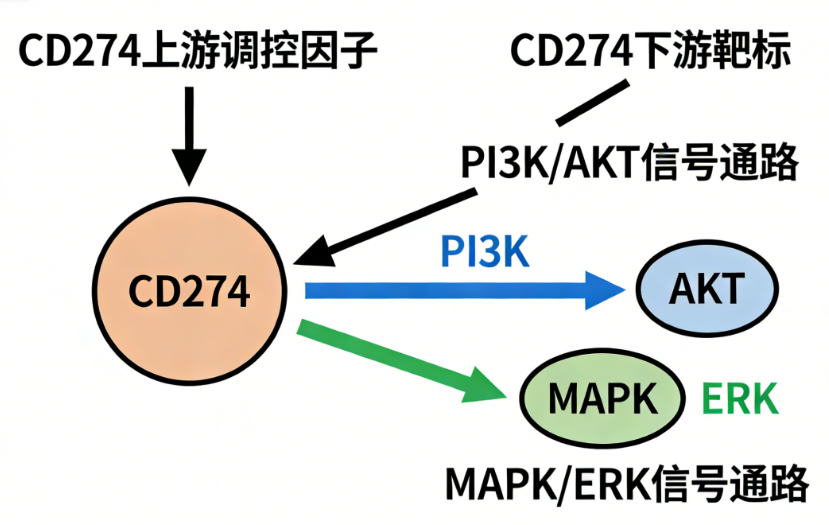
1. 分子特征与作用机制
CD274为I型跨膜糖蛋白,属于免疫球蛋白超家族。其表达具有高度动态性:在静息状态下,活化的免疫细胞(如T细胞、B细胞、树突状细胞)及上皮细胞表面表达量极低;而当机体发生免疫反应或炎症时,其表达量会显著上调。这种诱导性表达特性是其精准调控免疫稳态的基础。
CD274的唯一天然受体为PD-1,主要表达于活化的T细胞、B细胞及NK细胞表面。二者结合后,诱导CD274胞内段构象改变,招募SHP-1、SHP-2等磷酸酶。这些磷酸酶会去磷酸化TCR下游的信号分子,从而阻断免疫活化信号的传递。这一过程在实验室中常通过免疫共沉淀(Co-IP)和Western Blot技术进行验证,是免疫负调控机制研究的核心内容。
2. 核心信号通路与实验验证
CD274/PD-1轴的激活主要通过两条经典通路抑制免疫细胞功能,这也是实验室检测药物活性的重点指标:
- PI3K/AKT通路:CD274与PD-1结合后,抑制PI3K的激活,减少细胞内PIP3的生成,进而抑制AKT蛋白的磷酸化。这直接阻止了免疫细胞的增殖与活化,并促进其凋亡,避免免疫细胞过度积累引发炎症损伤。
- MAPK/ERK通路:该通路被抑制后,会显著减少免疫细胞中IFN-γ、TNF-α等炎症因子的分泌,减弱免疫反应的强度,同时抑制免疫细胞效应功能的发挥,保护自身组织不被过度攻击。
正常生理条件下,这一信号轴充当免疫应答的"负向调控因子",在清除病原体后及时"刹车",让免疫系统恢复静息状态。若该信号过度激活,会导致免疫耐受;若信号缺失,则易诱发自身免疫性疾病。
3. 靶向抗体药物研发现状
目前的CD274靶向药物主要分为阻断型抗体 (解除免疫抑制)和激动型抗体(强化免疫抑制)两大类,旨在通过调节免疫平衡来治疗相关疾病。
代表性药物:阿替利珠单抗(Atezolizumab)
- 类型:全人源IgG1型抗CD274阻断型单克隆抗体。
- 机制:通过特异性结合CD274胞外结构域,竞争性阻断其与PD-1的结合,从而解除CD274介导的免疫抑制信号,恢复免疫细胞的活性与效应功能,增强机体对病原体的清除能力。
- 技术特点:采用噬菌体展示技术筛选获得,具有高亲和力和特异性,目前已被用于多种免疫相关疾病的治疗研究。
代表性药物:度伐利尤单抗(Durvalumab)
- 类型:全人源IgG1型抗CD274阻断型单克隆抗体。
- 机制:高效结合CD274,阻断其与PD-1的相互作用,恢复免疫细胞的活化能力。其技术优势在于对Fc段进行了修饰,减少了与FcγR的非特异性结合,从而降低了抗体依赖的细胞毒性(ADCC)效应,更适合长期免疫调节治疗。
其他研发方向 :
除了单抗,目前还有激动型抗体(用于治疗免疫过度活化)、双特异性抗体(如同时靶向CD274与其他免疫检查点)以及纳米抗体等新型药物形式正在研发中,旨在实现更精准的免疫协同调控。
4. 未来技术发展趋势
结合行业前沿进展,CD274靶点的研发正朝着精准化、联合化与剂型创新的方向迭代:
- 药物形式创新:开发双特异性抗体(如CD274/CD3)、纳米抗体及分子胶类药物。纳米抗体凭借分子量小、组织穿透性强的优势,更易到达病变部位;分子胶则通过促进CD274自噬降解来调控蛋白丰度,为治疗提供了新路径。
- 联合治疗策略:探索CD274阻断型抗体与JAK抑制剂、抗炎单抗或疫苗的联合使用。例如,与疫苗联用可增强免疫原性;与细胞治疗联用可提升改造后细胞的体内存活率。
- 精准医疗落地:基于伴随诊断试剂筛选适用人群,结合单细胞测序技术动态监测信号通路活性,实现个体化用药,避免免疫失衡。