Efficient biosynthesis of serotonin and melatonin through combinatorial metabolic engineering in Escherichia coli
在大肠杆菌中通过组合代谢工程高效合成血清素与褪黑素

摘要
血清素与褪黑素是两种由色氨酸衍生而来的神经调节物质,具有重要的生物活性功能,在食品工业中应用前景广阔。然而,二者的微生物合成过程普遍存在合成效率低、依赖动物源辅因子以及胞内产物毒性等问题。本研究在大肠杆菌中首次构建了一条不依赖四氢生物蝶呤(BH4)的新型褪黑素生物合成途径 。首先,本研究取得了一项关键突破:对限速酶 ------ 不依赖 BH4 的色氨酸羟化酶(Tph)进行创新改造,提升了其可溶性与催化效率。随后,运用通路优化、辅因子工程等先进代谢工程策略,强化前体色氨酸以及血红素、S - 腺苷甲硫氨酸(SAM)等辅因子的供给。同时,通过转运工程手段促进褪黑素外排,解决了产物胞内毒性问题。最终,经改造的工程菌株在 5 L 生物反应器中进行补料分批发酵,血清素产量达 1.92 g/L,褪黑素产量达 3.40 g/L,为目前大肠杆菌中已报道的褪黑素最高产量。本研究构建了可规模化的色氨酸源活性代谢物绿色微生物合成平台,为其在食品领域的可持续工业化生产与应用奠定了坚实基础。
1 引言
血清素(5 - 羟色胺)与褪黑素(N - 乙酰基 - 5 - 甲氧基色胺)是一类极为重要的吲哚胺类分子,在调控人体情绪、睡眠 - 觉醒周期、神经内分泌活动等多种生理功能中发挥关键作用(Ahmad et al., 2023; Carhart-Harris & Nutt, 2017; Chowdhury et al., 2008; Pourhamzeh et al., 2022; Reiter et al., 2024)。
这类化合物在神经疾病治疗(Ahmad et al., 2023; Cummings, 2012; Stecher et al., 2024)、植物育种(Nawaz et al., 2015)及免疫调控(Slominski et al., 2025; H. Wu et al., 2019)领域的应用日益广泛,推动了其全球市场规模快速扩张(Juhnevica-Radenkova et al., 2020)。褪黑素已在多种动物、植物及微生物中被分离鉴定,如多边舌甲藻(Hardeland, 1999)、酿酒酵母(Rodriguez-Naranjo et al., 2012)和白色链霉菌(Shi et al., 2023)。
从色氨酸(Trp)到褪黑素的生物合成主要存在四条潜在途径,均以色氨酸为底物、血清素为关键中间产物(Back et al., 2016; Xie et al., 2022)。褪黑素的生物合成起始于色氨酸的羟基化反应,该步骤由 ** 色氨酸羟化酶(Tph)特异性催化生成 5 - 羟色氨酸(5-HTP);随后 5-HTP 经 色氨酸脱羧酶(Tdc)** 脱羧生成血清素。
与此同时,色氨酸也可先由 Tdc 脱羧生成色胺,再经 ** 色胺 5 - 羟化酶(T5H)羟基化形成血清素。此后,血清素在 血清素 N - 乙酰转移酶(SNAT)或 芳烷基胺 N - 乙酰转移酶(AANAT)催化下发生乙酰化反应;最终由 咖啡酸 O - 甲基转移酶(COMT)** 介导血清素与 N - 乙酰血清素的甲基化,完成整条合成途径(图 1A)。
值得注意的是,动植物间褪黑素的具体生物合成过程存在显著差异:植物途径具有较强灵活性,可根据生理状态选择先羟基化或先甲基化的合成路线;而动物则遵循保守的、以羟基化为起始的合成路径。这一差异推动了不同酶系的进化分化(图 1A)(Shi et al., 2023)。
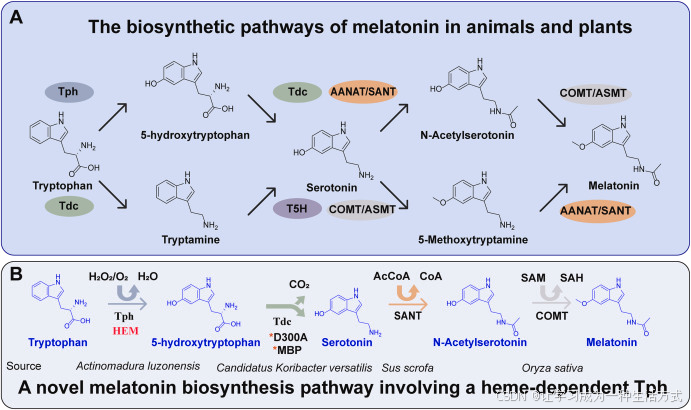
图 1 动植物褪黑素合成机制比较(Tan et al., 2016)及本研究褪黑素合成途径构建
(A)在动物中,血清素的合成严格以羟基化为起始步骤 (Vivi & Bentley, 2018);而在植物中,该途径受生理与环境因素调控,存在两条不同合成路径(Back et al., 2016)。(B)本研究构建的基于 ** 血红素依赖型色氨酸羟化酶(Tph)** 的新型褪黑素合成途径。HEM:血红素;AcCoA:乙酰辅酶 A;CoA:辅酶 A;SAM:S - 腺苷甲硫氨酸;SAH:S - 腺苷同型半胱氨酸;红色星号:本研究采用的策略。
传统褪黑素生产方法存在明显局限。目前,工业上主要通过植物提取与化学合成两种方式生产褪黑素。化学合成通常涉及多步反应,包括费歇尔吲哚合成或自由基介导反应(Xiaodong et al., 2025);而植物提取法则产量极低,每克植物材料仅能获得 5~10 mg 产物(Juhnevica-Radenkova et al., 2020; Pérez-Llamas et al., 2020)。因此,这两种方法环境影响大、生产成本高,可持续性与经济性均受限。
为解决上述问题,微生物细胞工厂被开发为绿色、高效的替代生产平台。研究者已采用多种工程改造策略实现血清素与褪黑素的生物合成(Xiaodong et al., 2025)。最初,研究者将绵羊来源的SNAT 基因与水稻来源的COMT 基因在大肠杆菌中异源表达,首次构建了以 5 - 羟色胺为底物的完整褪黑素生物合成途径 ,但产量仅为 1.465 mg/L(Byeon & Back, 2016)。
随后,通过对色氨酸羟化酶(Tph)进行定向进化,并强化四氢生物蝶呤(BH4)依赖的羟基化途径,实现了大肠杆菌中褪黑素的全从头合成 。在补料分批发酵中,外源添加色氨酸时褪黑素产量达 2 g/L,以葡萄糖为唯一碳源时产量为 1 g/L(Luo, Schneider, et al., 2020)。值得注意的是,色氨酸羟化酶严格依赖 BH4,而该辅因子在细菌中天然含量极低(Luo, Yang, et al., 2020)。因此,有研究通过引入外源 BH4 合成与回收途径实现胞内 BH4 供给,最终血清素浓度达 1.68 g/L(Shen et al., 2022),但胞内氧化还原状态需重新平衡以适配 BH4 内源供给。
近期研究发现,吕宋拟无枝菌 中的 Tph 是一种依赖血红素、不依赖 BH4 的新型羟化酶(Shi et al., 2023)。这些开创性研究证实了微生物法生产的可行性。尽管大肠杆菌合成褪黑素已实现克级产量,但进一步提升产能仍面临关键瓶颈:(1)异源酶活性低、稳定性差,尤其是限速酶 Tph(Shi et al., 2023)与甲基转移酶 COMT(Luo, Schneider, et al., 2020);(2)大肠杆菌中 BH4、SAM 等辅因子供给不足;(3)褪黑素的胞内毒性导致产物抑制,高浓度下抑制菌体生长。
值得关注的是,最新研究通过理性设计改造不依赖 BH4 的 Tph、优化电子传递通量、强化 NADPH pool 供给电子,使血清素产量提升 9 倍,达到 15.42 g/L(Xu et al., 2025),体现了该类 Tph 的高催化效率,为优化大肠杆菌褪黑素合成途径提供了可行思路。
本研究首次在大肠杆菌中系统构建了不依赖辅因子 BH4 的新型血清素与褪黑素生物合成途径 (图 1B)。将不同来源的Tph 、Tdc 、SNAT 、COMT 等基因导入大肠杆菌 C41 (DE3),构建可将色氨酸转化为褪黑素的工程菌株;随后提升关键酶 Tph 的催化活性与可溶性表达水平,强化羟基化步骤效率;进而调控褪黑素合成相关的代谢与转运途径,优化血红素、SAM 等辅因子供给,最终通过最优工程菌株与反应器水平发酵工艺优化,获得目前已报道的最高褪黑素产量。
2 材料与方法
2.1 菌株与培养基
本研究所构建菌株见表 S1。大肠杆菌 DH5α 用作 DNA 克隆宿主;BL21 (DE3) 与 C41 (DE3) 用于重组蛋白表达与代谢工程改造。所有工程菌株均由 BL21 (DE3) 和 C41 (DE3) 经迭代基因编辑获得。
常规克隆与种子培养采用 LB 培养基:胰蛋白胨 10 g/L、酵母提取物 5 g/L、氯化钠 10 g/L,pH 调至 6.5。
摇瓶发酵采用 TB 培养基:胰蛋白胨 12 g/L、酵母提取物 24 g/L、甘油 4 mL/L、KH₂PO₄ 2.31 g/L、K₂HPO₄ 12.54 g/L,pH 6.5。必要时添加抗生素:氨苄西林 100 μg/mL、卡那霉素 50 μg/mL、链霉素 50 μg/mL、氯霉素 34 μg/mL。
补料分批发酵采用改良 R 培养基(MR):葡萄糖 20 g/L、MgSO₄・7H₂O 0.8 g/L、酵母提取物 5 g/L、KH₂PO₄ 6.67 g/L、(NH₄)₂HPO₄ 4 g/L、柠檬酸 0.8 g/L、微量元素溶液 5 mL/L,pH 6.5。微量元素溶液含:CaCl₂ 1.35 g/L、ZnSO₄・7H₂O 2.2 g/L、MnSO₄・4H₂O 0.58 g/L、CuSO₄・5H₂O 1 g/L、(NH₄)₆Mo₇O₂₄・4H₂O 0.1 g/L、Na₂B₄O₇・10H₂O 0.2 g/L、35% HCl 10 mL/L、FeSO₄・7H₂O 4 g/L。
对 TB 培养基进行优化,系统考察诱导时间(12、14、16、18、20、22、24、26 h)、IPTG 浓度(0.2、0.4、0.6、0.8、1.0 mmol/L)、色氨酸浓度(0、1.25、2.5、3.75、5 mmol/L)、发酵温度(25、30、37℃)等单因素与组合效应。优化后 TB 培养基添加:色氨酸 2.5 mmol/L、IPTG 0.8 mmol/L、5 - 氨基乙酰丙酸(5-ALA)1 mmol/L、二硫苏糖醇(DTT)0.8 mmol/L、硫酸亚铁铵 1 mmol/L、抗坏血酸 0.8 mmol/L。
色氨酸、5 - 羟色胺购自上海麦克林;5 - 羟色氨酸、褪黑素购自上海源叶;5 - 氨基乙酰丙酸购自 Sigma-Aldrich。
2.2 质粒构建与 DNA 操作
为构建 pET-Tdc、pRSF-Tph、pRSF-COMT、pRSF-SANT 等质粒,对血清素与褪黑素合成关键酶基因进行大肠杆菌密码子优化并全基因合成(南京金斯瑞),包括:吕宋拟无枝菌 DSM 43766 Luz15 (色氨酸羟化酶,OM250071.1)、全能科里伯特菌 Ellin 345 Tdc (色氨酸脱羧酶,NC_008009.1)、家猪SNAT (血清素 N - 乙酰转移酶,XP_005656968.1)、水稻COMT (咖啡酸 O - 甲基转移酶,NM_001403482.1)。
在 Tph、Tdc、SNAT、COMT 的 N 端引入 6×His 标签。采用 pRSFDuet-1 与 pETDuet-1 两种相容质粒构建初始单步酶促合成途径。
为过表达YhjV ,以大肠杆菌基因组为模板 PCR 扩增,分别连接至 pCDFDuet-1 与 pACYDuet-1。本研究所用质粒见表 S1。
构建 pRSF-MBP∗TphD300A-Tdc、pET-Tdc-MBP∗TphD300A、pRSF-COMT-SANT、pET-COMT-SANT 时,将目的基因分别克隆至 pETDuet-1 与 pRSFDuet-1 的Nco Ι/Bam H Ι 和Nde Ι/Xho Ι 位点。MBP 标签片段经 PCR 扩增与测序验证后,通过 Gibson 组装连接至 Tph 的 N 端。利用特异性引物对 pETDuet-1 进行定点突变,改造色氨酸羟化酶编码序列。
采用基于 CRISPR-Cas9 的 pEcCas/pEcgRNA 系统敲除tnaA 、yddG 、speD 等基因。通过在线工具设计 sgRNA,经 Gibson 组装连接至 pEcgRNA;以靶基因上下游约 500 bp 序列为同源臂,融合 PCR 构建修复模板。将 pEcCas、pEcgRNA 与修复模板共电转至宿主,通过抗性筛选获得阳性敲除株,经菌落 PCR 与测序验证。
PrimeSTAR Max Premix 聚合酶购自宝生物(大连);限制性内切酶购自赛默飞世尔;基因组提取试剂盒购自天根(北京);质粒小提与 DNA 纯化试剂盒购自生工生物(上海)。
2.3 培养方法
摇瓶培养:重组菌株在含相应抗生素的 LB 培养基中 37℃过夜培养 12 h,取 500 μL 种子液接种至含 50 mL 基础发酵培养基的 250 mL 摇瓶,37℃、220 rpm 培养 3.5 h,加入 0.8 mmol/L IPTG 诱导,30℃继续培养 22 h。
5 L 发酵罐补料分批发酵:装液量 3 L MR 培养基,添加 5 g/L 色氨酸。单菌落接种至 LB 培养基,37℃、220 rpm 培养 12 h,转接至 MR 培养基至 OD₆₀₀≈2.0,以 10% 接种量接入发酵罐。初始温度 37℃,OD₆₀₀≈20 时降温至 30℃,添加 0.8 mmol/L IPTG 诱导。采用此诱导时机可提高体积产能,符合大肠杆菌异源蛋白补料发酵常用策略。
pH 由 50% 氨水自动维持在 7.0;溶氧控制在空气饱和度 30%,搅拌转速 400--800 rpm,通气量 3 L/min。补料液含葡萄糖 700 g/L、MgSO₄・7H₂O 8 g/L、色氨酸 5 g/L、酵母提取物 5 g/L、(NH₄)₂SO₄ 5 g/L,采用 pH-stat 与动态葡萄糖补料策略。90 h 补料发酵中通过持续添加抗生素维持质粒稳定性,保证选择压力且不增加代谢负担。
2.4 分析方法
菌体生长用紫外分光光度计(UVmini-1240,日本岛津)在 600 nm 处测定吸光度。采用安捷伦 1260 高效液相色谱仪配紫外 - 可见检测器对 5 - 羟色氨酸、血清素、褪黑素进行定量,以标准品保留时间与峰面积标定。血清素(5--500 mg/L)与褪黑素(5--100 mg/L)标准曲线线性关系良好,决定系数 R² 均大于 0.999。
5 - 羟色氨酸与血清素检测 取 1 mL 破壁发酵液,盐酸按 1:4(v/v)稀释,25℃、14462×g 离心 10 min,上清经 0.22 μm 滤膜过滤。采用反相 C18 柱(Diamonsil HPLC C18,4.6 × 250 mm,5 μm),柱温 25℃;流动相 10% 乙腈 + 90% 0.05 mol/L 磷酸二氢钾水溶液,等度洗脱;流速 0.8 mL/min,进样量 10 μL,检测波长 280 nm。褪黑素检测 取 1 mL 破壁发酵液,等体积甲醇稀释,超声 20 min,25℃、14462×g 离心 10 min,上清经 0.22 μm 滤膜过滤。C18 柱,柱温 25℃;流动相甲醇:水 = 40:60(v/v),流速 0.6 mL/min,检测波长 290 nm。
方法学验证:血清素检出限 LOD=1 mg/L,定量限 LOQ=5 mg/L;褪黑素 LOD=0.5 mg/L,LOQ=5 mg/L。
3 结果与讨论
3.1 大肠杆菌血清素生物合成途径构建
为在大肠杆菌中异源合成血清素,选取吕宋拟无枝菌来源的色氨酸羟化酶基因Tph 与全能科里伯特菌来源的色氨酸脱羧酶基因Tdc 构建合成途径。利用中拷贝质粒 pETDuet-1 与高拷贝质粒 pRSFDuet-1,在大肠杆菌 BL21 (DE3) 与 C41 (DE3) 中表达,获得 4 株工程菌:SE-B1(pET-Tdc-Tph)、SE-B2(pRSF-Tph-Tdc)、SE-C1(pET-Tdc-Tph)、SE-C2(pRSF-Tph-Tdc)(图 2A)。
优化了色氨酸(Trp)、5 - 羟色氨酸(5-HTP)、血清素的 HPLC-UV 定量方法,可在 10 min 内完成三种物质的定量分析(R²>0.999),保留时间分别为 8.46 min、4.74 min、5.45 min(图 2B)。
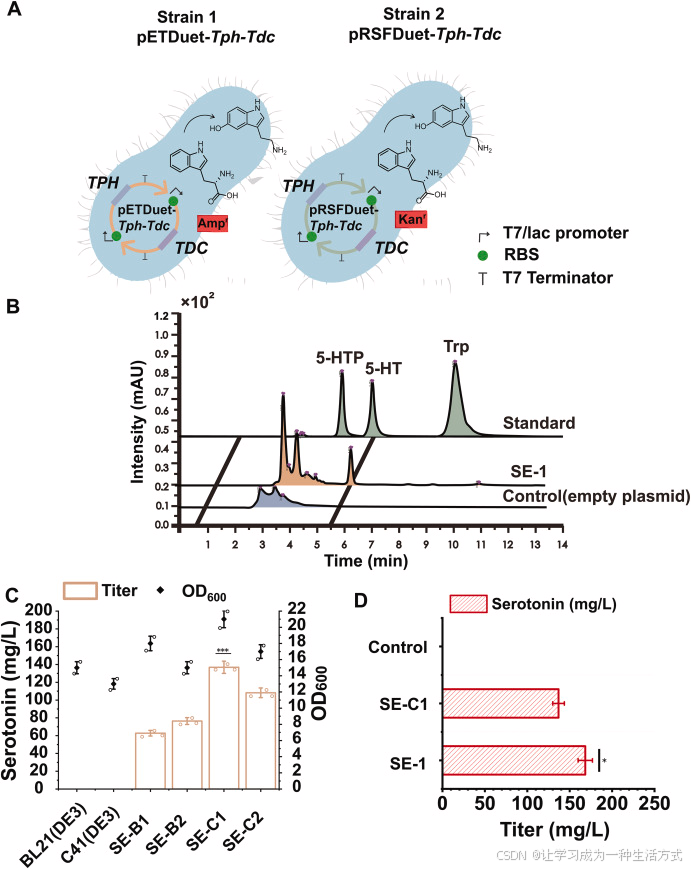
(A)三种含 pETduet-1 与 pRSFDuet-1 质粒的大肠杆菌菌株构建示意图。(B)菌株 SE-1 与空载对照菌株产血清素的 HPLC 分析图谱。(C)分别携带 pET-Tdc-Tph 与 pRSF-Tph-Tdc 质粒的 BL21 (DE3) 和 C41 (DE3) 宿主菌株的血清素产量与 OD₆₀₀值。(D)菌株 SE-C1 与插入 MBP 标签的菌株 SE-1 的血清素产量对比。RBS:核糖体结合位点;Control:未表达异源蛋白的宿主菌株。
对工程菌株的生物量与血清素产量进行测定。结果显示,四株工程菌的生物量相近(OD₆₀₀≈15),但血清素合成量相差达2.13 倍 (图 2C;SE-B1:64.11 mg/L;SE-C2:136.83 mg/L)。其中,重组菌株 SE-B1 在 48 h 时血清素产量为 64.74 mg/L,而相同发酵时间下,SE-C1 与 SE-C2 分别可合成 136.83 mg/L 和 108.23 mg/L 血清素。上述结果表明,宿主菌株与质粒拷贝数对血清素合成具有显著影响。
SDS-PAGE 分析显示,Tdc 蛋白(54.3 kDa)在重组菌株 TP-CD(含 pET-Tdc)与 SE-CP(含 pRSF-Tph)中均实现了良好的可溶性表达,而 Tph 蛋白(44.8 kDa)表达量显著偏低(图 S1)。同时,菌株 SE-CP 在 48 h 时中间产物 5 - 羟色氨酸的积累量仅为 69.06 mg/L(图 S2),说明Tph 催化的羟基化步骤是该合成途径的主要瓶颈 。
本研究采用麦芽糖结合蛋白(MBP)标签提升 Tph 在大肠杆菌中的表达水平(Jiang et al., 2024; Raran-Kurussi & Waugh, 2012)。MBP 并非通过改变亚细胞定位,而是依靠自身类分子伴侣活性,瞬时结合疏水区域以防止折叠过程中发生聚集,从而提升融合蛋白的可溶性(Nallamsetty & Waugh, 2006)。结果显示,菌株 SE-1(含 pET-Tdc-MBP∗Tph)的血清素产量提升至 168.33 mg/L,较重组菌株 SE-C1 提高了 23.02%(图 2D)。SDS-PAGE 验证表明,该融合策略显著提高了 Tph 的可溶性表达(图 S3,蛋白大小 87.5 kDa)。以上结果说明,提高 Tph 的可溶性表达是强化血清素合成的有效手段 。
3.2 Tph 蛋白工程改造以强化血清素生物合成
为进一步优化 Tph 酶的催化性能,本研究基于 AlphaFold 预测的蛋白结构开展理性设计改造(图 3A)。结构分析显示,该酶包含血红素结合口袋、底物激活位点等关键功能基序,涉及 Y106、Y109、H375 和 R295 等氨基酸残基(Shi et al., 2023)。在此基础上,选取位于预测底物结合空腔内、且与色氨酸吲哚环距离在 3 Å 范围内的一系列氨基酸位点进行饱和突变。虚拟饱和突变预测结果表明,D300 位点改造效果最为显著 (图 S4)。
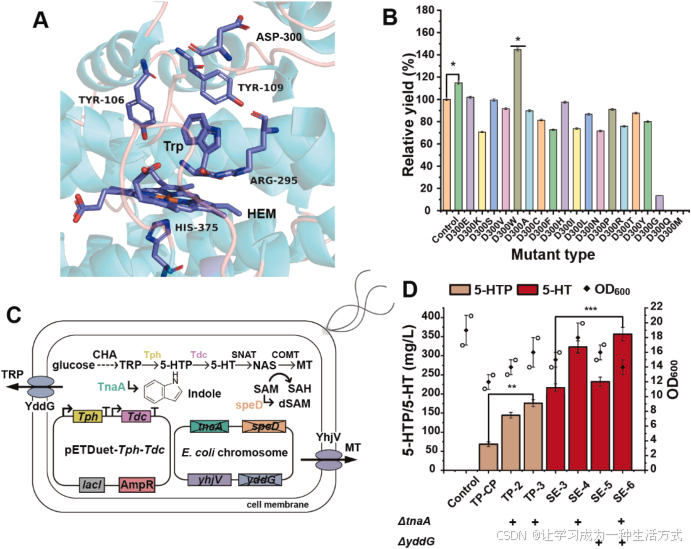
(A)Tph 蛋白结构及其与血红素、色氨酸和关键氨基酸残基的结合模式。(B)对 Tph 的 D300 位点进行饱和突变。(C)用于重组合成血清素与褪黑素的工程大肠杆菌菌株构建示意图。(D)代谢工程菌株的 5-HTP、血清素产量及 OD₆₀₀测定结果。CHA:分支酸;TRP:色氨酸;MT:褪黑素;Control:未表达异源蛋白的宿主菌株。
筛选结果显示,D300A 突变体 (SE-2 菌株,含 pET-Tdc-Tph^D300A)血清素产量达 198.11 mg/L,较 SE-C1 对照菌株提升 44.78%(图 3B)。我们推测,将体积较大、带负电的天冬氨酸残基(Asp300)替换为短小的非极性丙氨酸(Ala)可能通过双重机制发挥作用:(1) 减弱与底物吲哚环之间的静电排斥,利于底物结合;(2) 优化底物与血红素辅因子的空间取向和构象柔性。这些结构上的优化共同促使羟基化反应形成更有利的过渡态,加快反应动力学并提高产物得率。
将 MBP 标签与 pET-Tdc-Tph^D300A 融合,获得工程菌株 SE-3(含 pET-Tdc-MBP∗Tph^D300A),其 48 h 血清素产量达 217.09 mg/L,较 SE-2 菌株进一步提升 9.58%。由于 Tph 纯化存在技术困难,本研究未测定体外动力学参数;但突变体活性提升已由体内产量与比生产率升高的实验结果证实。
3.3 减少前体色氨酸流失以提高大肠杆菌血清素产量
由tnaA 编码的色氨酸酶催化的内源色氨酸降解途径,以及 YddG 转运蛋白介导的外排系统,会显著消耗大肠杆菌胞内色氨酸库(图 3C)。为强化色氨酸内源供给,在重组菌株 SE-3 中敲除tnaA 获得 SE-4(ΔtnaA );敲除yddG 获得 SE-5(ΔyddG );同时敲除tnaA 和yddG 获得双敲菌株 SE-6(ΔtnaA ΔyddG )。TP-2 由 C41ΔtnaA 转入 pRSF-Tph 构建;TP-3 由 C41ΔtnaA 转入 pRSF-MBP∗Tph 构建,以 MBP 融合提升 Tph 可溶性。
发酵结果显示,双敲除菌株 SE-6 产量最高,48 h 血清素达 357.01 mg/L,较 SE-3(217.09 mg/L)提升 64.45%(图 3D)。单敲菌株 SE-4 和 SE-5 在 48 h 的血清素产量分别为 323.49 mg/L 与 232.66 mg/L,较对照 SE-3 分别提高 49.01% 和 7.17%。结果表明,同时阻断色氨酸降解与外排可产生协同效应,最大限度保留可用于转化的前体库。上述敲除未对菌体生长造成负面影响(OD₆₀₀≈15)。
3.4 大肠杆菌褪黑素生物合成途径构建
以高效产血清素菌株 SE-6 为底盘,引入家猪来源的血清素 N - 乙酰转移酶(SNAT)与水稻来源的咖啡酸 O - 甲基转移酶(COMT),构建褪黑素合成途径(图 4A)。经 SDS-PAGE 验证,SNAT(24.3 kDa)与 COMT(40.6 kDa)在大肠杆菌中均实现可溶性表达(图 S5)。
为验证不同质粒组合对褪黑素合成的影响,采用 pETDuet-1 与 pRSFDuet-1 两种相容质粒进行模块组装。
- 策略 A(菌株 MT-1A):血清素模块(Tdc、MBP∗Tph^D300A)置于 pETDuet-1,褪黑素模块(SNAT、COMT)置于 pRSFDuet-1。
- 策略 B(菌株 MT-2B):血清素模块置于 pRSFDuet-1,褪黑素模块置于 pETDuet-1。
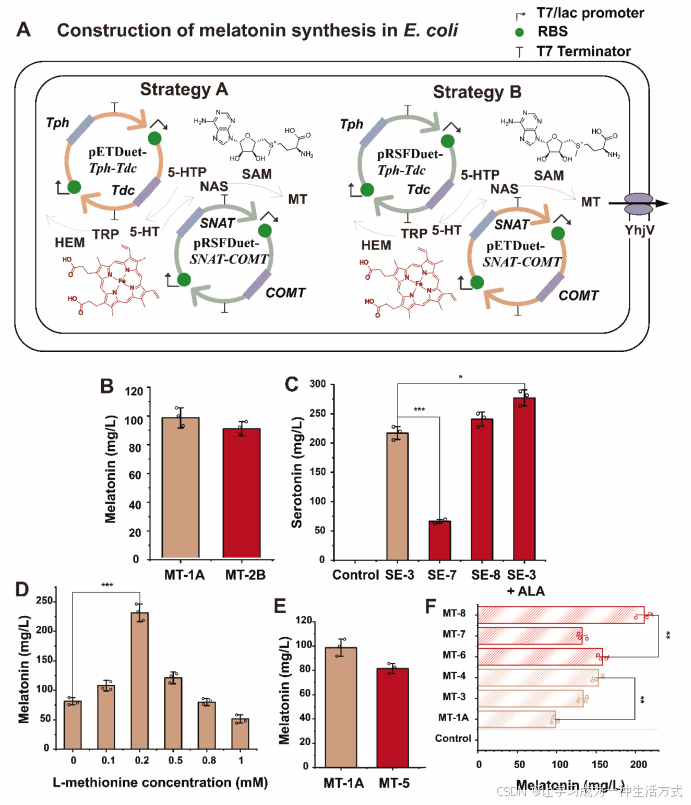
(A)大肠杆菌内褪黑素生物合成途径及两种外源基因导入策略示意图。(B)策略 A 与策略 B 对褪黑素产量的影响。(C)不同血红素强化方式对血清素产量的影响。(D)添加 L - 甲硫氨酸对褪黑素产量的影响。(E)敲除speD 基因对褪黑素产量的影响。(F)不同质粒介导yhjV 过表达对褪黑素产量的影响。RBS:核糖体结合位点;TRP:色氨酸;MT:褪黑素;SAM:S - 腺苷甲硫氨酸;Control:未表达异源蛋白的宿主菌株。
结果显示,基于 C41 (DE3) ΔtnaA 底盘构建的工程菌株 MT-1A 和 MT-2B 均成功合成褪黑素,其 HPLC 特征峰与标准品一致(保留时间:18.41 min,图 S6)。定量分析表明,MT-1A 在 48 h 产量为 98.69 mg/L(图 4B),略高于 MT-2B(91.08 mg/L),但差异未达统计学显著水平(P > 0.05)。这说明现有宿主 - 质粒组合并非限制整体途径通量的主要因素,途径效率更可能受酶动力学或辅因子供给限制。
3.5 辅因子工程强化血清素与褪黑素合成
3.5.1 提升血红素辅因子供给以强化血清素合成
Tph 是血红素依赖型酶,为强化胞内血红素合成与供给,本研究测试了三种策略:(1) 向 SE-3 菌株外源添加血红素合成前体 5 - 氨基乙酰丙酸(ALA,1 mmol/L)与 Fe²⁺;(2) 使用实验室进化获得的高产血红素底盘菌株 SE-HE1 构建 SE-7;(3) 通过内源代谢工程构建平衡型菌株 SE-HE2,强化hemE 表达并敲除降解基因yfeX 。
hemE 编码的尿卟啉原 Ⅲ 脱羧酶(UROD)介导 ALA 至血红素合成途径中,尿卟啉原 Ⅲ 向粪卟啉原 Ⅲ 的转化;而yfeX 已被证实编码血红素降解相关酶。
结果显示,外源添加 ALA 前体可使 SE-3 在 48 h 血清素产量提升至 277.16 mg/L(图 4C)。采用 SE-HE2 底盘的内源平衡策略(菌株 SE-8)使产量提升 10.95%,达到 240.86 mg/L。但血红素过量合成的底盘 SE-HE1(菌株 SE-7)导致产量显著下降(66.27 mg/L)。过量血红素会破坏自身合成途径的反馈抑制,造成代谢负担,尤其是在 HemA 催化步骤。添加 Fe²⁺具有双重作用:既是血红素合成最后一步亚铁螯合酶的底物,也有助于维持血红素处于功能所需的还原状态,防止氧化降解。这表明 Tph 蛋白活性需要充足的血红素供给,但过量积累会造成代谢负担;外源添加 ALA 可在一定程度上补充血红素,在本实验条件下效果优于内源改造。
3.5.2 提升 SAM 辅因子供给以强化褪黑素合成
COMT 催化的甲基化步骤依赖辅因子 SAM。为提高 SAM 可用性,首先外源添加前体 L - 甲硫氨酸。结果表明,外源添加 L - 甲硫氨酸可剂量依赖性提升褪黑素合成。在 0.2 mmol/L 最优浓度下,菌株 MT-1A 在 48 h 产量达 231.44 mg/L,提升 1.83 倍(图 4D)。
此外,敲除 SAM 脱羧酶基因speD 以减少 SAM 消耗,在 MT-1A 中敲除speD 获得 MT-5。但 ΔspeD 突变株产量并未显著提升(81.50 mg/L,图 4E)。我们推测,speD 敲除导致腐胺积累,可能激活其他 SAM 消耗途径(如腐胺甲基化),抵消了 SAM 供给增加的效应。这与早期研究认为敲除speD 可减少 SAM 消耗、进而提升褪黑素合成的结论不同,原因在于 SAM 代谢网络高度复杂,单纯敲除降解途径因全局代谢调控而效果有限。
3.6 转运蛋白工程强化褪黑素合成
为缓解褪黑素胞内积累造成的产物毒性与生长抑制,本研究过表达内源转运蛋白 YhjV 以促进褪黑素外排。YhjV 是一类功能未明确的转运蛋白,后续研究证实其与褪黑素分泌相关。
将yhjV 分别克隆至不同拷贝数的 pCDFDuet-1 与 pACYDuet-1,构建 pCDF-YhjV 和 pACY-YhjV,转入 MT-1A 获得 MT-3 与 MT-4。结果显示,YhjV 高表达显著提升褪黑素产量:48 h 时 MT-3 与 MT-4 分别达到 133.92 mg/L 和 152.80 mg/L,较出发菌株 MT-1A 分别提高 35.70% 和 54.83%(图 4F)。
在此基础上结合前述双敲除背景(ΔtnaA ΔyddG ),菌株 MT-8 的 48 h 褪黑素产量进一步提升至 211.36 mg/L。YhjV 过表达未对菌体生长造成负面影响(OD₆₀₀≈10,图 S7),证实转运蛋白工程可通过减少产物反馈抑制、促进分泌有效提升合成效率。
3.7 发酵罐水平血清素与褪黑素规模化生产
对高产菌株 SE-6 和 MT-8 的摇瓶发酵条件进行系统优化,确定最优参数:诱导温度 30℃,IPTG 浓度 0.8 mmol/L,诱导时间 20--22 h(图 S8--12)。此外,未敲除tnaA 的菌株最适色氨酸添加量为 2.5 mmol/L,敲除菌株则提升至 3.33 mmol/L(图 S13)。培养基由 LB 更换为 TB 以支持高密度培养,并添加 DTT 与抗坏血酸增强酶的氧化稳定性。
在摇瓶参数优化基础上,将菌株 SE-6 与 MT-8 在 MR 培养基中进行分批与补料分批发酵。在添加适量色氨酸、ALA、FeSO₄・7H₂O 与维生素 C 的 MR 培养基中,分批发酵 48 h 后,血清素与褪黑素浓度分别达到 610.74 mg/L 与 316.88 mg/L(图 5A、B)。分批发酵 17--30 h 产量速率下降,可能是关键代谢转换阶段,涉及全局应激响应与代谢流重分配。
为进一步提升产量,采用恒 pH 控制与梯度补料策略实施补料分批发酵。结果显示,血清素与褪黑素浓度持续升高,最终产量分别达到1.97 g/L 与3.40 g/L (图 5C、D)。这是目前大肠杆菌中已报道的最高褪黑素产量 ,证实本研究构建的微生物细胞工厂具备高效、可规模化生产潜力。
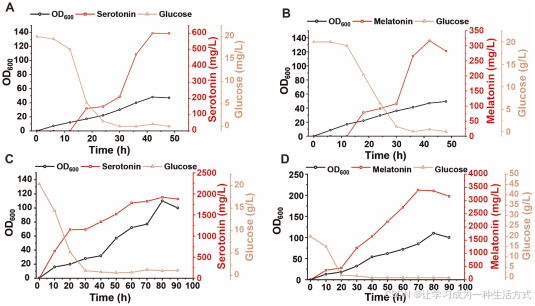
(A)菌株 SE-6 产血清素的分批发酵动态曲线。(B)菌株 MT-8 产褪黑素的分批发酵动态曲线。(C)优化补料条件下 SE-6 产血清素的补料分批发酵动态曲线。(D)优化补料条件下 MT-8 产褪黑素的补料分批发酵动态曲线。
4 结论
综上所述,本研究通过整合代谢工程策略 系统性破解了多个途径瓶颈,成功构建了一套不依赖 BH4 辅因子、可高效合成血清素与褪黑素的大肠杆菌体系。研究结果表明,对整条生物合成途径进行协同优化 ------ 包括前体(色氨酸)供给、辅因子(血红素、SAM)再生、关键酶(Tph)可溶性表达以及产物转运 ------ 是实现高水平合成的关键。
具体而言,本研究:
- 构建了平衡表达系统,优化 Tph、Tdc、SNAT、COMT 四酶级联反应的通量分配;
- 对限速酶色氨酸羟化酶(Tph)进行改造,同时提升其可溶性与催化活性;
- 实施多种辅因子高效再生策略;
- 通过靶向基因敲除消除竞争性代谢途径(tnaA );
- 筛选并利用高效转运蛋白促进产物外排。
在上述综合改造下,补料分批发酵实现了1.92 g/L 血清素 和3.40 g/L 褪黑素 的产量。尽管本研究的补料发酵已获得高滴度,但面向工业化放大仍面临氧气传递、底物利用效率、诱导剂成本等挑战。后续可通过使用廉价碳源、优化补料策略等方式进一步改进。
为更直观体现研究价值,本研究在补充材料中新增了详细对比表(表 S3),从产量、得率、辅因子依赖型等维度与已有文献进行了定量比较。虽然本研究血清素滴度(1.92 g/L)低于已报道的 15.42 g/L,但本体系采用了更简洁的设计思路 :仅通过单点突变 Tph^D300A 即实现不依赖 BH4,大幅降低代谢负担,同时具备平台通用性,并获得了目前大肠杆菌中最高的褪黑素滴度(3.40 g/L) ,更适合构建工业稳健型多产物细胞工厂。
血清素与褪黑素在医药与营养保健品领域应用广泛,在情绪调节、睡眠改善、抗氧化等方面发挥重要作用,凸显了构建高效微生物合成平台的重要意义。本研究建立了可规模化的色氨酸源活性代谢物绿色生物制造平台 ,为其在食品领域的可持续工业化生产与应用奠定了坚实基础。同时,本研究成功应用了新近发现的血红素依赖型羟化酶 ,为构建全细菌来源 的高效生物合成途径开辟了极具潜力的新方向。