Deciphering the galantamine biosynthetic pathway in Lycoris species lays the foundation for plant chassis-based production
解析石蒜属植物中加兰他敏的生物合成途径,为基于植物底盘的合成生产奠定基础

亮点
- 整合多组学技术鉴定了长筒石蒜 中加兰他敏高积累的关键通路基因与发育时期(S1 期)。
- LlNMT1 与LlAKR4 参与加兰他敏生物合成的下游转化步骤。
- 特异细胞色素 P450(LlCYP96T_clone20)对催化效率具有重要作用,其中Ile386 为影响酶功能的关键氨基酸残基。
摘要
加兰他敏是石蒜科中具有重要临床价值的生物碱,广泛用于阿尔茨海默病治疗。目前其植物来源供应受限且不可持续,而学界对石蒜属植物中加兰他敏生物合成机制的了解仍较为有限。本研究以加兰他敏含量极高的长筒石蒜为对象,首次系统解析了其加兰他敏生物合成通路。对高含量的长筒石蒜与低含量的岛屿石蒜进行比较生物碱代谢组分析,结果显示长筒石蒜中加兰他敏积累量约高出 10 倍,尤其在 11 月的 S1 发育阶段,所有前体代谢物均显著富集。结合 PacBio 全长转录组与 Illumina 短读长转录组分析,共鉴定出 83 个差异表达的异喹啉类生物碱合成相关基因,其中 53 个在长筒石蒜中上调表达。进一步通过差异基因--代谢物网络关联分析,并结合本氏烟草瞬时表达体系进行功能验证,鉴定出N - 甲基转移酶 LlNMT1 :该酶与 NtCYP96T6 共表达可将 4'-O - 甲基降球花碱转化为雪花莲碱;同时鉴定出醛酮还原酶 LlAKR4 ,可介导雪花莲碱向加兰他敏的转化。此外,本研究克隆了参与 4'-O - 甲基降球花碱氧化环化的细胞色素 P450 候选基因,分别从长筒石蒜和岛屿石蒜中获得 21 个和 18 个 CYP96T 类序列。经系统发育筛选得到 10 个候选基因,其中仅LlCYP96T_clone20 与 LiCYP96T_clone1 可在共表达 LlAKR4 和 LlNMT1 的烟草中产生与加兰他敏匹配的特征峰,且 LlCYP96T_clone20 的催化信号强度高出约 2.89 倍。对上述 10 个 CYP96T 类蛋白进行结构模拟后进一步发现,靠近血红素辅因子的保守残基Ile386 对催化效率具有关键作用。综上,本研究不仅阐明了石蒜属中从 4'-O - 甲基降球花碱到加兰他敏的下游生物合成途径,也为在工程化植物底盘中实现异源合成、推动其临床与工业化应用奠定了坚实的分子基础。
引言
石蒜属(Lycoris )植物隶属于石蒜亚科,以其独特的花部形态及在东亚悠久的药用历史而闻名(Cahlíková 等,2020)。作为鳞茎类地下芽植物,石蒜属物种不仅对环境波动具有出色的适应性,还能在地下器官中积累种类丰富的次生代谢产物。其中,** 石蒜科生物碱(Amaryllidaceae alkaloids, AmAs)** 是一类结构多样且具有重要药理活性的异喹啉生物碱(Martin,1987;He 等,2015;Desgagné-Penix,2021)。这类化合物具有抗病毒、抗肿瘤、神经保护及抗炎等广泛的生物活性,是药物研发的重要资源(Omoruyi 等,2021;Jayawardena 等,2024;Nair & van Staden,2024;Tallini 等,2024)。
加兰他敏 是最具临床应用价值的石蒜科生物碱之一,属于苯并呋喃并苯并氮卓类生物碱,可作为可逆性乙酰胆碱酯酶抑制剂(Woodruff-Pak 等,2001)。加兰他敏已被批准用于阿尔茨海默病的治疗,也是美国 FDA 认证的少数可有效改善认知症状的药物之一(Tan 等,2014)。目前,加兰他敏的工业化生产仍高度依赖从雪花莲属、雪滴花属、水仙属及石蒜属等天然植物中提取(Heinrich & Teoh,2004;Tsvetkova 等,2013),原因在于其全化学合成效率低下,且微生物合成途径仍面临诸多技术挑战(Santos 等,2020;Kaur 等,2022;Zhang 等,2022;Gao 等,2023)。然而,天然植株中加兰他敏含量普遍较低,且多种来源植物已被列入世界自然保护联盟(IUCN)濒危物种红色名录。这些局限促使研究者不断致力于解析加兰他敏的生物合成途径,并在异源体系中实现其人工重建。
前期研究通过放射性同位素标记、饲喂实验以及在烟草与酵母中的异源表达,为解析加兰他敏生物合成途径奠定了坚实基础(图 1A)(Mehta 等,2024)。加兰他敏及其他石蒜科生物碱的生物合成起始于初级代谢前体 ------ 苯丙氨酸和酪氨酸。苯丙氨酸在苯丙氨酸解氨酶(PAL)催化下生成反式肉桂酸,随后经肉桂酸 - 4 - 羟化酶(C4H)在对位羟基化形成对香豆酸,再经间位羟基化生成咖啡酸;或通过对羟基苯甲醛转化为 3,4 - 二羟基苯甲醛(Suhadolnik 等,1963;Li 等,2018)。酪氨酸首先在酪氨酸脱羧酶(TYDC)催化下脱羧生成酪胺,该酶是生物碱合成途径中的保守酶(Lehmann & Pollmann,2009;Wang 等,2019)。上述两个中间体 ------3,4 - 二羟基苯甲醛与酪胺经希夫碱缩合并进一步还原,生成降球花碱(norbelladine) (Singh 等,2018;Majhi 等,2023)。降球花碱是合成各类石蒜科生物碱的关键核心中间体。下一步,在降球花碱 4'-O - 甲基转移酶(NOMT)催化下,其 4' 位发生 O - 甲基化,生成4'-O - 甲基降球花碱(4OMN) 。尽管该酶活性早在 20 世纪 60 年代便在Narcissus bowdenii 粗酶液中被检测到,但直至近年才通过大肠杆菌异源表达完成生化功能鉴定,证实其具有阳离子依赖性与位点选择性(Kilgore 等,2014)。
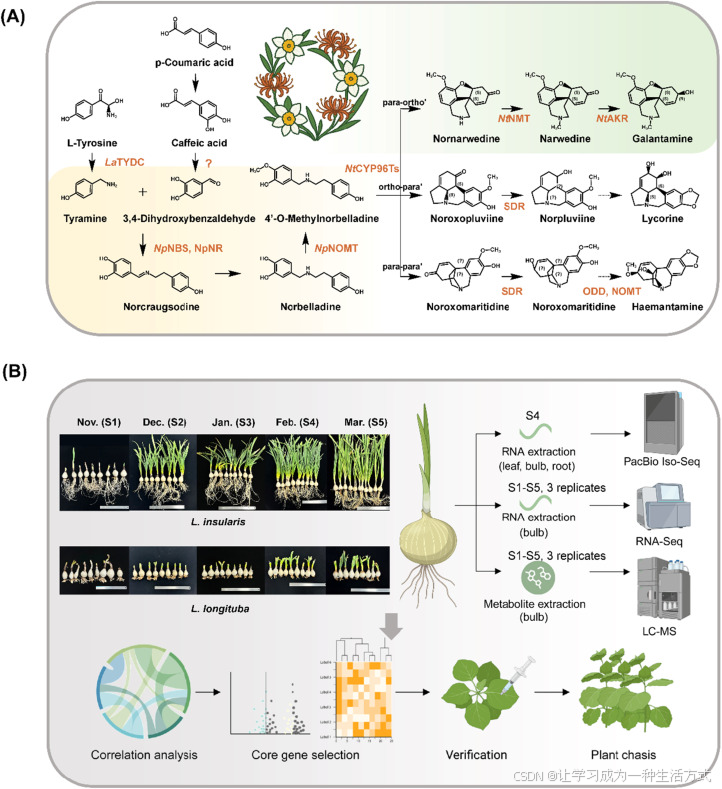
图 1 解析石蒜属与水仙属植物中加兰他敏生物合成途径的整合研究策略
(A)推测的加兰他敏生物合成途径以酪胺和 3,4 - 二羟基苯甲醛为起始,二者在 NBS/NR 催化下缩合生成去甲克绕戈定 。该中间体进一步转化为降球花碱,随后经 NOMT 催化发生 O - 甲基化,并在 CYP96T 同源蛋白介导下发生位点选择性酚类氧化偶联,形成不同的生物碱骨架。随后在 NMT 与 AKR 家族酶的催化下经连续还原反应生成加兰他敏。羟基化、去甲基化等后续修饰(如 SDR、ODD 家族酶催化)进一步丰富了生物碱骨架的多样性。(B)采用代谢组与转录组联合分析策略研究石蒜属植物中加兰他敏的生物合成。于 2023 年 11--12 月及 2024 年 1--3 月设置 5 个时间点(S1--S5),分别采集长筒石蒜与岛屿石蒜不同发育时期的鳞茎样品,开展转录组与代谢组分析。同步进行短读长 RNA 测序、长读长全长转录组测序及液相色谱 - 质谱代谢谱检测。通过表达量 - 代谢物关联分析筛选核心合成候选基因,结合聚类分析排序后在烟草中进行功能验证,为基于植物底盘的合成生产奠定基础。
该生物合成途径后续以 4'-O - 甲基降球花碱(4OMN)为底物,在细胞色素 P450 酶催化下发生酚类氧化偶联而分支。** 对位 - 对位'(p-p')、邻位 - 对位'(o-p')、对位 - 邻位'(p-o')** 三种不同偶联方式分别决定了血球胺碱、石蒜碱、加兰他敏等产物的核心骨架结构(Martin,1987)。在加兰他敏合成途径中,对位 - 邻位'偶联生成 N - 去甲基雪花莲碱,再经连续甲基化形成加兰他敏。上述酚类偶联反应的位点选择性与催化机制表明,细胞色素 P450 酶在生物碱结构多样化过程中发挥核心作用。已知 P450 酶可在植物与哺乳动物系统中催化 C-C 偶联、C-O 偶联、羟基化、氧化重排等多种反应。已有研究揭示 CYP719A1、CYP80G2、CYP121 等参与 C-C 型酚类偶联反应(Hansen 等,2021;Schnabel 等,2021;Hao 等,2024);而在水仙属植物中,该反应由 CYP96 家族成员 NtCYP96T6 催化(Mehta 等,2024)。但石蒜属中负责该步骤的酶系统尚未被鉴定,该属是否存在 CYP96T 家族直系同源蛋白或功能分化的同源蛋白仍不明确。
本研究聚焦长筒石蒜的生物合成潜能,该物种加兰他敏含量显著高于同属的岛屿石蒜(图 1B)。基于转录组数据与代谢谱分析,我们鉴定到一个候选 N - 甲基转移酶 LlNMT1,该酶与 NtCYP96T6 共表达可催化 4OMN 生成雪花莲碱,即加兰他敏合成途径中的关键中间体。通过本氏烟草瞬时表达系统进行功能验证,证实了其催化活性。同时,通过共表达分析鉴定到醛酮还原酶 LlAKR4,可将雪花莲碱转化为加兰他敏,完成该途径的最终还原步骤。随后我们筛选到多个 CYP96T 同源基因作为 4OMN 氧化偶联的候选基因。为探究其功能,我们在异源体系中克隆并表达了代表性 CYP96T 类基因,并通过体内酶活实验评估其催化效率。本研究为解析石蒜科生物碱的酶学多样化机制提供了新见解,也为利用可持续生物来源生产加兰他敏奠定了基础。
结果
长筒石蒜中高积累加兰他敏及其生物合成前体
为解析不同石蒜属植物中石蒜科生物碱的积累水平,选取岛屿石蒜(低加兰他敏含量)与长筒石蒜(高加兰他敏含量)(Li 等,2020)的鳞茎进行生物碱代谢组分析。根据石蒜属物候特性,于 2023 年 11--12 月及 2024 年 1--3 月设置 5 个时间点采集鳞茎样品(S1--S5)。岛屿石蒜于 12 月展叶,1--2 月进入旺盛生长期;长筒石蒜则至 1 月仍处于休眠状态,2--3 月才萌发叶片。采样覆盖休眠期与旺盛生长期,可代表不同发育阶段的代谢特征。
为明确长筒石蒜与岛屿石蒜不同发育时期加兰他敏及其合成前体的积累规律,我们采用超高效液相色谱 - 串联质谱(UPLC-MS/MS)平台共鉴定出 266 个生物碱代谢物(附表 1)。两种石蒜间加兰他敏含量存在极显著差异(图 2A)。在整个生长期内,长筒石蒜鳞茎中加兰他敏含量约为岛屿石蒜的 10 倍。此外,加兰他敏前体去甲雪花莲碱 的积累模式与加兰他敏高度一致。值得注意的是,8 - 去甲基海风酮(去甲海风酮)在前期研究中被认为是去甲雪花莲碱合成的竞争性底物,其在长筒石蒜不同生长期的积累模式与去甲雪花莲碱完全相反。
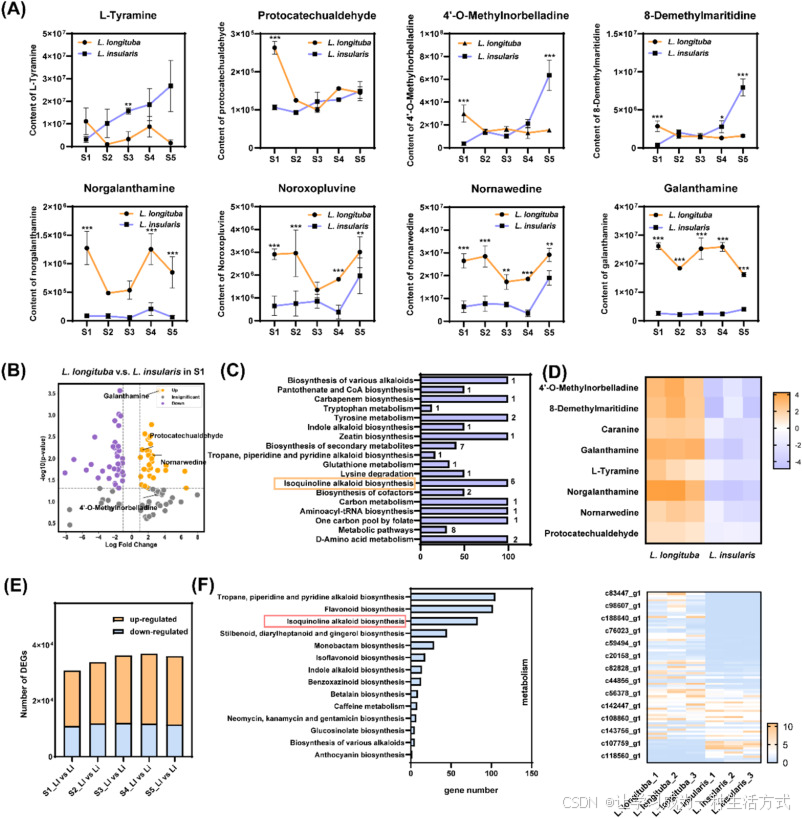
图 2 长筒石蒜与岛屿石蒜不同生长期的代谢组与转录组分析
(A)异喹啉生物碱生物合成途径相关代谢物在不同生长期的分布模式。星号表示差异显著(t 检验,n=3)。*p<0.1,**p<0.05,***p<0.01。数据以平均值 ± 标准差表示。(B)S1 时期长筒石蒜与岛屿石蒜差异代谢物火山图。每个点代表一个代谢物:紫色为下调差异代谢物,橙色为上调差异代谢物,灰色为无显著差异代谢物。横轴为两组间相对代谢物丰度的 log2 倍数变化(log2FC),绝对值越大表示丰度差异越大。代谢物筛选标准为变量投影重要度(VIP)+ 倍数变化(FC)+p 值。纵轴为差异显著性水平(-log10 p 值),点的大小反映 VIP 值。(C)(D)S1 时期长筒石蒜与岛屿石蒜异喹啉生物碱生物合成途径差异代谢物的 KEGG 富集与聚类分析。(E)长筒石蒜与岛屿石蒜不同生长期差异表达基因(DEGs)数量统计。(F)S1 时期长筒石蒜与岛屿石蒜异喹啉生物碱生物合成途径差异表达基因的 KEGG 富集与聚类分析,展示通路特异性富集与表达模式。
为进一步解析两种石蒜生物碱代谢物的差异,对各生长期进行差异代谢物分析。结果显示,从 S1 到 S5 分别鉴定出 103、89、94、89 和 115 个差异代谢物(图 2B,附图 1A)。其中 48 个代谢物在全部五组中均存在显著差异,包括加兰他敏及其生物合成前体去甲雪花莲碱。对各时期差异代谢物的 KEGG 通路分析表明,S1 时期富集到 ** 异喹啉生物碱生物合成途径(ko00950)** 的差异代谢物数量最多(图 2C,附图 1B),包括 8 - 去甲基海风酮(去甲海风酮)、小檗碱、卡腊宁、加兰他敏、L - 酪胺和原儿茶醛(3,4 - 二羟基苯甲醛)。此外,虽未归入 ko00950 但属于加兰他敏合成途径的去甲雪花莲碱也被检出。上述差异代谢物在 S1 时期的长筒石蒜中均显著上调(图 2D)。总体而言,这些结果清晰地显示加兰他敏合成途径中特定代谢物呈时期特异性富集,为解析物种特异性代谢差异提供了基础。
长筒石蒜中异喹啉生物碱合成基因显著富集并转录激活
由于石蒜属基因组尚未测序组装,本研究对 S5 时期采集的根、茎、叶样品进行了全长转录组测序,作为转录组分析的参考序列。长筒石蒜全长转录组共获得 196,596 条序列,最长转录本 9,046 bp,平均长度 2,030 bp(附表 2,附图 2A),转录本 GC 含量为 39.89%。在 S1--S5 时期,我们比较两种石蒜的差异表达基因,将原始测序数据归一化为 FPKM 值,以消除基因长度与测序深度对表达定量的影响。统计分析共检测到 363,834 条转录本(平均长度 768 bp),192,260 个独立组装基因(平均长度 1,009 bp)。差异表达分析显示,从 S1 到 S5 分别鉴定出 30,899、33,904、36,297、36,940 和 36,069 个差异表达基因(图 2E),其中 10,236 个基因在全部五组中均差异显著(附图 2B)。
对差异表达基因的 KEGG 富集分析显示,S1 时期有83 个基因富集于异喹啉生物碱生物合成途径 (图 2F,附图 2E),其中 53 个上调、30 个下调。综合代谢组与转录组结果一致表明:S1 是长筒石蒜与岛屿石蒜鳞茎中加兰他敏及其前体差异积累最关键的时期 。因此,本研究对 S1 时期的代谢组与转录组开展关联分析,以挖掘长筒石蒜中加兰他敏的生物合成基因。
LlNMT1 是催化雪花莲碱生成的关键 N - 甲基转移酶
为进一步挖掘长筒石蒜与岛屿石蒜加兰他敏合成途径的关键差异基因,本研究构建了基因共表达网络。对 S1 时期石蒜的生物碱代谢组与转录组数据进行加权基因共表达网络分析(WGCNA)。聚类分析首先将 6 个样品分为两个明显的簇(附图 3A),表明两种石蒜的基因表达模式存在显著差异。对软阈值功率 1--20 进行网络拓扑分析,确定了兼顾无标度特性与平均连通性的最优参数,选取阈值为 18,最终将 30,899 个基因聚类为 30 个模块,最大模块含 15,299 个基因,最小模块仅 5 个基因(附图 3B、3C)。与其他模块相比,青绿色模块与蓝色模块和加兰他敏含量高度相关 :青绿色模块呈正相关,蓝色模块呈负相关(附图 3D、E),提示青绿色模块可能在加兰他敏积累中发挥重要作用。因此将青绿色与蓝色模块确定为与加兰他敏含量最相关的核心模块。
为明确上述模块是否包含加兰他敏合成相关基因,分别对青绿色模块(15,299 个基因)与蓝色模块(9,253 个基因)内所有基因与加兰他敏含量进行关联分析,分别获得 3,495 和 1,710 个与加兰他敏共表达的基因(附表 3)。考虑到 4'-O - 甲基降球花碱(4OMN)向雪花莲碱的转化涉及氧化环化与 N - 甲基化,我们首先在共表达基因集中筛选甲基转移酶候选基因。结果发现多个与加兰他敏共表达的甲基转移酶,包括生育酚 O - 甲基转移酶、DNA 甲基转移酶、MPBQ/MSBQ 甲基转移酶、组蛋白 H3- 赖氨酸 9 N - 三甲基转移酶以及腺苷甲硫氨酸依赖型 rRNA 甲基转移酶等(附表 3)。
为进一步缩小石蒜属 N - 甲基转移酶(LlNMT)候选范围,对注释为生育酚 O - 甲基转移酶的基因进行系统发育分析。其中LlNMT1 与 LlNMT4 和已功能验证的水仙属 NMT1(NtNMT1)序列相似性最高 (图 3A)。两个基因在长筒石蒜中均显著上调,且 LlNMT1 富集程度最为突出(图 3B)。因此,选取 LlNMT1 与 LlNMT4 作为 N - 甲基转移酶候选基因,与已功能验证的合成途径 P450 酶 NtCYP96T6 在本氏烟草中进行瞬时共表达验证(图 3C)。外源饲喂 4OMN 底物后,三组表达组合均出现代谢响应,但只有 LlNMT1 组在 2.14 min 处产生雪花莲碱特征峰 ,说明在 NtCYP96T6 共表达条件下,LlNMT1 可催化 N - 甲基化生成雪花莲碱。综上,LlNMT1 被鉴定为石蒜属中参与加兰他敏前体合成的关键 N - 甲基转移酶(图 3C)。
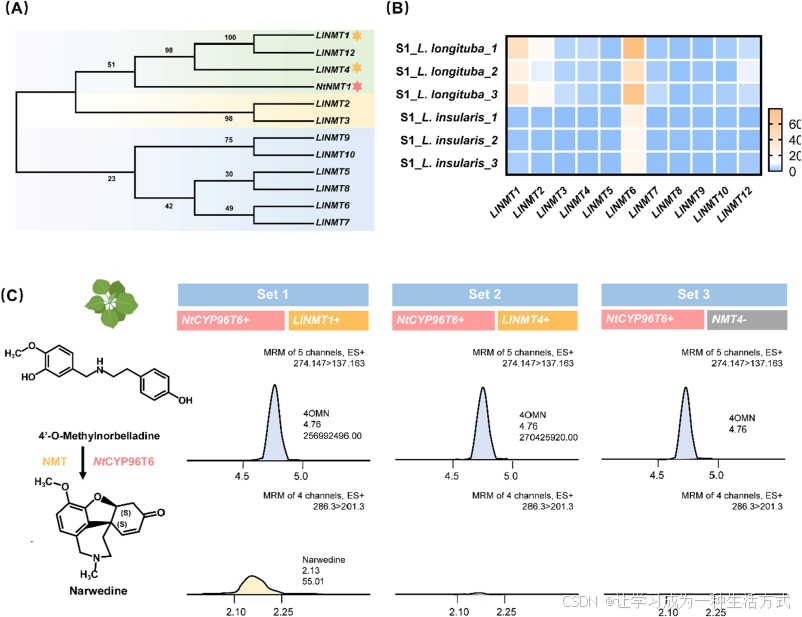
图 3 长筒石蒜与岛屿石蒜中 N - 甲基转移酶(NMT)候选基因的鉴定
(A)系统发育分析,筛选与水仙 NtNMT1 亲缘关系近的候选基因;(B)11 个 NMT 候选基因在长筒石蒜与岛屿石蒜中的表达富集谱;(C)在本氏烟草中将 LlNMT1、LlNMT4 分别与 NtCYP96T6 瞬时共表达,进行功能验证。饲喂 4OMN 底物后,对叶片进行提取并开展 LC-MS 分析。组合 1--3 分别为:组合 1,NtCYP96T6 + LlNMT1;组合 2,NtCYP96T6 + LlNMT4;组合 3,仅 NtCYP96T6。色谱图横轴为保留时间。
LlAKR4 作为醛酮还原酶,催化雪花莲碱向加兰他敏转化
雪花莲碱向加兰他敏的转化涉及醛基还原为羟基的步骤,因此我们进一步分析了加兰他敏相关基因与 NAD (P) 结合型 Rossmann 折叠蛋白家族成员的共表达关系。分析结果显示,多个醛酮还原酶(AKR)家族基因 为潜在候选基因(图 4A)。为进一步筛选具有功能相关性的候选基因,我们将石蒜 AKR 基因与已功能验证的水仙加兰他敏合成基因 NtAKR1 进行系统发育比较。在石蒜候选基因中,LlAKR4 与 LlAKR24 和 NtAKR1 序列相似性最高 (图 4B)。随后选取这两个基因进行克隆与功能验证。
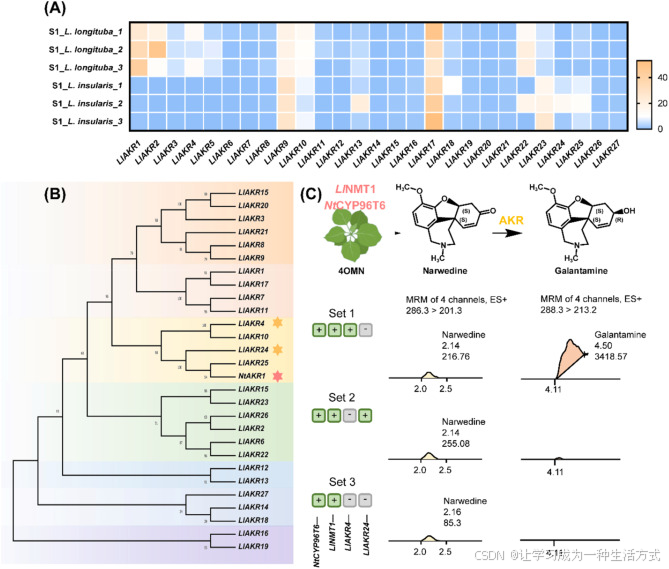
图 4 长筒石蒜与岛屿石蒜中 AKR 候选基因的鉴定
(A)27 个 AKR 候选基因在长筒石蒜与岛屿石蒜中的表达富集谱;(B)系统发育分析,筛选与水仙 NtAKR1 亲缘关系较近的候选基因;(C)在本氏烟草中将 LlAKR4、LlAKR24 分别与 NtCYP96T6 和 LlNMT1 瞬时共表达,进行功能验证。饲喂 4OMN 底物后提取叶片并进行 LC-MS 分析。三组实验分别为:组合 1,NtCYP96T6 + LlNMT1 + LlAKR4;组合 2,NtCYP96T6 + LlNMT1 + LlAKR24;组合 3,NtCYP96T6 + LlNMT1。色谱图横轴为保留时间。
将每个 AKR 候选基因与 LlNMT1 和 NtCYP96T6 在本氏烟草中瞬时共表达。代谢谱结果显示,三组均成功合成雪花莲碱。值得注意的是,组合 1 可进一步将雪花莲碱转化为加兰他敏 ,证实其具有醛还原酶活性(图 4C)。基于两种酶在加兰他敏积累水平上的差异,选取LlAKR4 用于后续石蒜 CYP96T 家族基因的筛选。
鉴定出两个石蒜 CYP96T 家族成员
为加兰他敏生物合成中氧化偶联步骤的关键催化酶
为探究在加兰他敏合成限速步骤 ------ 氧化偶联反应中,长筒石蒜与岛屿石蒜 CYP96T 酶的功能分化,本研究首先从两个物种中分别扩增 CYP96T 基因家族成员。基于长筒石蒜的 21 个 CYP96T 克隆、岛屿石蒜的 18 个 CYP96T 克隆,以及参考序列(NtCYP96T1、NtCYP96T5、NtCYP96T6、NtCYP96T8、LrCYP96T、NpCYP96T1、NpCYP96T2、NpCYP96T3、NpCYP96T5)开展系统发育分析,这些序列氨基酸一致性约为 84.88%(图 5A)。
从不同进化分支选取 10 个代表性克隆进行后续研究:长筒石蒜的 LlCYP96T_clone1、8、12、14、20,以及岛屿石蒜的 LiCYP96T_clone1、5、13、16、17,同时纳入已功能验证的 NtCYP96T1 和 NtCYP96T6 作为对照(图 5A)。对预测氨基酸序列的多序列比对显示,在细胞色素 P450 经典的 6 个底物识别位点(SRSs)内存在明显的氨基酸残基变异(附图 4)。SRS 结构域的差异提示石蒜 CYP96T 同源蛋白间可能存在功能分化,这或许是两个物种加兰他敏合成能力差异的分子基础。
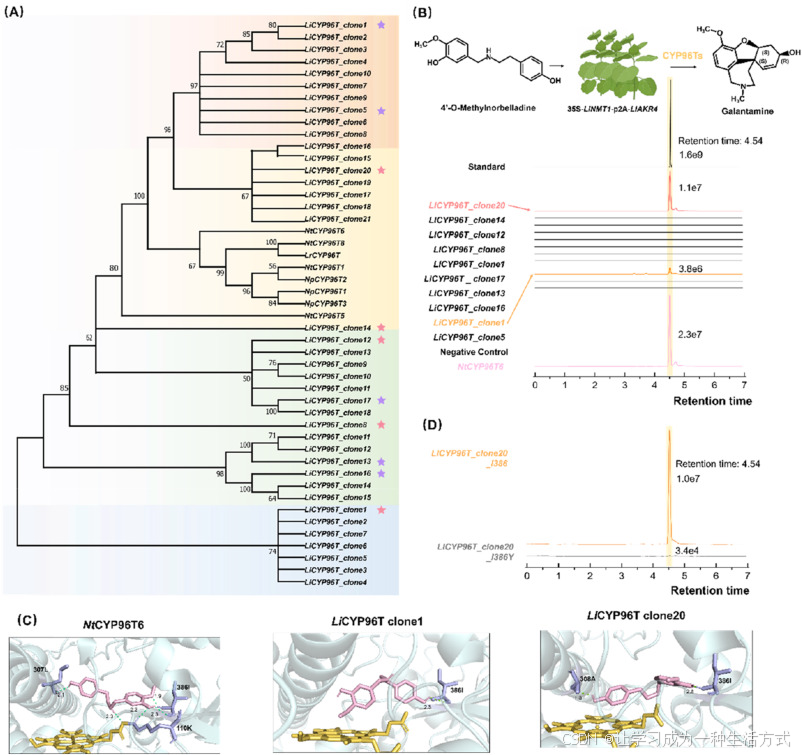
图 5 石蒜属 CYP96T 家族候选基因的系统发育与功能鉴定
(A)从长筒石蒜(LlCYP96T 克隆)与岛屿石蒜(LiCYP96T 克隆)克隆得到的 CYP96T 同源蛋白,与水仙参考 CYP96T 序列(NtCYP96T)构建的最大似然法系统发育树。末端节点标注克隆名称,主要分支以阴影区分以便观察;关键节点显示自举检验值(≥50)。星号标记用于功能验证的克隆。(B)在稳定表达 35S-LlNMT1-p2A-LlAKR4 的烟草叶片中瞬时表达各 CYP96T 基因,进行功能验证。饲喂 4OMN 底物后提取叶片并进行 LC-MS 分析。LC-MS 提取离子流图(EIC)展示了加兰他敏标准品、阴性对照、阳性对照 NtCYP96T6 及多个 CYP96T 候选克隆的结果。曲线叠加并纵向偏移以便区分。在 NtCYP96T6(阳性对照)、LiCYP96T_clone1 和 LlCYP96T_clone20 样品中,在 4.54 min 处(灰色竖条标记)出现与加兰他敏标准品保留时间一致的特征峰。(C)代表性 CYP96T 同源蛋白模型与 4OMN 的预测结合模式。三幅局部放大图分别显示 4OMN(粉色棍状模型)在(左)LlCYP96T_clone20、(中)LiCYP96T_clone1、(右)NtCYP96T6 活性中心内得分最高的对接构象。血红素辅基以黄色棍状 / 表面模型展示,以凸显底物与催化铁中心的相对位置。构成底物结合口袋并在文中讨论的关键蛋白侧链以青色棍状模型显示并标注。(D)野生型 LlCYP96T_clone20(I386)与 I386Y 突变体在 4.54 min 处产物生成的 LC-MS 色谱图。与野生型相比,I386Y 突变使峰强度显著降低,表明催化活性大幅下降。
为验证克隆得到的石蒜 CYP96T 家族基因的催化功能,我们首先构建了共表达 LlNMT1 与 LlAKR4 的转基因烟草株系(35S::LlAKR4-p2A-LlNMT1)。不同株系表达量存在差异,其中株系 1 和 3 的 LlNMT1 与 LlAKR4 转录水平显著更高,被进一步用于石蒜 CYP96T 的功能验证(附图 5A)。在 35S::LlAKR4-p2A-LlNMT1 植株叶片中瞬时表达 CYP96T 候选基因后,阳性对照 NtCYP96T6、LlCYP96T_clone20 和 LiCYP96T_clone1 样品均在 4.54 min 处出现与加兰他敏标准品一致的特征峰,其中 LlCYP96T_clone20 的信号强度约为 LiCYP96T_clone1 的 2.89 倍(图 5B)。所有被测 CYP96T 克隆的相对表达量相近,无显著差异(附图 5B)。此外,体外酶活实验表明,在 LlNMT1 与 LlAKR4 存在下,LlCYP96T_clone20 和 LiCYP96T_clone1 可催化 4OMN 转化为加兰他敏,与其在多步催化级联反应中的功能一致(附图 5C)。上述结果证明,LlCYP96T_clone20 与 LiCYP96T_clone1 分别是长筒石蒜和岛屿石蒜中,催化加兰他敏合成氧化偶联步骤的关键 CYP96T 酶 。LlCYP96T_clone20 更高的催化效率,可能是长筒石蒜加兰他敏积累量更高的部分原因。
为探究石蒜 CYP96T 酶的关键催化残基,我们利用 AlphaFold3 预测了 LlCYP96T_clone20、LiCYP96T_clone1、NtCYP96T6 及其他 CYP96T 同源蛋白与血红素辅基的复合物模型,并与 4OMN 进行分子对接。结果显示,LlCYP96T_clone20、LiCYP96T_clone1 和 NtCYP96T6 在 386 位具有完全相同的活性残基(异亮氨酸 Ile386)(图 5C),而其他克隆不具备这一特征(附图 5D)。该残基位于底物识别位点 5(SRS5),且靠近血红素辅基。4OMN 与各蛋白的结合能分别为:LlCYP96T_clone20 −7.68 kcal/mol、LiCYP96T_clone1 −7.59 kcal/mol、NtCYP96T6 −7.78 kcal/mol。尽管 LiCYP96T_clone1 也含有保守的 Ile386 并具有催化活性,但 LlCYP96T_clone20 整体底物识别位点构象与底物定位更优,与血红素作用更强、底物结合更稳定,因此催化效率更高。此外,我们对 386 位残基进行定点突变(I386Y)以评估其对酶功能的贡献。突变体酶的催化活性较野生型显著降低(图 5D),表明 386 位残基对催化效率至关重要。以上结果提示,保守的 Ile386 及其局部微环境可能影响血红素结合位点与酶的催化效率。
讨论
多组学整合加速解析植物特异代谢物生物合成途径
植物特异代谢是生化进化的顶峰,支撑了极为丰富的化学多样性,使固着生长的植物能够与环境动态互作。与保守且对生长生存必需的初生代谢不同,特异代谢具有支系特异性扩张和极强的催化创新能力(Moore et al. 2014; Weng et al. 2021)。通过适应性进化,植物招募了多样的酶家族,尤其是细胞色素 P450 单加氧酶(CYP)、甲基转移酶和氧化还原酶,生成结构多样、兼具生态与药理功能的天然产物(Bennett and Wallsgrove 1994; Ono and Murata 2023; An et al. 2024)。这些代谢物作为防御物质、引诱剂或信号分子,决定植物的生态适应性(Stevenson et al. 2017; Kato-Noguchi and Kato 2023; Upadhyay et al. 2025)。其中,石蒜科生物碱(AmAs)是结构与功能多样性最突出的家族之一,加兰他敏、石蒜碱、血球胺碱等化合物具有强效神经保护与细胞毒活性(Desgagné-Penix 2021)。解析其生物合成过程,不仅能揭示植物扩展化学库的进化策略,也为在异源系统中利用这些途径、开展合成生物学研究,以及理性代谢工程实现药理活性物质可持续生产奠定基础。
核苷酸序列数据的爆发式增长与前沿分析技术的普及,使得利用计算框架定位植物特有基因与代谢通路成为可能(Fan et al. 2025)。与诱导处理方法相比,基于物种间或组织间自然差异的比较分析可最大限度减少非特异性胁迫响应或代谢重编程等干扰因素(Wang et al. 2018; Chowdhury et al. 2022; Xu and Fu 2022),从而更真实地反映体内生物合成的生理调控状态(Zhai et al. 2025)。通过多组学整合关联分析,已系统挖掘出黄酮类(Peng et al. 2024)、萜类(Mai et al. 2025; Wang et al. 2025)和生物碱(Xu et al. 2024)合成途径的关键酶。对水仙不同器官的多组学分析已阐明单子叶植物中石蒜科生物碱的合成途径;而由共同前体 4'-O - 甲基降球花碱(4OMN)衍生出的高度结构多样性,也体现了氧化偶联与后续修饰反应如何推动该支系化学新颖性的进化,凸显了酶特异性、催化创新与代谢网络组织间的精细互作(Mehta et al. 2024)。
然而,石蒜属完整基因组测序与组装的缺失,限制了加兰他敏合成途径的解析。本研究对石蒜进行了全长转录组测序,为通路相关基因的克隆与功能鉴定提供了宝贵资源。通过代谢组与转录组联合分析,系统鉴定了长筒石蒜与岛屿石蒜中参与石蒜科生物碱合成的关键酶。我们发现 N - 甲基转移酶(NMT)和醛酮还原酶(AKR)具有显著差异的表达模式,并与中间产物及终产物丰度高度相关,证明这些酶家族是决定物种间加兰他敏积累差异的核心因子(图 2E)。对合成酶的功能验证不仅填补了石蒜属加兰他敏下游合成途径的空白,也为后续代谢工程提供了可用的功能元件。
CYP96T 介导的氧化偶联:功能与机制解析
细胞色素 P450 单加氧酶(CYP)通过位点选择性酚类氧化偶联,决定代谢物结构多样性(Liyanage et al. 2025),正是其底物选择性造就了产物的高度多样化(Hansen et al. 2021; Hu et al. 2023)。例如,罂粟中 CYP719B1 与千金藤属 CYP80G10 催化的吗啡合成酚类偶联步骤,虽均生成吗啡烷型生物碱,但底物立体构型不同(R- vs S - 网状番荔枝碱),反映了独立的进化起源(An et al. 2024)。此外,CYP 基因的复制与新功能化,为特异代谢产物多样化提供了酶学基础(Liu et al. 2025; Qiu et al. 2025)。在水仙中,近缘 CYP 旁系同源基因的功能特化形成了不同的氧化偶联模式,进而促进石蒜科生物碱结构多样化。在本氏烟草中的瞬时表达实验表明,忽地笑 CYP96T 同源蛋白中的 Ile123、Leu124 等残基影响 4OMN 氧化偶联的位点选择性(对位 - 对位' vs 对位 - 邻位')(Liu et al. 2024)。对位点选择性关键位点的反向定点突变显示,将 CYP96T1 第 308 位丙氨酸替换为 NtCYP96T6 对应的亮氨酸,可使 CYP96T1 获得类似 NtCYP96T6 的对位 - 邻位'偶联催化能力(Mehta et al. 2024)。但综合综述指出,尽管 CYP96T 家族是石蒜科生物碱结构多样化的核心,但其位点特异性功能机制仍缺乏系统解析(Jayawardena et al. 2024; Liyanage et al. 2025)。
通过对 10 个候选基因的酶学验证与分子对接分析,我们鉴定出石蒜 CYP96T 同源蛋白中的Ile386 是影响催化活性的关键功能位点 。这一发现拓展了已知的 CYP96T 功能残基位点(如 Ile123/Leu124、Leu308),这些位点均位于底物结合口袋内部或附近,参与 4OMN 的位点选择性酚类氧化偶联。已有研究表明,LaCYP96T1、LaCYP96T2 等 CYP96T 亚型可催化多种 C-C 酚类偶联方式(p-o'、p-p'、o-p'),位点选择性由活性中心结构的细微差异决定。结构分析显示,Phe124、Val307 等残基影响底物相对于血红素铁 - 氧中心的取向,从而决定偶联产物类型(Lamichhane et al. 2025)。与这些靠近口袋的决定位点不同,Ile386 位于催化血红素远端,提示其以更间接的方式调控催化。越来越多证据表明,P450 家族中远端残基可通过重塑底物进出通道(Meng et al. 2021; Spanke et al. 2025)、稳定利于底物结合的构象状态(Verras et al. 2006),或影响 I - 螺旋、BC 环、FG 环等调控底物定位的结构元件动态,进而调控催化效率(Basudhar et al. 2015; Benkaidali et al. 2019)。我们的突变结果支持这一机制:386 位突变显著改变催化效率,符合对氧化偶联的变构或构象调控效应。总体而言,将 Ile386 位点与已有位点整合,并结合当前 CYP96T 调控机制的研究空白,本研究在分子机制上对 CYP96T1 及其在石蒜科生物碱合成中的作用提供了重要进展。
向加兰他敏途径的从头重建与优化迈进
异源重建已成为解析复杂植物特异代谢途径、实现高价值天然产物可持续生产的重要策略(Li et al. 2023; Seshadri et al. 2025)。通过在微生物或植物宿主中功能重建合成酶,既可解析酶促机制,也可建立规模化生产体系。近期研究已成功重建多种代谢物的完整或部分合成途径,包括单萜吲哚生物碱(Stander et al. 2023)、苄基异喹啉生物碱(Tian et al. 2024)和紫杉醇(Liang et al. 2025),产量与稳定性较天然来源显著提升。在此基础上,本研究功能验证了从 4OMN 到加兰他敏各步骤的关键酶:4OMN →(LlCYP96T_clone20 氧化偶联、LlNMT1 N - 甲基化)→ 雪花莲碱 →(LlAKR4 醛酮还原)→ 加兰他敏 。我们构建了稳定共表达 LlNMT1 与 LlAKR4 的烟草株系,为评估 CYP96T 同源蛋白提供了均一、可靠的平台,减少了农杆菌混合瞬时侵染带来的表达波动与信号干扰,也为后续在植物体内完整重建加兰他敏途径奠定了关键基础。
目前,异源系统中加兰他敏合成仍依赖外源添加 4OMN,主要原因是从咖啡酸到 3,4 - 二羟基苯甲醛(3,4-DHBA)的上游酶促转化机制尚未解析(Liyanage et al. 2025)。因此,未来工作将聚焦于鉴定并表征该步骤的关键酶,以实现从初生代谢物开始的加兰他敏从头合成。同时,结构分析表明 CYP96T 酶的活性中心构象可能对催化效率起重要作用。针对这些位点的定向进化与理性突变,有望进一步提升催化效率与特异性,最终在植物底盘或微生物平台实现高效、可控的加兰他敏生物合成。
材料与方法
植物材料
长筒石蒜(L. longituba )与岛屿石蒜(L. insularis )样品采自浙江省农业科学院园林植物与花卉研究所苗圃。生长期 S1--S5 为当年 11 月至次年 3 月的五个连续物候阶段。岛屿石蒜:S1(11 月)为花后休眠初期;S2(12 月)休眠解除、开始萌芽;S3(1 月)活跃萌芽与营养生长初期;S4(2 月)营养生长快速期;S5(3 月)营养生长后期,叶片完全展开。长筒石蒜:S1--S2(11--12 月)为深度休眠期;S3(1 月)开始萌芽;S4(2 月)营养生长初期;S5(3 月)营养生长中期。
用于代谢组与转录组分析的样品分别取自鳞茎的内、中、外三层组织,每 3 株单株混合为 1 个生物学重复,每个发育时期设置 3 个重复。用于全长转录组分析的样品为长筒石蒜根、鳞茎、叶组织的混合样本。
用于核心基因功能验证的本氏烟草(N. benthamiana )种植于营养土中,室温培养,光照周期 16 h 光照 / 8 h 黑暗。选取萌发后 4--5 周的植株用于农杆菌介导的瞬时转化。
化学试剂
除特殊说明外,所有生化试剂均购自商业供应商,包括加兰他敏(货号 B20592,源叶,中国)、雪花莲碱(货号 S85604,源叶,中国)和 4'-O - 甲基降球花碱(货号 N345029,阿拉丁,中国)。
代谢物提取
长筒石蒜与岛屿石蒜不同发育期鳞茎经真空冷冻干燥后,使用研磨仪在 30 Hz 条件下粉碎 1.5 min 至细粉。精确称取 50 mg 粉末,加入 1200 μL 预冷(-20 °C)含内标的 70% 甲醇提取。样品质量不足 50 mg 时,按每 50 mg 组织 1200 μL 的比例调整提取液体积。每 30 min 涡旋 30 s,共重复 6 次。12000 rpm 离心 3 min 后取上清,经 0.22 μm 微孔滤膜过滤后转入进样瓶,用于 UPLC-MS/MS 分析。
本氏烟草瞬时表达样品的干燥叶片使用含 10 mm 不锈钢珠的 50 mL 管研磨成粉,以 80:20(v/v)甲醇 - 水溶液提取,提取比例为每 mg 干重 2 mL。加入提取液后充分涡旋,室温孵育 2 h,每 30 min 涡旋一次。16000 × g 离心 5 min 去除沉淀,上清经 0.45 μm 亲水 PTFE 滤板过滤后用于 LC-MS 分析。
基于 UPLC-MS/MS 的生物碱代谢分析
样品采用 ExionLC™ AD 超高效液相色谱系统串联 QTRAP 质谱系统进行分析。色谱柱为 Agilent SB-C18(1.8 μm,2.1 mm × 100 mm)。流动相 A 为含 0.1% 甲酸的水溶液,流动相 B 为含 0.1% 甲酸的乙腈。梯度洗脱程序:起始 95% A+5% B,9 min 内线性变为 5% A+95% B 并维持 1 min;1.1 min 内恢复至 95% A+5% B,平衡 2.9 min。流速 0.35 mL/min,柱温 40 °C,进样量 2 μL。
洗脱液进入电喷雾电离(ESI)三重四极杆 - 线性离子阱质谱。ESI 参数:离子源温度 550 °C;喷雾电压 + 5500 V(正模式)/-4500 V(负模式);气帘气 25 psi;离子源气 1 为 50 psi,离子源气 2 为 60 psi;碰撞诱导解离设为高。以多反应监测(MRM)模式采集数据,氮气为碰撞气。对每个 MRM 离子对优化去簇电压(DP)与碰撞能量(CE)。
代谢组数据分析
数据标准化后使用 R 语言 prcomp 函数进行无监督主成分分析(PCA)。对样本与代谢物进行层次聚类分析(HCA)并以热图展示;使用 cor 函数计算样本间皮尔逊相关系数(PCC)并以热图呈现。HCA 与 PCC 均使用 R 包 ComplexHeatmap 绘制。
组间比较中,差异代谢物筛选标准为:变量投影重要度(VIP)> 1,且 | log₂倍数变化 |≥ 1.0。VIP 值通过正交偏最小二乘判别分析(OPLS-DA)获得,使用 R 包 MetaboAnalystR 进行分析,并进行 200 次置换检验以避免过拟合。
代谢物通过 KEGG Compound 数据库注释,并映射至 KEGG 通路。对含显著差异代谢物的通路进行代谢集富集分析(MSEA),超几何检验 p < 0.05 为显著富集。
RNA 提取与转录组测序
总 RNA 采用乙醇沉淀结合 CTAB-PBIOZOL 法提取,沉淀溶于 50 μL DEPC 水。使用 Qubit 与 Qsep400 检测 RNA 浓度、纯度与完整性。
全长转录组由上海派森诺生物科技有限公司构建 PacBio 单分子实时(SMRT)文库,基于 PacBio Sequel II 平台测序。经 ICE 聚类纠错与 CD-HIT 去冗余后,选取每个基因座最长转录本为代表性 unigene。30 个样品各获得约 7 G 干净数据,测序错误率 0.03%。Unigene 在 NR、Pfam、EggNOG、Swiss-Prot、GO、KEGG 数据库完成功能注释。
短读长转录组:总 RNA 经 Oligo (dT) 磁珠富集 mRNA 并片段化,以随机六聚体引物合成 cDNA 第一条链,dUTP 法合成第二条链以实现链特异性。经末端修复、加 A 尾、连接接头后,选取 250--350 bp 片段进行 PCR 扩增与纯化构建文库。文库经 Qubit、Qsep400 与 qPCR 质控后,在 Illumina NovaSeq™ 6000 平台进行双端 150 bp 测序。
转录组数据分析
原始数据使用 fastp 质控,去除含接头、低质量与高 N 比例的 reads。干净数据使用 Trinity 进行无参组装,Corset 聚类去冗余。TransDecoder 预测编码序列(CDS)并推导氨基酸序列。使用 DIAMOND 与 HMMER 将转录本比对至 KEGG、NR、Swiss-Prot、GO、COG/KOG、TrEMBL、Pfam 数据库完成功能注释。
使用 RSEM 定量转录本表达水平,以 FPKM 标准化。有生物学重复的样本使用 DESeq2 进行差异表达分析,Benjamini-Hochberg 法校正 p 值。校正后 p < 0.05 且 | log₂FC|≥ 1 为差异表达基因。对差异基因进行 KEGG 与 GO 富集分析,采用超几何检验。
实时荧光定量 PCR(RT-qPCR)
为验证候选基因表达并选择内参基因,首先评估 HIS、UBQ、18S RNA、UBC、ACT 在两种石蒜中的表达稳定性,确定18S RNA 稳定性最优(附图 2C)。
随机选取 6 个基因进行 RT-qPCR 验证,使用 SYBR Green Master Mix 在 QuantStudio 3 仪器上完成反应,每个反应 3 次技术重复。采用 2ˆ-ΔΔCt 法计算相对表达量,以 18S RNA 为内参。RT-qPCR 表达趋势与转录组结果一致(附图 2D),证明转录组数据可靠。引物序列见附表 5。
CYP96T 家族蛋白系统发育分析
从 NCBI 下载石蒜属及其他石蒜科植物 CYP96T 家族蛋白序列,使用 MAFFT v7.490(L-INS-i 策略)比对,MEGA 11 手动修剪低质量比对区域与空位。基于贝叶斯信息准则(BIC)选择最优替代模型,使用 MEGA 11 构建最大似然(ML)系统发育树,自举检验 1000 次评估分支可靠性。
生物合成候选基因克隆
从长筒石蒜中扩增 LlNMT1、LlNMT4、LlAKR4、LlAKR24、LlCYP96T_clone1/8/12/14/20 的 CDS;从岛屿石蒜中扩增 LiCYP96T_clone1/5/13/16/17。CDS 序列见附表 4。水仙 NtCYP96T6(GenBank: PP708068)、NtAKR1(PP708064)、NtNMT1(PP708075)序列来自 NCBI。所有基因经 BamHI 酶切位点克隆至 pWMB110 载体。引物见附表 5。
农杆菌介导的瞬时表达
本氏烟草瞬时表达参照已报道方法(Mehta et al. 2024)。含重组质粒的农杆菌 GV3101 在 LB 固体或液体培养基(50 μg/mL 卡那霉素 + 30 μg/mL 庆大霉素)中 30 °C 培养。收集菌体并重悬于诱导缓冲液(10 mM MES pH 5.6、10 mM MgCl₂、150 μM 乙酰丁香酮),室温孵育 2--3 h,调 OD₆₀₀至 0.3。共表达菌株等比例混合,用无针头注射器浸润 4--5 周龄烟草叶片背面。每个处理来自 3 株植株的 3 片叶片。
3--4 d 后,在相同叶片浸润 200 μM 4OMN。1--2 d 后取样,液氮速冻并冻干,用于后续代谢物提取。
转基因烟草 K326 植株获得
构建双元载体 pCAMBIA1300-35S-LlNMT-p2A-LlAKR-NOS,由 CaMV 35S 启动子驱动 LlNMT1 与 LlAKR4,两基因由自剪切 2A 肽(p2A)连接,以潮霉素抗性基因为筛选标记。
重组质粒热激转化农杆菌 GV3101,菌落 PCR 验证后采用叶盘法转化烟草 K326。共培养 2 d 后,转入含 25 mg/L 潮霉素与 250 mg/L 头孢霉素的芽诱导培养基。抗性愈伤组织分化的芽切下转入生根培养基,生根幼苗移栽至营养钵,培养至结实并收获 T₁代种子。
体外酶活实验
将 LlNMT1、NtCYP96T6、LlAKR4、LlCYP96T_clone20、LiCYP96T_clone1 及拟南芥细胞色素 P450 还原酶 ATR1 的 CDS 克隆至 pGEX-GST 载体,在大肠杆菌中表达并通过 GST 亲和层析纯化。
体外反应体系(1 mL)含 50 mM HEPES(pH 7.5)、10 mM NADPH、10 mM MgCl₂、5 mM DTT、5% 甘油,加入各 50 μg 纯化蛋白。根据实验设计组合 CYP96T、LlNMT1、LlAKR4 与 ATR1。30 °C 孵育 1 h,过滤终止反应,产物经 LC-MS 分析。
加兰他敏与雪花莲碱的 LC-MS 检测
采用 Waters ACQUITY Premier UPLC-TQ-MS 系统,BEH Shield RP18 T3 色谱柱(1.7 μm,2.1 × 100 mm)。进样量 10 μL,柱温 35 °C。流动相 A 为 0.1% 氨水溶液,B 为含 0.1% 氨水的乙腈,流速 0.2 mL/min。梯度程序:0--1 min 95:5;5 min 15:85;5.01--7 min 恢复 95:5。
质谱采用电喷雾正离子模式,MRM 定量。加兰他敏定量离子对为 288.30 M+H⁺ / 213.00 M--OH--C₃H₇N⁺・m/z。通过保留时间与碎片谱图与标准品比对进行定性。
蛋白结构预测与分子对接
使用 AlphaFold3 预测石蒜 CYP96T - 血红素复合物三维结构,选取预测对齐误差(PAE)低、局部距离差异测试(pLDDT)高的最优模型。使用 AutoDock Vina(1.1.2)进行分子对接,底物为 4OMN。蛋白结构预处理:去除水分子、添加极性氢、分配 Gasteiger 电荷;4OMN 结构能量最小化并转为 PDBQT 格式。对接网格覆盖保守催化残基所在的潜在活性中心。按结合亲和力排序,对最优构象进行可视化与相互作用分析。
统计分析
使用 GraphPad Prism 与 R 软件进行统计分析,数据以平均值 ± 标准差(SD)表示,生物学重复数≥3。组间差异采用 t 检验,显著性标注:*p < 0.1,**p < 0.05,***p < 0.01。