O-methylation modifications in the biosynthetic pathway of dibenzocyclooctadiene lignans
二苯并环辛二烯型木脂素生物合成途径中的 O-甲基化修饰

N-甲基转移酶晶体-文献精读115_cyanogramide-CSDN博客
两种参与茶树O-甲基化儿茶素生物合成的O-甲基转移酶的特征分析-文献精读20_characterization of two o-methyltransferases invol-CSDN博客
马兜铃染色体水平基因组--文献精读176_化石 95%最高后验密度 怎么设置-CSDN博客
研究亮点
- 首次报道参与二苯并环辛二烯类木脂素(DBCODs)修饰的O - 甲基转移酶(OMT) 。
- SchiOMT12 与SchiOMT16 表现出广泛的底物特异性,并阐明了其甲基转移选择性差异的机制。
摘要
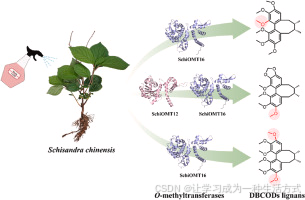
五味子(Schisandra chinensis )是常用于肝炎治疗的经典中药材,其主要活性成分为二苯并环辛二烯类木脂素 ,这类化合物普遍存在多位点O - 甲基化 修饰。然而,参与该修饰过程的 O - 甲基转移酶(OMT)此前尚未见报道。本研究对经茉莉酸甲酯处理的五味子进行转录组分析,结合表达谱、系统发育分析与异源表达,对 O - 甲基转移酶进行功能鉴定。研究筛选得到 4 个 OMT 基因:SchiOMT4、SchiOMT12、SchiOMT16 和 SchiOMT22 ,它们可催化咖啡酸与咖啡醛的 C-3 位 O - 甲基化,生成阿魏酸与松柏醛。此外,SchiOMT12 和 SchiOMT16 可催化五味子素 L2 的 C-3 位甲基化;SchiOMT16 还可对五味子酚 的 C-14 位进行甲基化,并对五味子素 J 的 C-3 和 C-12 位实现连续 O - 甲基化 。分子对接结果进一步阐明了 SchiOMT16 与 SchiOMT12 的催化位点选择性,揭示了二者催化活性差异的原因。本研究首次鉴定出参与二苯并环辛二烯类木脂素后修饰的甲基转移酶 ,证实了 OMT 在其生物合成中具有底物谱广、甲基化位点选择性强 的特点,并发挥重要调控作用。
1. 引言
** 二苯并环辛二烯类木脂素(DBCODs 木脂素)** 是五味子属植物特有的天然代谢产物,在免疫调节与抗肿瘤药物研发中展现出极高的应用潜力。五味子(Schisandra chinensis )为落叶木质藤本植物,作为传统药用植物在中国已有两千余年的应用历史。《神农本草经》与《本草纲目》中均有关于五味子的记载。近年来,研究者围绕五味子的化学成分及药理活性开展了大量研究。DBCODs 木脂素因其独特的化学结构与显著的生物活性(包括抗氧化、抗炎、抗病毒及抗肿瘤等)受到学界广泛关注。
现代药理研究表明,五味子酚 可显著抑制肝星状细胞活化,从而改善肝纤维化;五味子甲素 不仅具有显著的抗肿瘤作用,还能改善小鼠记忆损伤,显示出作为阿尔茨海默病记忆增强剂的潜力;五味子乙素 可显著抑制结肠癌细胞的生长与转移,并具有镇静催眠作用;五味子素 J 则通过激活内皮型一氧化氮合酶诱导血管舒张。
DBCODs 木脂素多样的药理活性主要源于其丰富的修饰位点与取代基类型。常见取代基包括羟基、甲基、亚甲二氧基、乙酰基、当归酰基、苯甲酰基和丙二酰基等,其中羟基与甲基的取代位点最多。亚甲二氧基主要分布于 C-2/C-3 和 C-12/C-13 位,酰基取代则多发生在 C-6 或 C-9 位。在已报道的 DBCODs 木脂素中,几乎所有化合物均含有甲基取代基。O - 甲基化修饰 主要体现为取代位点的多样性与甲基数目差异,进而形成结构多样的产物。
尽管 Huang 等通过氧化还原化学合成方法成功实现了 DBCOD 类化合物的全合成,但其天然生物合成途径仍不明确。如图 1 所示,DBCODs 木脂素来源于苯丙烷途径,经前体合成、骨架构建及后续多步修饰,最终形成结构多样的 DBCODs 木脂素。
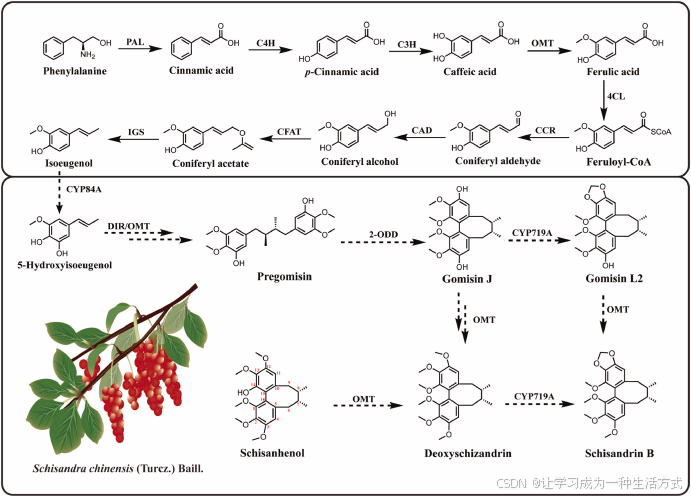
图 1 二苯并环辛二烯类木脂素的生物合成途径
PAL:苯丙氨酸解氨酶;C4H:反式肉桂酸 4 - 单加氧酶;C3H:对 - 香豆酸 3 - 羟化酶;OMT:O - 甲基转移酶;4CL:4 - 香豆酸辅酶 A 连接酶;CCR:肉桂酰辅酶 A 还原酶;CAD:肉桂醇脱氢酶;CFAT:松柏醇酰基转移酶;IGS:异丁香酚合成酶;CYP:细胞色素 P450 单加氧酶;DIR:手性导向蛋白;2-ODD:2 - 酮戊二酸 / 铁离子依赖型双加氧酶。
DBCODs 木脂素的O - 甲基化修饰 既发生在核心骨架形成前的上游途径,也出现在骨架形成后的后修饰阶段。骨架形成前的 O - 甲基化主要集中在苯丙烷单体的C-3 位 ,是苯丙烷生物合成途径中的一个重要代谢分支点。苯丙烷途径的代谢产物松柏醇是木脂素合成的关键前体。对上游途径 C-3 位 O - 甲基化修饰的研究,可为明确五味子中 DBCODs 木脂素合成的代谢流向提供直接证据。
在骨架形成后的 O - 甲基化方面,DBCODs 木脂素分子结构的典型特征是苯丙烷前体单元通过 C-7/C-8 与 C-15/C-16 位连接,形成独特的八氢环结构。这使得骨架上存在多个活性位点(邻位、间位、对位),甲基可在这些位点以不同组合方式发生取代。根据 O - 甲基化发生的次数,可形成单、二、三甚至多甲基化衍生物,各自具有独特的结构与化学性质。此外,O - 甲基化会影响邻近官能团的电子效应与空间位阻,显著改变分子特性,增强其生物活性并提高生物利用度。尽管 DBCODs 木脂素生物合成途径中的部分酶已逐步得到鉴定,但负责该类特征骨架 O - 甲基化修饰的OMT 仍未见报道。鉴定具有催化多样性的 DBCODs 木脂素 O - 甲基转移酶,对完善其生物合成网络、阐明联苯八氢环核心形成过程中的位点选择性至关重要。
本研究基于茉莉酸甲酯(MeJA)处理的五味子转录组数据,共鉴定出 28 个 OMT 基因。通过表达谱分析与系统发育分析进一步筛选出候选 OMT 编码基因,经异源表达与体外酶活实验,分别验证其在苯丙烷上游途径及后续修饰步骤中的 O - 甲基化功能。同时,通过同源建模与分子对接探究SchiOMT16 与SchiOMT12 在 O - 甲基转移选择性上的差异。本研究为进一步阐明 DBCODs 木脂素的生物合成机制奠定了基础。
2. 材料与方法
2.1 植物材料与化合物标准品
五味子幼苗采自中国辽宁省抚顺市新宾满族自治县东韩家村,种植于云南省昆明市盘龙区西南生物多样性实验实验室温室。采用 1 mM 茉莉酸甲酯(MeJA,Sigma-Aldrich,No.392707)进行激素胁迫处理,叶面喷施 100 mL,根部浇灌 100 mL。分别在 MeJA 处理 0、6、12、24、48 h 后采集根、茎、叶样品用于转录组测序。
咖啡酸、阿魏酸、咖啡醛、松柏醛、咖啡醇、五味子素 J、五味子素 K1、五味子酚、五味子甲素、五味子素 L2、五味子乙素、S - 腺苷甲硫氨酸(SAM)购自云南西力生物技术股份有限公司;MeJA 购自西格玛奥德里奇(上海)贸易有限公司。
2.2 RNA 提取与 cDNA 制备
采集五味子新鲜根、茎、叶组织,每份样品 100 mg,经液氮充分低温研磨。使用 HiPure HP Plant RNA MiniKit 试剂盒(美基生物,中国广州)提取总 RNA,通过 1% 琼脂糖凝胶与 NanoDrop 2000 检测 RNA 质量,提取的 mRNA 于 - 80 ℃保存。
使用 PrimeScript™ II 第一链 cDNA 合成试剂盒(6210A;宝生物,北京)合成第一链 cDNA,产物于 - 20 ℃保存备用。
2.3 转录组测序与分析
由诺禾致源公司构建测序文库。采用 Trizol 试剂盒(普洛麦格,美国)提取五味子根、茎、叶总 RNA,通过高通量测序平台获得原始数据。去除含接头序列、N 比例超过 10% 及低质量 reads(质量值 Q≥30 碱基占比<50%)后得到 Clean reads。使用 Trinity 软件(v2.15.1)进行de novo 组装,k-mer 设为 25;通过 RapClust(v0.1.2)聚类得到最终 Unigene,并用 Salmon(v1.9.0)计算表达量。利用 TransDecoder 软件(v5.7.0)预测 Unigene 的编码序列(CDS)。将预测 CDS 通过 DIAMOND(v2.1.8)比对本地 Nr、KEGG、KOG、TrEMBL、SwissProt 数据库,选取最优匹配序列作为最终注释序列。随后通过 PfamScan(v1.6)比对 Pfam 数据库(v35.0),InterProScan(v5.63--95.0)进行 GO 注释,KofamScan(v1.3.0)进行 KO 注释。
2.4 候选基因克隆与载体构建
使用 TBtools 软件分析目标基因开放阅读框(ORF),利用 Snapgene 设计带表达载体 pET-28a 同源臂的候选基因克隆引物,引物序列见补充表 S1。以反转录 cDNA 为模板,使用 Phanta 高保真 DNA 聚合酶(诺唯赞,南京)进行 PCR 扩增。经限制性内切酶Bam HI(赛默飞世尔,美国)线性化的 pET-28a 载体,通过无缝克隆与目的基因片段连接,重组质粒转化大肠杆菌 DH5α 感受态细胞。测序正确后提取质粒,转化蛋白表达菌株 BL21(DE3)感受态细胞。
2.5 DBCODs 木脂素途径基因鉴定与 OMT 系统发育树构建
使用 PfamScan v1.6 工具基于 Pfam v36.0 数据库注释五味子蛋白序列,保留 E 值<1e-5 的序列。通过筛选酶基因家族保守结构域对应的 Pfam 编号,注释 DBCODs 木脂素生物合成途径相关候选基因。使用 MAFFT v7.52 进行多序列比对,trimAl v1.4.1 修剪序列,最终通过 IQ-TREE v2.2.2.7 构建最大似然法(ML)系统发育树。利用 R v4.4.1 中 ggtree v3.12.0 包对进化树进行可视化与优化。
2.6 同源重组与蛋白表达
取 20 μL 阳性转化的大肠杆菌 BL21(DE3)甘油菌接种至摇管过夜活化,按 1%(v/v)接种量转接至 400 mL 含卡那霉素的 LB 培养基,37 ℃、220 rpm 振荡培养。待 OD₆₀₀₀ₙₘ达到 0.2--0.8 时,加入 400 μL 0.2 mM IPTG 诱导蛋白表达,18 ℃、220 rpm 诱导 14--16 h。
诱导结束后收集菌体,细胞破碎后分离沉淀与上清。上清液经镍柱(Ni-NTA)纯化,依次使用 20 mM、50 mM、300 mM 咪唑溶液梯度洗脱。纯化后蛋白采用 Millipore 超滤管浓缩,最终纯化蛋白用于酶活检测。SchiOMT 氨基酸序列信息见补充文件 S1。
2.7 体外酶活检测
为鉴定 OMT 功能,在 200 μL 体系中进行体外酶促反应:底物浓度 0.2 mM,辅因子 SAM 0.4 mM,纯化蛋白 100 μL,用 50 mM Tris--HCl(pH 8.0)补足体积。OMT 酶活鉴定反应条件为 35 ℃孵育 2 h。
反应结束后加入等体积甲醇终止,12000 rpm 离心 15 min,取上清使用高效液相色谱仪(1260,安捷伦,美国)检测。
色谱柱采用 Luna® 5 μm C18 (2),100 Å,250 × 4.6 mm(飞诺美,美国)。不同底物采用不同检测方法:
- 咖啡酸、阿魏酸:流动相水:乙腈 = 90:10,15 min 变为 65:35;流速 1 mL/min;柱温 35 ℃;检测波长 320 nm。
- 咖啡醛、松柏醛:流动相水:乙腈 = 75:25;流速 1 mL/min;柱温 35 ℃;检测时间 18 min;波长 330 nm。
- 五味子素 J、K1、五味子酚、五味子甲素:流动相水:甲醇 = 25:75;流速 1 mL/min;柱温 35 ℃;检测时间 20 min;波长 254 nm。
- 五味子素 L2、五味子乙素:流动相水:乙腈 = 15:85;流速 1 mL/min;柱温 35 ℃;检测时间 10 min;波长 254 nm。
2.8 分子对接
使用 AlphaFold2 构建蛋白三维结构模型,通过 SAVES 服务器评估模型质量。采用 AutoDockTools 软件进行分子对接分析,PyMOL 软件可视化对接结果。
3. 结果
3.1 五味子转录组分析与功能注释
茉莉酸甲酯处理广泛用于筛选植物次生代谢生物合成途径相关基因,可诱导生物碱、萜类、苯丙烷类等次生代谢产物合成。本研究通过分析 MeJA 诱导的时空基因表达模式,鉴定五味子 DBCODs 木脂素生物合成途径关键候选基因。经 MeJA 处理后共获得 377.11 Gb 有效数据,组装得到 86148 条转录本,去冗余后保留 85032 条 Unigene。样本重复性热图证明转录组数据可靠(图 2a)。Unigene 平均长度 794 bp,N50 为 1429 bp,GC 含量 41.93%。基于 KEGG、KOG、Nr、TrEMBL、SwissProt 五大数据库完成功能注释,结果如图 2b 所示。
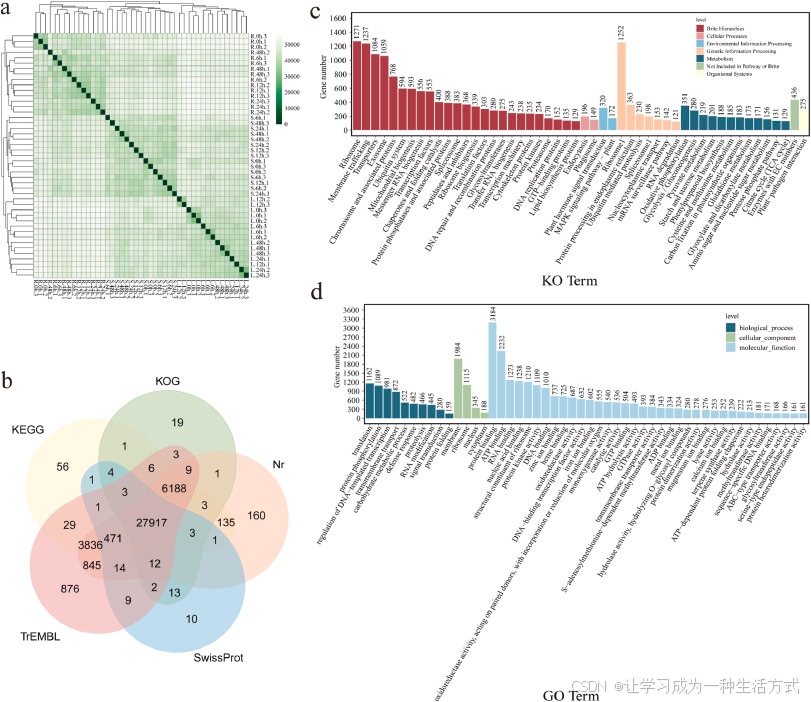
图 2 转录组分析 (a)样本重复性热图。(b)五味子在 KEGG、KOG、Nr、TrEMBL 和 SwissProt 数据库注释的韦恩图。五味子 Unigene 的(c)KEGG 注释与(d)GO 注释功能富集分析。
为进一步对 Unigene 进行功能预测与分类,开展了 KEGG 与 GO 分析(图 2c、d)。共有 18451 条 Unigene 注释到 50 条 KEGG 通路,32156 条 Unigene 注释到 50 个 GO 条目。这些数据基本覆盖了全部生命活动,清晰展现了五味子的基因富集通路与功能分布特征。值得注意的是,在 KEGG 注释中,有 185 条 Unigene 与 **"苯丙烷生物合成"相关,在代谢模块中丰度较高。苯丙烷生物合成是 DBCODs 木脂素前体生成的核心途径,也是其骨架构建的起始环节。在 GO 分析中,343 条 Unigene 富集于 "S - 腺苷甲硫氨酸依赖的甲基转移酶活性"** 分子功能条目,这与 DBCODs 木脂素多位点 O - 甲基化修饰的特征高度相关。高质量的转录组数据为本研究奠定了基础,为筛选参与 DBCODs 木脂素合成的候选基因提供了关键信息。
3.2 DBCODs 木脂素生物合成途径候选基因的表达模式分析
基因表达热图可直观呈现生物合成途径中基因的表达趋势。已有研究证实,DBCODs 木脂素是由两分子苯丙烷衍生物二聚形成的天然产物,且多条证据表明木脂素合成相关基因受茉莉酸甲酯调控。因此,本研究基于 MeJA 诱导的转录组数据进行时空差异表达富集分析,筛选阈值设为 log₂| 倍数变化 |>1 且校正后 P 值<0.01。结果显示,响应 MeJA 的差异基因数量在根中最多,叶次之,茎中最少(附图 S1)。
尽管 DBCODs 木脂素骨架形成的下游通路仍不明确,为进一步挖掘参与其合成的其他酶家族,我们结合转录组注释与 Pfam 结构域编号鉴定了该途径的潜在同源基因。转录组共鉴定出 4 个 PAL、3 个 C4H、28 个 OMT、33 个 4CL、48 个 CCL、50 个 CAD ,并分析了这些同源基因在五味子不同组织中的差异响应(附表 S2)。基于根部差异表达数据与本地 BLAST 比对结果,选取与已报道功能基因同源性最高的基因代表该家族,构建基因表达模式图,详细信息见附表 S3,其中包括已在该物种中报道具有催化功能的 ScCFAT45 和 ScIGS1 。
基因表达谱展示了五味子苯丙烷途径同源基因在 MeJA 处理后不同时间点的相对表达水平(图 3a)。结果显示,尽管通向松柏醇的苯丙烷合成基因在同一时间点并未呈现一致的上调或下调趋势,但均对 MeJA 呈现不同程度的响应,整体表现为先升后降。SchiPAL2 、ShiCYP102 、Schi4CL29 、SchiCAD32 在 12 h 或 24 h 显著响应,相对表达量达到峰值后下降;SchiOMT04 与 SchiCCR24 在 6 h 即达到表达高峰。
在五味子中已验证功能的基因里,SchiBAHD10 (ScCFAT45 )与 SchiIGS08 (ScIGS1 )呈现两种截然不同的表达模式:SchiBAHD10 整体呈上调趋势,在 48 h 表达量最高;而 SchiIGS08 在 6 h 达到峰值,随后先降后升(图 3a)。这表明不同基因通过不同调控机制响应 MeJA 处理。我们尝试通过已有报道的途径基因的共表达趋势筛选候选基因,但由于苯丙烷途径庞大复杂、分支众多,相关基因并未呈现统一表达模式。因此,我们选取该物种中已报道功能的 SchiBAHD10 和 SchiIGS08 作为诱饵基因 ,开展后续分析。
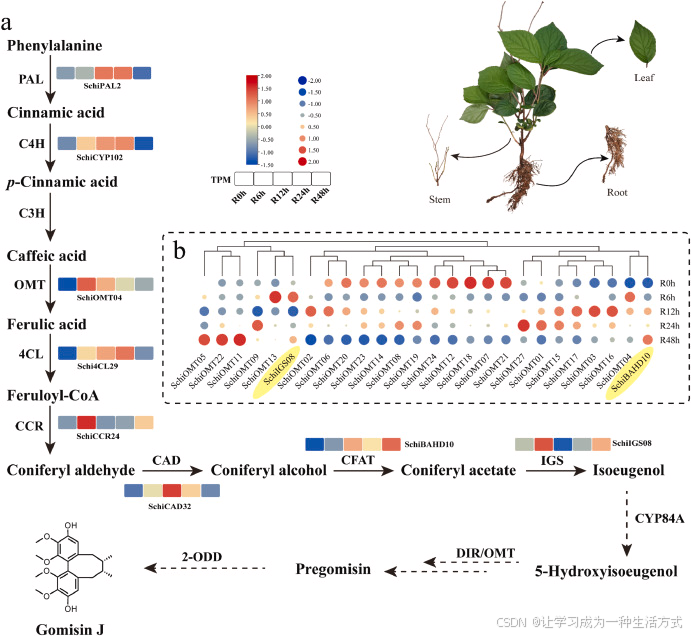
图 3 参与二苯并环辛二烯类木脂素生物合成的 SchiOMTs 筛选
(a)茉莉酸甲酯(MeJA)胁迫下,五味子根部二苯并环辛二烯类木脂素合成途径中苯丙烷通路同源基因的表达模式。每个色块代表对应基因的表达量。(b)用于五味子转录组分析的三种组织样本。(c)SchiOMT 候选基因与 SchiBAHD10、SchiIGS08 表达模式的相关性分析。
已有功能注释的基因常被用作诱饵基因 ,以挖掘生物合成途径中尚未报道的催化步骤,是一种高效的基因筛选策略。本研究以 SchiBAHD10 和 SchiIGS08 为诱饵基因,通过表达趋势分析,筛选出响应 MeJA 且表达模式一致的 OMT 作为候选基因(图 3b)。
其中,SchiOMT04、SchiOMT16、SchiOMT03、SchiOMT17、SchiOMT15、SchiOMT01、SchiOMT27 与催化松柏醇转化为乙酸松柏醇酯的 SchiBAHD10 时空表达模式相似;而SchiOMT05、SchiOMT22、SchiOMT11、SchiOMT09、SchiOMT13 则与催化乙酸松柏醇酯生成异丁香酚的 SchiIGS08 表达模式相近。
相似的时空表达模式提示,这些候选基因可能与功能明确的基因参与同一条生物合成途径,为未知功能基因的鉴定提供了重要参考。
3.3 参与二苯并环辛二烯类木脂素生物合成的 OMT 候选基因系统发育分析
O - 甲基化是众多天然产物合成中的关键步骤,也是一类普遍存在的后修饰反应 。在植物中,O - 甲基转移酶(OMT)以氧原子为催化位点,通常以含羟基化合物为底物,参与简单苯丙烷、黄酮、生物碱等多种次生代谢物的合成,在调控植物多种生理功能中发挥重要作用。
本研究在五味子转录组中共注释到28 个 OMT 候选基因 。经开放阅读框(ORF)分析,其中23 个具有完整编码序列(CDS) 。以这 23 条 SchiOMT 为参考序列,结合其他植物 OMT 序列构建了系统发育树(图 4),所用序列信息见附表 S4。
系统发育分析显示,这些 OMT 可分为四大分支 :
10 个 SchiOMT 归为简单苯丙烷类 OMT 该分支中功能已鉴定的基因主要参与苯丙烷生物合成,多催化咖啡酸 C3 位的 O - 甲基化,而这一位点也是木脂素前体的关键修饰位点。因此,该分支很可能包含参与 DBCODs 木脂素上游中间体 O - 甲基化 的基因。
5 个 SchiOMT 归为黄酮类 O - 甲基转移酶 这类酶具有高度的位点选择性,可催化黄酮分子上特定位点羟基的甲基化。例如 MtHI4OMT、LjHI4OMT、GmSOMT2、CrOMT6 催化 C4′位羟基甲基化,而 POMT-7、MpOMT2 分别作用于 C7 和 C8 位。
4 个 SchiOMT 归为可能参与生物碱 O - 甲基化的分支 。
其余 5 个候选基因形成一个独立分支 ,提示它们可能对本研究关注的 DBCODs 类化合物结构具有特异性催化潜力。
综上,结合表达模式相关性分析 与系统发育分析 ,本研究选取与 SchiBAHD10、SchiIGS08 时空表达模式相近,以及归类为功能未知、可能催化简单苯丙烷类底物的候选 OMT(共 20 个),进行蛋白异源表达与功能验证,以确定其催化功能。
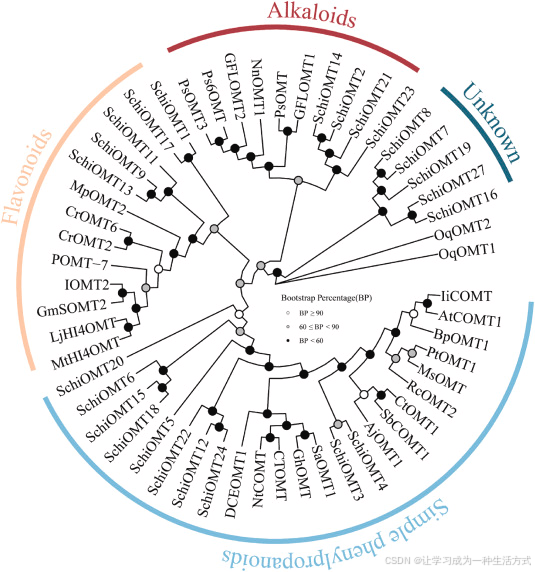
图 4 O - 甲基转移酶(OMT)系统发育树
3.4 O - 甲基转移酶的异源表达与功能鉴定
甲基转移酶催化的 O - 甲基化修饰可显著提升天然产物的稳定性、溶解性及生物活性等多种生物学特性。为验证候选 OMT 的功能,本研究将其在大肠杆菌中进行异源表达,以 S - 腺苷甲硫氨酸(SAM)为甲基供体,通过体外酶活实验检测催化活性。蛋白 SDS-PAGE 分析见附图 S2,结果证实目的蛋白成功异源表达,并获得体外重组蛋白。
为验证苯丙烷上游途径 C-3 位同源基因的功能,本研究以咖啡酸、咖啡醛和咖啡醇 为底物进行检测。结果显示:SchiOMT4、SchiOMT12、SchiOMT16 对咖啡酸和咖啡醛均具有催化活性;SchiOMT22 可催化咖啡醛转化为松柏醛。
HPLC-MS 分析进一步证实,质荷比m/z 为 193.05 ([M-H]⁻) 和 177.05 ([M-H]⁻) 的产物分别与阿魏酸、松柏醛标准品一致(图 5a--e)。值得注意的是,SchiOMT4 对咖啡酸催化活性极高 ,可将 0.2 mM 底物几乎完全转化;同时,SchiOMT4、SchiOMT12 和 SchiOMT22 均可高效催化咖啡醛完全消耗。
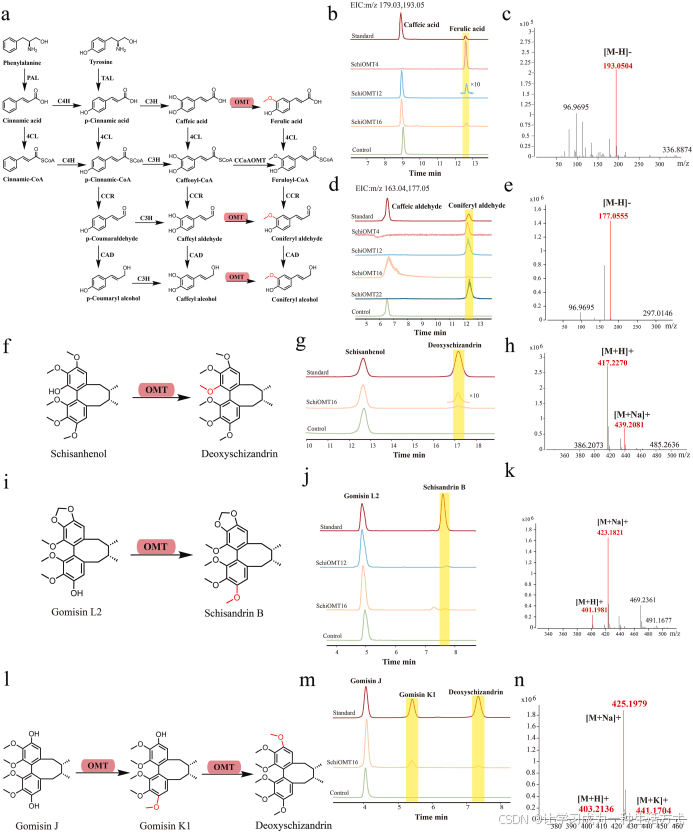
图 5 SchiOMT 的功能鉴定 (a)苯丙烷上游完整合成通路示意图。(b)以咖啡酸为底物,体外 LC-MS 验证 SchiOMT 催化咖啡酸生成阿魏酸。(c)阿魏酸标准品质谱图。(d)以咖啡醛为底物,体外 LCMS 验证 SchiOMT 催化咖啡醛生成松柏醛。(e)松柏醛标准品质谱图。(f)SchiOMT 催化五味子酚 C14 位 O甲基化。(g)以五味子酚为底物,HPLC 验证 SchiOMT 体外催化生成五味子甲素。(h)五味子甲素标准品质谱图。(i)SchiOMT 催化五味子素 L2 的 C13 位 O甲基化。(j)以五味子素 L2 为底物,HPLC 验证 SchiOMT 体外催化生成五味子乙素。(k)五味子乙素标准品质谱图。(l)SchiOMT 可连续催化五味子素 J 的 C3 和 C12 位 O甲基化。(m)HPLC 验证 SchiOMT 催化五味子素 J 先在 C3 位甲基化生成五味子素 K1,再经 C12 位甲基化生成五味子甲素。(n)五味子素 K1 标准品质谱图。
二苯并环辛二烯类木脂素两侧苯环的 C1--C3 及 C12--C14 位主要被羟基、亚甲二氧基或甲氧基取代。本研究对 C3、C12、C14 位的 O甲基化活性进行了探究。
将五味子酚与 SAM 及纯化蛋白共孵育后发现:SchiOMT16 可催化其C14 位 O甲基化 生成五味子甲素,产物m/z 为 417.22 ([M+H]⁺)、439.20 ([M+Na]⁺),与标准品一致(图 5f--h)。
SchiOMT12 与 SchiOMT16 均可催化五味子素 L2 转化为五味子乙素,表明其对C3 位 进行了修饰,二级质谱显示m/z 为 401.19 ([M+H]⁺)、423.18 ([M+Na]⁺)(图 5i--k)。
更有意思的是,以五味子素 J 为底物时,SchiOMT16 可连续两步催化 O甲基化 :先在 C3 位甲基化生成五味子素 K1,再在 C12 位进一步甲基化生成五味子甲素。五味子素 K1 的特征m/z 为 403.21 ([M+H]⁺)、425.19 ([M+Na]⁺)、441.17 ([M+K]⁺),与五味子甲素的质谱信号匹配(图 5l--n)。详细样品质谱图见附图 S3。
以上结果表明:SchiOMT12 和 SchiOMT16 既参与 DBCODs 木脂素骨架形成前的 O甲基化,也参与骨架形成后的后修饰甲基化 。因此,我们进一步检测了二者对更多途径中间体(阿魏酸、松柏醛、松柏醇、异丁香酚、前五味子素)的催化活性,发现均有催化作用(附图 S4--S8)。实验证实,SchiOMT12 和 SchiOMT16 底物谱广泛,参与 DBCODs 木脂素生物合成的多个 O甲基化步骤 。
3.5 SchiOMT16 与 SchiOMT12 的 O甲基化选择性差异
系统发育分析与多序列比对显示,本研究鉴定的 4 个有催化活性的甲基转移酶均属于I 型甲基转移酶 (附图 S9)。该类酶具有保守的 N 端辅助结构域(利于同源二聚化)和 SAM 依赖的甲基转移酶结构域,可将甲基从 SAM 转移到底物的活性羟基上,生成甲基化产物。
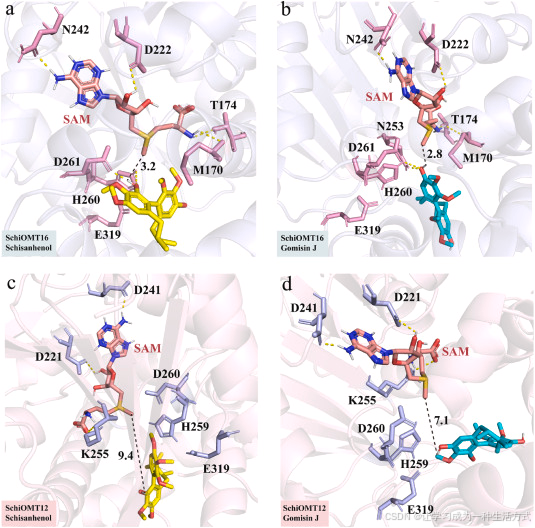
功能实验结果显示,SchiOMT12 与 SchiOMT16 仅在五味子酚和五味子素 J 上表现出催化活性差异 。我们通过分子对接 模拟底物、SAM 与 OMT 蛋白的结合模式,从分子模型层面解释两种酶的催化选择性差异(图 6)。
图 6 SchiOMT16 与 SchiOMT12 的分子对接模型 (a)五味子酚结合于 SchiOMT16 活性中心的对接构象。(b)五味子素 J 结合于 SchiOMT16 活性中心的对接构象。(c)五味子酚结合于 SchiOMT12 活性中心的对接构象。(d)五味子素 J 结合于 SchiOMT12 活性中心的对接构象。
SAM 在 SchiOMT16 中与 Asn242、Asp222、Thr174 和 Met170 形成强氢键(图 6a、b);而在 SchiOMT12 中,SAM 通过 Asp221、Asp241 和 Lys255 形成强氢键(图 6c、d)。这些氨基酸残基对小分子在催化口袋内的锚定至关重要。SchiOMT16 与 SAM 之间的氢键数量多于 SchiOMT12,表明前者对 SAM 具有更高的亲和力。
在 I 型甲基转移酶中,催化依赖于保守的HisAspGlu 催化三联体 。His 与 Asp 之间形成氢键以稳定底物的活性羟基,Glu 则增强 His 的 ND1 氮原子碱性,促进底物去质子化以启动催化。在 SchiOMT16 中,His260 和 Asp261 与五味子酚的 C14 羟基形成氢键,同时 His260 也与五味子素 J 的 C3 羟基形成氢键,利于羟基脱质子生成酚阴离子,进而进攻 SAM 上活泼的甲基,将甲基转移至底物催化位点。取代位点的选择由 SAM 与羟基间的相对距离决定。
在 SchiOMT12 与两种底物的对接中,HisAspGlu 催化三联体均未与底物形成氢键;SAM 的甲基与五味子酚 C14 羟基距离为 9.4 Å(SchiOMT16 中为 3.2 Å),与五味子素 J C3 羟基距离为 7.1 Å(SchiOMT16 中为 2.8 Å)。这解释了 SchiOMT12 对五味子酚和五味子素 J 无明显催化活性的原因。同源建模与分子对接结论与酶功能实验结果一致,为两种 OMT 的催化差异提供了分子机制解释。
4. 讨论
五味子因临床可显著降低肝炎患者血清谷丙转氨酶(ALT)水平而受到重视,并由此开发出抗肝炎药物 "联苯双酯滴丸",其核心药效物质正是二苯并环辛二烯类木脂素。目前对 DBCODs 木脂素的研究多集中于植物化学与药理活性,但其完整生物合成途径与催化机制仍不明确,尤其是两个苯丙烷单元直接偶联并环化形成八元环的关键步骤尚未解析。此外,阐明这类活性化合物多位点 O甲基化的功能,是解析其代谢网络的重要环节。
O-甲基转移酶是植物中主要的甲基转移酶类,以 SAM 为甲基供体,催化苯丙烷、黄酮、生物碱等次生代谢产物的普遍后修饰。已有研究在五味子中报道了 200 余种 DBCODs 木脂素,五味子甲素、五味子乙素、五味子素 J、K1、N 等代表性化合物均具有不同位点、多位点的 O甲基化修饰。目前 DBCODs 木脂素生物合成的代谢与分子基础仍不清楚。在木脂素类途径中,仅在鬼臼毒素生物合成中报道过 OMT,OMT1 催化 (−)-5′- 去甲基丫脂素生成重要前体 (−)- 丫脂素。而在其他植物中,具有广谱底物特异性和多位点 O甲基化修饰能力的 OMT 并不少见。例如,台湾白橘 CdFOMT5 可催化槲皮素、柚皮素、表儿茶素的 C3、C5、C6、C7 位 O甲基化;石斛属 DcOMT 可催化多种不同羟基 / 甲氧基取代的酚类物质。其原因在于 OMT 通常由较大的 C 端催化结构域和较小的 N 端结构域组成:C 端主要结合 SAM 与酚类底物,N 端主要参与二聚化。OMT 相对保守的结构域赋予了底物多样性,使植物能够执行更广泛的生理功能。本研究鉴定的 SchiOMT 中,SchiOMT16 底物杂泛性更强 ,不仅可催化苯丙烷单体,还能对五味子酚、五味子素 L2、五味子素 J 等 DBCODs 衍生物进行 O甲基化。
本研究结果明确了苯丙烷上游途径的代谢流向,并证明五味子 OMT 是一类广谱特异性酶。SchiOMT12 和 SchiOMT16 既参与上游苯丙烷单体的 O甲基化,也参与 DBCODs 木脂素骨架形成后的后修饰甲基化 。有趣的是,二者仅在五味子酚和五味子素 J 上表现出催化选择性差异。但 SchiOMT12 能够催化含亚甲二氧基的 DBCODs 化合物五味子素 L2 发生 O甲基化。五味子酚、五味子素 J 与五味子素 L2 在结构上仅相差一个亚甲二氧基桥,而这一差异对 OMT 的底物识别可能至关重要。已有研究报道当归中 AdOMT1 和 AdOMT2 因官能团差异而对香豆素和苯丙烷类表现出催化活性差异。
从酶-辅因子-底物结合角度看,OMT 蛋白的活性空腔较大,可能无法形成合适的酶底物复合物构象,导致 SAM 的甲基不能有效靠近底物羟基,增加精准催化难度。甲基化遵循 SN2 亲核取代机制,受体羟基必须足够接近 SAM 的甲基才能高效发生转移,最终导致 O甲基转移酶活性差异。
本研究分子对接模型显示,SchiOMT12 和 SchiOMT16 均具有辅因子结合口袋:SAM 在 SchiOMT16 中与 N242、D222、T174、M170 形成氢键;在 SchiOMT12 中与 D221、D241、K255 形成强氢键,利于辅因子结合。但五味子酚可与 SchiOMT16 的 D261、H260 形成强氢键,五味子素 J 可通过 N253、D261 与 SchiOMT16 作用,从而稳定底物并使其靠近 SAM 的活泼甲基,使催化残基完成甲基转移。相反,SchiOMT12 与五味子酚、五味子素 J 均未形成可促进催化的氢键。因此,D261、H260 和 N253 可能是决定 SchiOMT12 与 SchiOMT16 催化差异的关键位点 。亚甲二氧基桥对 SchiOMT12 催化活性的影响,以及造成二者活性差异的关键氨基酸,仍值得进一步深入研究。未来将围绕这一方向开展实验验证,以阐明 OMT 对 DBCODs 木脂素的分子催化机制。
O-甲基化是阿魏酸、血球胺、小檗碱、姜黄素等多种药用植物重要天然产物与活性化合物生物合成的关键步骤。近年来,通过在微生物宿主中异源表达 O甲基转移酶,已实现苯丙烷、香料、激素、抗生素等多种高价值天然产物的生物合成。但多数 OMT 存在催化效率低、底物谱窄等问题,成为天然产物高效合成的瓶颈。在木脂素途径单体(如阿魏酸、松柏醇)的微生物细胞工厂构建中,OMT 被确定为关键催化酶与限速酶。通过 OMT 优化改造,酿酒酵母中阿魏酸产量可达 148.34 mg/L,松柏醇可达 124.9 mg/L。Chen 等还以阿魏酸为代谢中间体,系统工程化实现了松脂素、落叶松脂素等复杂木脂素的首次从头合成。
本研究首次鉴定出对 DBCODs 木脂素具有催化活性的 SchiOMT12 和 SchiOMT16,尽管催化效率相对有限。值得注意的是,在苯丙烷合成模块中,SchiOMT4 对咖啡酸转化效率极高 ,SchiOMT12 和 SchiOMT22 对咖啡醛也具有显著催化活性。这些 OMT 可作为优化微生物宿主、提高 O-甲基化产物合成的潜在基因元件。通过理性蛋白质工程可提高 OMT 对底物的结合亲和力,结合高效酶筛选与代谢工程策略,可优化天然产物人工合成途径。将改造后的 OMT 整合进微生物平台,可显著提升生物合成效率与可持续性,最终实现高价值分子的低成本合成。
综上,本研究填补了 DBCODs 木脂素多样性形成过程中 OMT 功能的空白。揭示 SchiOMT12 和 SchiOMT16 为双功能杂化酶 ,深化了对 OMT 底物甲基转移选择性的认识,并从分子对接角度解析了催化活性差异。本研究提供了 DBCODs 木脂素合成必需的关键基因元件,对进一步阐明其完整生物合成途径、推进合成生物学高效生产具有重要价值。未来将通过酶工程进一步挖掘五味子 OMT 的催化能力,完善天然生物合成途径功能解析,最终实现 DBCODs 木脂素的代谢工程合成。
5. 结论
本研究首次鉴定出参与二苯并环辛二烯类木脂素生物合成的 O甲基转移酶 。通过对茉莉酸甲酯处理的五味子进行转录组分析,筛选并鉴定出 4 个参与 DBCODs 木脂素 O甲基化修饰的 OMT,经表达模式、系统发育与异源表达验证其功能。
- SchiOMT4、SchiOMT12、SchiOMT16、SchiOMT22 催化上游苯丙烷单体 C-3 位 O-甲基化,将咖啡酸、咖啡醛转化为阿魏酸、松柏醛。
- SchiOMT12 和 SchiOMT16 还可催化 DBCODs 木脂素骨架形成后的 O-甲基化,对五味子素 L2 具有催化活性。
- SchiOMT16 可催化更多 DBCODs 相关化合物:五味子酚 C-14 位甲基化、五味子素 J 连续 C-3 和 C-12 位甲基化。
- 分子对接进一步阐明了 SchiOMT12 与 SchiOMT16 的催化活性差异机制。
研究表明,五味子 OMT 具有广谱底物特异性 ,其 O甲基化位点的多样性与选择性在 DBCODs 木脂素生物合成调控中发挥关键作用。