在生物制药研发的前沿领域,靶点的选择与机制解析是药物开发的基石。CD33(Siglec-3) 作为唾液酸结合免疫球蛋白样凝集素家族的重要成员,是一种分子量约为67kDa的I型跨膜糖蛋白。它主要表达于髓系细胞表面,在免疫调控、信号传导及细胞分化中发挥关键作用。
本文将从技术研发视角,系统梳理CD33的分子结构特征、ITIM依赖的抑制性信号传导机制、已上市抗体药物概况以及未来的技术迭代方向,为相关领域的开发者与科研人员提供参考。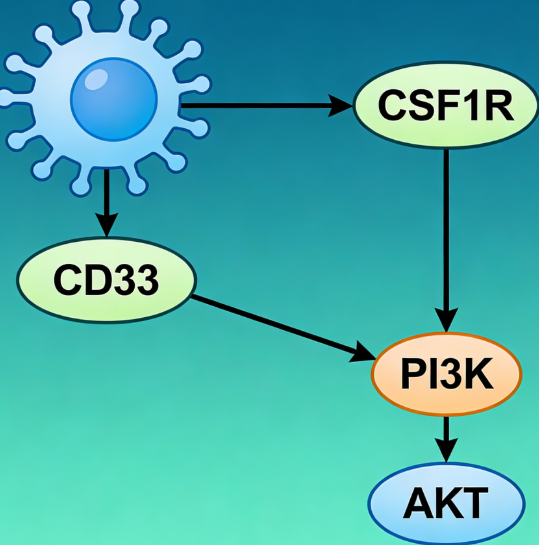
1. CD33靶点的作用机制:结构与信号传导解析
CD33的分子功能实现依赖于"配体结合-信号激活-功能响应"的级联路径。其核心机制主要体现在以下三个维度:
1.1 介导ITIM依赖的抑制性信号传导
CD33最核心的功能是作为抑制性免疫受体。当其胞外区与唾液酸配体结合后,胞内区的**免疫受体酪氨酸抑制基序(ITIM)**中的酪氨酸残基会被磷酸化,进而招募SHP-1、SHP-2等磷酸酶。这些酶通过去磷酸化作用,抑制下游的促活化信号通路(如MAPK、NF-κB通路),从而防止免疫反应过度亢进,维持免疫系统稳态。
1.2 调控髓系细胞分化与动态平衡
CD33主要表达于单核细胞、巨噬细胞及树突状细胞等髓系细胞表面。在造血分化过程中,其表达水平呈动态变化:早期髓系祖细胞表达较高,成熟粒细胞表达较低。生理状态下,CD33通过调控髓系细胞的分化与成熟,保障人体先天免疫功能的正常发挥。
1.3 参与多组织稳态调节
除了造血系统,CD33在神经系统的小胶质细胞中也有表达。它通过调控小胶质细胞的吞噬功能,影响相关异常蛋白的清除。此外,CD33还能与LAIR-1等受体相互作用,并存在多种剪接异构体,这些特性进一步增加了其功能的复杂性与调控的精细度。
2. CD33靶向药物现状:从单抗到ADC技术
随着对CD33机制的深入理解,靶向该分子的药物已实现临床转化。目前的药物开发主要分为诊断与治疗两大类,且新型药物形式正在不断涌现。
2.1 诊断类应用
基于CD33在髓系细胞中的高特异性表达,诊断类单克隆抗体已广泛应用于流式细胞术(Flow Cytometry) 及免疫组化等检测技术中。它们作为核心试剂,辅助区分髓系来源细胞,为病理分型及基础科研提供数据支持。
2.2 治疗类单抗与作用机制
已上市的治疗类单抗主要通过两种机制发挥作用:
- 信号阻断: 竞争性结合CD33胞外区,抑制其与唾液酸配体的结合,从而调节髓系细胞的功能平衡。
- 免疫杀伤(ADCC): 利用抗体的Fc段结合NK细胞或巨噬细胞表面的Fc受体,触发抗体依赖性细胞介导的细胞毒作用(ADCC),特异性清除高表达CD33的异常细胞。
2.3 抗体偶联药物(ADC)
ADC药物是CD33靶向治疗的重要突破。以吉妥珠单抗为例,其由人源化抗CD33单抗与细胞毒性物质通过可切割连接子偶联而成。其作用分为三步:特异性结合、细胞内吞、溶酶体切割释放毒性物质。这种"生物导弹"模式能精准递送毒素,减少对正常组织的损伤。
3. 未来技术趋势:分子优化与场景拓展
结合当前生物技术的发展趋势,CD33靶点的研究正朝着更精准、更多元的方向迭代。
3.1 药物分子结构优化
未来的研发重点在于对抗体分子进行精细化改造。通过抗体工程技术(如人源化、亲和力成熟),提升药物对CD33的特异性,减少脱靶效应。同时,针对ADC药物,优化连接子(Linker)的稳定性 与**毒性载荷(Payload)**的选择,是降低全身不良反应、提升治疗窗口的关键。
3.2 联合治疗策略
单一靶点的治疗往往面临耐药性挑战,因此联合治疗策略(如靶向药物联合免疫调节剂)成为研究热点。通过多通路协同干预,不仅能增强疗效,还能调节局部微环境。此外,结合伴随诊断技术(如基因剪接异构体检测),实现患者的精准分层,是推动个体化医疗落地的必经之路。
3.3 应用场景多元化
目前CD33靶向药物的应用主要集中在造血系统异常相关疾病的干预。未来,随着对小胶质细胞功能研究的深入,其应用将逐步向神经系统相关疾病干预 、炎症性疾病调控等领域延伸。