一、CRISPAR-CAS9原理
CRISPAR-cas9系统敲降原理分为三步:
**1-**识别:向导RNA (gRNA)与目标DNA序列互补配对
(如P53****的编码序列) ,gRNA引导Cas9蛋白找到特定的切割位点。gRNA由CRISPR RNA (crRNA)和反式激活crRNA(tracrRNA)组成,就像一个"导航系统",带着Cas9蛋白在三碱基对PAM区域周围准确找到目标。
**2-**切割:
Cas9蛋白在找到目标后,像剪刀一样切断DNA双链,造成DNA双链断裂(DSB)。
**3-**修复:
DSBs刺激细胞修复系统启动,主要是非同源末端连接 (NHEJ,精确修复)或同源导向修复(HDR)。在修复过程中,可能发生插入或缺失,实现基因功能性沉默,或通过提供特定的DNA模板,实现对基因的精确编辑。
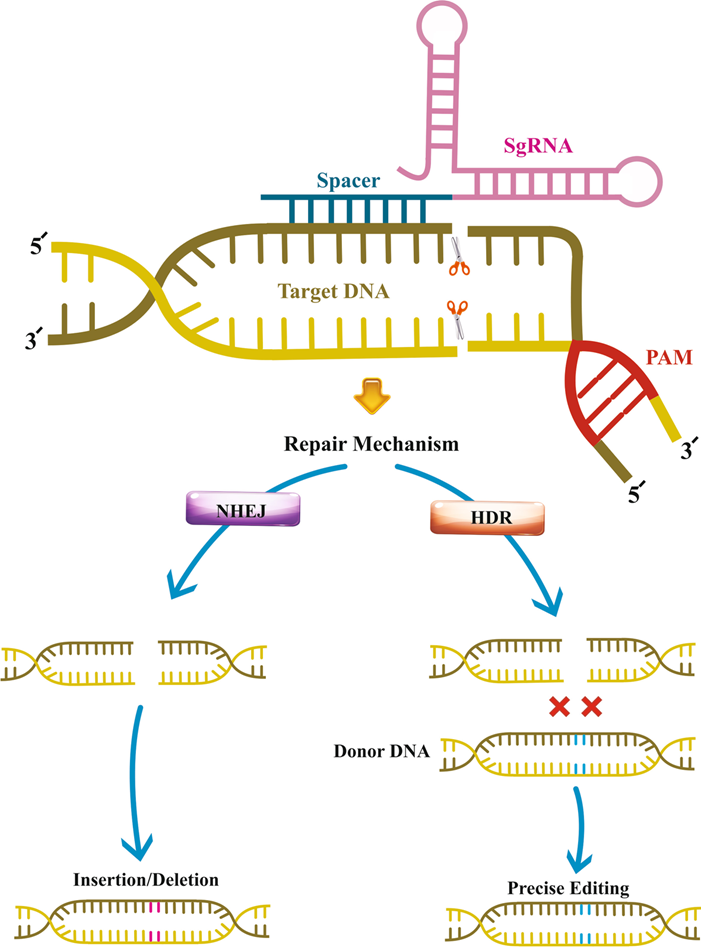
CRISPR/Cas9 application in cancer therapy: a pioneering genome editing tool.
Cell Mol Biol Lett 27, 35 (2022).
二、如何确认一个质粒敲掉的是基因的哪个外显子呢?
以PX330-P53质粒为例
1. 确认sgRNA序列,一般在gRNA scaffold前边,一般20bp左右。
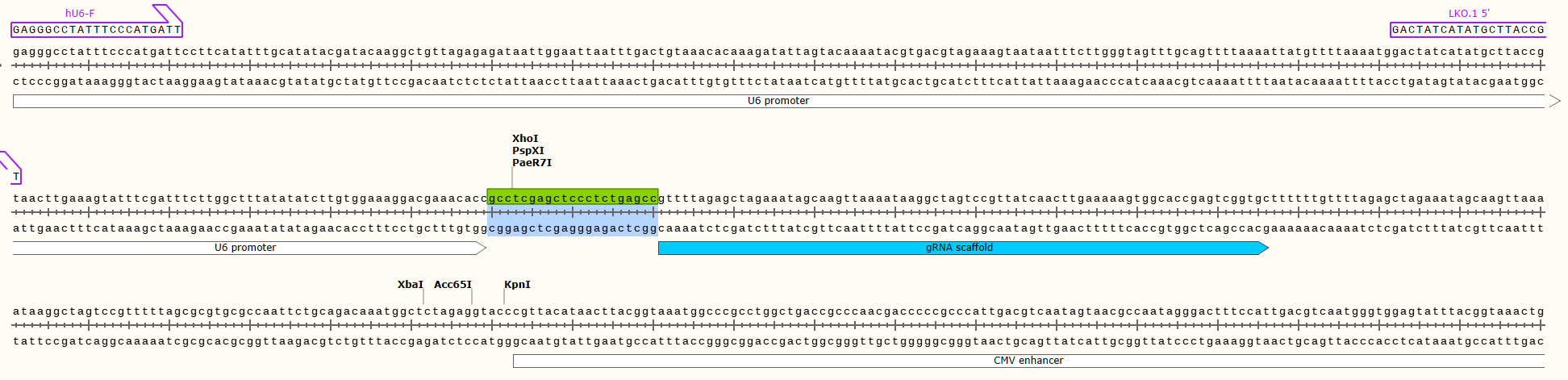
2. 将靶向序列复制粘贴进BLAST网站,输出结果如下,Download All下载文件后,得到匹配序列的具体信息位置
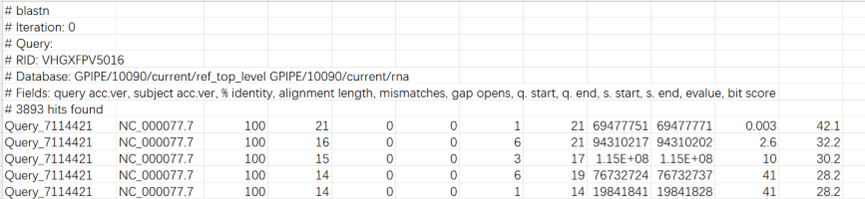
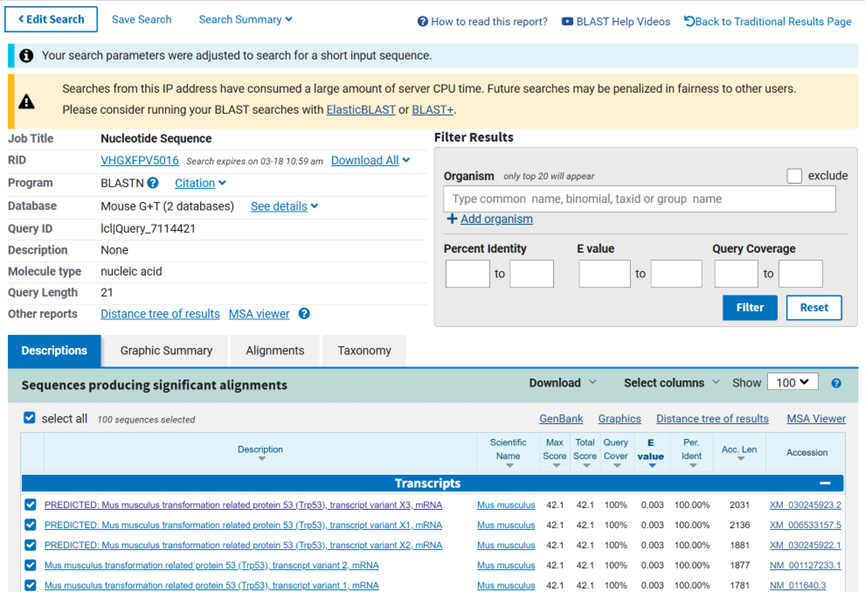
3. 将Chr11: 69477751-69477771输入UCSC网站,得到该sgRNA靶向的是小鼠的P53第二外显子。
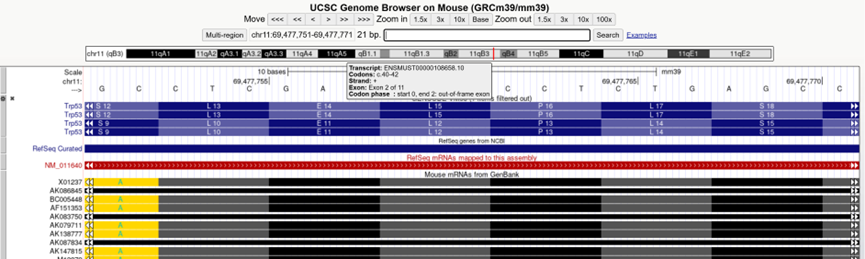
三、如何验证该基因是否敲掉了?
敲降某个基因设计sgRNA时,一个质粒中可以设计一个或两个sgRNA。
单sgRNA在基因组产生一个双链断裂(DSB),导致小片段插入或缺失,一般导致移码突变Ⅹ基因功能丧失;双sgRNAs在基因组产生两个DSBs,删除两个靶点间序列导致大片段缺失。
(一)基因层面:PCR
提取目标样本DNA,进行PCR后,①凝胶电泳,敲除条带更浅(这种方法不一定可行)②sanger测序看峰图,突变样本可能出现混合峰图,阴性对照样本应该是单个峰图(推荐sanger测序)。
(二)蛋白层面:WB/IHC
直接提蛋白跑电泳或做IHC,文献显示,小鼠样本中,crispar-cas敲除效率只有大概3%。