引言
上一篇我们解决了植物IP-MS"怎么做"的问题,厘清了动植物样本的核心差异并给出了全流程实操SOP。但在实际研究中,很多研究者即便操作完全规范,依然会得到大量假阳性结果,其根本原因就是对照组设计不符合植物系统的特殊性。
动物细胞实验常用的空载体转染对照,在植物中远远不够。**植物的生长发育、环境响应具有极强的时空特异性,基因型、组织部位、发育阶段、处理时间的微小差异,都会导致蛋白组和互作网络的剧烈重塑。**那今天我们就针对不同研究目的,带大家详解植物IP-MS的对照组设计策略。
一、所有实验的基础:底层阴性对照设计
无论研究方向如何,所有IP-MS实验都必须先设置这两类阴性对照,排除非特异性结合的干扰。
1. 表位标签消除对照(Tag-only Control)
**错误做法:**用未转化的野生型植物作为对照。
正确做法: 使用相同启动子驱动、仅表达游离标签蛋白的转基因植株作为对照**(如** GFP-only、HA-only 株系)。
▶ 原理: 融合标签本身可能与植物内源蛋白发生非特异性结合,纳米抗体也存在本底吸附倾向。通过对比**"靶蛋白-标签实验组"** 与**"仅标签对照组"**的质谱丰度,可精准排除所有与标签、抗体、磁珠结合的假阳性蛋白。
▶ **筛选标准:**严格要求log2 (FC)>2 且FDR<1.0%。
2. 遗传与环境背景的绝对一致性
对照组与实验组的植物必须满足:
▶ 相同的遗传背景**++(如同一种生态型、同一代转基因株系)++**
▶ 完全一致的生长条件**++(土壤/水培配方、光照周期、温度、湿度)++**
▶ 完全相同的收获时间点**++(如严格控制在早晨开灯后2小时,消除生物钟的影响)++**
▶ 相同的组织部位和发育阶段**++(如均取莲座叶第3-4片、均取根尖分生区)++**
二、生长发育机制研究的对照设计
植物发育是高度时空特异性的过程,蛋白互作往往只在特定细胞类型、特定发育阶段发生。
1. 空间与发育时间窗对照
▶ 若研究某蛋白在花序分生组织分化中的功能,**不能用整株植物提取蛋白,需精准解剖收集花序分生组织,**以同时期的叶肉组织作为对照,验证互作的组织特异性。
▶ 若研究根系发育,**需将根尖分为分生区、伸长区、成熟区分别进行IP-MS,相互对比,**揭示互作复合物的空间分布。
▶ 针对动态发育过程,**需设置多个发育时间点对照,**如胚胎发生的球形期、心形期、鱼雷期,追踪互作网络的动态重组。
2. 内源回补突变体的高阶对照(顶级期刊标准)
**传统缺陷:**35S组成型强启动子过表达会导致蛋白非生理性过量积累和异位定位,引入大量假阳性互作。
最优方案: 构建**"内源启动子驱动靶蛋白-标签/靶基因缺失突变体"**的遗传体系。
▶ **操作:**先用CRISPR-Cas9获得靶基因的纯合缺失突变体,再通过农杆菌转化,用该基因自身的天然启动子驱动带标签的靶蛋白回补突变体。
▶ 优势: 确保靶蛋白以生理丰度、在正确的细胞类型中表达,捕获最真实的原生互作网络。
三、逆境胁迫与抗病免疫研究的对照设计
植物胁迫响应是快速、动态的信号级联过程,互作网络在数分钟内就会发生显著变化。
1. 绝对平行的模拟处理对照
▶ 非生物胁迫(旱、盐、冷、热等): 实验组进行胁迫处理的同时,必须在同一人工气候箱内设置正常生长条件的对照组,两组植株日历年龄完全一致,同步取样淬灭。例如:实验组停水9天,对照组正常浇水9天,第9天同时取样。
▶ 生物胁迫(病原体侵染): 实验组接种病原体的同时,对照组需在相同叶片位置进行模拟接种**(如注射不含病原体的MgCl2缓冲液、注射同源无毒菌株)**,排除机械损伤导致的本底互作噪音。
2. 时序动态演进对照
单一终点时间点的采样会丢失大量关键信号。需设计多时间点的动态采样体系,例如:
▶ 0小时(基线对照)
▶ 15分钟(极早期信号事件,如钙离子内流、ROS爆发)
▶ 1小时(早期信号传导)
▶ 6小时(转录重编程)
▶ 24小时(稳态适应)
++通过纵向对比不同时间点互作蛋白的丰度消长,可重构出逆境信号从感知、传递到响应的完整时间轴。++
四、代谢调控网络研究的高阶对照:催化死亡突变体诱捕
代谢相关互作的最大特点是瞬时性和超弱亲和力:**酶与底物结合后会立即催化反应并解离,传统IP-MS几乎无法捕获这类瞬时互作。**此时需要采用"催化死亡突变体诱捕法"。
1. 实验原理
通过定点突变技术,将代谢酶**(激酶、磷酸酶、泛素连接酶等)** 催化活性中心的关键氨基酸残基替换为无活性的氨基酸**(如E→A、D→N)**,得到"催化死亡"突变体。该突变体丧失了催化功能,但保留了完整的底物结合口袋,能将底物"卡住"在结合位点,从而在IP过程中被稳定富集。
2. 精密组别设置
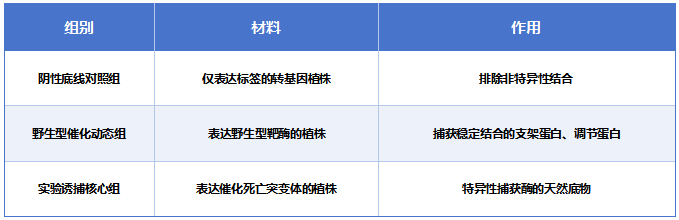
3. 数据解析逻辑
▶ **酶的底物:**在催化死亡组中高丰度富集,但在野生型组中丰度极低或未检出
▶ **支架/别构调节蛋白:**在野生型组和催化死亡组中丰度无显著差异
五、前沿补充:传统IP-MS的局限与替代方案
传统IP-MS依赖蛋白的稳定结合,**对于膜内瞬时互作、强疏水性蛋白互作的捕获能力有限。**近年来,TurboID邻近标记质谱(PL-MS)成为植物互作组学的重要补充:
▶ 原理: 将TurboID酶与靶蛋白融合,在活细胞内对靶蛋白周围10nm范围内的所有蛋白进行生物素共价标记
▶ 优势: 可使用严苛的变性裂解条件溶解细胞壁和膜蛋白,**能捕获瞬时互作,且标记时间仅需10-30分钟,**避免了热激胁迫和假阳性
总结
植物IP-MS实验的成功,是生化参数精准优化与实验逻辑严谨设计的结合。从裂解液配方的微调、RuBisCO的靶向耗竭,到针对不同研究目的的对照组矩阵设计,每一个细节都决定着数据的可信度。
随着高分辨质谱技术的进步,以及AlphaFold蛋白结构预测、TurboID邻近标记等工具的融合,我们终将能够绘制出植物细胞全景式、高时空分辨率的蛋白互作网络,为解析植物生长发育和逆境响应的分子机制提供更坚实的基础。
⬇️⬇️⬇️
50%以上验证成功率!IP-MS蛋白互作组学解决方案
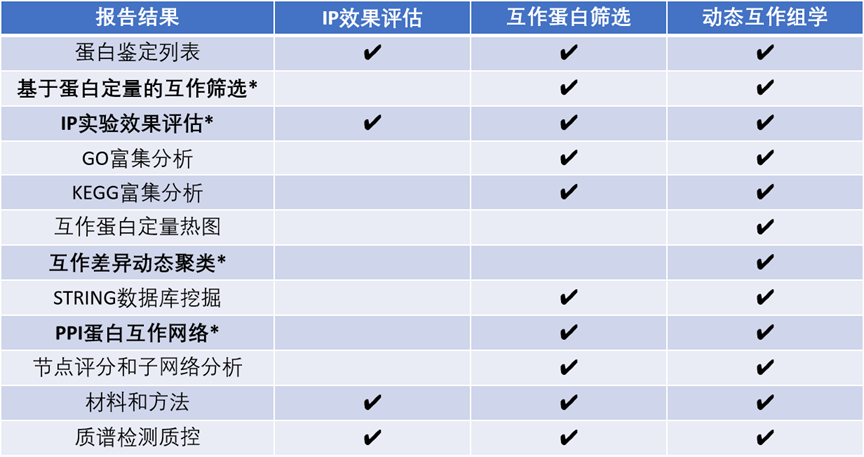
包含三项子项目:
**√ IP-MS效果评估:**评估IP-MS实验效果,提升后续实验成功率,缩短试错周期;
**√ 互作蛋白筛选:**筛选鉴定诱饵蛋白的相互作用蛋白,辅助选择关键互作蛋白;
**√ 动态互作组学:**分析不同实验条件下与诱饵蛋白相关的蛋白相互作用的动态变化。
提供IP实验获得的beads样品→以高分辨液质联用系统进行检测→基于质谱检测数据出具检测和分析报告(如下表):
参考资料
-
Lupette J, Chambaud C, Buridan M, et al. Unveiling the molecular identity of plant autophagic compartments: A proteo-lipidomic study in Arabidopsis thaliana. bioRxiv. Preprint posted online August 28, 2025. doi:10.1101/2025.08.25.671700
-
van Andel E, Roosjen M, van der Zanden S, et al. Highly Specific Protein Identification by Immunoprecipitation-Mass Spectrometry Using Antifouling Microbeads. ACS Appl Mater Interfaces. 2022;14:23102-23116. doi:10.1021/acsami.1c22734
-
Singh R, Liyanage R, Gupta C, Lay JO Jr, Pereira A, Rojas CM. The Arabidopsis Proteins AtNHR2A and AtNHR2B Are Multi-Functional Proteins Integrating Plant Immunity With Other Biological Processes. Front Plant Sci. 2020;11:232. doi:10.3389/fpls.2020.00232
-
Wiese C, Abele M, Ravikumar R, et al. Regulation of adaptive growth decisions via phosphorylation of the TRAPPII complex in Arabidopsis. J Cell Biol. 2024;223(5):e202311125. doi:10.1083/jcb.202311125
-
Zagorščak M, Abdelhakim L, Rodriguez-Granados NY, et al. Integration of multi-omics data and deep phenotyping provides insights into responses to single and combined abiotic stress in potato. Plant Physiol. 2025;197:kiaf126. doi:10.1093/plphys/kiaf126
-
Nephali L, Piater LA, Dubery IA, et al. Biostimulants for Plant Growth and Mitigation of Abiotic Stresses: A Metabolomics Perspective. Metabolites. 2020;10(12):505. doi:10.3390/metabo10120505