01
文献学习

今天分享的文献是由中山大学肿瘤防治中心蔡木炎团队联合中山大学计算机科学与工程学院、天津医科大学肿瘤医院、中山大学附属第六医院等多中心团队于2026年1月13日在《PLOS Medicine》(中科院1区top,IF=9.9)上发表的研究"Multiview deep-learning-enabled histopathology for prognostic and therapeutic stratification in stage II colorectal cancer: A retrospective multicenter study"即基于多视角深度学习的组织病理学在II期结直肠癌预后及治疗分层中的应用,该研究提出并验证了一个名为SurvFinder 的可解释深度学习框架,用于从II期结直肠癌(CRC)患者的H&E染色全切片图像(WSI)中自主识别与预后相关的组织生物标志物,并整合多视角特征进行风险分层与辅助化疗决策支持。
创新点:① 提出多视角深度学习框架,整合组织空间分布与形态学特征,全面捕捉肿瘤微环境信息。② 模型能自主识别三级淋巴结构作为预后标志物,实现无标注全切片图像的特征挖掘。③融合可解释人工智能技术,增强模型透明度,辅助理解决策依据与生物学机制。
临床价值:① 显著提升Ⅱ期结直肠癌复发风险预测准确性,优于传统临床病理指标,助力个体化预后评估。② 可识别辅助化疗获益人群,优化治疗决策,避免低危患者过度治疗与高危患者治疗不足。③基于常规H&E切片自动化分析,成本低、易推广,有望成为临床实用的辅助分层工具。
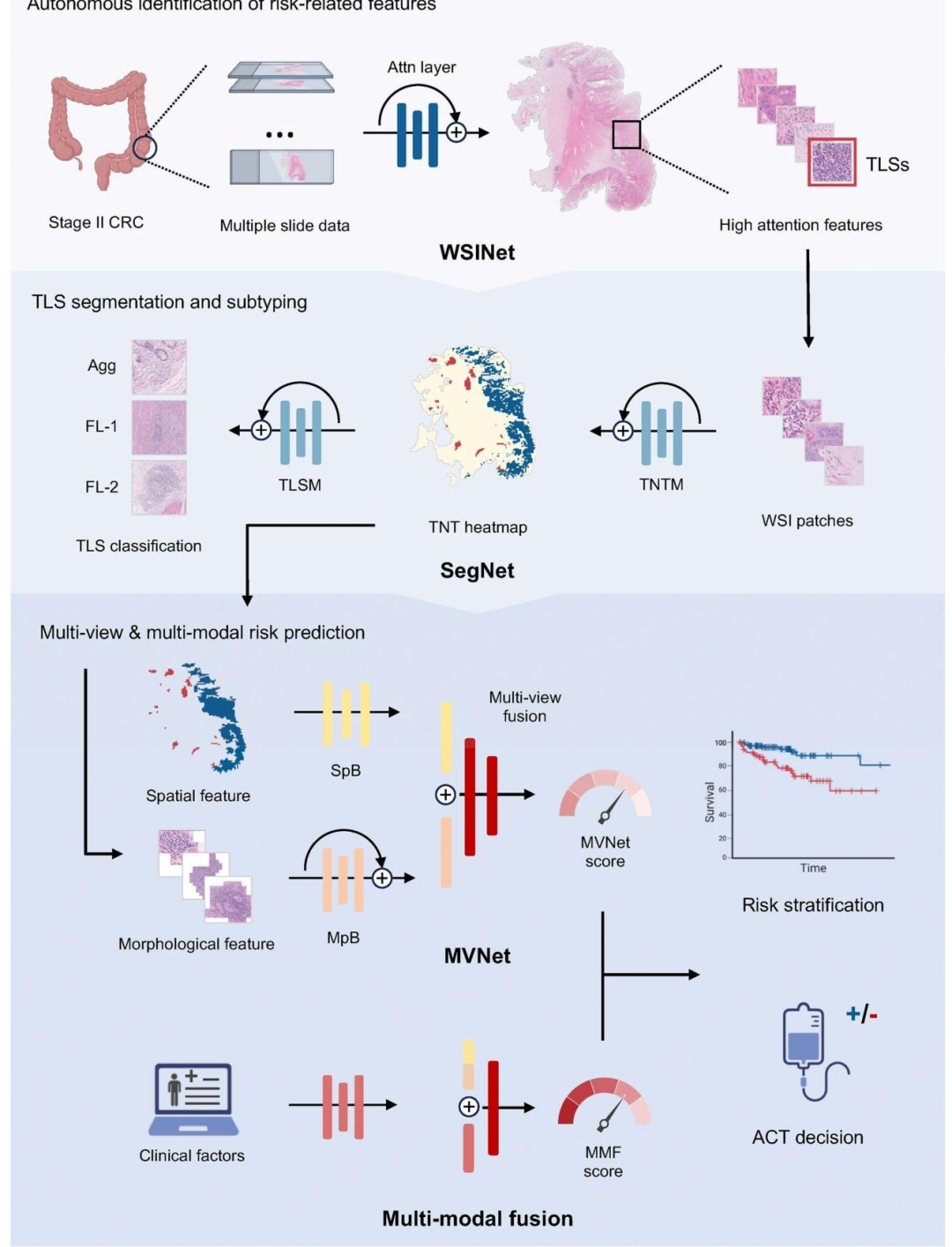
图 1:SurvFinder框架工作流程
风险相关组织特征自主识别:以II期结直肠癌多切片数据为输入,通过WSINet(注意力机制模型)识别高关注度组织特征,核心锁定三级淋巴结构(TLSs)。
预后生物标志物多分类分割:SegNet包含两个子模型------TNTM(TLS-正常-肿瘤组织分类模型)生成组织预测热图,TLSM(TLS亚型分类模型)将TLS进一步分为Agg(聚集型)、FL-1(初级滤泡)、FL-2(次级滤泡)三类。
多视角与多模态风险预测:MVNet通过空间分支(SpB)提取TLS位置/面积等空间特征、形态分支(MpB)提取TLS成熟度等形态特征,经多视角融合生成风险评分;MMF(多模态融合模型)整合MVNet特征与临床因素,最终输出用于风险分层和辅助化疗(ACT)决策的预测结果。
02
研究背景及目的
研究背景
II期结直肠癌是全球第三大常见恶性肿瘤,尽管已接受标准手术治疗,仍有约20%的患者面临肿瘤复发的风险 ,导致其成为癌症相关死亡的主要原因之一。目前,临床决策主要依赖美国国家综合癌症网络指南推荐的高危临床病理特征 (如pT4分期、局部穿孔、淋巴结采样不足等)来判断是否需行辅助化疗。然而,辅助化疗对传统高危患者的疗效有限,且伴随显著的毒副作用、经济负担及约0.5%-1%的死亡率 ,凸显了现有分层工具的不足。近年来,基因与分子生物标志物(如错配修复状态、循环肿瘤DNA等)虽显示出潜力,但其临床应用受限:仅少数患者(<15%)为错配修复缺陷型 ,且多数检测成本高昂、操作复杂,难以在临床广泛推广。因此,亟需一种高效、可及且基于常规临床数据的预后预测工具 。苏木精-伊红染色组织病理切片作为每位患者的常规检查项目,蕴含丰富的形态学信息,结合近年来数字病理与深度学习技术的快速发展,为从全切片图像中自动提取预后相关特征提供了可能。本研究旨在利用深度学习技术,挖掘这些常规切片中的隐藏信息,以弥补现有分层方法的不足,为II期结直肠癌的个体化治疗提供新思路。
研究目的
本研究旨在开发并验证一个可解释的深度学习框架------SurvFinder ,以从常规H&E染色全切片图像中自主识别与预后和治疗反应相关的组织学生物标志物 ,从而实现II期结直肠癌患者的精准风险分层与治疗指导。具体目标包括:首先,构建一个能够从海量病理图像中自动学习并提取关键预后特征 的模型,尤其关注三级淋巴结构 等具有潜在生物学意义的组织形态;其次,通过多视角融合技术 ,整合TLS的空间分布、形态成熟度等多维度特征,构建一个超越单一特征或传统临床参数的高性能预后预测模型 ;再者,利用可解释人工智能技术 揭示模型决策依据,确保其预测结果具有临床可理解性与生物合理性,增强医生信任度;最后,在多中心回顾性数据集 (共1,604名患者,6,950张切片)上严格验证模型的泛化能力,评估其在识别高危复发人群及预测辅助化疗获益 方面的效能。最终,本研究希望通过提供一个自动化、低成本、可解释的AI辅助工具,帮助临床医生更准确地区分II期结直肠癌患者的复发风险,优化辅助化疗决策,实现真正的个体化精准医疗。
03
数据和方法
研究数据
来源:4个独立队列(3个中国多中心队列 + TCGA公开数据)
样本量:6950张H&E切片,来自1604例II期CRC患者
队列划分:
内部训练/验证集(Internal-CRCII):743例
外部验证集1(External-CRCII-1):352例
外部验证集2(External-CRCII-2):331例
TCGA验证集(TCGA-CRCII):178例
技术方法
(1)模型架构(SurvFinder框架)
WSINet:注意力机制多实例学习模型,从WSIs中识别预后相关组织特征(如TLSs),聚合切片特征生成患者水平预测。
SegNet:包含2个分类器------TNTM(TLS-正常-肿瘤组织分类)和TLSM(TLS表型分类:Agg/FL-1/FL-2),生成组织热图并分割生物标志物区域。
MVNet:多视角融合模型,含空间分支(SpB,提取TLS位置、面积、与肿瘤距离等特征)和形态分支(MpB,提取TLS成熟度等形态特征),实现特征融合预测。
MMF:多模态融合模型,整合MVNet特征与14项临床病理参数(如肿瘤分化、MMR状态),生成最终预后评分。
(2)训练与验证
训练策略:Internal-CRCII队列5折交叉验证,模型训练500个epoch(预后模型)/100个epoch(分类模型),优化器采用AdamW/SGD,损失函数为交叉熵。
验证策略:外部队列直接应用训练后模型(无重训练),避免信息泄露。
评估指标:AUROC(预测准确性)、Kaplan-Meier生存分析(风险分层)、Cox回归分析(独立预后价值)。
(3)可解释性分析
使用注意力热图、SHAP方法解释模型决策
结合病理学家注释,验证特征生物学意义
04
实验结果
(1)模型性能
WSINet:内部队列AUROC=0.695(95% CI:0.639-0.751),识别出TLSs为关键预后特征。
SegNet:TNTM(组织分类)AUROC均>0.999,TLSM(TLS表型分类)AUROC=0.91-0.985,分割准确性优异。
MVNet:四个队列AUROC分别为0.827、0.805、0.805、0.712,显著优于单分支模型和传统临床参数(HR=8.23,95% CI:5.43-12.47,p<0.001)。
MMF:多模态融合后性能进一步提升,各队列AUROC均高于MVNet和单纯临床模型。
(2)风险分层与化疗指导
风险分层:MVNet将患者分为高低风险组,所有队列中两组无复发生存(RFS)差异显著(p<0.0001)。
化疗获益:高风险组接受ACT后RFS显著改善(Internal-CRCII:p=0.023;External-CRCII-1:p=0.026;External-CRCII-2:p=0.00081),低风险组无显著获益。
(3)可解释性结果
空间特征:肿瘤边缘1-4.5mm处的TLSs与良好预后强相关。
形态特征:成熟TLS(FL-2)在无复发组更常见,不成熟TLS(Agg/FL-1)在复发组更富集。
不良预后特征:肿瘤平均面积增大与复发风险升高相关。
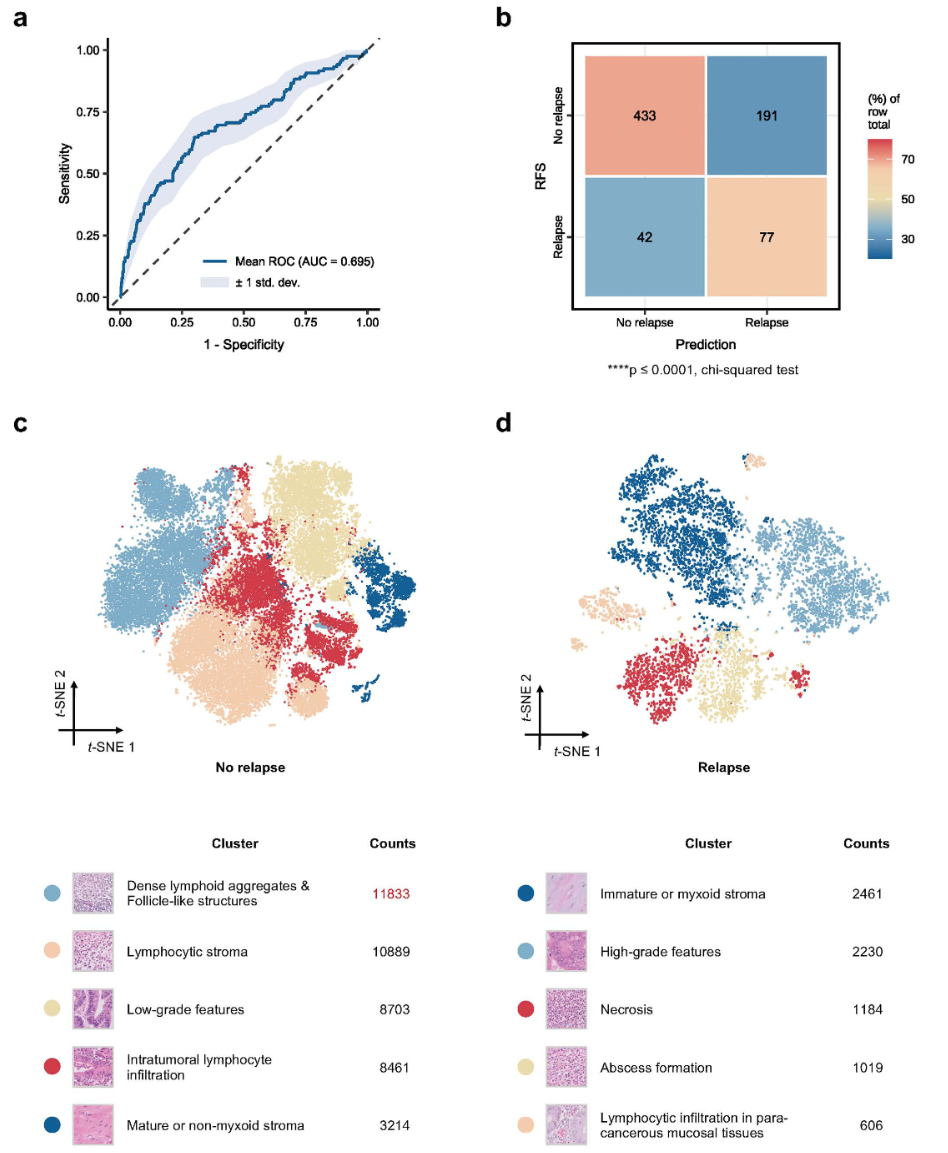
图 2:WSINet识别预后相关组织生物标志物的性能与解释
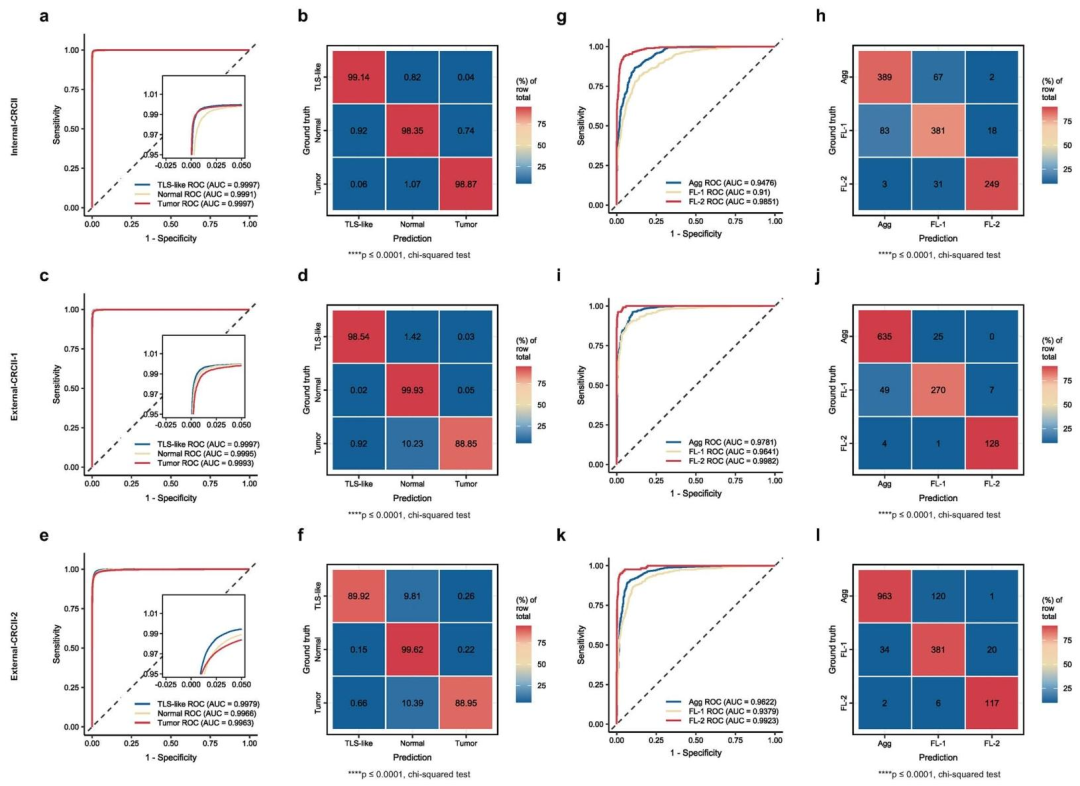
图 3:SegNet对多类别组织生物标志物的分割性能
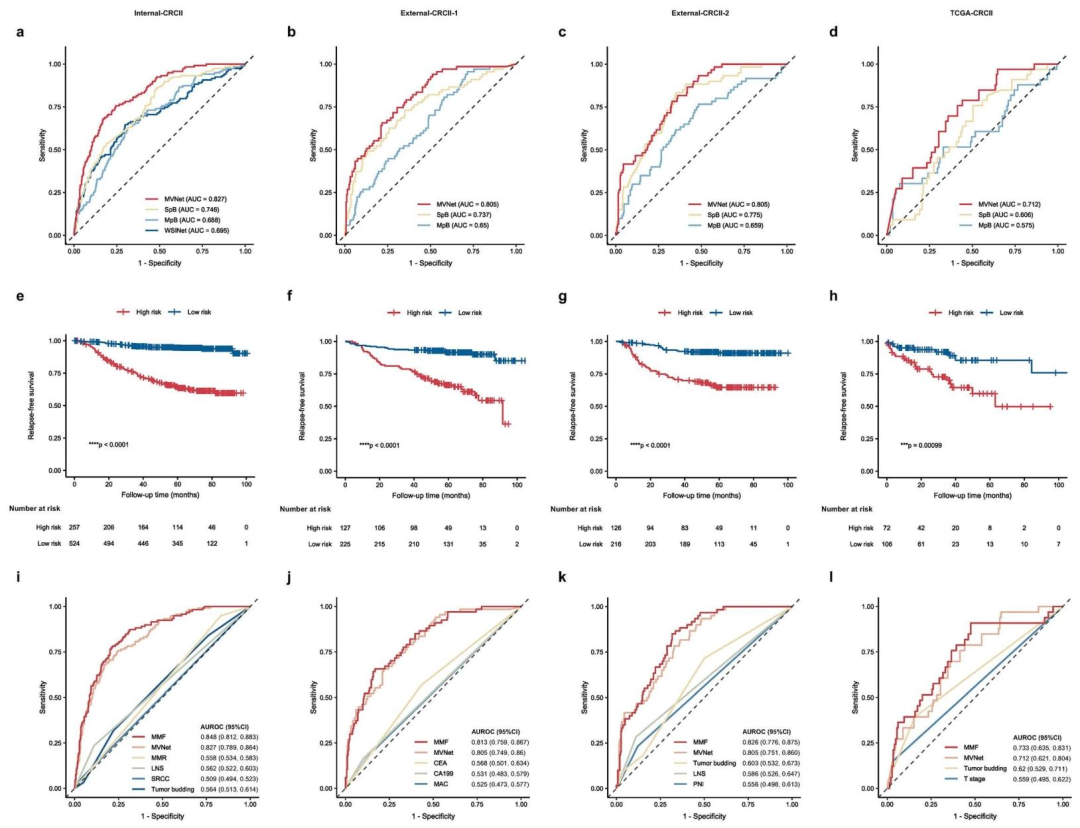
图 4:SurvFinder的预测与预后性能
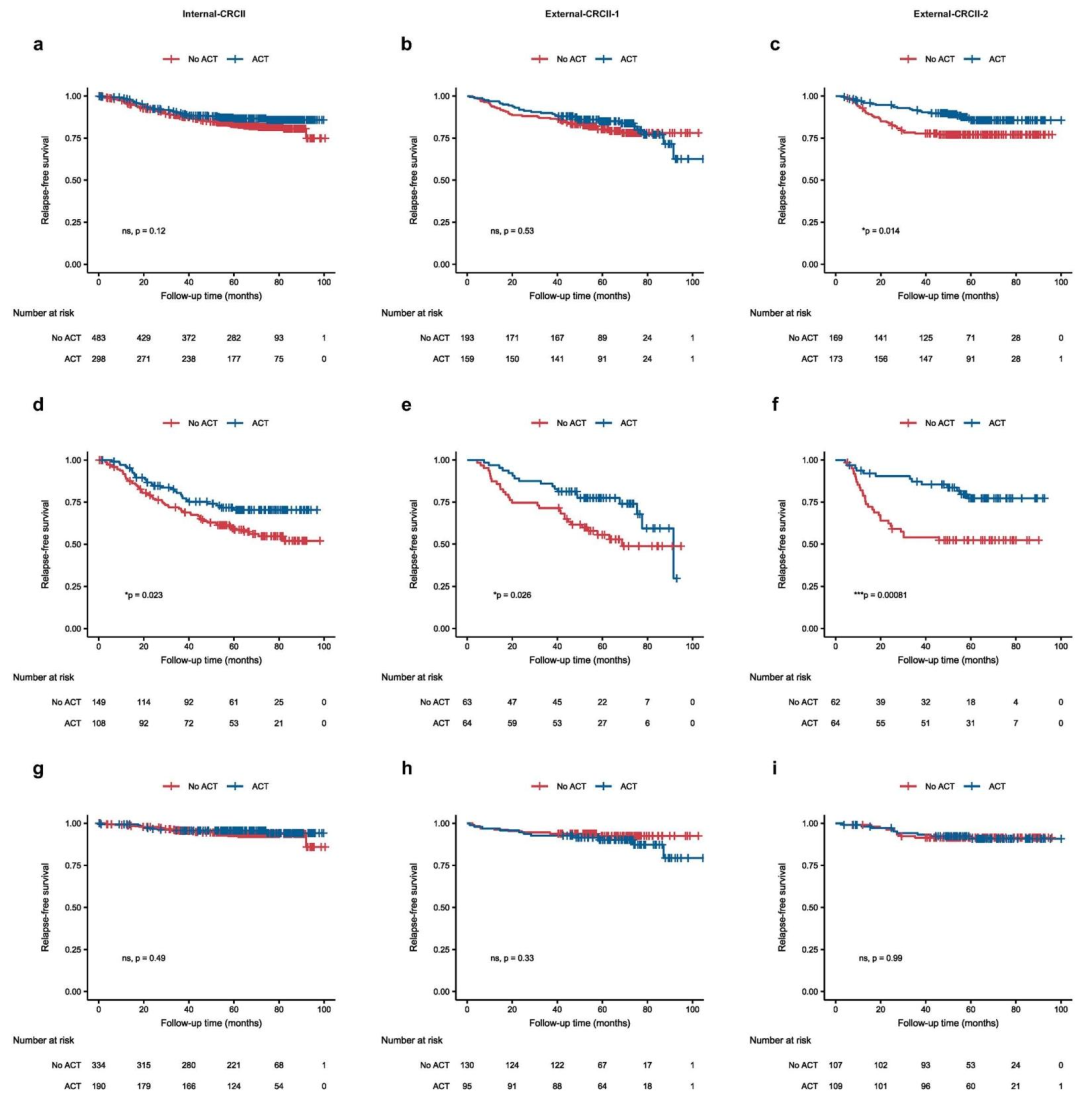
图 5:SurvFinder指导辅助化疗(ACT)决策的性能
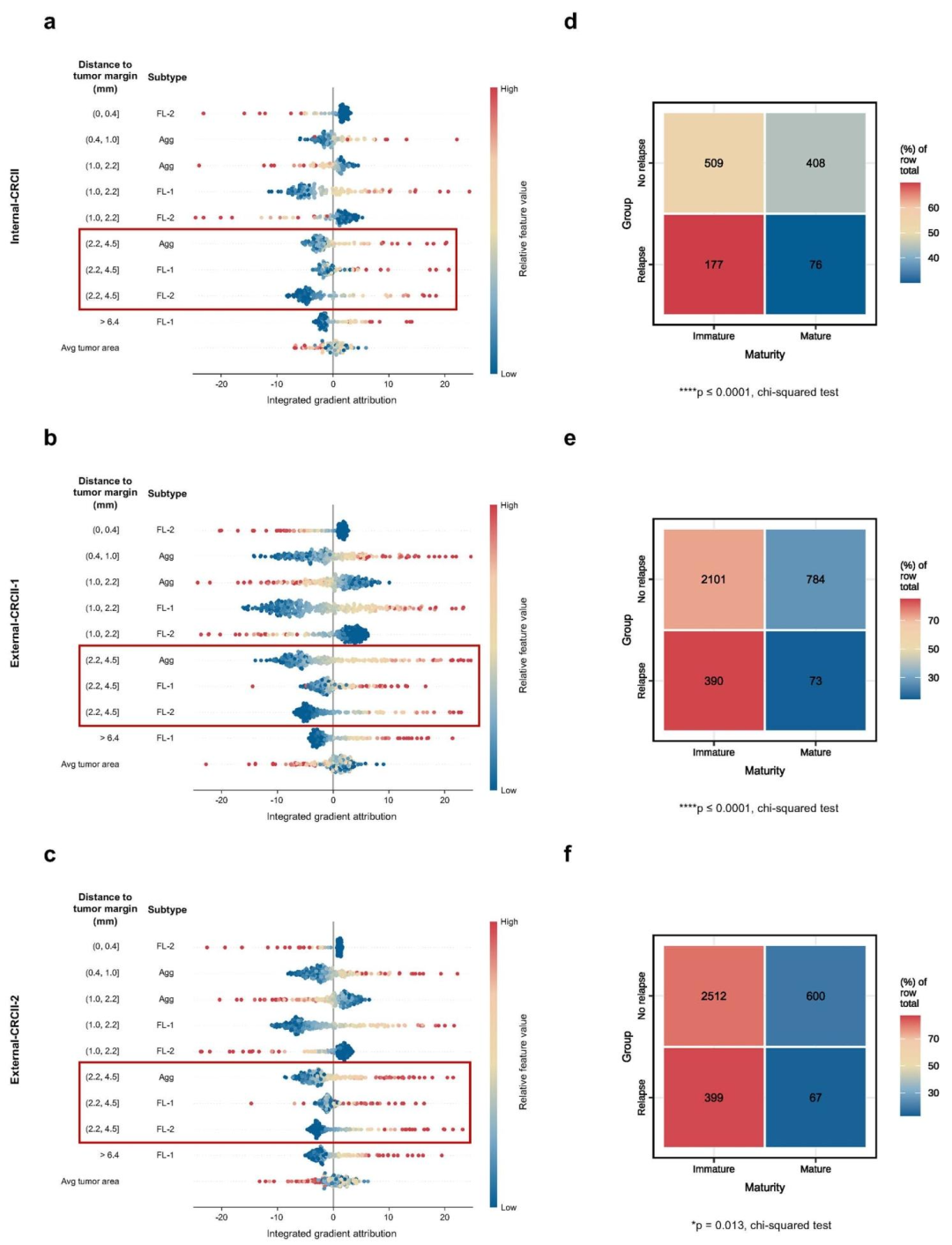
图 6:SurvFinder的可解释性分析
05
研究结论
本研究通过开发并验证名为 SurvFinder 的可解释深度学习框架,成功利用常规 H&E 染色病理全切片图像(WSIs) ,实现了对 II 期结直肠癌(CRC)患者的自动化、个体化预后与治疗分层 。该研究首次通过多中心回顾性数据(共计1,604名患者)系统证实,深度学习能够自主识别出三级淋巴结构(TLS)作为关键的组织学生物标志物 。通过整合TLS的空间分布(如距肿瘤边缘的距离)与形态学成熟度等多视角特征 ,模型(MVNet)在四个独立数据集中均展现出显著优于传统临床病理参数的预测性能(AUROC最高达0.827)和独立的预后价值(风险比HR=8.23) 。更重要的是,模型能够有效识别出可能从辅助化疗(ACT)中获益的高危患者亚组 ,为个体化治疗决策提供了新依据。尽管存在回顾性研究的固有局限 ,且模型尚未进行前瞻性临床部署验证,但该工作证明了人工智能从常规病理切片中提取可解释、可临床转化特征的巨大潜力 ,为开发 AI 辅助的标准化风险分层工具奠定了重要基础。
参考文献:Zhao Z, Chen D, Wang R, Zhang X, Wen X, Zheng X, Liu S, Chen H, Zhang Y, Huang D, Zheng C, Ma M, Xie D, Sun Y, He X, Cai M. Multiview deep-learning-enabled histopathology for prognostic and therapeutic stratification in stage II colorectal cancer: A retrospective multicenter study. PLoS Med. 2026 Jan 13;23(1):e1004614. doi: 10.1371/journal.pmed.1004614.