01
导语
各位同学,大家好。现在做影像组学,如果还只停留在"提取特征---建个模型---算个AUC",那就像拿着一把尺子量出了肿瘤大小,却说不出它为什么长得快 。别人一问:你的影像特征到底对应什么生物学过程?背后有没有通路、细胞亚群、关键基因在撑腰?瞬间就成了黑箱本箱 。而真正能发高分、经得起推敲的研究,都在干同一件事------给影像组学找"生物学娘家" ,让MRI上的每个纹理、每个信号异质性,都能和微观的ECM重塑、TGF‑β信号、ITGB8高表达亚群对上话。今天咱们就通过这篇2026年发表于《Research》的膀胱癌论文,看看作者如何用深度学习算出一个"混合肿瘤‑间质比例(MTSR)" ,然后一路从批量转录组追到单细胞、从WGCNA追到SHAP,最后再反过来用mpMRI的放射组学去预测这个MTSR ,形成"表型→机制→影像 "的完美闭环。咱们一起拆解这套"不硬凑、有因果、可复现 "的机制挂靠方法论,帮大家从"只会算分的工具人",升级成"能讲清疾病故事的影像组学研究者"。

**★题目:**A Deep Learning-Generated Mixed Tumor--Stroma Ratio for Prognostic Stratification and Multi-omics Profiling in Bladder Cancer
(基于深度学习生成的混合肿瘤-间质比用于膀胱癌预后分层与多组学分析)
★期刊:《Research》(中科院1区,IF=10.9)
**★研究疾病:**膀胱癌
**★生物学机制:**ITGB8-WNT轴
**★发表时间:**2026年1月
02
研究背景-从 "临床问题" 落到 "生物学问题"
膀胱癌是泌尿系统最常见的恶性肿瘤之一,其高复发率和进展倾向 给临床管理带来持续挑战。根据肌层浸润深度,膀胱癌分为非肌层浸润性和肌层浸润性两类,两者的治疗策略和预后差异显著。目前,病理学检查是膀胱癌分期和分级判定的金标准 ,其中苏木精-伊红染色是观察组织结构和细胞细节的常规技术。然而,传统病理诊断依赖人工阅片,不仅耗时费力,而且存在显著的观察者间变异 ,尤其是在肿瘤与正常组织边界模糊、组织类型混杂的复杂病例中。此外,尽管TNM分期系统为治疗决策提供了基础框架,但同一分期患者预后差异巨大 ,提示现有分期系统无法充分捕捉肿瘤生物学行为的异质性。近年来,数字病理和人工智能技术的兴起 为全切片图像的自动化分析提供了可能。通过深度学习模型,可以自动识别和分类不同组织类型、检测细微组织学特征,甚至预测临床结局。其中,肿瘤-间质比例 作为反映肿瘤与微环境相互作用的量化指标,在多种癌症中被证实与预后相关,但其在膀胱癌中的自动化量化方法、多中心验证、分子机制及术前无创评估仍属空白。因此,亟需开发一种可重复、可解释的深度学习工具,系统解析肿瘤-间质混杂程度的生物学内涵,并将其转化为临床可用的预后标志物。
03
研究目的(明确写出"三层目的")
本研究旨在围绕膀胱癌中混合肿瘤-间质比例,完成从技术开发、临床验证到机制解析与影像转化的三层研究目标 。第一层(技术层) :构建一个基于ResNet50的卷积神经网络模型,实现对膀胱癌H&E染色全切片图像的全自动分割与分类 (共9类组织+背景),并量化计算混合肿瘤-间质比例,以消除人工评估的主观变异。第二层(临床层) :在多中心、大样本外部队列中系统验证混合肿瘤-间质比例的预后价值 ,通过Cox回归、Kaplan‑Meier分析、meta分析及nomogram构建,证明其作为独立预后因子的稳定性和临床实用性,并比较其与TNM分期的预测效能。第三层(机制层与转化层) :利用批量RNA测序和单细胞RNA测序 ,从通路富集、免疫浸润、细胞异质性、伪时间轨迹及转录因子调控网络等多个维度,揭示高/低混合肿瘤-间质比例肿瘤的分子程序差异 ,锁定关键驱动基因(如ITGB8);同时,构建基于术前多参数MRI的影像组学随机森林模型,实现混合肿瘤-间质比例的无创术前预测,为非侵入性风险分层和精准治疗决策提供依据。
04
研究思路(最核心:怎么挂靠机制)
本研究的核心思路是以深度学习量化的病理表型(混合肿瘤-间质比例)为锚点,向上连接临床预后,向下深入多组学机制,再横向拓展至影像组学无创预测 ,形成"表型驱动机制、机制解释表型、影像映射表型 "的闭环逻辑。第一步,模型开发与预后验证 :采用TCGA膀胱癌全切片图像训练ResNet50模型,实现像素级组织分类,计算混合肿瘤-间质比例;然后在5个独立外部队列中验证其对总生存期的预测价值,并结合N分期构建nomogram。第二步,机制挂靠------从批量组学到单细胞 :首先通过WGCNA识别与混合肿瘤-间质比例显著相关的基因模块,GSEA富集分析发现高混合肿瘤-间质比例肿瘤中TGF‑β、WNT、ECM重塑等通路激活;然后利用单细胞RNA测序,精准定位一个ITGB8高表达的尿路上皮细胞亚群 ,该亚群处于终末分化状态、WNT信号活跃、凋亡抑制,并通过SCENIC分析揭示BPTF、SOX4等上游转录因子。第三步,细胞通讯与功能验证 :通过配体-受体分析证明ITGB8高表达细胞作为"发送者"主导信号输出。第四步,影像组学转化 :从术前mpMRI中提取T2WI和DCE序列的放射组学特征,经mRMR筛选后构建随机森林分类器,实现混合肿瘤-间质比例高/低状态的术前预测。通过这一递进式思路,将宏观影像、病理表型与微观分子机制有机串联,为膀胱癌的精准分层提供了从机制到临床的全链条证据。
05
数据和方法(机制部分怎么设计)
数据 :本研究共纳入来自TCGA的379例膀胱癌患者(450张WSI) 用于模型训练、内部验证及预后分析;来自5个外部队列(GD2H、STPH、YJSH、ZSSY、PN)的1 053例患者(1 271张WSI) 用于外部验证MTSR的预后价值;来自GD2H队列的6例新鲜肿瘤组织(高MTSR 3例,低MTSR 3例) 用于单细胞RNA测序 以解析分子机制;来自STPH队列的109例患者(125张WSI)的术前mpMRI数据 用于构建影像组学模型以无创预测MTSR状态。
方法 :H&E全切片图像标注 (9类组织+背景,Reinhard颜色归一化)→ ResNet50 训练 (迁移学习,SGD,内外部验证)→ 全切片分割及组织比例计算 (滑动窗口,边缘过滤)→ 预后分析 (Cox回归、Kaplan‑Meier、固定/随机效应meta分析、nomogram构建)→ 批量转录组分析 (WGCNA识别MTSR相关模块,GSEA/GSVA通路富集,CIBERSORT免疫浸润)→ 单细胞分析 (Seurat聚类、UMAP,Monocle伪时间轨迹,SCENIC转录因子调控网络,细胞通讯分析)→ 影像组学模型 (mpMRI中T2WI与DCE序列ROI勾画,PyRadiomics提取1781个特征/序列,mRMR筛选10个关键特征,随机森林分类器训练与验证)。
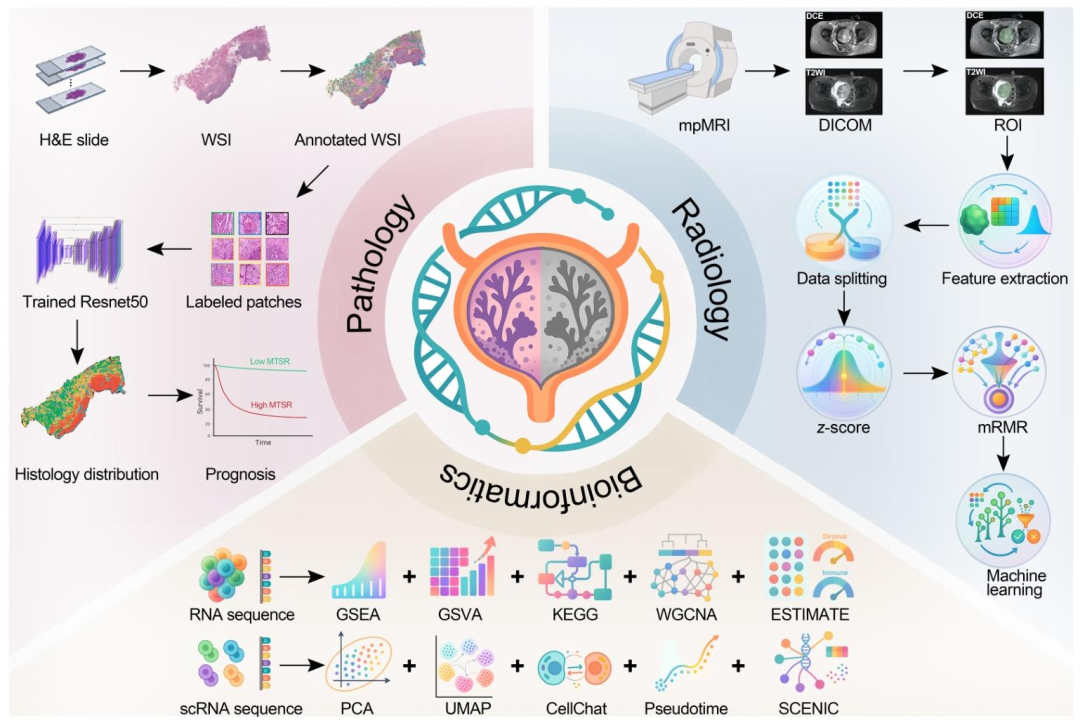
图 1:研究整体工作流程图
06
研究结果("从表型到机制")
1. 模型性能 :ResNet50对9类组织及背景的分类准确率均超过90%,Cohen's κ > 0.95,t‑SNE显示不同组织类别在特征空间形成清晰分离的簇,证明模型具有卓越的判别能力和可重复性。
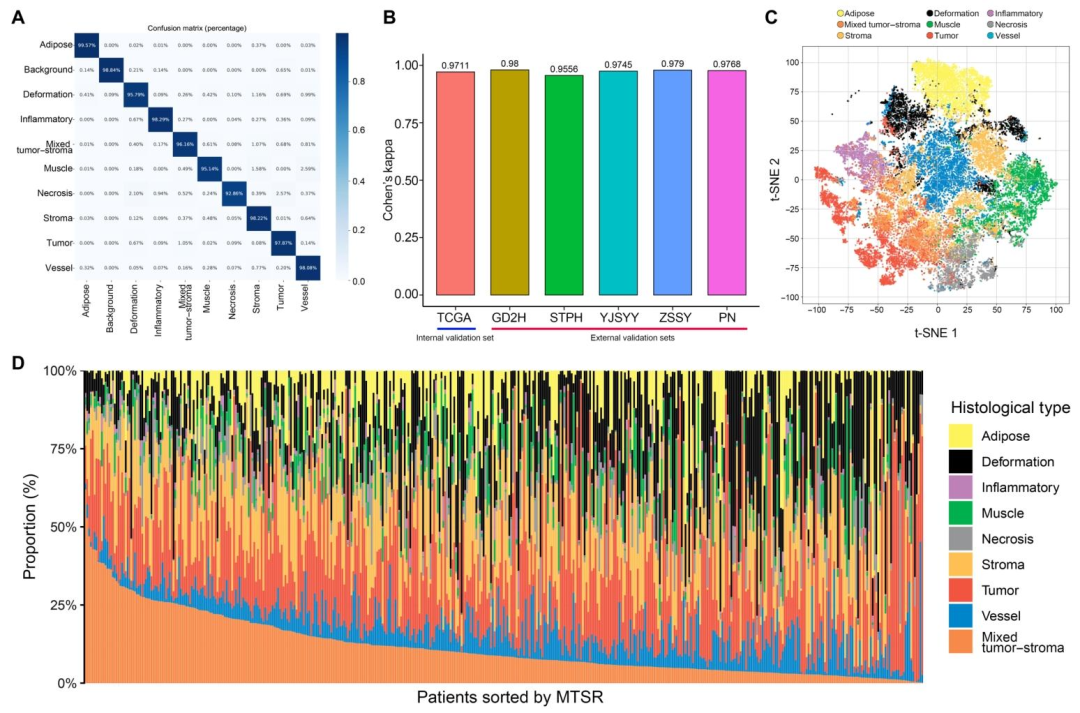
图 2(模型性能) :图2A混淆矩阵显示ResNet50对10类组织(含混合肿瘤‑间质)分类准确率>90%,图2B显示Cohen's κ >0.95,图2C的t‑SNE可视化展示不同组织类别的深度特征在空间中形成清晰分离的簇。这些结果证明深度学习模型能够精准识别"混合肿瘤‑间质"这一关键组织学表型,为后续将该表型与分子机制(如ECM重塑、TGF‑β信号)关联提供了可靠的技术基础。
2. MTSR的预后价值 :在TCGA及5个外部队列中,高MTSR患者的总生存期显著缩短(所有P < 0.001),固定效应meta分析合并HR = 1.04(95% CI: 1.03--1.05),且MTSR与N分期是独立的预后因子。
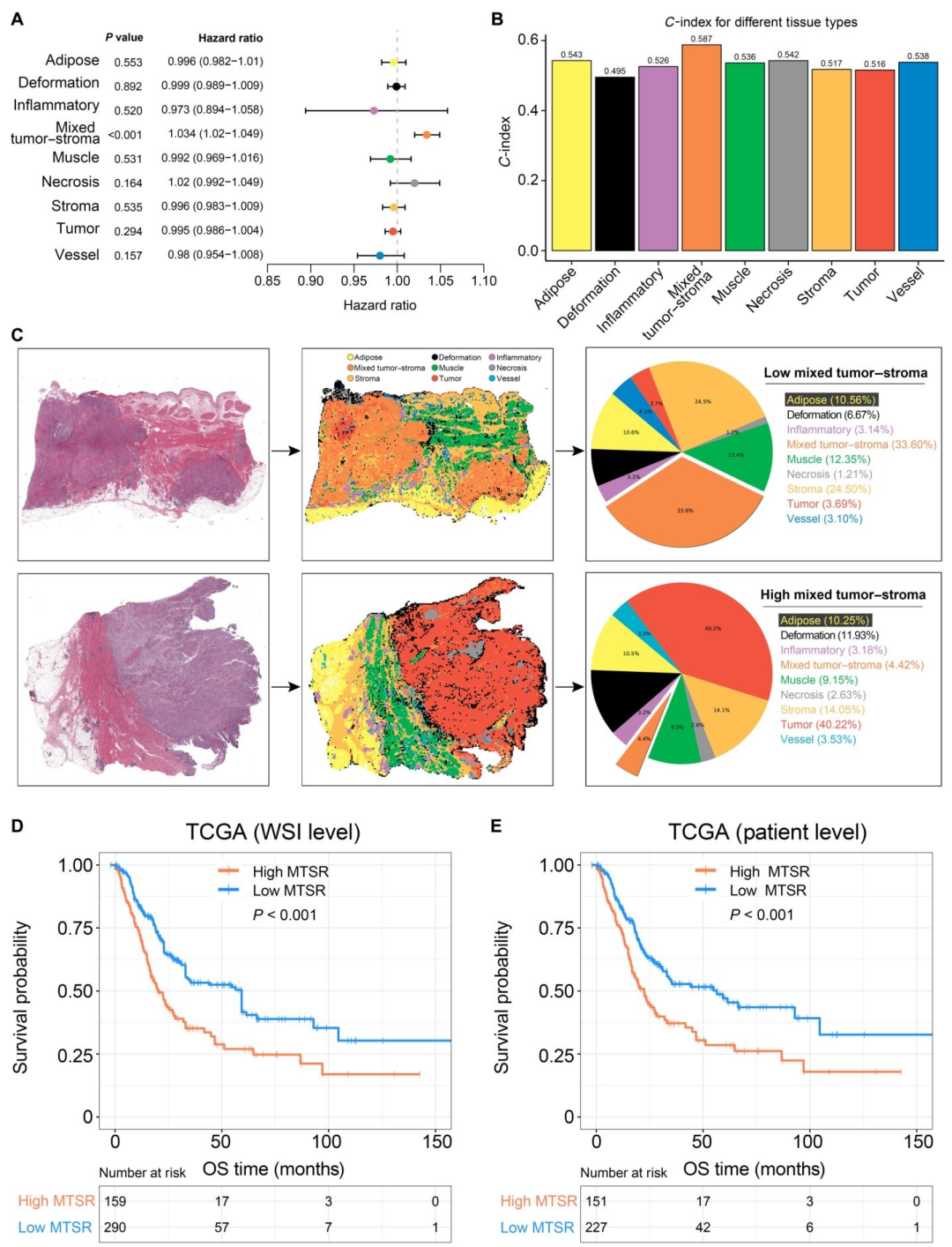
图 3(MTSR预后价值) :图3A单变量Cox回归显示MTSR是唯一有显著预后意义的组织比例(HR=1.034),图3B中MTSR的C‑index最高(0.587),图3C展示高/低MTSR的代表性WSI,图3D‑E的Kaplan‑Meier曲线表明高MTSR患者总生存期显著缩短。该图确立了MTSR作为独立预后生物标志物的地位,而预后差异本质上由肿瘤‑间质互作的分子程序(如WNT、TGF‑β)驱动,为后续影像组学预测MTSR提供了临床必要性。
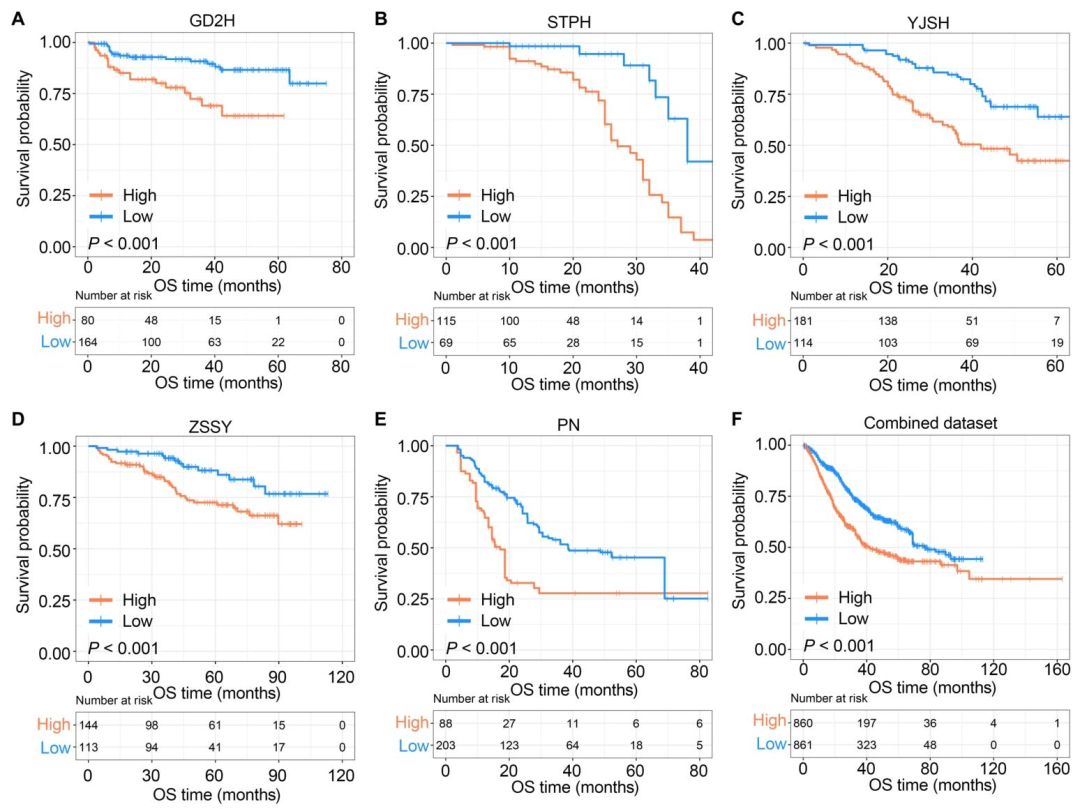
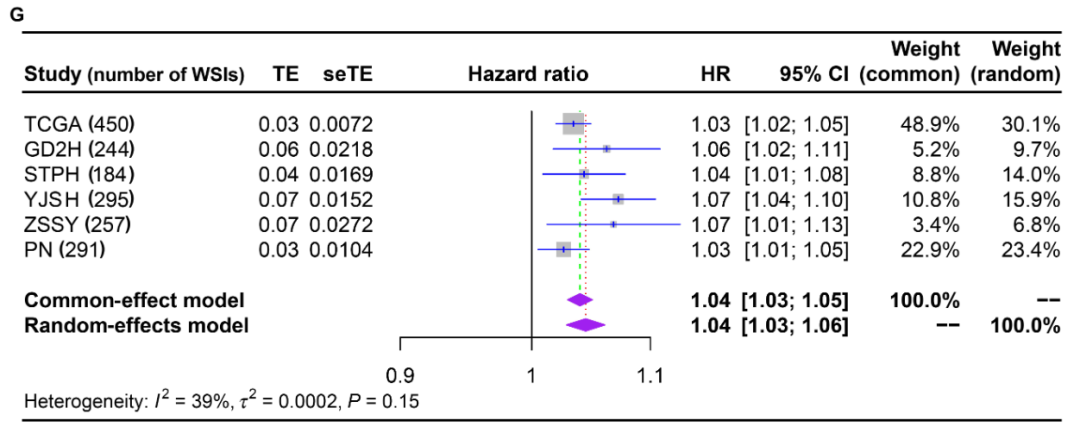
图 4(外部验证) :图4A‑E显示在5个独立外部队列(GD2H、STPH、YJSH、ZSSY、PN)中,高MTSR患者均具有更差的总生存期(所有P<0.001),图4F合并队列分析一致,图4G固定效应meta分析合并HR=1.04(95%CI:1.03‑1.05)。该图验证了MTSR预后价值的跨中心稳健性,说明MTSR反映的肿瘤‑间质混杂程度是一个普遍存在的生物学特征,而非单中心偏倚,从而支持利用影像组学在不同医疗中心间推广MTSR术前预测。
3. 预后模型构建 :联合MTSR与N分期的nomogram在C‑index和时间依赖AUC上均优于单一指标,校准曲线显示预测与观察结局高度一致,决策曲线证实其临床净获益优于传统病理特征。
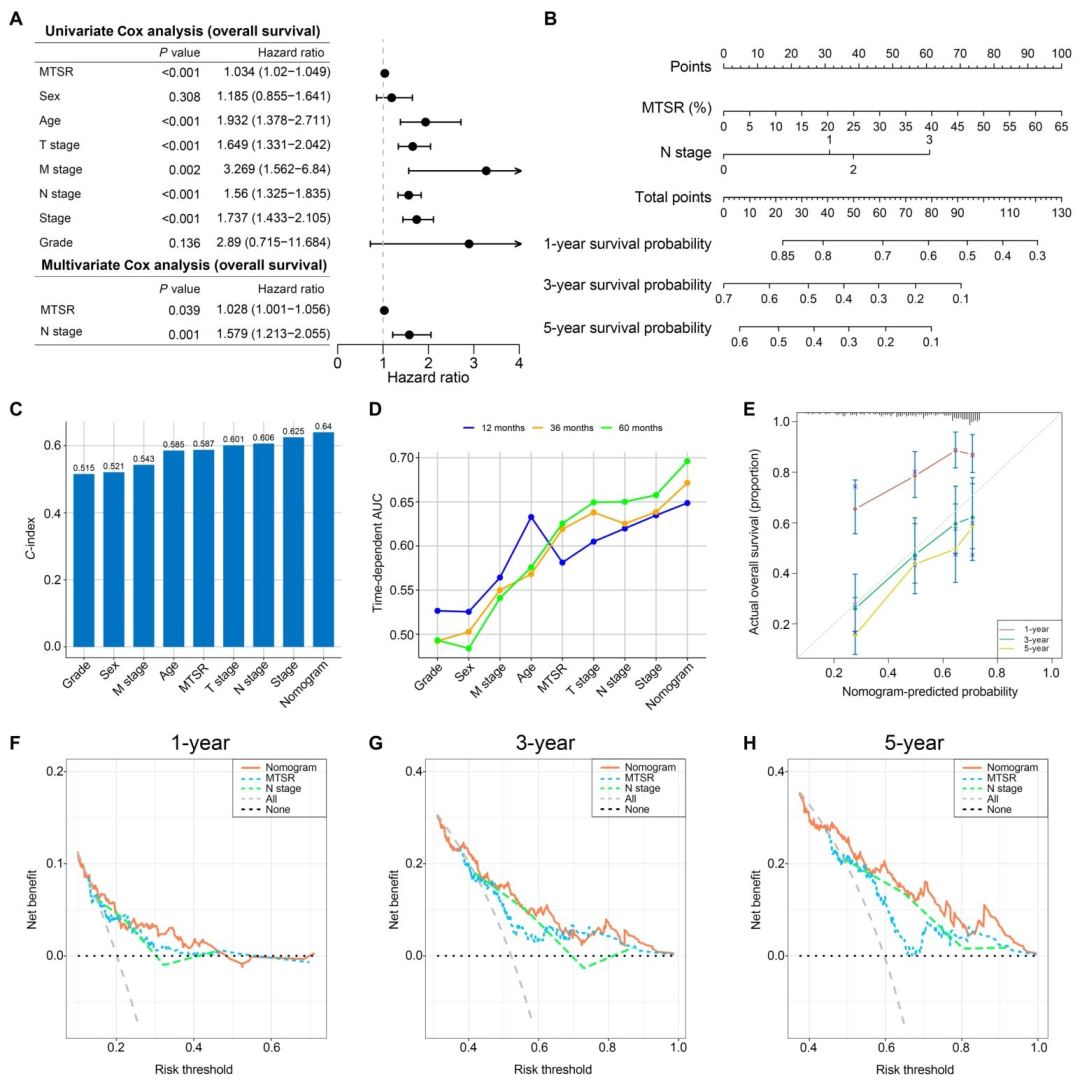
图 5(预后nomogram) :图5A多变量Cox显示MTSR和N分期为独立预后因子,图5B构建nomogram,图5C‑D显示MTSR+N分期的C‑index和AUC优于单一指标,图5E校准曲线显示良好一致性,图5F‑H决策曲线证明nomogram的临床净获益最高。该图表明MTSR具有与病理TNM分期相当的预后信息量,联合使用可提升风险分层效能。从机制上看,MTSR整合了间质微环境(ECM、免疫细胞)的侵袭性信号,这些信号同样可被影像纹理特征间接捕捉。
4. 批量转录组特征 :高MTSR肿瘤富集TGF‑β/WNT信号、ECM受体交互、细胞黏附分子;低MTSR肿瘤富集尿路上皮分化及干扰素‑γ通路。高MTSR组M0/M1/M2巨噬细胞浸润显著增加。
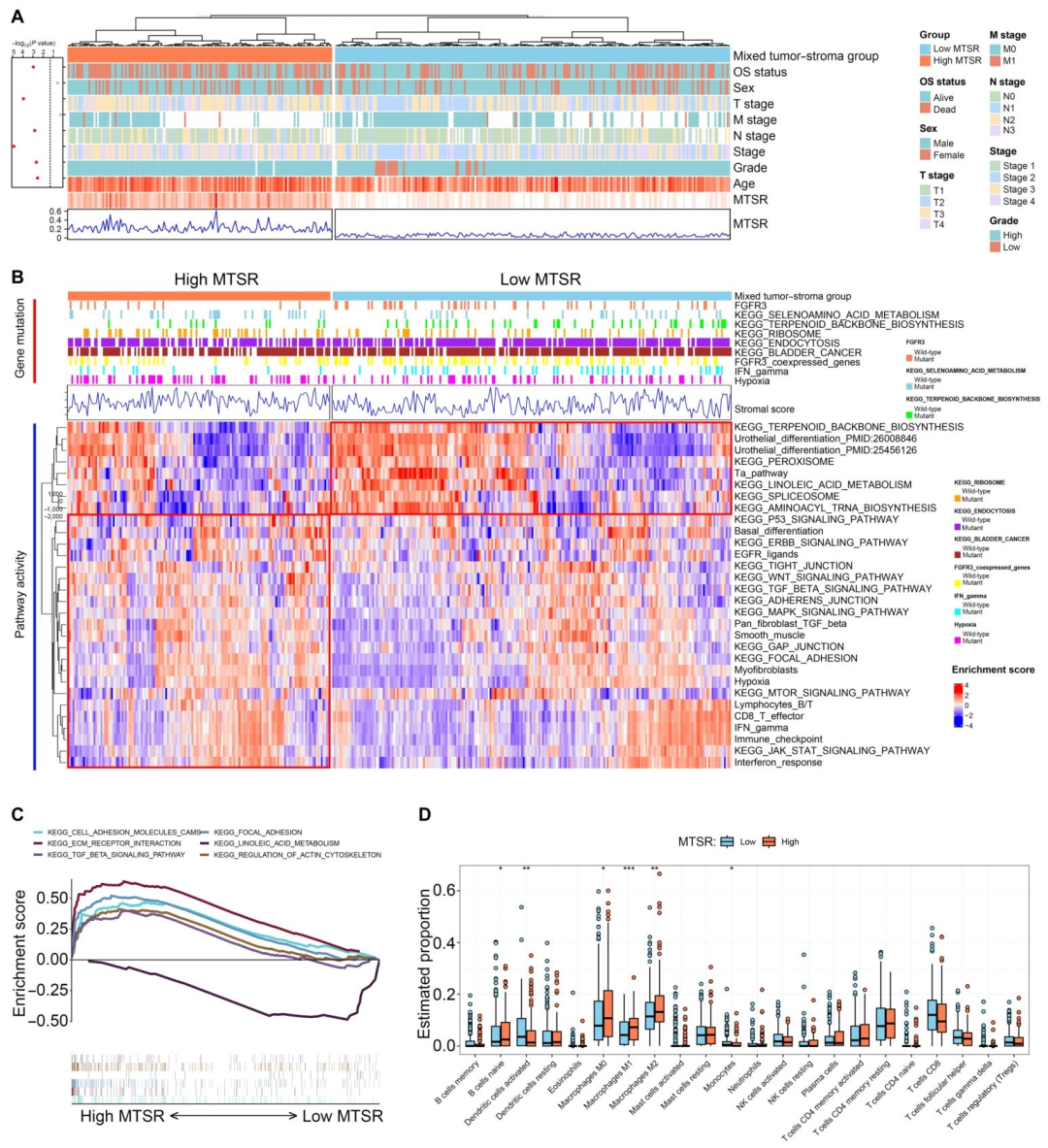
图 6(批量转录组特征) :图6A显示高MTSR患者男性多、年龄大、分期晚;图6B通路富集表明高MTSR富集WNT、TGF‑β、mTOR等经典致癌通路 ;图6C GSEA证实ECM受体交互、细胞黏附分子在高MTSR中富集;图6D免疫浸润显示高MTSR组M0/M1/M2巨噬细胞浸润增加。该图从分子层面解释了高MTSR为何预后差------即激活了促进侵袭和免疫抑制的信号轴,为影像组学特征(如异质性、纹理粗糙度)提供了生物学来源(胶原沉积、细胞密度不均)。
5. 单细胞机制解析 :高MTSR肿瘤中鉴定出一个ITGB8高表达的尿路上皮亚群(cluster 8),该亚群处于终末分化状态,WNT通路活性升高、凋亡受抑,且作为"发送者"主导细胞间通讯。
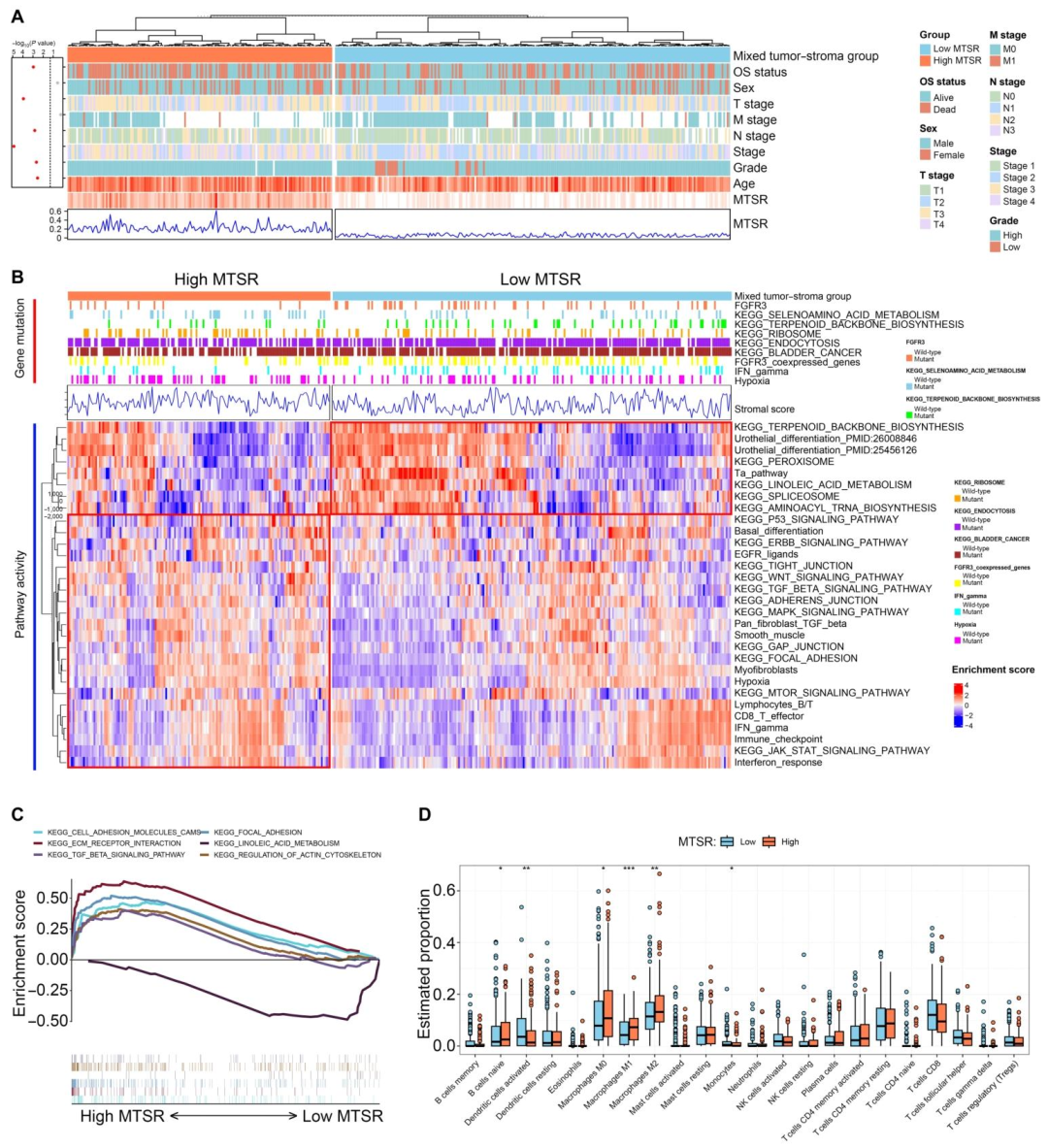
图 7(单细胞机制) :图7A‑B的UMAP显示高MTSR与低MTSR肿瘤细胞组成差异显著,cluster 8为关键尿路上皮亚群;图7C显示cluster 8中WNT信号升高、凋亡降低 ;图7D细胞通讯分析显示该亚群作为"发送者"主导信号输出;图7E‑F的KEGG富集证实PI3K/Akt、ECM受体、WNT通路富集。该图将MTSR表型精准定位到ITGB8高表达的功能亚群,揭示了其发送信号、活化间质的能力。影像组学中的纹理异质性可反映这种活跃的细胞‑间质交互区域。
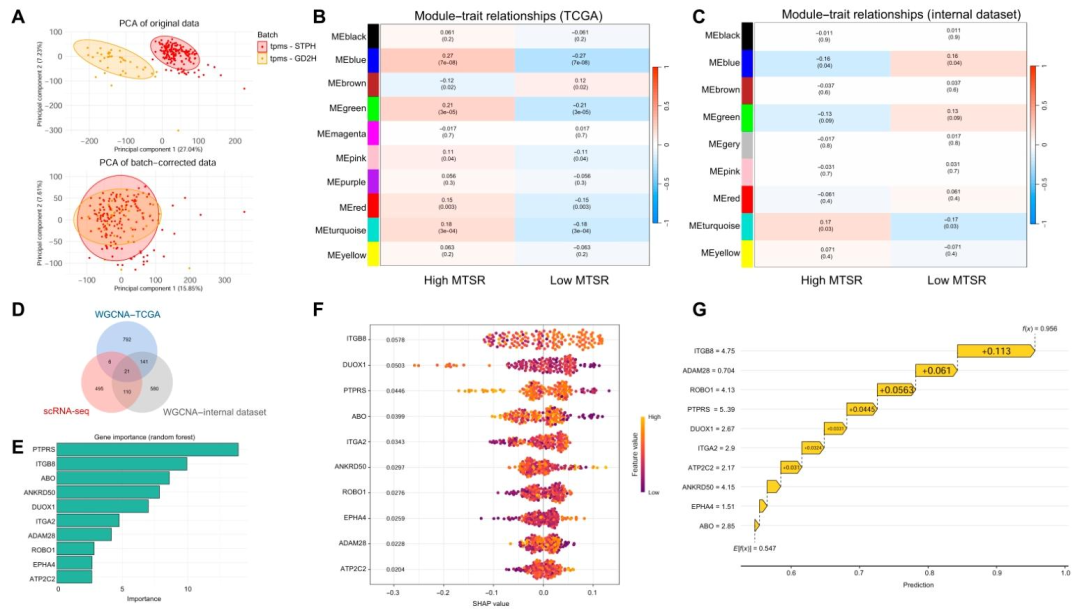
图 8(基因模块与关键预测因子) :图8A批次校正后PCA显示数据整合良好;图8B‑C的WGCNA显示高MTSR与多个基因模块正相关;图8D韦恩图筛选出21个交集基因;图8E随机森林重要性排序显示ITGB8、PTPRS、ABO 为前三;图8F‑G的SHAP分析确认ITGB8贡献最大且正向驱动高MTSR预测。该图通过机器学习(随机森林+SHAP)从多组学数据中锁定ITGB8为核心机制基因,这种"组学筛选+可解释AI"的思路同样可迁移至影像组学,用于筛选与ITGB8表达相关的影像特征。
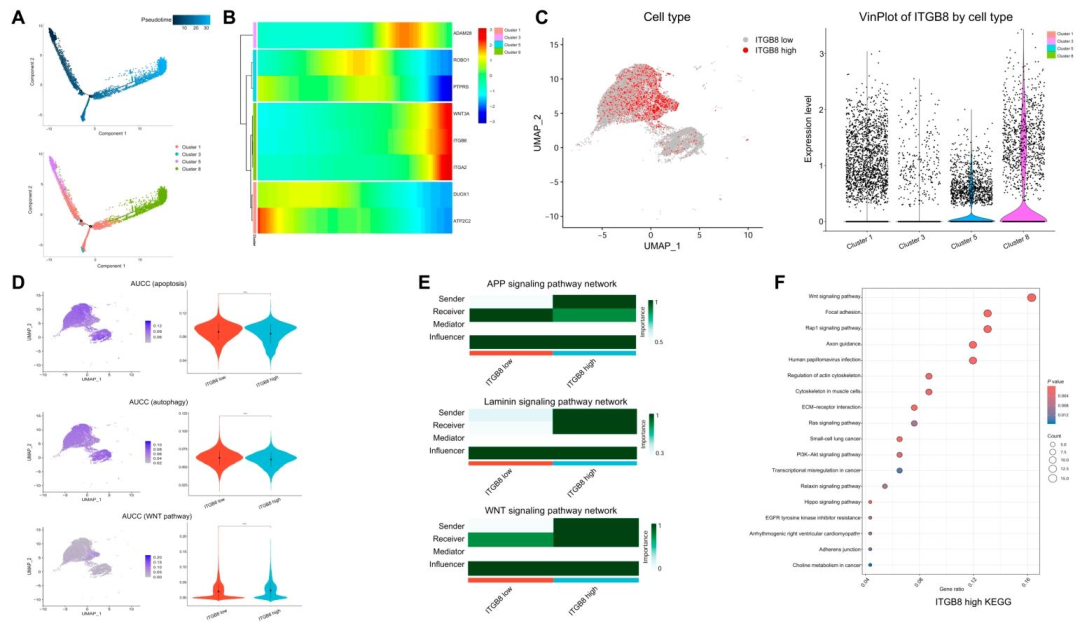
图 9(ITGB8高表达细胞的伪时间与调控网络) :图9A伪时间轨迹显示cluster 8位于终末分化端;图9B热图显示ITGB8和WNT3A沿伪时间逐渐升高;图9C显示ITGB8主要在cluster 8富集;图9D再次验证ITGB8高表达细胞中WNT高、凋亡低;图9E显示ITGB8高细胞作为"发送者";图9F富集分析确认WNT通路最显著;图S9(补充)展示BPTF、SOX4等转录因子活性。该图构建了从ITGB8到WNT通路再到终末分化的因果链条,解释了高MTSR肿瘤的侵袭性来源。影像组学可尝试预测ITGB8表达状态,间接挂靠该机制轴。
6. 影像组学预测 :基于mpMRI(T2WI + DCE)构建的随机森林模型在训练集和验证集中预测MTSR高/低状态的准确率分别为0.701和0.710,AUC分别为0.746和0.657,实现了MTSR的无创术前评估。
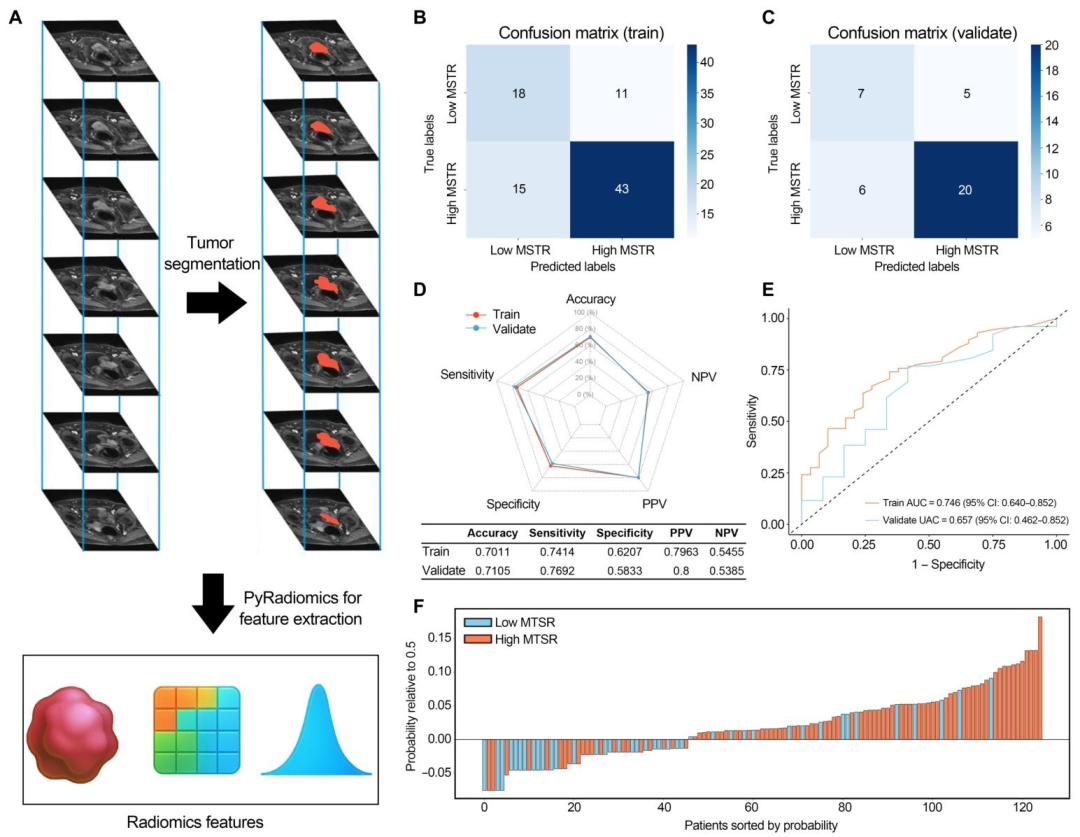
图 10(影像组学预测MTSR) :图10A展示从mpMRI的T2WI和DCE序列中勾画肿瘤ROI并提取放射组学特征;图10B‑C混淆矩阵和雷达图显示随机森林模型在训练集(准确率0.701)和验证集(0.710)表现稳健,敏感度0.741‑0.769,阳性预测值0.796‑0.800;图10D的ROC曲线显示AUC训练集0.746、验证集0.657;图10E瀑布图展示个体预测一致性。该图实现了影像组学对MTSR的无创术前预测 ,其生物学依据在于:MTSR反映的ECM重塑、胶原沉积、细胞密度异质性等微观特征,可转化为MRI图像上的纹理、形态和信号异质性等可量化放射组学特征,从而将宏观影像与微观ITGB8/TGF‑β/WNT机制轴桥接起来。
07
讨论(把机制故事讲圆)
本研究通过深度学习自动量化膀胱癌H&E切片中的混合肿瘤‑间质比例 ,并系统验证了其作为独立预后标志物 的稳定性和多中心可重复性。与人工评估相比,该模型消除了观察者间变异,实现了像素级的精确组织分类 ,尤其适用于肿瘤与间质边界模糊的复杂病例。更为重要的是,研究不仅停留在预后关联层面,而是深入揭示了MTSR背后的生物学机制 :高MTSR肿瘤中,ITGB8高表达的尿路上皮细胞亚群通过激活TGF‑β/WNT信号轴,促进细胞外基质重塑、抑制凋亡、驱动上皮‑间充质转化,并形成以"发送者"为主导的细胞通讯网络。这一机制与已知的ITGB8功能高度吻合------ITGB8可与αv亚基形成异二聚体,结合并激活潜伏态TGF‑β,进而刺激癌相关成纤维细胞收缩胶原、极化巨噬细胞向M2表型转化,形成正反馈环路。单细胞伪时间轨迹分析进一步揭示,这些ITGB8高表达细胞位于分化终末段,但仍表现出侵袭性特征,提示肿瘤‑间质互作可驱动肿瘤细胞向更具侵袭潜能的终末状态演化 。从临床转化角度看,本研究构建的mpMRI影像组学模型虽准确率中等(AUC约0.71),但首次证明了利用常规术前影像无创评估MTSR的可行性 ,为无法获取病理组织的患者提供了风险分层的替代工具。值得注意的是,MTSR在NMIBC和MIBC亚组中均具有预后区分能力,提示其适用于全阶段膀胱癌患者。本研究的局限性包括:外部队列虽大但仍以中国人群为主,泛化性需进一步验证;MRI影像组学模型性能有待提升,未来可纳入弥散加权成像序列或多中心数据增强;ITGB8的功能机制仍需体外共培养和动物模型实验验证。总体而言,本研究建立了"病理表型→多组学机制→影像预测"的全链条研究范式,为膀胱癌的精准分层和个体化治疗提供了新的生物标志物和理论依据。
08
这篇文献的可借鉴思路
这篇文献为影像组学/数字病理如何挂靠生物学机制 提供了极佳的可复制的范例。第一,以量化病理表型为枢纽 :不直接预测基因突变或通路,而是从H&E切片中提取一个可解释的、具有预后价值的组织比例指标(MTSR) ,该指标本身具有生物学内涵(肿瘤‑间质互作),因此天然适合向下游挖掘机制。第二,递进式多组学验证策略 :从批量转录组(WGCNA + GSEA) 初步筛选相关通路和基因模块,再通过单细胞RNA测序 精准定位关键细胞亚群和标志基因(ITGB8),接着利用伪时间轨迹 和SCENIC转录因子网络 构建从基因到细胞功能的因果链,最后用细胞通讯分析 阐明该亚群在微环境中的角色。这种从宏观到单细胞、从关联到因果的递进逻辑,极大增强了机制故事的可信度。第三,关键基因锁定方法 :将WGCNA得到的hub基因、单细胞差异基因和临床相关基因取交集,再结合随机森林重要性排序和SHAP解释 ,从数千个基因中精准筛选出ITGB8,避免了盲目假设。第四,影像组学的机制挂靠方式 :不是直接预测抽象的基因突变,而是预测已明确与机制相关的表型(MTSR) ,使影像特征(纹理、异质性)与微观过程(胶原沉积、ECM重塑、血管异质性)建立合理的生物学联系,即使模型AUC不高,也能讲通故事。第五,临床转化闭环 :从病理模型出发,构建预后模型,再反向构建影像预测模型,形成了"病理诊断→预后评估→术前无创预测 "的完整闭环,符合精准医学的临床需求。如果你正在设计类似研究,建议借鉴这一"表型驱动→单细胞定位→关键基因锁定→影像映射"的四步框架,并始终确保每一步都有明确的生物学问题驱动。
09
结语
总而言之,这篇文献告诉我们:影像组学的真正价值,不在于模型AUC从0.71卷到0.72,而在于你能不能拍着胸脯说------"我影像特征的变化,背后站着一条清晰的生物学机制链" 。作者从H&E切片中算出的MTSR,之所以能用来训练mpMRI模型,不是因为他们运气好,而是因为MTSR本身已经被单细胞和批量组学证实与ITGB8/TGF‑β/WNT轴深度绑定 ,ECM的胶原沉积、细胞密度的不均一,天然就能在T2WI和DCE图像上留下"纹理指纹"。所以,大家以后设计影像组学研究时,不妨先问自己三个问题:我要预测的表型有生物学故事吗?这个故事能不能在组织切片或组学数据里找到证据?影像特征和这个证据之间有没有合理的生理/病理桥梁? 只有把这三点串起来,你的影像组学才不是"算命 ",而是"诊断 ";不是"黑箱",而是"明灯 "。希望大家都能借这篇论文的思路,少走弯路,做出有机制、有深度、能发高分的真科研!
参考文献:He Y, Xie J, Zhong S, Zhan C, Dai F, Lai H, Wang M, He Y, Patel H, Chen ZS, Zhong B, Qiu X, Guo Y, Zheng Z. A Deep Learning-Generated Mixed Tumor-Stroma Ratio for Prognostic Stratification and Multi-omics Profiling in Bladder Cancer. Research (Wash D C). 2026 Jan 26;9:1053. doi: 10.34133/research.1053.