AlphaFold2 到 AlphaFold3:不只是预测蛋白结构,而是进入分子互作分析时代
出处:智澈乐尚网络工作平台
摘要
很多人第一次听说 AlphaFold,都会把它简单理解成一个"根据蛋白序列预测三维结构"的工具。
这个理解没有错,但已经不够完整。
从 AlphaFold2 到 AlphaFold3,AlphaFold 的能力正在从单蛋白结构预测 ,逐渐扩展到蛋白复合物、蛋白-核酸、蛋白-配体、蛋白-离子以及分子互作结构预测。
这意味着,对于做蛋白结构、酶催化、蛋白互作、分子对接、药物设计、突变分析和分子动力学模拟的人来说,AlphaFold 不再只是"给你一个蛋白模型",而是可以作为一整套结构研究流程的起点。
不过,AlphaFold 结果并不是"生成一个结构就结束"。
真正有价值的是:如何提交合理任务、如何判断预测结果是否可信、如何分析 pLDDT、PAE、ipTM、Contact Probability,以及如何把结果继续用于对接、动力学和实验设计。
如果你手里已经有蛋白序列、互作蛋白、配体体系或者想研究的复合物,但不知道怎么整理任务、提交预测和解读结果,这篇文章可以先帮你建立一个完整认识。
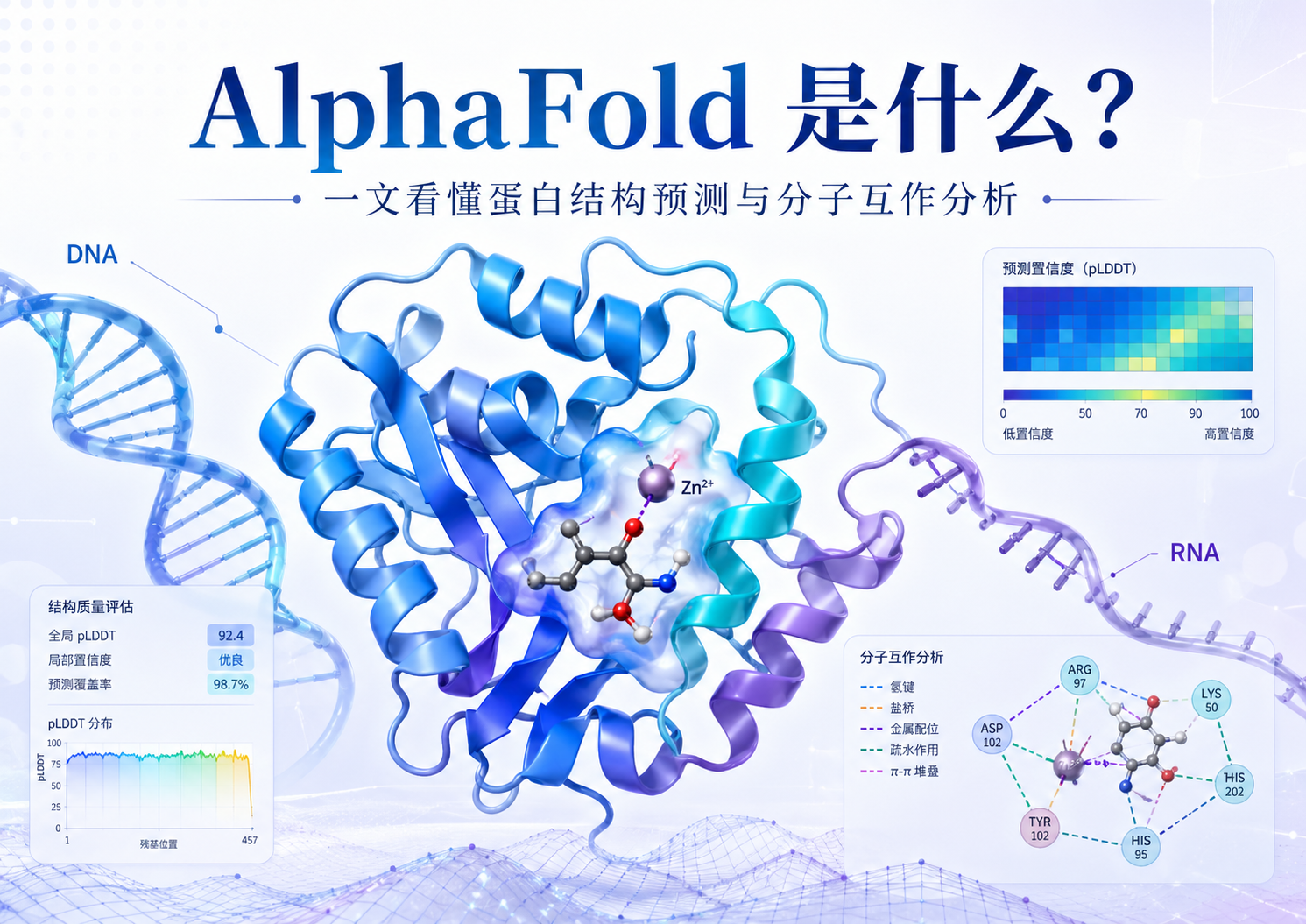
一、AlphaFold3 分析后可以得到那些东西?
AlphaFold 最核心的价值,是把"从蛋白氨基酸序列预测三维结构"这件事推到了一个新的高度。
通过分析后可以得到:
互相作用图:
- 互相作用图
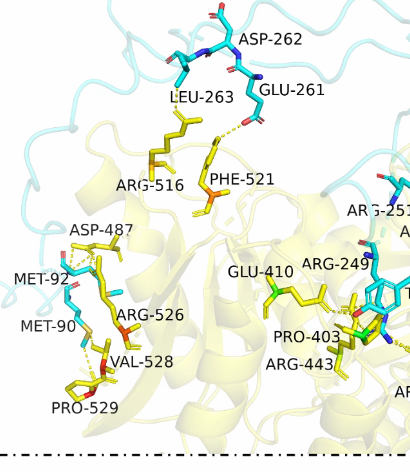
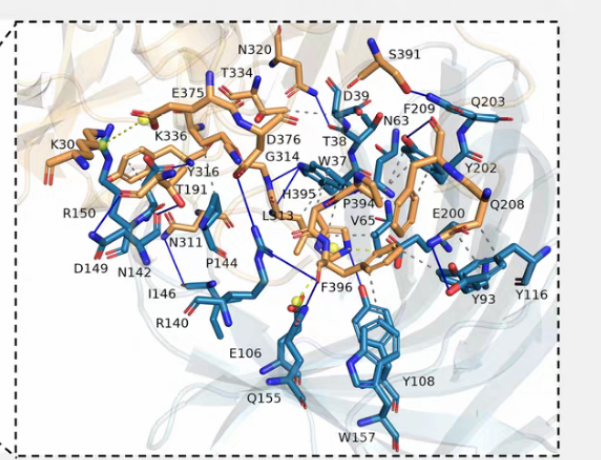

- 表面作用力图
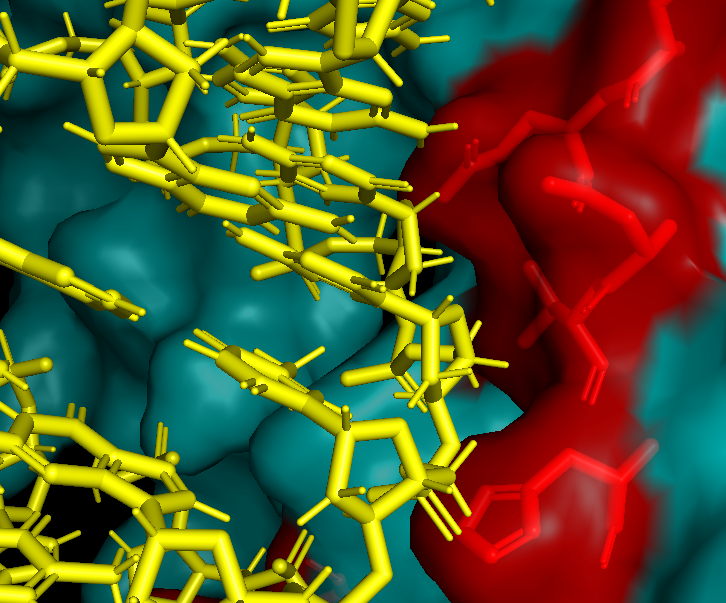
二、AlphaFold3 升级在哪里?
如果说 AlphaFold2 的关键词是:
蛋白结构预测
那么 AlphaFold3 的关键词更接近于:
生物分子复合物与互作预测
AlphaFold3 不只是继续预测蛋白结构,而是进一步扩展到更复杂的生物分子体系。
它可以用于蛋白、DNA、RNA、配体、离子以及部分化学修饰相关体系的结构预测和相互作用分析。
这对科研工作流的影响非常大。
因为很多课题真正关心的不是"一个蛋白单独长什么样",而是:
- 两个蛋白是否可能形成复合物;
- 结合界面在哪里;
- 关键残基是否靠近;
- 核酸是否可能被特定蛋白识别;
- 配体或离子是否位于合理结合区域;
- 预测模型是否能支持后续机制假设。
AlphaFold3 的升级,本质上是把结构预测从"单个蛋白对象"推进到"分子系统对象"。
这也意味着,它更适合用于:
- 蛋白-蛋白互作分析;
- 蛋白-DNA 互作分析;
- 蛋白-RNA 互作分析;
- 蛋白-配体复合物初步建模;
- 蛋白-金属离子体系参考;
- 多分子复合物结构假设构建;
- 后续对接和动力学模拟前的结构准备。
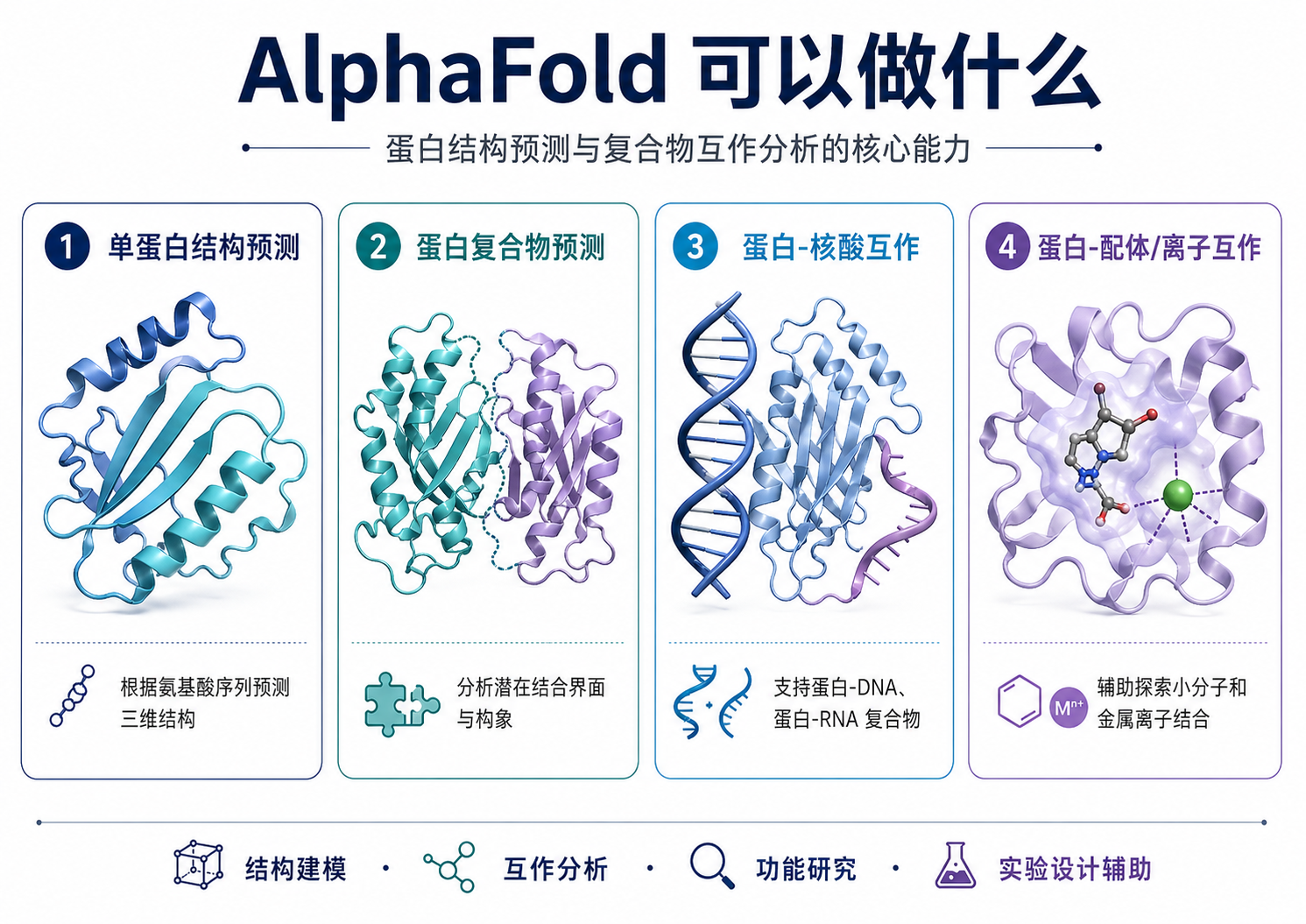
三、AlphaFold3 能做哪些常见任务?
1. 单蛋白结构预测
这是 AlphaFold 最基础、也是最常用的功能。
如果你手里只有一条蛋白序列,又找不到对应实验结构,那么可以通过 AlphaFold 预测其三维结构。
适合场景包括:
- 新蛋白结构初步建模;
- 未解析蛋白的结构预测;
- 蛋白结构域识别;
- 活性位点附近构象观察;
- 柔性区和无序区初步判断;
- 作为对接、动力学模拟、突变分析前的结构基础。
不过需要注意,单蛋白预测也不是所有区域都同样可信。
一些低 pLDDT 区域可能代表柔性区、无序区,也可能说明模型对该区域没有较高把握。
所以,预测结构不能只看"整体像不像",还要看置信度。
2. 蛋白复合物预测
对于做蛋白互作的人来说,AlphaFold3 比 AlphaFold2 更吸引人的地方,就是它可以更直接地参与复合物预测。
例如:
- A 蛋白和 B 蛋白是否可能接触;
- 哪些残基可能位于结合界面;
- 两条链之间相对位置是否可信;
- 复合物整体构象是否合理;
- 界面区域是否适合进一步突变验证。
对于蛋白-蛋白互作研究来说,AlphaFold3 可以先帮助我们建立一个结构假设。
但这里要特别强调:
AlphaFold3 预测出一个复合物模型,不等于证明两者一定真实互作。
真正分析时要重点结合:
- ipTM;
- 链间 PAE;
- Contact Probability;
- 界面残基是否合理;
- 已知文献和实验背景;
- 后续对接、动力学或实验验证。
也就是说,AlphaFold3 很适合做"互作结构假设生成",但不能直接替代实验结论。
3. 蛋白与 DNA/RNA 互作预测
很多生物学问题都涉及蛋白与核酸的识别,例如:
- 转录因子识别 DNA;
- RNA 结合蛋白识别 RNA;
- 核酸酶与底物结合;
- 蛋白参与转录、翻译或调控过程;
- 蛋白-核酸复合物结构假设构建。
AlphaFold3/AlphaFold Server 对蛋白-DNA、蛋白-RNA 等体系提供了更直接的预测能力。
这对做转录调控、RNA 结合蛋白、核酸酶、蛋白-核酸复合物研究的人来说非常有帮助。
它可以让我们更直观地观察:
- 蛋白是否靠近核酸;
- 结合区域是否集中;
- 关键碱基或残基是否形成合理接触;
- 核酸方向和蛋白表面是否匹配;
- 后续是否值得做突变或 EMSA、SPR、ITC 等实验验证。
4. 蛋白与配体、离子体系预测
AlphaFold3 的另一个升级点,是扩展到了配体、离子和化学修饰等体系。
这对做药物分子、酶催化、金属离子结合、辅因子参与机制的人来说很有吸引力。
例如你可能会关心:
- 小分子是否进入蛋白口袋;
- 配体是否靠近关键活性位点;
- 金属离子是否位于可能的配位环境;
- 辅因子是否与蛋白形成合理空间关系;
- 结构是否适合后续 docking 或 MD。
不过这一类结果更需要谨慎。
因为配体结合、金属配位、酶催化反应、共价反应等体系,往往涉及更复杂的化学机制。
AlphaFold3 可以提供结构假设,但不应直接替代专业对接、量化计算、分子动力学模拟或实验验证。
比如金属离子结合体系,常常还需要结合:
- 配位残基;
- 配位距离;
- 配位数;
- 电荷状态;
- 力场参数;
- 量化计算或 DFT;
- 光谱或突变实验。
所以,对于蛋白-配体和蛋白-离子体系,AlphaFold3 更适合作为"初步结构参考"和"后续模拟起点"。
四、AlphaFold2 和 AlphaFold3 的区别,可以这样理解
简单来说:
AlphaFold2 更像是"蛋白单体结构预测工具"。
AlphaFold3 更像是"生物分子复合物结构预测工具"。
可以这样对比:
| 对比项 | AlphaFold2 | AlphaFold3 / AlphaFold Server |
|---|---|---|
| 核心能力 | 蛋白结构预测 | 复合物结构与分子互作预测 |
| 常见输入 | 蛋白序列 | 蛋白、DNA、RNA、配体、离子等 |
| 典型用途 | 单蛋白建模、结构参考 | 蛋白互作、核酸互作、配体/离子互作 |
| 关注重点 | pLDDT、PAE、结构域 | pLDDT、PAE、ipTM、接触概率、界面 |
| 适合方向 | 单蛋白结构研究 | 复合物、机制分析、互作研究 |
| 注意事项 | 柔性区和无序区需谨慎 | 互作结果更需要结合指标和实验验证 |
所以,如果你的课题只是想看一个蛋白的大致结构,AlphaFold2/AlphaFold DB 的结果可能已经很有价值。
但如果你的问题是:
- 两个蛋白会不会结合?
- 蛋白和核酸怎么靠近?
- 配体可能在哪里?
- 金属离子是否参与结合?
- 多分子复合物结构是否合理?
那么 AlphaFold3/AlphaFold Server 会更适合作为起点。
3张图链接)
五、AlphaFold 结果不能只看结构图,还要看指标
很多人拿到 AlphaFold 结果以后,第一反应是打开模型,看结构漂不漂亮。
但真正做科研分析时,这远远不够。
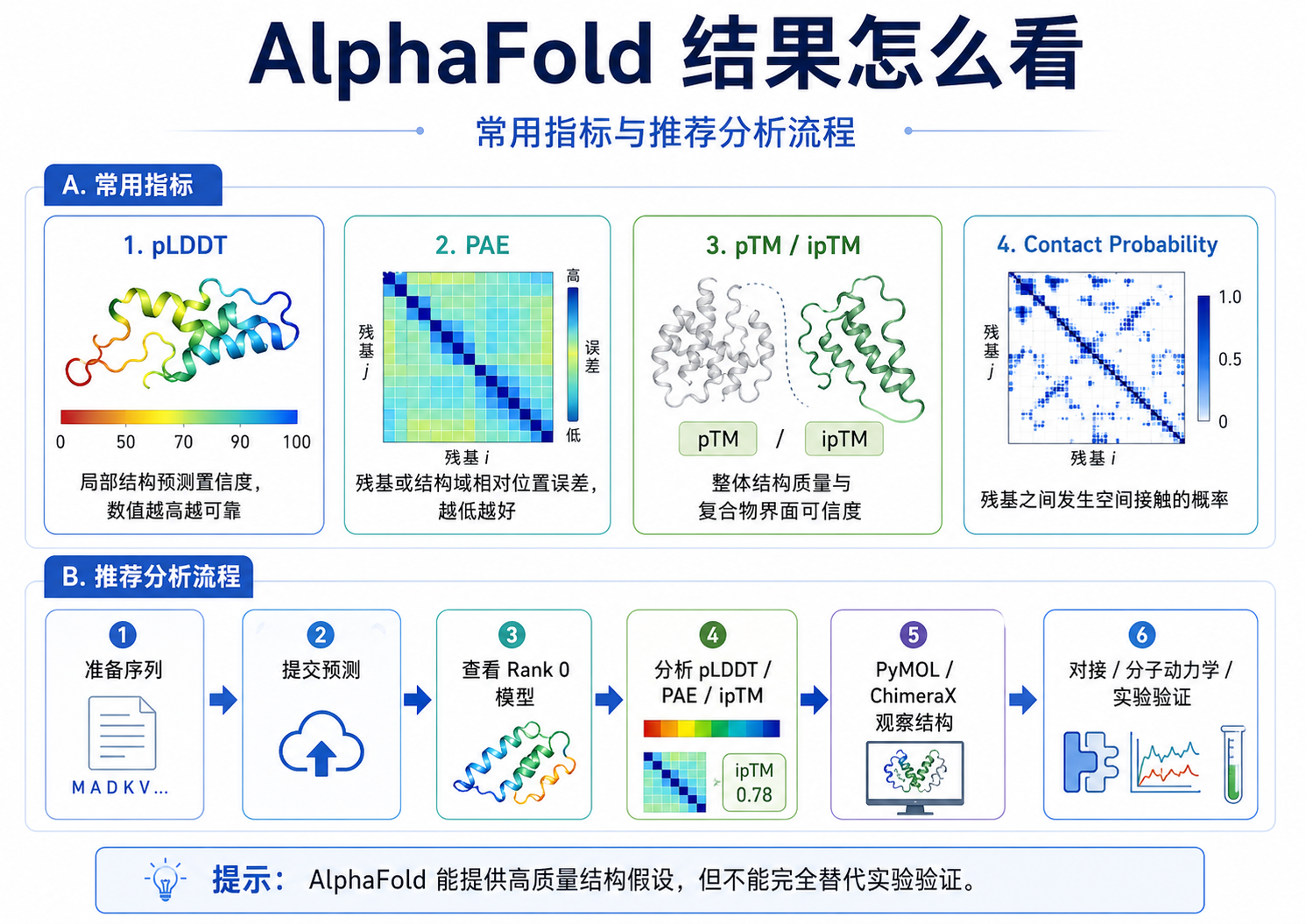
因为一个模型"看起来像结构",不代表它一定可信。
尤其是复合物预测,更不能只靠肉眼判断。
一般需要重点看下面几个指标。
1. pLDDT:局部结构可信度
pLDDT 主要反映局部结构预测置信度。
一般来说:
- 高 pLDDT 区域更可信;
- 低 pLDDT 区域可能是柔性区、无序区或预测不稳定区域;
- 不建议在低置信度区域过度解读精细结构。
对于单蛋白结构,pLDDT 是非常重要的第一判断指标。
2. PAE:结构区域相对位置是否可信
PAE 主要反映两个残基或结构区域之间相对位置的预测误差。
对于复合物来说,PAE 特别重要。
因为你不仅要知道每条链内部结构是否可信,还要知道:
- A 链和 B 链之间的位置关系是否可信;
- 结构域之间相对方向是否稳定;
- 复合物界面是否可能只是模型随机摆放;
- 哪些区域之间关系可靠,哪些区域不可靠。
很多复合物结构看起来贴在一起,但如果链间 PAE 很高,就需要非常谨慎。
3. pTM 和 ipTM:整体结构与界面可信度
pTM 主要用于评估整体结构预测质量。
ipTM 更关注复合物界面的预测可信度。
对于蛋白复合物研究来说,ipTM 往往比单纯看结构图更重要。
如果 ipTM 较低,即使结构图看起来两个蛋白靠在一起,也不能轻易下结论。
如果 ipTM 较高,同时界面 PAE 较低、接触概率也支持,那么这个复合物模型才更值得进一步分析。
4. Contact Probability:残基接触概率
Contact Probability 可以帮助判断哪些残基之间可能发生空间接触。
对于蛋白互作界面分析,它非常有参考价值。
例如:
- 哪些残基可能参与界面;
- 是否有连续接触区域;
- 接触是否集中在合理表面;
- 是否支持后续突变验证;
- 是否能辅助解释互作机制。
所以,在 AlphaFold3 复合物分析中,Contact Probability 是非常值得关注的指标。
六、AlphaFold 适合接到哪些后续分析?
AlphaFold 的价值不应该停留在"生成一个结构文件"。
真正高效的用法,是把它接入后续结构分析流程。
常见后续分析包括:
1. PyMOL / ChimeraX 结构观察
可以用于:
- 展示整体构象;
- 标记关键残基;
- 观察结合界面;
- 制作论文图和汇报图;
- 对比不同 rank 模型;
- 检查结构是否有明显异常。
2. 分子对接
对于蛋白-配体体系,如果没有实验结构,可以先用 AlphaFold 预测蛋白结构,再进一步进行 docking。
但要注意,对接前通常还需要:
- 结构清理;
- 加氢;
- 补全缺失残基;
- 检查口袋;
- 设置 box;
- 准备配体;
- 选择合适力场和参数。
AlphaFold 结构可以作为起点,但不是直接拿来就一定适合对接。
3. 分子动力学模拟
对于蛋白复合物、蛋白-配体体系,AlphaFold 模型可以进一步进入 MD 模拟,用于观察体系稳定性。
例如:
- 复合物界面是否稳定;
- 配体是否保持结合;
- 关键氢键是否存在;
- RMSD、RMSF、Rg、SASA 等指标如何;
- 结合自由能是否支持互作假设。
4. 突变分析
AlphaFold 结果可以辅助突变设计,例如:
- 界面残基突变;
- 活性位点突变;
- 稳定性相关残基突变;
- 结合口袋附近残基突变;
- 酶工程方向的理性改造。
5. 实验设计辅助
AlphaFold 不能替代实验,但可以帮助实验更有针对性。
例如:
- 设计点突变;
- 设计截短体;
- 选择互作验证区域;
- 选择可能的关键残基;
- 为分子实验提供结构依据。
七、为什么很多人需要别人协助做 AlphaFold 预测和结果分析?
AlphaFold Server 本身并不难打开,难的是整个流程真正做顺。
很多同学会遇到这些问题:
- 序列不知道怎么整理;
- 多链复合物不知道怎么提交;
- 配体、离子、核酸体系不知道怎么配置;
- 结果下载后不知道每个文件是什么;
- 不知道 rank 0、ranking score、pLDDT、PAE、ipTM 怎么看;
- 有结构但不知道怎么判断是否可信;
- 不知道怎么导入 PyMOL / ChimeraX;
- 不知道怎么继续做对接或动力学;
- 不知道怎么整理成报告和图片。
尤其是 AlphaFold3 的结果目录里,会包含很多 JSON、CIF、MSA、template、confidence 等文件。
如果没有处理过,第一次看会很乱。
所以实际项目里,真正有价值的服务不是"点一下预测",而是:
从序列整理、任务配置、结构预测、结果下载、置信度分析、结构可视化到报告整理的一整套流程。
这也是为什么我更建议把 AlphaFold 当成一个结构研究工作流,而不是一个单点工具。
八、我这里可以协助你做哪些 AlphaFold 相关处理?
如果你已经有蛋白序列、互作对象、配体体系或者想研究的复合物,可以进一步交流。
目前可以协助的内容包括:
- 蛋白序列整理;
- AlphaFold2 / AlphaFold3 预测任务配置;
- 单蛋白结构预测;
- 蛋白-蛋白复合物预测;
- 蛋白-DNA / RNA 互作结构预测思路整理;
- 蛋白-配体 / 离子体系结构分析思路整理;
- AlphaFold Server 结果下载和归档;
- pLDDT、PAE、pTM、ipTM、Contact Probability 指标解读;
- Rank 模型筛选;
- PyMOL / ChimeraX 结构观察;
- 结合界面残基分析;
- 结果图和报告整理;
- 后续对接、分子动力学模拟流程建议。
需要说明的是:
AlphaFold 预测结果属于计算结构假设,不能直接替代实验验证。
但它可以帮助你更快建立结构基础,减少前期盲目试错,并为后续实验、对接和模拟提供更清晰的方向。
九、与我联系
PC端电脑通过
点击 PC端分子对接软件合集 ------ "能看到某宝对应的分子对接软件商品!!!。
手机淘宝通过:
点击 手淘分子对接软件合集 "------能看到某宝对应的分子对接软件商品!!!
如果你希望把这类工具更快落地到自己的科研流程里,也可以直接联系我进一步沟通。
十、总结:AlphaFold3 让结构预测进入"互作分析时代"
AlphaFold2 让很多人第一次感受到 AI 结构预测的效率。
它解决了很多"没有蛋白结构怎么办"的问题。
而 AlphaFold3 的出现,则进一步把问题推进到:
- 蛋白之间如何互作;
- 蛋白如何识别 DNA/RNA;
- 小分子和离子如何参与结构关系;
- 多分子复合物能否形成合理构象;
- 这些结构能否支持后续机制分析。
所以,AlphaFold3 的意义不只是升级了一个模型,而是让结构预测更接近真实的生物分子体系。
当然,AlphaFold3 仍然不是万能答案。
真正可靠的研究结论,仍然需要结合置信度指标、专业结构判断、对接、动力学模拟和实验验证。
如果你手里已经有蛋白序列,想做结构预测、复合物预测、互作分析,或者想把 AlphaFold 结果进一步整理成可展示、可汇报、可继续模拟的分析报告,欢迎进一步交流。
博客平台:智澈乐尚网络工作平台
如果你希望把 AlphaFold2 / AlphaFold3 预测结果更快落地到自己的科研流程里,也可以直接联系我沟通。