Design and construction of an artificial pathway for biosynthesis of acetaminophen in Escherichia coli
大肠杆菌中对乙酰氨基酚人工生物合成通路的设计与构建

研究要点
- 鉴定并表征了2 个参与对乙酰氨基酚(AAP)合成 的关键酶。
- 设计并构建人工合成通路 ,实现对乙酰氨基酚的从头生物合成 。
- 借助动态调控 策略,工程菌株以甘油为碳源,对乙酰氨基酚产量达 120.03 mg/L 。
摘要
对乙酰氨基酚(AAP)是应用最广泛的药物原料之一,具有解热、镇痛活性。作为非天然化合物,目前工业上以苯酚等石油基碳源 为原料、通过化学合成法生产对乙酰氨基酚,该方式可持续性差且环境不友好。
本研究设计并构建了一条人工生物合成通路 ,实现利用简单碳源从头合成 对乙酰氨基酚。通过挖掘并拓展天然酶的底物谱,本研究鉴定并功能表征了对氨基苯甲酸(p-ABA)单加氧酶 与对氨基苯酚(p-AP)N - 乙酰转移酶 ;两种酶可实现大肠杆菌以对氨基苯甲酸为前体合成对乙酰氨基酚。
随后,通过筛选对氨基苯甲酸合酶、强化谷氨酰胺供给,构建对氨基苯甲酸高产菌株 ,摇瓶发酵产量可达 836.43 mg/L。进一步组装完整生物合成通路,首次实现大肠杆菌以甘油为唯一碳源从头合成对乙酰氨基酚 。
最终,利用温度诱导调控元件 对通路基因进行动态表达调控 ,经通路改造后对乙酰氨基酚产量提升至 120.03 mg/L。
本研究不仅构建了可合成对乙酰氨基酚的微生物底盘平台,也证明了可依托现有酶资源挖掘新型生化反应,进而完成人工生物合成通路的理性设计与构建。
1. 引言
对乙酰氨基酚(AAP),又称扑热息痛,是全球应用最广泛的解热镇痛药物之一(Clissold, 1986; Saragiotto et al., 2019)。它是泰诺、必理通、埃克塞德林等多种知名非处方药(OTC)的核心有效成分(Hamilton, 2012; Saragiotto et al., 2019),也可用于合成贝诺酯 ------ 另一种兼具镇痛、解热与抗炎活性的常用药物(Similä et al., 1975)。AAP 已被世界卫生组织(WHO, 2019)列入基本药物目录 。据统计,2021 年全球 AAP 市场规模约为 7.723 亿美元,预计 2025 年将达到 7.932 亿美元(DecisionDatabases.com, 2021)。
目前,AAP 的工业化生产依赖以石化原料 为底物的化学合成工艺。例如,以苯酚为起始物,在高温高压下经硝酸与乙酸酐催化,通过硝化、氢化、乙酰化 三步反应制备 AAP(Wilbert et al., 1961)。然而,化学合成法存在反应条件苛刻、副产物多、环境不友好等缺陷(Ellis, 2002; Joncour et al., 2014; Vodnala et al., 2019)。利用微生物细胞工厂 从可再生原料生物合成 AAP,是解决上述问题的可行方案。
由于 AAP 是人工合成化合物 ,自然界中尚未发现其天然生物合成途径,因此必须从头设计人工合成通路 。近年来,已有多项研究提出 AAP 人工生物合成路线:如一项美国专利报道了以 ** 分支酸、对氨基苯甲酸(p-ABA)、对氨基苯酚(p-AP)** 为中间产物的通路(Anderson et al., 2017);一项 iGEM 项目则提出以分支酸、邻氨基苯甲酸与 p-AP 为中间体的通路(Jack Baskin School of Engineering, 2017)。但上述通路及关键酶均未经过实验验证与功能表征,至今仍未实现从简单碳源微生物合成 AAP 。
从化学结构看,AAP 可由p-AP 经 N - 乙酰化 生成。芳基酰胺酶(AAA)属于水解酶家族,可将酰基苯胺水解为羧酸与苯胺(Ko et al., 2010);该反应在特定条件下可逆,即以羧酸为酰基供体、芳香化合物为受体,催化生成酰基苯胺。已有研究发现,一种细菌来源的 AAA 在酸性条件(pH 5.5)下,可通过添加高浓度 p-AP 与乙酸合成 AAP(Ko et al., 2010)。但多数微生物宿主在中性温和环境下生长,无法满足该反应条件。
另一种策略是采用N - 乙酰转移酶 ,以乙酰 - CoA (而非乙酸)为酰基供体,将 p-AP 乙酰化生成 AAP。基于 eQuilibrator 网站(http://equilibrator.weizmann.ac.il)的热力学计算表明:N - 乙酰转移酶催化乙酰化反应的吉布斯自由能变化 ΔrG'°net 为−17.5 kJ/mol ,而芳基酰胺酶催化的乙酰化反应为 13.5 kJ/mol(Thompson et al., 2018)。这说明N - 乙酰转移酶路线在热力学上更具优势 ,是实现 AAP 高效生物合成的理想选择。
除缺乏功能性 p-AP N - 乙酰转移酶外,p-AP 生物合成通路缺失 是 AAP 生物合成的另一大瓶颈。从结构上看,p-AP 与微生物叶酸合成的天然中间体 p-ABA 高度相似(Davis, 1951; Koma et al., 2014)。通过对比 p-AP 与 p-ABA 的化学结构,我们推测:氧化还原酶 可催化 p-ABA 发生脱羧还原 ,进而生成 p-AP。但目前尚未鉴定出能催化该反应的关键酶。
本研究设计并构建了一条人工生物合成通路 ,首次实现以甘油为碳源从头合成 AAP (图 1)。研究中筛选并功能表征了两种关键酶:p-AP N - 乙酰转移酶 (催化 p-AP 生成 AAP)与p-ABA 单加氧酶 (催化 p-ABA 生成 p-AP)。随后,通过强化莽草酸途径 、过表达 p-ABA 合酶优化 p-ABA 合成,摇瓶产量达 836.43 mg/L。最后,整合完整通路实现 AAP 从头合成,并利用温度响应型调控系统 减少副产物积累,大幅提升 AAP 产量。
本研究首次通过人工设计与构建生物合成通路实现微生物合成 AAP ,为利用可再生碳源大规模生物制造 AAP 奠定了基础。
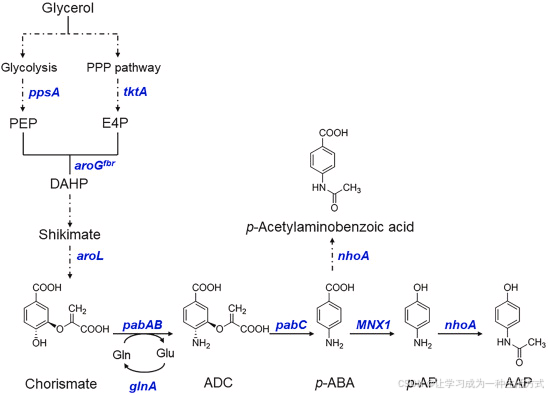
图 1 对乙酰氨基酚从头生物合成的新型人工通路
蓝色基因为通路中过表达 基因。PEP:磷酸烯醇式丙酮酸;E4P:D - 赤藓糖 - 4 - 磷酸;DAHP:3 - 脱氧 - D - 阿拉伯庚酮糖 - 7 - 磷酸;ADC:4 - 氨基 - 4 - 脱氧分支酸;p-ABA:对氨基苯甲酸;p-AP:对氨基苯酚;AAP:对乙酰氨基酚。
tktA 编码转酮醇酶;ppsA 编码磷酸烯醇式丙酮酸合成酶;aroG<sup>fbr</sup> 编码抗反馈抑制的 3 - 脱氧 - 7 - 磷酸庚酮糖醛缩酶突变体;aroL 编码莽草酸激酶 II;pabAB 编码 4 - 氨基 - 4 - 脱氧分支酸合酶;pabC 编码氨基脱氧分支酸裂解酶;MNX1 编码对氨基苯甲酸单加氧酶;nhoA 编码对氨基苯酚 N - 乙酰转移酶。
2 材料与方法
2.1 培养基、菌株与质粒
LB 培养基 (胰蛋白胨 10 g、酵母提取物 5 g、氯化钠 10 g,加去离子水定容至 1 L),用于菌种活化、质粒扩增与蛋白表达。
改良 M9Y 甘油培养基 (甘油 20 g、酵母提取物 5 g、磷酸氢二钠 6 g、磷酸二氢钾 3 g、氯化铵 1 g、氯化钠 0.5 g、七水硫酸镁 246.5 mg、二水氯化钙 14.7 mg,加去离子水定容至 1 L),用于底物饲喂实验以及对氨基苯甲酸、对氨基苯酚和对乙酰氨基酚的从头合成 发酵。
根据实验需要向培养基中添加抗生素:氨苄青霉素 100 μg/mL、卡那霉素 50 μg/mL、氯霉素 25 μg/mL。蛋白过表达、底物饲喂及摇瓶发酵实验中,于培养 3 h 时加入 0.5 mM 异丙基 -β-D - 硫代半乳糖苷(IPTG) 诱导表达。
大肠杆菌 Trans5α 用于质粒构建与克隆扩增;BL21 Star (DE3) 用于酶活测定相关蛋白异源表达;野生型大肠杆菌 BW25113/F' 用于底物饲喂实验及目标产物从头合成。
质粒骨架:pZE12-luc(高拷贝)、pCS27(中拷贝)、pSA74(低拷贝) ;质粒 pBV 用于温度调控型 对乙酰氨基酚从头合成;pETDuet-1 用于蛋白表达。
本研究所用菌株与质粒详见表 1。
Table 1. Strains and plasmids used in this study.
|---------------------------|----------------------------------------------------------------------------------------------------------------|-------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------|
| Strain | Genotype | Source |
| E. coli BW25113/F′ | Δ(araD-araB)567, ΔlacZ4787(::rrnB-3), λ-, rph-1, Δ(rhaD-rhaB)568, hsdR514 [F′ proAB lacIqZDM15Tn10 (TetR)] | Yale CGSC |
| E. coli Trans5α | F-ϕ80d lacZΔM15 Δ(lacZYA-argF) U169 end A1 recA1 hsdR17 (rk -, mk +) supE44λ- thi-1 gyrA96 relA1 phoA | Stratagene |
| E. coli BL21 Star (DE3) | F − ompT hsdS B (r B- m B- ) gal dcm (DE3) | Invitrogen |
| CX0 | BW25113/F′ ΔnhoA | This study |
| CX1 | BW25113/F′ carrying pZE-AAA | This study |
| CX2 (control) | BW25113/F′ carrying pZE12-luc | This study |
| CX3 | BW25113/F′ carrying pZE-nhoA | This study |
| CX4 | CX0 carrying pZE-MNX1 | This study |
| CX5 | CX0 carrying pZE-EcpabABC and pCS-APTA | This study |
| CX6 | CX0 carrying pZE-BspabABC and pCS-APTA | This study |
| CX7 | CX0 carrying pZE-ScABZ1-ABZ2 and pCS-APTA | This study |
| CX8 | CX0 carrying pZE-EcpabABC and pCS-APTA-glnA | This study |
| CX9 | BW25113/F′ carrying pZE-EcpabABC-MNX1 and pCS-APTA-glnA | This study |
| CX10 | BW25113/F′ carrying pZE-EcpabABC-MNX1-nhoA and pCS-APTA-glnA | This study |
| CX11 | BW25113/F′ carrying pZE-EcpabABC-MNX1, pCS-APTA-glnA and pSA-nhoA | This study |
| CX12 | CX0 carrying pZE-EcpabABC-MNX1, pCS-APTA-glnA and pBV-nhoA | This study |
| Plasmid | Description | Source |
| pZE12-luc | pLlacO1; luc ; ColE1 ori ; Amp R | href="#bib23" Lin et al., (2013) |
| pCS27 | pLlacO1; p15A ori; Kan R | [Lin et al., (2013)](#bib23" Lin et al., (2013) pCS27 pLlacO1; p15A ori; KanR Lin et al., (2013) pSA74 pLlacO1; pSC101 ori; CmR Lin et al., (2013) pBV pR/pL; pUC ori; CmR This study pETDuet-1 two T7 promoters; two MCS; pBR322 ori; AmpR Novagen pCS-APTA pCS27 containing aroL, ppsA, tktA, aroGfbr from Escherichia coli MG1655 href="#bib29" Shen et al., (2017) pZE-AAA pZE12-luc containing AAA from bacterium CSBL00001 This study pET-AAA pETDuet-1 containing AAA from bacterium CSBL00001 This study pZE-nhoA pZE12-luc containing nhoA from Escherichia coli MG1655 This study pET-nhoA pETDuet-1 containing nhoA from Escherichia coli MG1655 This study pZE-MNX1 pZE12-luc containing MNX1 from Candida parapsilosis CBS604 Shen et al., (2017) pET-MNX1 pETDuet-1 containing MNX1 from Candida parapsilosis CBS604 Shen et al., (2017) pZE-EcpabABC pZE12-luc containing pabA, pabB, pabC from Escherichia coli MG1655 This study pZE-BspabABC pZE12-luc containing pabA, pabB, pabC from Bacillus subtilis 168 This study pZE-ScABZ1-ABZ2 pZE12-luc containing ABZ1, ABZ2 from Saccharomyces cerevisiae This study pCS-APTA-glnA pCS-APTA containing glnA from Escherichia coli MG1655 This study pZE-EcpabABC-MNX1 pZE12-luc containing pLlacO1-pabABC and pLlacO1-MNX1 This study pSA-nhoA pSA74 containing nhoA from Escherichia coli MG1655 This study pBV-nhoA pBV-CL containing nhoA from Escherichia coli MG1655 This study) |
| pSA74 | pLlacO1; pSC101 ori; Cm R | [Lin et al., (2013)](#bib23" Lin et al., (2013) pCS27 pLlacO1; p15A ori; KanR Lin et al., (2013) pSA74 pLlacO1; pSC101 ori; CmR Lin et al., (2013) pBV pR/pL; pUC ori; CmR This study pETDuet-1 two T7 promoters; two MCS; pBR322 ori; AmpR Novagen pCS-APTA pCS27 containing aroL, ppsA, tktA, aroGfbr from Escherichia coli MG1655 href="#bib29" Shen et al., (2017) pZE-AAA pZE12-luc containing AAA from bacterium CSBL00001 This study pET-AAA pETDuet-1 containing AAA from bacterium CSBL00001 This study pZE-nhoA pZE12-luc containing nhoA from Escherichia coli MG1655 This study pET-nhoA pETDuet-1 containing nhoA from Escherichia coli MG1655 This study pZE-MNX1 pZE12-luc containing MNX1 from Candida parapsilosis CBS604 Shen et al., (2017) pET-MNX1 pETDuet-1 containing MNX1 from Candida parapsilosis CBS604 Shen et al., (2017) pZE-EcpabABC pZE12-luc containing pabA, pabB, pabC from Escherichia coli MG1655 This study pZE-BspabABC pZE12-luc containing pabA, pabB, pabC from Bacillus subtilis 168 This study pZE-ScABZ1-ABZ2 pZE12-luc containing ABZ1, ABZ2 from Saccharomyces cerevisiae This study pCS-APTA-glnA pCS-APTA containing glnA from Escherichia coli MG1655 This study pZE-EcpabABC-MNX1 pZE12-luc containing pLlacO1-pabABC and pLlacO1-MNX1 This study pSA-nhoA pSA74 containing nhoA from Escherichia coli MG1655 This study pBV-nhoA pBV-CL containing nhoA from Escherichia coli MG1655 This study) |
| pBV | pR/pL; pUC ori; Cm R | This study |
| pETDuet-1 | two T7 promoters; two MCS; pBR322 ori ; Amp R | Novagen |
| pCS-APTA | pCS27 containing aroL , ppsA , tktA , aroG fbr from Escherichia coli MG1655 | href="#bib29" Shen et al., (2017) |
| pZE-AAA | pZE12-luc containing AAA from bacterium CSBL00001 | This study |
| pET-AAA | pETDuet-1 containing AAA from bacterium CSBL00001 | This study |
| pZE-nhoA | pZE12-luc containing nhoA from Escherichia coli MG1655 | This study |
| pET-nhoA | pETDuet-1 containing nhoA from Escherichia coli MG1655 | This study |
| pZE-MNX1 | pZE12-luc containing MNX1 from Candida parapsilosis CBS604 | [Shen et al., (2017)](#bib23" Lin et al., (2013) pCS27 pLlacO1; p15A ori; KanR Lin et al., (2013) pSA74 pLlacO1; pSC101 ori; CmR Lin et al., (2013) pBV pR/pL; pUC ori; CmR This study pETDuet-1 two T7 promoters; two MCS; pBR322 ori; AmpR Novagen pCS-APTA pCS27 containing aroL, ppsA, tktA, aroGfbr from Escherichia coli MG1655 href="#bib29" Shen et al., (2017) pZE-AAA pZE12-luc containing AAA from bacterium CSBL00001 This study pET-AAA pETDuet-1 containing AAA from bacterium CSBL00001 This study pZE-nhoA pZE12-luc containing nhoA from Escherichia coli MG1655 This study pET-nhoA pETDuet-1 containing nhoA from Escherichia coli MG1655 This study pZE-MNX1 pZE12-luc containing MNX1 from Candida parapsilosis CBS604 Shen et al., (2017) pET-MNX1 pETDuet-1 containing MNX1 from Candida parapsilosis CBS604 Shen et al., (2017) pZE-EcpabABC pZE12-luc containing pabA, pabB, pabC from Escherichia coli MG1655 This study pZE-BspabABC pZE12-luc containing pabA, pabB, pabC from Bacillus subtilis 168 This study pZE-ScABZ1-ABZ2 pZE12-luc containing ABZ1, ABZ2 from Saccharomyces cerevisiae This study pCS-APTA-glnA pCS-APTA containing glnA from Escherichia coli MG1655 This study pZE-EcpabABC-MNX1 pZE12-luc containing pLlacO1-pabABC and pLlacO1-MNX1 This study pSA-nhoA pSA74 containing nhoA from Escherichia coli MG1655 This study pBV-nhoA pBV-CL containing nhoA from Escherichia coli MG1655 This study) |
| pET-MNX1 | pETDuet-1 containing MNX1 from Candida parapsilosis CBS604 | [Shen et al., (2017)](#bib23" Lin et al., (2013) pCS27 pLlacO1; p15A ori; KanR Lin et al., (2013) pSA74 pLlacO1; pSC101 ori; CmR Lin et al., (2013) pBV pR/pL; pUC ori; CmR This study pETDuet-1 two T7 promoters; two MCS; pBR322 ori; AmpR Novagen pCS-APTA pCS27 containing aroL, ppsA, tktA, aroGfbr from Escherichia coli MG1655 href="#bib29" Shen et al., (2017) pZE-AAA pZE12-luc containing AAA from bacterium CSBL00001 This study pET-AAA pETDuet-1 containing AAA from bacterium CSBL00001 This study pZE-nhoA pZE12-luc containing nhoA from Escherichia coli MG1655 This study pET-nhoA pETDuet-1 containing nhoA from Escherichia coli MG1655 This study pZE-MNX1 pZE12-luc containing MNX1 from Candida parapsilosis CBS604 Shen et al., (2017) pET-MNX1 pETDuet-1 containing MNX1 from Candida parapsilosis CBS604 Shen et al., (2017) pZE-EcpabABC pZE12-luc containing pabA, pabB, pabC from Escherichia coli MG1655 This study pZE-BspabABC pZE12-luc containing pabA, pabB, pabC from Bacillus subtilis 168 This study pZE-ScABZ1-ABZ2 pZE12-luc containing ABZ1, ABZ2 from Saccharomyces cerevisiae This study pCS-APTA-glnA pCS-APTA containing glnA from Escherichia coli MG1655 This study pZE-EcpabABC-MNX1 pZE12-luc containing pLlacO1-pabABC and pLlacO1-MNX1 This study pSA-nhoA pSA74 containing nhoA from Escherichia coli MG1655 This study pBV-nhoA pBV-CL containing nhoA from Escherichia coli MG1655 This study) |
| pZE-EcpabABC | pZE12-luc containing pabA , pabB , pabC from Escherichia coli MG1655 | This study |
| pZE-BspabABC | pZE12-luc containing pabA , pabB , pabC from Bacillus subtilis 168 | This study |
| pZE-ScABZ1-ABZ2 | pZE12-luc containing ABZ1 , ABZ2 from Saccharomyces cerevisiae | This study |
| pCS-APTA-glnA | pCS-APTA containing glnA from Escherichia coli MG1655 | This study |
| pZE-EcpabABC-MNX1 | pZE12-luc containing pLlacO1-pabABC and pLlacO1-MNX1 | This study |
| pSA-nhoA | pSA74 containing nhoA from Escherichia coli MG1655 | This study |
| pBV-nhoA | pBV-CL containing nhoA from Escherichia coli MG1655 | This study |
2.2 质粒构建
质粒 pCS-APTA、pZE-MNX1 与 pET-MNX1 为本实验室前期研究构建(Shen 等,2017)。经密码子优化的芳基酰胺酶基因 AAA (来源菌株:CSBL00001)由上海生工生物工程股份有限公司人工合成。将 AAA 基因 与大肠杆菌 MG1655 来源 nhoA 基因 分别利用 Acc65I 和 XbaI 酶切位点克隆至 pZE12-luc 载体,获得重组质粒 pZE-AAA 与 pZE-nhoA;再分别通过 BamHI 和 XhoI 位点将两个基因插入 pETDuet-1 载体,构建 pET-AAA 与 pET-nhoA。
为实现对氨基苯甲酸(p-ABA)从头合成,将大肠杆菌 MG1655 来源 pabA、pabB、pabC 基因通过 Acc65I、AatII、BamHI、XbaI 多克隆位点插入 pZE12-luc 载体,得到质粒 pZE-EcpabABC;将枯草芽孢杆菌 186 来源 pabA、pabB、pabC 基因经 Acc65I、SacI、BamHI、XbaI 位点克隆至 pZE12-luc,构建 pZE-BspabABC;将酿酒酵母来源 ABZ1、ABZ2 基因利用 Acc65I、BamHI、XbaI 位点插入 pZE12-luc,得到 pZE-ScABZ1-ABZ2。
将表达操纵子 PLlacO1-glnA 经 SpeI 与 SacI 位点插入 pCS-APTA 质粒,构建 pCS-APTA-glnA。为实现对氨基苯酚(p-AP)合成,将操纵子 PLlacO1-MNX1 插入 pZE-EcpabABC 的 SpeI、SacI 位点,获得 pZE-EcpabABC-MNX1。将 nhoA 基因分别克隆:经 Acc65I、BamHI 插入 pSA74 载体得到 pSA-nhoA;经 BamHI、PstI 插入 pBV-CL 载体。
2.3 蛋白表达
将质粒 pET-AAA、pET-nhoA、pET-MNX1 分别转化至大肠杆菌 BL21 Star (DE3) 感受态细胞,用于蛋白表达与纯化。单菌落接种于含 100 μg/mL 氨苄青霉素的 4 mL LB 培养基,37 ℃ 预培养 12 h;按 1% 接种量转接至 50 mL 含同等抗生素的 LB 培养基,37 ℃ 培养 3 h;加入 0.5 mM IPTG 诱导,16 ℃ 低温培养 22 h 完成蛋白表达。
2.4 AAA、NhoA 与 MNX1 体外酶活测定
AAA 与 NhoA 酶活测定参照 Ko 等人方法并稍加修改(Yamamura 等,2000)。总反应体系 2 mL:含 50 mM Tris-HCl(pH 7.0)、2000 μM 乙酸(AAA 反应)或 670 μM 乙酰辅酶 A(NhoA 反应)、0~300 μM p-ABA / 0~150 μM p-AP / 0~30 μM AAP,以及 1.58 μM AAA 或 4.05 μM NhoA;37 ℃ 孵育 10 min,加入 20%(体积分数)硫酸终止反应。
MNX1 酶活测定参照本课题组前期方法(Shen 等,2017)。总体系 1.5 mL:50 mM 磷酸钾缓冲液(pH 7.0)、300 μM 黄素腺嘌呤二核苷酸(FAD)、500 μM 还原型烟酰胺腺嘌呤二核苷酸(NADH)、0~300 μM p-ABA、0.26 μM MNX1;37 ℃ 反应 10 min。
采用高效液相色谱(HPLC)检测产物生成速率,计算酶活力;利用 OriginPro8.5 对米氏方程进行非线性回归,拟合表观动力学参数。所有实验均设置至少三次生物学重复。
2.5 底物饲喂实验
将携带 pZE-AAA、pZE-nhoA、pZE-MNX1 的大肠杆菌 BW25113/F' 菌株接种于 4 mL LB 培养基,37 ℃ 过夜培养;取 500 μL 过夜菌液转接至 50 mL 含 100 μg/mL 氨苄青霉素的 M9Y 甘油培养基,37 ℃ 培养 3 h;加入 0.5 mM IPTG 诱导后,调整培养温度至 30 ℃,外源加入底物 p-ABA、p-AP 或 AAP;每 12 h 取样,HPLC 检测代谢产物。饲喂实验均设置至少三次重复。
2.6 p-ABA、p-AP 与 AAP 的从头生物合成
采用添加相应抗生素的 M9Y 甘油培养基进行从头合成发酵;以大肠杆菌 BW25113/F' 与 CX0 作为生产菌株。菌株先在 4 mL LB 培养基中 37 ℃ 过夜活化;取 500 μL 种子液转接至 50 mL M9Y 甘油培养基,37 ℃、250 rpm 培养 3 h;加入 0.5 mM IPTG 诱导,30 ℃ 继续培养 48 h;每 12 h 取样,HPLC 定量检测。所有摇瓶实验均设置至少三次重复。
2.7 代谢产物分析
采用岛津高效液相色谱仪、反相 Diamonsil C18 色谱柱,定量检测 p-ABA、p-AP、AAP 及对乙酰氨基苯甲酸。流动相:甲醇(A 相)-- 含 0.1% 磷酸纯水(B 相),流速 1 mL/min,柱温 40 ℃。洗脱程序:5%~50% 甲醇洗脱 15 min;50%~100% 甲醇洗脱 2 min;100%~5% 甲醇平衡 3 min;5% 甲醇稳定淋洗 5 min。检测波长 280 nm,对上述四种代谢产物进行定量分析。
3 结果与分析
3.1 对氨基苯酚 N - 乙酰转移酶的筛选与功能表征
本研究以大肠杆菌天然中间产物 对氨基苯甲酸(p-ABA) 为前体,设计一条全新的对乙酰氨基酚(AAP)人工生物合成通路:p-ABA 经单加氧酶催化生成 p-AP,再由 p-AP N - 乙酰转移酶乙酰化生成 AAP。其中,p-AP 向 AAP 的转化 是整条通路的核心步骤。
已有研究表明,菌株 CSBL00001 来源的芳基酰胺酶 AAA 在酸性条件下可可逆催化 p-AP 乙酰化生成 AAP(Ko 等,2012),但该酶在生理温和条件下是否仍具备合成活性尚不明确。本研究在 pH 7.0 中性条件下开展体外酶活测定,分别以 p-AP 和 AAP 为底物测定催化动力学参数。如表 2 及附图 S1 所示:在中性条件下,AAA 对 AAP 的底物亲和力高出 p-AP 约 10 倍,催化周转数相近;动力学参数为:AAP 的 K ₘ = 4.06 ± 0.25 mM,k cat = 150.85 ± 2.85 min⁻¹;p-AP 的 K ₘ = 42.76 ± 5.28 mM,k cat = 146.61 ± 6.87 min⁻¹。结果证实:在生理温和条件下,AAA 更倾向于催化 AAP 水解生成 p-AP 与乙酸 ,不利于正向合成 AAP。
|-------------------|-------------------|--------------------------------------|---|-------------------------------------------------------------|---|---------------------------------------------------------------------------------------------------------------------|
| Enzyme | Substrate | K m (mM) || k cat (min −1 ) | k cat / K m (mM −1 min −1 ) ||
| AAA | p-AP | 42.76 ± 5.28 || 146.61 ± 6.87 | 3.43 ||
| AAA | AAP | 4.06 ± 0.25 || 150.85 ± 2.85 | 37.16 ||
| NhoA | p-ABA | 19.19 ± 2.80 || 338.84 ± 17.45 | 17.66 ||
| NhoA | p-AP | 29.59 ± 3.20 || 83.01 ± 3.37 | 2.81 ||
| NhoA | AAP | N.D. |||||
| Enzyme | Substrate | K m (μM) | k cat (min −1 ) ||| k cat / K m (μM −1 min −1 ) |
| MNX1 | p-ABA | 136.02 ± 34.53 | 2.76 ± 0.26 ||| 0.02 |
| NahG | p-ABA | N.D. |||||
| PaantABC | p-ABA | N.D. |||||
| PfantABC | p-ABA | N.D. |||||
| PpbenABCD | p-ABA | N.D. |||||
Data are presented as mean ± s.d. (n = 3).
为进一步评估芳基酰胺酶 AAA 的体内催化活性,本研究分别以 ** 对氨基苯酚(p-AP)和 对乙酰氨基酚(AAP)** 为底物开展饲喂实验。将质粒 pZE-AAA 转入大肠杆菌 BW25113/F′,获得菌株 CX1;同时将空载体 pZE12-luc 转入同一宿主菌株,构建对照菌株 CX2。
培养 48 h 结果显示:向培养液中添加 1200 mg/L p-AP 时,菌株 CX1 可生成 216.45 mg/L AAP(图 2A)。与之相符,以 1200 mg/L AAP 为底物饲喂时,菌株 CX1 可将其水解生成 705.54 mg/L p-AP(图 2B)。
上述体内实验结果证实:AAA 更倾向于催化 AAP 水解,而非正向合成 AAP ,与体外酶活测定结论一致。AAA 的催化偏好与其反应吉布斯自由能变(ΔrG'°net)密切相关:在生理温和条件(25 ℃、pH=7)下,该反应吉布斯自由能变为 13.5 kJ/mol,表明正向合成反应在热力学上自发程度低、难以进行 ;而在酸性条件(pH<4)下,ΔrG'°net<0,反应才可自发向合成方向进行。
由于 AAA 在常规微生物培养条件下以逆反应水解为主 ,严重限制其在 AAP 生物合成中的应用,因此有必要筛选并鉴定其他具有功能的对氨基苯酚 N - 乙酰转移酶 。
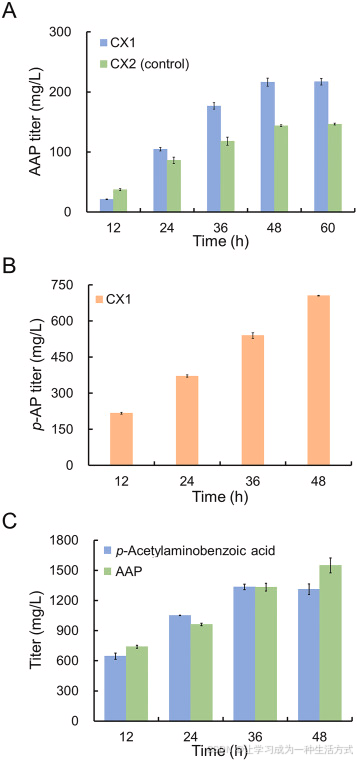
图 2 对氨基苯酚 N - 乙酰转移酶的筛选与功能表征
(A) 菌株 CX1(BW25113/F′ 携带 pZE-AAA)与对照菌株 CX2(BW25113/F′ 携带空质粒 pZE12-luc)表达 AAA,以对氨基苯酚(p-AP)为底物合成对乙酰氨基酚(AAP);(B) 菌株 CX1 表达 AAA,以对乙酰氨基酚(AAP)为底物转化生成对氨基苯酚(p-AP);(C) 菌株 CX3(BW25113/F′ 携带 pZE-NhoA)表达 NhoA,合成对乙酰氨基酚(AAP)与对乙酰氨基苯甲酸。所有数据均为三次生物学独立重复 的平均值 ± 标准差。
有意思的是,空载对照菌株 CX2 在添加 p-AP 底物后,仍可合成 143.66 mg/L 的 AAP(图 2A),说明大肠杆菌自身存在一种未知的内源 p-AP N - 乙酰转移酶 。通过大肠杆菌数据库 EcoCyc 检索(Kuznetsova 等,2005),注释到一个推定 N - 乙酰转移酶NhoA ,归类为芳基胺 N - 乙酰转移酶。由于 p-AP 属于芳基胺类化合物,因此推测 NhoA 可识别 p-AP 并催化生成 AAP。
为验证该推测,本研究测定了 NhoA 的酶动力学参数。如表 2 及附图 S2 所示:NhoA 对 p-AP 确实具有催化活性,底物结合亲和力 Km=29.59±3.20 mM,比 AAA 高出 1.5 倍;尽管 NhoA 催化周转数 kcat=83.01±3.37 min−1 略低,但以 AAP 为底物时未检测到逆水解活性 。
此外,考虑到 p-ABA 与 p-AP 结构相似,本研究同时测定了 NhoA 对 p-ABA 的催化能力。结果显示,NhoA 对 p-ABA 活性更高:Km=19.19±2.80 mM,kcat=338.84±17.45 min−1(表 2、附图 S2)。表明 NhoA 可同时利用 p-AP 和 p-ABA 作为底物,且更偏好以 p-ABA 为底物 。
随后通过饲喂实验评价 NhoA 的体内转化效率。将质粒 pZE-nhoA 转入大肠杆菌 BW25113/F′,命名为菌株 CX3,分别以 p-AP 和 p-ABA 为外源底物。由图 2C 可见:培养 48 h 后,1500 mg/L p-AP 可被 CX3 转化生成 1549.18 mg/L AAP,摩尔转化率达 75% ;以 1500 mg/L p-ABA 为底物时,生成 1311.82 mg/L 对乙酰氨基苯甲酸(图 2C)。以上结果证明:NhoA 在体内可高效催化 p-AP 生成 AAP ;但当体系中同时存在 p-AP 与 p-ABA 时,易生成对乙酰氨基苯甲酸这一副产物。
为进一步确认 NhoA 是大肠杆菌中主导型内源 p-AP N - 乙酰转移酶 ,本研究在 BW25113/F′中敲除 nhoA 基因,获得菌株 CX0。以 p-AP 进行底物饲喂发酵,CX0 发酵液中检测不到 AAP 生成 ,证实 NhoA 是大肠杆菌体内负责 p-AP 乙酰化的关键内源酶。综上,NhoA 对 p-AP 具有优异催化活性,可高效合成 AAP。
3.2 挖掘新型生化反应实现对氨基苯甲酸向对氨基苯酚的生物转化
获得性能优良的 p-AP N - 乙酰转移酶后,p-ABA 转化生成 p-AP 成为本人工通路的关键限速步骤。从反应机制分析,该过程需要单加氧酶 催化:使 p-ABA 的羧基发生脱羧还原 ,转化为羟基。
本课题组前期研究发现:恶臭假单胞菌 DOT-T1E 来源水杨酸 1 - 单加氧酶 NahG ,可催化水杨酸脱羧羟基化生成邻苯二酚(Lin 等,2014);荧光假单胞菌、铜绿假单胞菌来源邻氨基苯甲酸 1,2 - 双加氧酶 PfantABC、PaantABC ,以及恶臭假单胞菌 KT2440 来源苯甲酸 1,2 - 双加氧酶 PpbenABCD ,均可催化邻氨基苯甲酸还原生成邻苯二酚(Lin 等,2014;Sun 等,2013);此外,近平滑假丝酵母 CBS604 来源4 - 羟基苯甲酸 1 - 羟化酶 MNX1 ,可催化对羟基苯甲酸水解生成对苯二酚(Shen 等,2017)。
鉴于上述酶的反应机制相似、底物结构相近 ,且酶具有底物杂泛性 ,本研究推测这 5 种酶均具备催化 p-ABA 生成 p-AP 的潜力。对纯化后的 5 种候选酶进行动力学参数测定,结果显示:仅 MNX1 对 p-ABA 具有催化活性 ,Km=136.02±34.53 μM,kcat=2.76±0.26 min−1(表 2、附图 S3);其余 4 种酶未检测到催化活性。
进一步开展体内饲喂实验验证 MNX1 功能。选用 nhoA 敲除菌株 CX0 作为宿主,避免生成的 p-AP 被乙酰化消耗;将 pZE-MNX1 转入 CX0,获得菌株 CX4。如图 3 所示:以 800 mg/L p-ABA 为底物,菌株 CX4 可生成 553.31 mg/L p-AP,发酵液中仍剩余 99.27 mg/L 未利用的 p-ABA。该结果证实 MNX1 可催化 p-ABA 转化为 p-AP,但整体催化效率仍有待提升 。
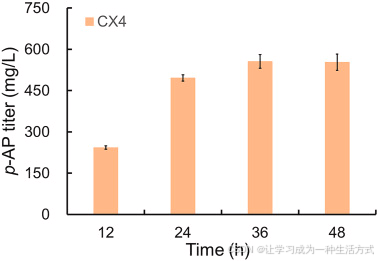
图 3 鉴定对氨基苯甲酸单加氧酶实现 p-ABA 向 p-AP 生物转化
菌株 CX4(CX0 携带 pZE-MNX1)合成对氨基苯酚(p-AP)的产量。所有数据均为三次生物学独立重复的平均值 ± 标准差。
3.3 高产对氨基苯甲酸(p-ABA)菌株的构建
在完成对氨基苯甲酸单加氧酶与对氨基苯酚 N - 乙酰转移酶的功能表征后,本研究进一步开展p-ABA 高产菌株 构建。在微生物体内,p-ABA 是参与叶酸合成的天然代谢物(Koma et al., 2014),由莽草酸途径 关键中间产物分支酸 转化生成。分支酸经4 - 氨基 - 4 - 脱氧分支酸合酶 PabAB 催化生成 4 - 氨基 - 4 - 脱氧分支酸,再由氨基脱氧分支酸裂解酶 PabC 催化生成 p-ABA(He et al., 2004)。
本研究选取三个不同来源的 PabABC 酶体系:大肠杆菌 MG1655、枯草芽孢杆菌 168、酿酒酵母 (Averesch and Rothschild, 2019; Averesch et al., 2016; Koma et al., 2014),已有文献证实三者均具备合成 p-ABA 的能力。为比较催化活性,将 EcpabABC 、BspabABC 、ScABZ1-ABZ2 分别克隆至 pZE12-luc 载体,获得重组质粒 pZE-EcpabABC、pZE-BspabABC、pZE-ScABZ1-ABZ2。
分支酸的充足供给是分支酸衍生物高产 的关键因素。在大肠杆菌中,分支酸的过量合成会受到苯丙氨酸、酪氨酸、色氨酸三种芳香族氨基酸的反馈抑制 (Kikuchi et al., 1997; Pittard et al., 2005)。目前已报道多种代谢工程策略优化分支酸通路,包括:通路关键基因过表达、解除反馈抑制、通过失活磷酸转移酶系统(PTS)糖转运系统或下调糖酵解与三羧酸循环,提升磷酸烯醇式丙酮酸(PEP)供给等(Fujiwara et al., 2020; Huccetogullari et al., 2019; Kogure et al., 2016; Noda et al., 2016)。
本课题组前期研究证实,过表达分支酸强化质粒 pCS-APTA (携带 aroL、ppsA、tktA 及抗反馈抑制突变基因 aroG<sup>fbr</sup> )可显著提升胞内分支酸通量(Lin et al., 2013)。为实现 p-ABA 高效合成,将 pCS-APTA 分别与 pZE-EcpabABC、pZE-BspabABC、pZE-ScABZ1-ABZ2 共转化,获得菌株 CX5、CX6、CX7。
如图 4 结果所示:携带大肠杆菌 MG1655 来源 pabABC 的菌株 CX5 合成 p-ABA 能力最强,培养 36 h 产量达 528.71 mg/L ;而含枯草芽孢杆菌、酿酒酵母来源 PabABC 的菌株 CX6、CX7 产量仅分别为 335.13 mg/L、31.51 mg/L。上述结果表明,大肠杆菌 MG1655 来源的 PabABC 是最适合用于 p-ABA 合成的功能酶。
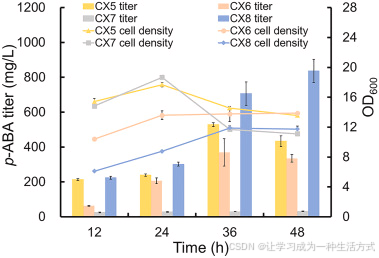
图 4 不同菌株以甘油为唯一碳源从头合成对氨基苯甲酸(p-ABA)
菌株 CX5:共表达质粒 pCS-APTA + pZE-EcpabABC;菌株 CX6:共表达质粒 pCS-APTA + pZE-BspabABC;菌株 CX7:共表达质粒 pCS-APTA + pZE-ScABZ1-ABZ2;菌株 CX8:共表达质粒 pZE-EcpabABC + pCS-APTA-glnA。所有数据均为三次生物学独立重复的平均值 ± 标准差。
为进一步提升 p-ABA 产量,本研究分析了 PabABC 的反应机制,发现谷氨酰胺 为 PabAB 提供氨基供体。据此推测,提高胞内谷氨酰胺供给量可促进 p-ABA 合成。因此,本研究过表达大肠杆菌来源谷氨酰胺合成酶基因 glnA ,构建谷氨酸--谷氨酰胺循环通路,增强谷氨酰胺合成与供给(Sun 等,2013)。将质粒 pCS-APTA-glnA 与 pZE-EcpabABC 共转化至大肠杆菌 BW25113/F′,获得菌株 CX8。
发酵结果显示,菌株 CX8 的 p-ABA 产量进一步提升至 836.43 mg/L (图 4),较对照菌株 CX5 提高 58%,为目前大肠杆菌摇瓶发酵报道的最高产量。据文献所知,该产量也是迄今为止大肠杆菌合成 p-ABA 的最高摇瓶水平。
3.4 对乙酰氨基酚(AAP)的从头生物合成
在成功构建高效 p-ABA 合成通路基础上,进一步开展 AAP 从头合成研究。首先利用大肠杆菌内源 p-AP N - 乙酰转移酶 NhoA,尝试 AAP 从头合成。将质粒 pCS-APTA-glnA 与 pZE-EcpabABC-MNX1 转入大肠杆菌 BW25113/F′,得到菌株 CX9。
如图 5A 所示,菌株 CX9 培养 48 h 可合成 53.31 mg/L AAP ,同时胞内积累 136.46 mg/L p-AP 与 32.34 mg/L p-ABA,说明MNX1 与 NhoA 催化活性不足 是整条通路的限速步骤。该结果同时证实,本研究设计的 AAP 人工合成通路可在大肠杆菌中正常运作。
为进一步提高 AAP 产量,将 nhoA 基因置于高拷贝质粒 上过表达,构建携带 pZE-EcpabABC-MNX1-nhoA 与 pCS-APTA-glnA 的菌株 CX10。出乎意料的是,菌株 CX10 发酵液中未检测到 AAP、p-ABA 和 p-AP ,仅大量生成副产物对乙酰氨基苯甲酸,产量高达 336.90 mg/L(图 5B)。
该副产物生成规律可由体外酶活结果解释(表 2):NhoA 更偏好识别 p-ABA 而非 p-AP 作为底物;且以 p-ABA 为底物时,NhoA 催化活性远高于 MNX1。一旦胞内积累 p-ABA,会优先被 NhoA 乙酰化生成对乙酰氨基苯甲酸,而难以被 MNX1 还原为 p-AP。
基因组本底单拷贝 nhoA 的菌株 CX9 可产 53.31 mg/L AAP,而高拷贝过表达 nhoA 的 CX10 完全检测不到 AAP,说明nhoA 表达量过高反而抑制 AAP 合成 。
为此,将 nhoA 构建至低拷贝质粒 pSA-nhoA,将 pCS-APTA-glnA、pZE-EcpabABC-MNX1、pSA-nhoA 共转入 BW25113/F′,命名为菌株 CX11。菌株 CX11 可合成 14.32 mg/L AAP,但产量仍低于未外源过表达 nhoA 的 CX9;培养 48 h 仍积累 312.06 mg/L 对乙酰氨基苯甲酸副产物(图 5C)。
上述结果表明:降低 nhoA 表达水平可小幅减少副产物积累,但仍需开发更有效的调控策略,进一步提升 AAP 合成产量。
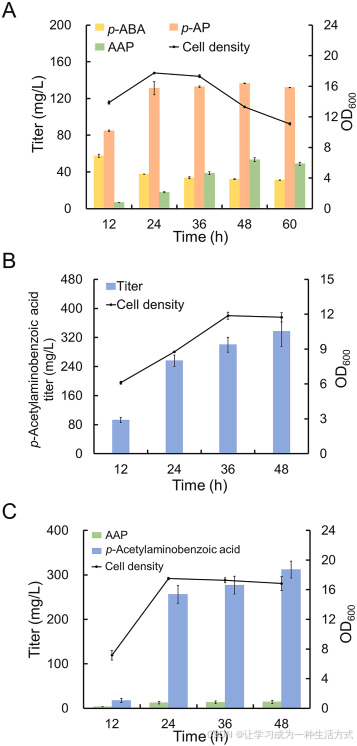
图 5 大肠杆菌以甘油为碳源从头合成对乙酰氨基酚(AAP)
(A) 共表达质粒 pCS-APTA-glnA 与 pZE-EcpabABC-MNX1 的菌株 CX9 合成 p-ABA、p-AP 及 AAP 的产量;(B) 共表达质粒 pCS-APTA-glnA 与 pZE-EcpabABC-MNX1-nhoA 的菌株 CX10 生成副产物对乙酰氨基苯甲酸的产量;(C) 共表达质粒 pCS-APTA-glnA、pZE-EcpabABC-MNX1 与 pSA-nhoA 的菌株 CX11 生成对乙酰氨基苯甲酸与 AAP 的产量。所有数据均为三次生物学独立重复的平均值 ± 标准差。
3.5 对乙酰氨基酚合成的动态调控
如上所述,NhoA 对 p-ABA 和 p-AP 具有底物杂泛性,易引发副产物生成,是限制 AAP 产量的关键瓶颈。由于 p-ABA 是合成 p-AP 的上游前体,我们推测:待大部分 p-ABA 转化为 p-AP 后再启动 nhoA 表达 ,可有效减少副产物生成。
为实现 nhoA 表达延迟、同时避免使用昂贵化学诱导剂,利用胞内信号或发酵过程信号对 nhoA 进行动态调控 是理想策略。相比于代谢物、光、pH 等常见调控信号,温度 具有灵敏、通用、均一可控等优势,非常适合用于代谢通路动态调控(Shen et al., 2019)。
本研究采用温度诱导调控系统 :包含噬菌体 λ 启动子 P<sub>R</sub>/P<sub>L</sub> 与温度敏感型阻遏蛋白 CI857,仅通过切换培养温度即可实现基因表达的动态开关(Harder et al., 2018; Zhou et al., 2016)。构建质粒 pBV-nhoA,将 nhoA 置于 P<sub>R</sub>/P<sub>L</sub> 启动子调控之下:30 ℃ 培养时,活化的 CI857 结合 P<sub>R</sub>/P<sub>L</sub> ,抑制 nhoA 表达 ;升温至 42 ℃ 后,CI857 热失活并解除对启动子的抑制,启动 nhoA 表达 。
将质粒 pZE-EcpabABC-MNX1、pCS-APTA-glnA 与 pBV-nhoA 共转入菌株 CX0,获得工程菌株 CX12。设置不同温度切换时间 (0 h、3 h、6 h、9 h、12 h)筛选最优发酵条件。
由图 6A 及附图 S4 可知,不同时间由 30 ℃ 升温至 42 ℃,AAP 积累产量差异显著。发酵 9 h 进行温度切换 时,菌株 CX12 培养 48 h 的 AAP 产量达到最高,为 120.03 mg/L ,较无延迟调控组(0 h 即刻升温)产量提升 2 倍;同时副产物对乙酰氨基苯甲酸产量由 387.87 mg/L 降至 307 mg/L(图 6B)。
上述结果表明:延迟 nhoA 表达 可有效削减副产物生成、显著提升 AAP 合成产量。
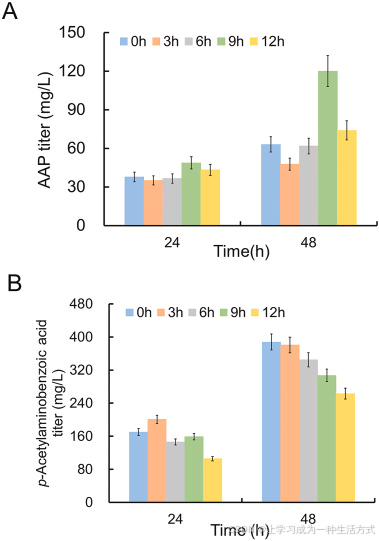
图 6 利用携带 pCS-APTA-glnA、pZE-EcpabABC 与 pBV-nhoA 的菌株 CX12 对乙酰氨基酚(AAP)合成进行动态调控
(A) 不同温度切换时间下的 AAP 产量;(B) 不同温度切换时间下对乙酰氨基苯甲酸副产物产量。所有数据均为三次独立实验的平均值 ± 标准差。
4. 讨论
随着代谢工程与合成生物学技术的发展,通过人工设计生物合成通路 ,可使微生物宿主合成非天然化合物(Lee 等,2021;Wang 等,2020)。人工通路的构建通常需要将已知酶催化的天然生化反应进行重组与整合,嵌入合成通路中(Kim 等,2021)。但该策略往往受限于可用新型生化反应资源不足 。
本研究基于已知酶催化机制,挖掘全新生化反应,设计了一条对乙酰氨基酚(AAP)人工生物合成通路。通过功能表征对羟基苯甲酸单加氧酶 与大肠杆菌内源芳基胺 N - 乙酰转移酶 ,鉴定出两条关键生化反应:p-ABA 转化为 p-AP、p-AP 转化为 AAP。依托上述发现,本研究实现了微生物利用简单碳源从头合成非天然化合物 AAP 。本工作证明:挖掘并拓展已知酶的底物杂泛性 ,是构建人工通路、合成非天然化合物的有效途径。
然而,酶的底物杂泛性并非总能有利于目标产物合成。当一种杂泛酶可同时催化多个通路中间物时,往往会诱发副产物生成 (Wang 等,2017)。在本研究通路中,NhoA 可同时乙酰化 p-ABA 与 p-AP,造成副产物对乙酰氨基苯甲酸 大量积累。
为解决该问题,本研究引入温度诱导调控系统 延迟 nhoA 表达,最终将 AAP 产量提升至 120.03 mg/L。值得注意的是,副产物对乙酰氨基苯甲酸产量仍居高不下,维持在 300 mg/L 左右。因此,后续仍需进一步优化,引导更多碳流从 p-ABA 流向 p-AP 合成支路。
通过蛋白质工程 强化 MNX1 催化效率、改造 NhoA 底物特异性,是后续优化的可行方向;但目前 MNX1 与 NhoA 的晶体结构尚未解析,给定点理性改造 带来较大困难。此外,构建微生物共培养体系 ,降低 NhoA 与 p-ABA 的接触机会,也有望进一步提高 AAP 产量。