01
导语
各位同学,大家好。影像组学发展到现在,如果还停留在"提取一堆特征、套几个模型、比一比C-index",那只能说你会算命,但不会看病 。别人一问:你这个特征为什么选进来?它跟肿瘤的恶性行为有什么关系?凭什么就能指导治疗?------你大概率只能沉默。真正能发高分的影像组学研究,都在做同一件事:给影像特征找个"生物学户口" ,让CT上的灰度差异,能对应到细胞、通路、微环境的真实变化上。今天我们就用这篇25年发表的肝癌PA-TACE预测研究,拆解一下如何不硬凑、不牵强、有理有据地把影像表型挂靠到免疫抑制微环境,让你从"调参侠"升级为"能讲机制故事的研究者"。

**★题目:**Development and Validation of a CT-based Online Calculator for Prognosis and Postoperative Adjuvant Transcatheter Arterial Chemoembolization Benefit Prediction in Resected Hepatocellular Carcinoma: A Multicenter Retrospective Cohort Study
(基于CT的在线计算器在肝细胞癌切除术后预后及辅助经导管动脉化疗栓塞获益预测中的开发与验证)
★期刊:《International Journal of Surgery》(中科院2区,IF=10.3)
**★研究疾病:**肝细胞癌(HCC)
**★生物学机制:**肿瘤微环境(TME)的免疫抑制性特征
**★发表时间:**2025年12月
02
研究背景-从 "临床问题" 落到 "生物学问题"
肝细胞癌(HCC)是全球范围内发病率高、死亡率高的恶性肿瘤,手术切除(SR)是早期HCC的主要治疗手段 ,但术后复发率居高不下,5年总体生存率仍不理想。为降低复发风险,临床上尝试使用术后辅助经导管动脉化疗栓塞(PA-TACE) ,但其疗效存在显著争议:部分研究显示PA-TACE可延长高危患者的生存期,而另一些研究则未观察到明确获益,甚至提示可能带来不必要的毒副作用。这种争议的核心原因在于,PA-TACE的疗效可能存在显著的患者异质性 ,即只有特定亚群的患者能够真正从中获益,而其他患者则可能无效或受损。因此,如何个体化预测PA-TACE的生存获益 ,成为临床决策中的关键难题。目前常用的肝癌分期系统(如AJCC、BCLC、CNLC)主要基于肿瘤负荷、肝功能等宏观指标,难以精准指导辅助治疗选择。近年来,增强CT影像特征 (如瘤内动脉、边缘不光滑、静脉侵袭预测因子等)已被证实与HCC的侵袭性、微血管侵犯及预后密切相关,提示影像学可能反映肿瘤的生物学行为。然而,影像特征是否能用于预测PA-TACE的个体化获益 ,以及这种预测背后的生物学机制 (如肿瘤微环境状态)仍不清楚。为此,本研究从一个核心生物学问题出发:为什么部分HCC患者能从PA-TACE中获益,而其他患者不能?是否与肿瘤微环境的免疫状态有关? 并尝试通过影像-临床-转录组多模态数据,构建可量化PA-TACE生存获益的预测工具,同时揭示其潜在的生物学基础。
03
研究目的(明确写出"三层目的")
本研究设定了三个层层递进的研究目的 ,从临床预测到治疗决策,再到机制解释。第一层目的(临床预测层) :基于术前增强CT影像特征和常规临床病理变量,构建并验证两个独立的生存预测模型------单纯手术切除(SR-only)预后模型 和术后辅助TACE(PA-TACE)预后模型 ,实现对HCC患者术后5年总体生存概率的个体化预测,并开发一个在线计算器工具 ,便于临床医生使用。第二层目的(治疗决策层) :借助虚拟孪生分析(virtual-twin analysis) ,将上述两个模型应用于每一位患者,量化其接受PA-TACE相较于仅接受SR的生存获益程度(以5年生存率差异和限制性平均生存时间差异表示),进而根据获益大小将患者划分为推荐组(获益显著) 、小获益组 和负获益组 ,最终形成明确的PA-TACE推荐/不推荐方案 ,从而指导术后个体化治疗。第三层目的(生物学机制层) :通过独立RNA测序队列 ,比较推荐组与非推荐组患者的肿瘤组织转录组差异,识别差异表达基因和富集通路,揭示PA-TACE获益的潜在肿瘤微环境特征 ,解释为何推荐组患者更可能从PA-TACE中获益。三层目的相互支撑,从"能否预测"到"如何指导治疗"再到"为什么有效",形成了完整的临床-生物学研究闭环。
04
研究思路(最核心:怎么挂靠机制)
本研究的核心思路是以影像-临床模型为桥梁,将治疗获益分组与肿瘤生物学机制挂靠 ,具体分为四个步骤。第一步:构建双模型 。从三家医疗机构回顾性纳入1770例HCC术后患者(SR-only组1224例,PA-TACE组500例),利用术前增强CT提取语义影像特征(如瘤内动脉、边缘、晕环、静脉侵袭预测因子等),结合临床病理变量(如MVI、AFP、肝功能等),采用逐步回归分别构建SR-only预后nomogram 和PA-TACE预后nomogram ,并经过内部和外部验证,证明其预测性能优于传统分期系统。第二步:虚拟孪生量化获益 。将上述两个模型同时应用于每一位患者,分别预测其在"接受SR-only"和"接受PA-TACE"两种假设下的5年生存概率,计算差值作为个体化PA-TACE生存获益 。以0%和6%为界值,将患者分为负获益、小获益和大获益三组,并将后两者合并为"不推荐组",大获益组为"推荐组"。第三步:推荐方案验证 。通过Kaplan-Meier曲线、多因素分析和倾向评分匹配,验证推荐组患者接受PA-TACE后生存显著改善,而不推荐组无获益甚至受损;同时量化推荐组若全部接受PA-TACE,平均5年OS概率可提高19.4%,限制性平均生存时间延长22.5个月。第四步:机制挂靠 。利用独立的RNA测序队列(46例),比较推荐组与非推荐组肿瘤组织的转录组差异。差异表达和富集分析显示 :推荐组上调基因富集于中性粒细胞趋化、脂肪酸合成、胶原形成 等通路,下调基因富集于B细胞活化调控 通路,提示推荐组肿瘤微环境呈现免疫抑制性特征 (B细胞功能受抑、炎症/基质活化)。这一机制发现恰好解释了为什么此类患者更可能从PA-TACE诱导的免疫原性细胞死亡中获益,从而将影像表型、治疗获益与生物学机制三者成功挂靠。
05
数据和方法(机制部分怎么设计)
数据: 本研究共纳入来自三家医疗机构的1770例 肝细胞癌术后患者,其中SR-only组1224例 、PA-TACE组500例 。将来自两家机构的患者按7:3随机分为开发队列(1040例) 用于构建SR-only和PA-TACE预后nomogram,内部验证队列(448例) 用于模型内部验证;来自第三家机构的236例 作为外部验证队列 ;另设独立RNA测序队列(46例),其中推荐组17例、非推荐组29例,用于比较两组间的转录组差异以揭示生物学机制。
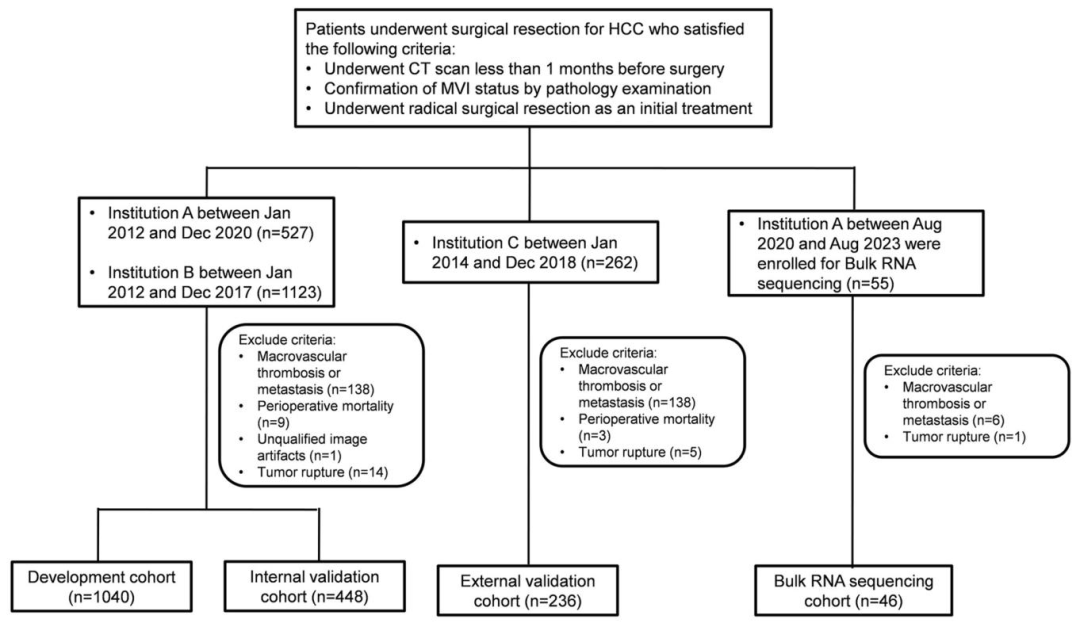
图 1:患者入组流程图
**方法:**提取术前CT语义影像特征与临床病理变量 → 采用逐步回归(AIC准则)分别构建SR-only和PA-TACE预后nomogram → 通过虚拟孪生分析将两个模型应用于每位患者,计算PA-TACE相较于SR-only的5年生存获益 → 以0%和6%为界值划分负获益、小获益、大获益组,将大获益组定义为"推荐组",其余为"非推荐组" → 采用Kaplan-Meier、多因素分析和倾向评分匹配验证推荐组患者接受PA-TACE后生存显著改善 → 对RNA测序队列进行差异表达基因分析和富集分析,比较推荐组与非推荐组的肿瘤微环境特征 → 将影像表型、治疗获益与免疫抑制性微环境(B细胞下调、中性粒细胞趋化等)挂靠,解释机制。
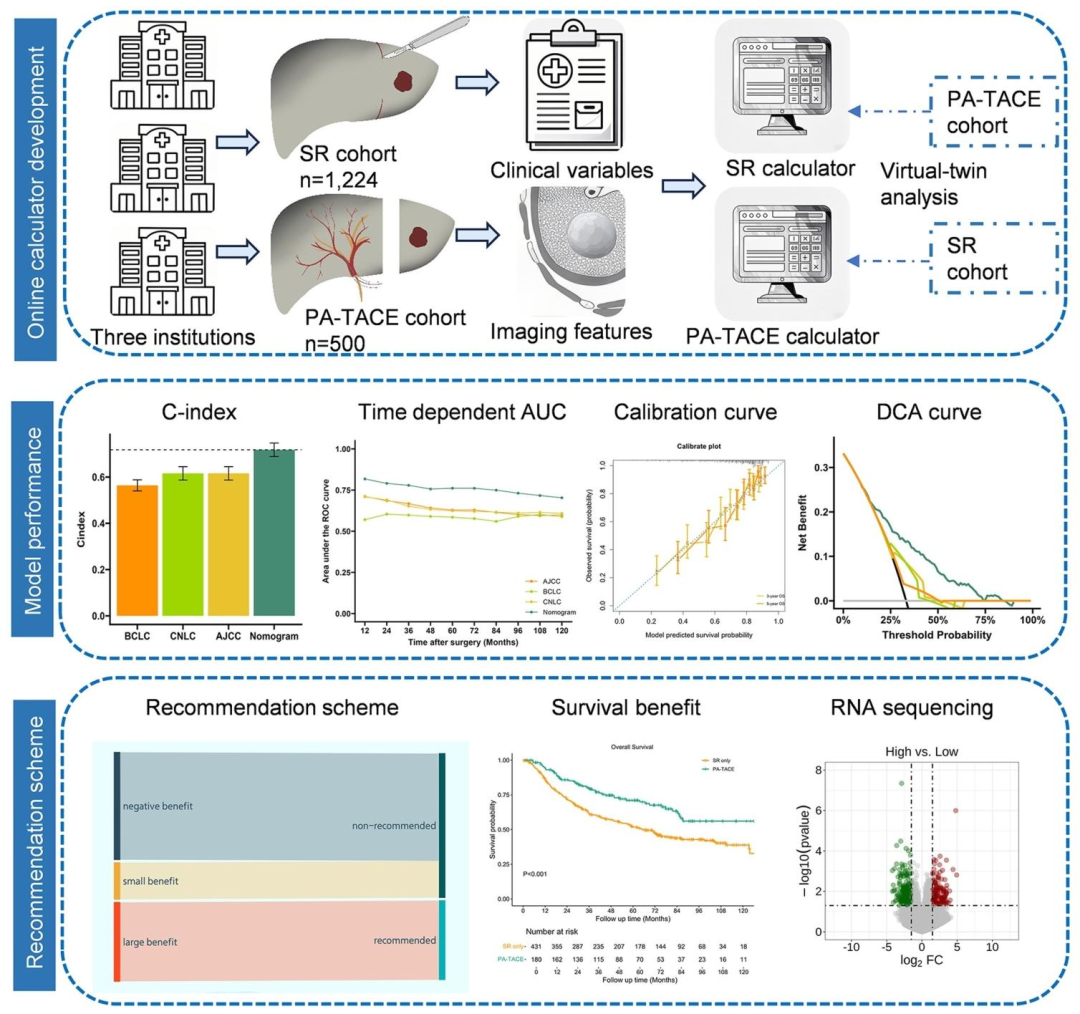
图 2:研究整体工作流程图
06
研究结果("从表型到机制")
1. 表型层面 :SR-only与PA-TACE nomogram在开发、内部验证及外部验证队列中C-index分别≥0.694和≥0.701 ,预测误差低(IBS≤0.176),显著优于AJCC、CNLC、BCLC分期系统,校准良好,表明影像-临床联合模型可精准预测术后生存。
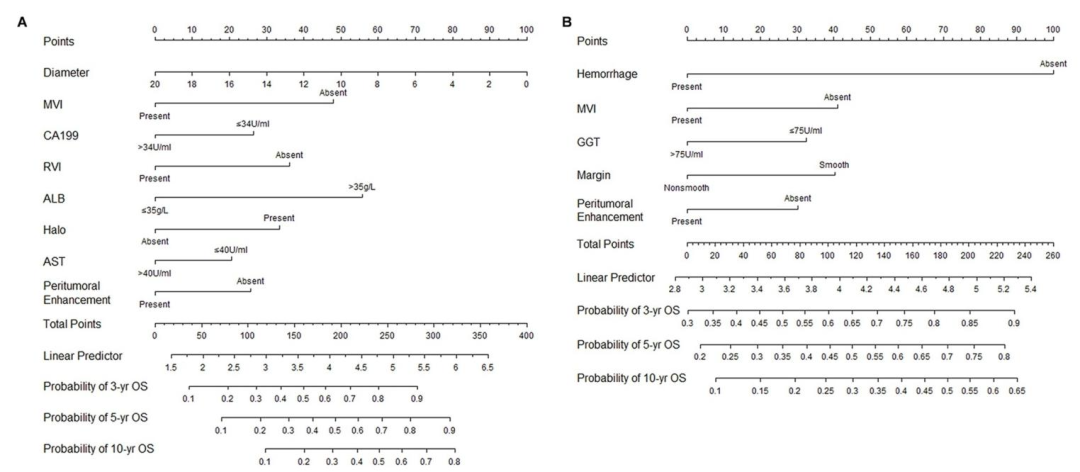
图 3(SR-only与PA-TACE nomogram) :A图为SR-only nomogram,纳入肿瘤直径、MVI、CA19-9、RVI、白蛋白、晕环、AST、瘤周强化 8个变量;B图为PA-TACE nomogram,纳入出血、MVI、GGT、边缘、瘤周强化 5个变量。其中RVI(放射基因组静脉侵袭)、晕环、瘤周强化、边缘 等CT语义特征成为关键预测因子,说明影像特征可替代部分基因表达信息,将影像表型直接嵌入预后预测,为后续机制探索提供变量基础。
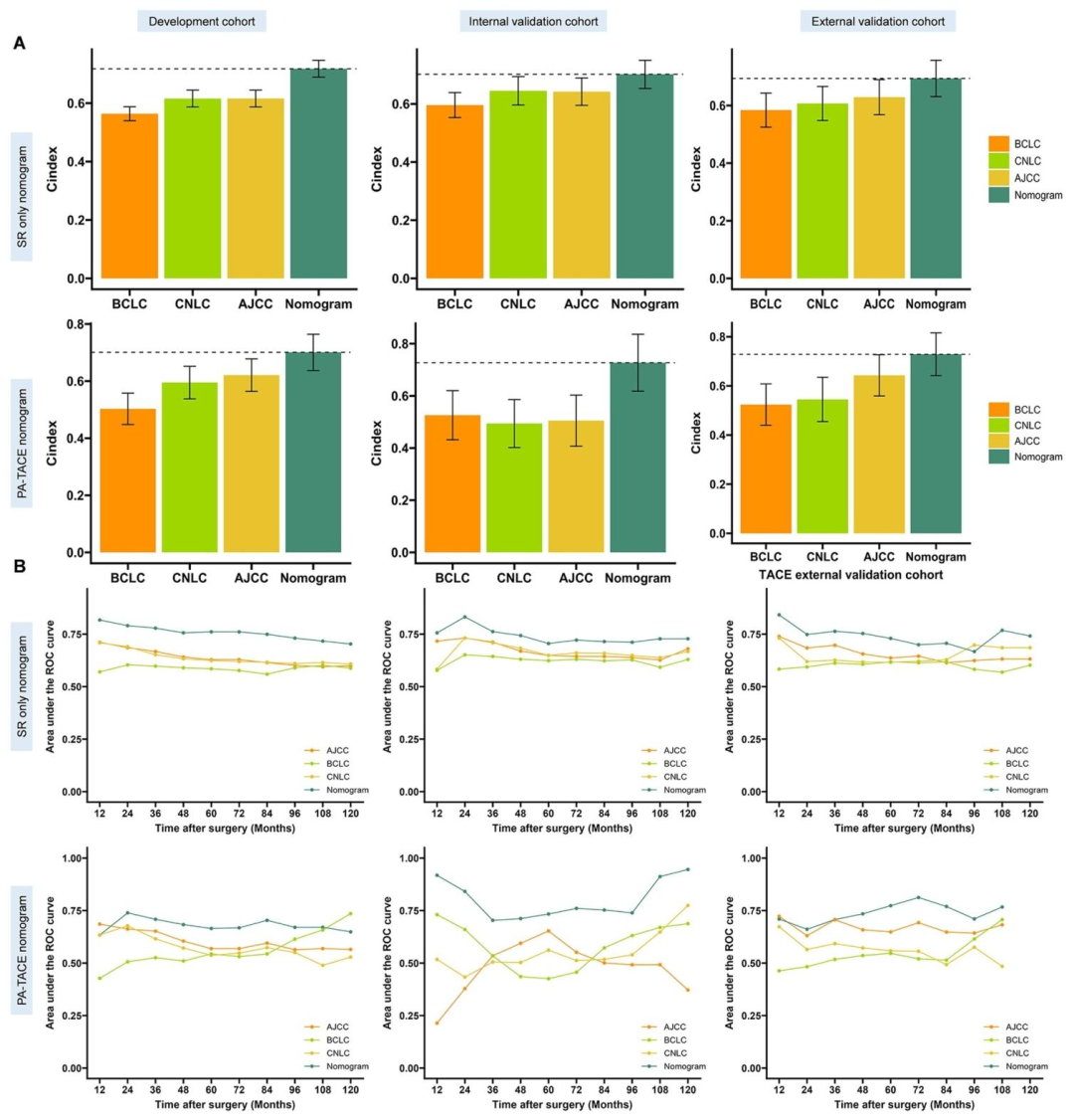
图 4(模型与分期系统的C-index和AUC比较) :通过时间依赖性C-index和AUC曲线,比较SR-only nomogram、PA-TACE nomogram与AJCC、CNLC、BCLC分期系统在开发、内部验证、外部验证三个队列中的预测性能。结果显示两个nomogram的C-index(≥0.694)和AUC均显著优于传统分期系统 ,证明影像-临床联合模型具有更强的预后判别能力,影像特征补充了分期系统无法捕获的肿瘤生物学异质性信息。
2. 治疗获益分层 :35.4%患者被推荐接受PA-TACE ,推荐组5年OS概率平均提高19.4% ,限制性平均生存时间延长22.5个月 ;43.6%患者需调整术后治疗方案,验证了推荐方案的临床决策价值。
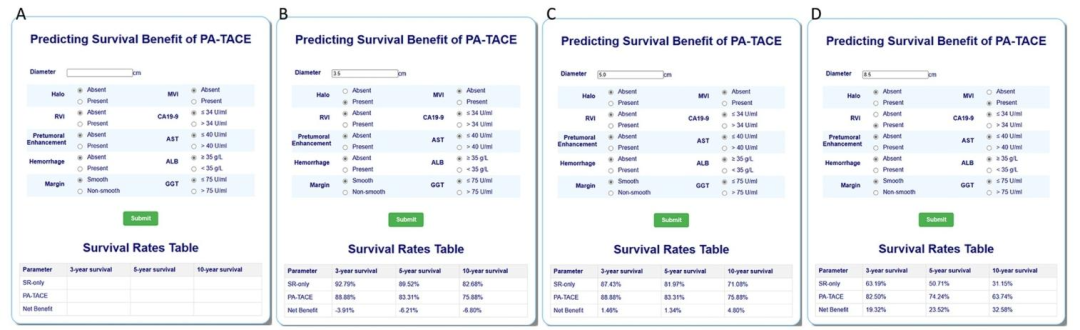
图 5(在线计算器界面及三类获益示例) :展示了基于两个nomogram开发的Web计算器。A图为空白输入界面,需输入MVI、RVI、晕环、瘤周强化等影像变量及临床变量;B、C、D图分别显示负获益、小获益、大获益 三类患者的输出结果。该图体现了影像特征直接转化为临床决策工具的过程,使得PA-TACE的个体化生存获益可量化、可视化,实现了从影像表型到治疗推荐的转化。
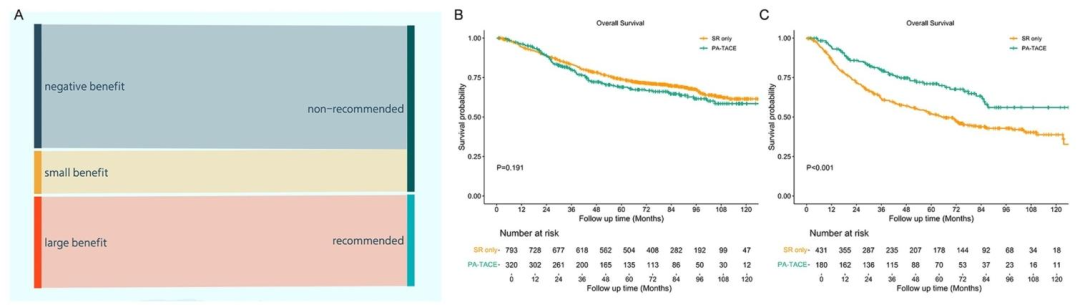
图 6(推荐方案与PA-TACE获益关系的Sankey图及生存曲线) :A图为Sankey图,展示35.4%患者被划分为推荐组(大获益),64.6%为非推荐组 ;B图显示非推荐组中,PA-TACE与SR-only的5年OS无显著差异(HR=1.171,P=0.191);C图显示推荐组中,PA-TACE显著改善OS(5年OS率:71.1% vs 51.9%,HR=0.538,P<0.001)。该图证明了影像模型筛选出的推荐组确实能从PA-TACE中显著获益,为后续机制探索提供了可靠的分组标签。
3. 机制层面 :RNA-seq显示,推荐组较非推荐组上调中性粒细胞趋化、胶原形成等通路,下调B细胞活化调控通路 ,提示肿瘤微环境呈免疫抑制性特征,为PA-TACE获益提供了生物学解释。
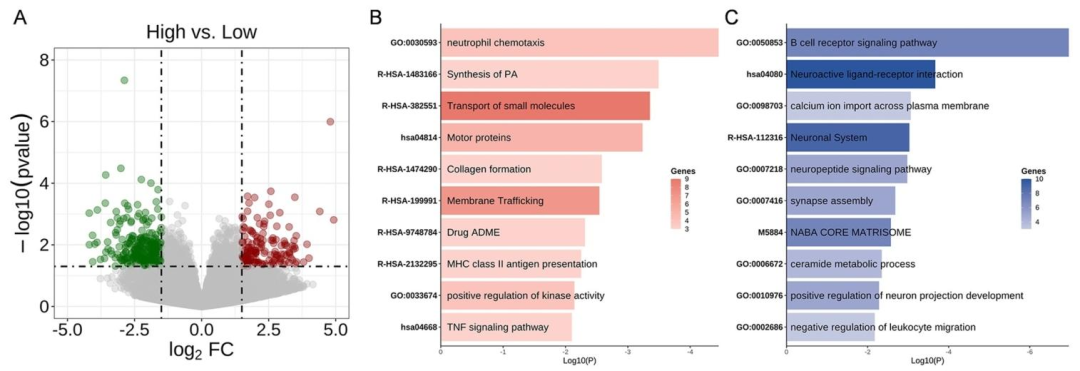
图 7(RNA-seq机制分析) :A图为火山图,展示推荐组 vs 非推荐组中157个上调基因、268个下调基因 ;B图为上调通路的富集分析,包括中性粒细胞趋化、脂肪酸合成、胶原形成 等;C图为下调通路富集分析,突出B细胞活化调控 。这些结果提示推荐组呈现免疫抑制性肿瘤微环境 (B细胞功能受抑、炎症/基质活化),从生物学层面解释了为何此类患者更易从PA-TACE诱导的免疫原性细胞死亡中获益,完成了影像表型→治疗获益→免疫机制的完整挂靠。
07
讨论(把机制故事讲圆)
本研究的讨论围绕PA-TACE疗效异质性的核心矛盾 展开,并成功将影像表型、治疗获益与肿瘤生物学机制串联成一个闭环故事。首先,作者指出既往PA-TACE研究结论冲突的根本原因在于未对患者进行获益分层 ,而本研究通过SR-only和PA-TACE双模型构建及虚拟孪生分析,首次实现了个体化量化PA-TACE的生存获益 ,并明确了推荐组(35.4%)与不推荐组(64.6%)的划分。其次,讨论强调了影像特征的关键价值 :肿瘤直径、RVI、晕环缺失、瘤周强化等语义特征不仅显著提升预后预测性能(C-index优于传统分期系统),而且这些特征可能间接反映了肿瘤的侵袭潜力和微环境状态 ,为机制挂靠提供了表型基础。第三,最核心的机制解释 是:RNA-seq发现推荐组肿瘤呈现免疫抑制性微环境 ------B细胞活化相关基因下调、中性粒细胞趋化和胶原形成等通路上调。作者据此提出:PA-TACE可通过诱导局部缺血、缺氧和免疫原性细胞死亡,释放肿瘤抗原,在本就处于免疫抑制状态的TME中 更有效地激活残余的抗肿瘤免疫反应,从而产生生存获益;相反,非推荐组可能已有较强的内在免疫监视,单纯手术已足够,额外添加PA-TACE不仅无益反而可能带来不必要的毒副作用。这一机制解释与近年TACE联合免疫治疗的研究趋势高度一致 ,也为后续探索"TACE+免疫"的联合策略提供了生物学依据。讨论还坦诚指出模型的局限性(回顾性设计、影像特征为语义而非组学、机制队列样本较小),但强调在线计算器的临床转化价值 ------可实时输出个体化的PA-TACE生存获益概率,辅助医患共同决策。总体而言,讨论成功地将**"影像预测→治疗获益→免疫抑制微环境→PA-TACE协同效应"**这一逻辑链条讲圆,使文章从单纯的技术报告上升为具有生物学深度的临床研究。
08
这篇文献的可借鉴思路
这篇文献为影像组学如何挂靠生物学机制 提供了极具操作性的范例,其核心思路可概括为**"三步挂靠法"** ,值得广泛迁移至其他癌种和治疗场景。第一步:以影像-临床模型为桥梁,形成治疗获益分组标签 。作者并未直接做影像特征与基因表达的关联(传统放射基因组学需要大样本、强信号,难度高),而是先构建SR-only和PA-TACE两个预后模型,通过虚拟孪生分析计算个体化治疗获益,进而将患者划分为"推荐组"与"非推荐组"。这一步的关键在于不需要影像与基因一一对应 ,而是用"治疗获益"作为中间表型,极大降低了机制研究的门槛。第二步:用独立的小型转录组队列验证分组标签的生物学差异 。本研究仅用46例RNA-seq数据(推荐组17例、非推荐组29例)即发现了显著的通路富集差异,说明只要分组明确、效应足够强,中等样本量也能支撑机制解释 。这提示我们在设计类似研究时,可以预留30~50例的组织样本用于转录组、蛋白组或代谢组分析,而不必追求高通量影像-基因组学的大规模队列。第三步:从富集通路中提炼出与治疗方式逻辑自洽的机制故事 。本研究将"B细胞下调、中性粒细胞趋化、胶原形成"解读为免疫抑制性TME,并与PA-TACE诱导的免疫原性细胞死亡形成协同假说,使机制解释既扎根于数据,又具有临床直觉上的合理性。此外,本文还有几个可借鉴的设计亮点:①多中心开发+内部+外部验证 保证了模型的泛化能力;②虚拟孪生分析 可迁移到任何两种治疗策略比较的场景(如化疗vs不化疗、免疫vs手术);③在线计算器 大幅提升了临床实用性和文章影响力;④语义影像特征 比深度学习特征更易于临床医生理解和采纳。总之,如果你希望在自己的研究中实现"影像→机制"的挂靠,可以按照本文的**"先分层、再测序、后富集"**三步策略,用较少的机制样本讲出一个完整的生物学故事。
09
结语
总而言之,这篇文献给我们演示了一套低成本、高说服力的影像-机制挂靠范式 :不追求昂贵的影像基因组学,而是先用影像+临床模型筛出治疗获益人群,再用小样本转录组去验证微环境差异 ,最后用免疫抑制性TME 把"为什么推荐组能从PA-TACE中获益"讲得明明白白。做影像组学,比的从来不是算分多快、模型多花哨,而是能不能让图像说出肿瘤的生物学秘密 。希望大家今后都能像这篇文章一样,从"算得准"走向"讲得通",做出有深度、有温度、能落地的影像学研究。
参考文献:Li X, Liang X, Chen S, Geng Z, Li Z, Liang J, Zhong L, Qi Z, Liang W, Pan X, Liu Z, Liang C, Quan X. Development and validation of a CT-based online calculator for prognosis and postoperative adjuvant transcatheter arterial chemoembolization benefit prediction in resected hepatocellular carcinoma: a multicenter retrospective cohort study. Int J Surg. 2025 Dec 10. doi: 10.1097/JS9.0000000000004456.