01
文献学习

今天分享的文献是由中南大学湘雅二医院肖煜东教授等团队于2026年5月在放射学领域顶刊《Radiology 》(中科院1区top,IF=15.2)上发表的研究"CT Radiomics-based Machine Learning to Identify Intratumoral Fibrosis and Underlying Angiogenesis in Hepatocellular Carcinoma "即基于CT放射组学的机器学习识别肝细胞癌瘤内纤维化及其潜在血管生成,该研究开发并验证了一种基于CT影像的放射组学模型(Rad-ITF评分),用于无创性评估肝细胞癌(HCC)中的瘤内纤维化(ITF)分级。研究发现,高Rad-ITF评分的HCC患者在接受TACE治疗后预后更差(进展生存期更短、应答率更低),并且肿瘤组织中血管生成相关基因表达显著上调。该模型在多个独立队列中表现出良好的诊断性能(AUC最高达0.86),并具有作为TACE联合抗血管生成治疗筛选工具的潜力。
创新点:①首次构建CT影像组学模型无创识别HCC瘤内纤维化(ITF)等级 ,替代有创病理活检,实现术前精准分级。②揭示高ITF等级与 血管生成通路(VEGFR3/PDGFRA)上调的分子关联 ,通过多组学及空间转录组验证。③建立XGBoost模型(Rad-ITF评分)同时预测ITF及TACE预后,整合了影像、病理、转录组与临床结局。
临床价值:①避免术前活检风险 ,利用常规CT影像即可评估ITF,为无法/不愿穿刺 的HCC患者提供决策依据。②优化TACE治疗分层 :高Rad-ITF评分患者疗效差、PFS短,提示应联合抗血管生成药物 或调整方案。③筛选抗血管生成治疗优势人群 :高评分组血管生成基因高表达,指导TACE+靶向联合治疗策略,提高个体化精准度。
02
研究背景和目的
研究背景
肝细胞癌(HCC)是一种高度异质性的恶性肿瘤,其复杂的肿瘤微环境对疾病进展和治疗响应具有重要影响。瘤内纤维化(ITF) 是细胞外基质重塑所导致的组织学改变,在实体瘤中可见,但在HCC中相对少见。然而,部分HCC亚型(如硬癌样亚型)可表现为高ITF等级 ,并与不良预后密切相关。目前,经动脉化疗栓塞术(TACE) 是中期HCC的一线治疗方案,但其疗效仍不理想。这可能与ITF形成的物理屏障 有关:致密的细胞外基质沉积、增加的基质硬度、降低的血管通透性以及升高的间质流体压力,共同阻碍了栓塞剂和化疗药物的有效递送。此外,新近证据表明,ITF还可能促进肿瘤血管生成 ,进而影响抗血管生成治疗的疗效。鉴于ITF在预后判断和治疗指导中的潜在重要意义,术前无创评估ITF等级 显得尤为关键。然而,常规HCC诊断流程中并不包括全面的组织学评估,且传统影像特征(如靶样外观)的解读存在显著的观察者间变异性 (κ值仅为0.20--0.61)。影像组学作为一种新兴的无创方法,能够定量提取高维度图像特征,反映潜在的肿瘤病理生理特征,有望成为替代性生物标志物。但迄今为止,基于CT影像组学进行ITF分级及其与TACE预后关联的研究仍十分有限,亟需深入探索。
研究目的
本研究旨在开发并验证一个基于CT影像组学的机器学习模型 ,用于术前无创地分类肝细胞癌(HCC)中的瘤内纤维化(ITF)等级 ,并进一步评估该模型所判定的ITF分级与接受TACE治疗的HCC患者预后 以及肿瘤血管生成水平 之间的关联。具体而言,研究团队首先利用多中心回顾性与前瞻性队列,以组织病理学Sirius红染色和HE染色为金标准,将患者分为低ITF等级与高ITF等级,通过特征提取与筛选构建了XGBoost模型,即Rad-ITF评分 ,并在内部和外部验证集中验证其诊断效能。其次,在结局测试队列中,根据Rad-ITF评分将接受TACE的中期HCC患者分为高低两组,比较两组间的无进展生存期(PFS) 和肿瘤缓解率 ,以评估模型对治疗结局的预测价值。最后,利用TCGA公共数据库及前瞻性收集的基因组测试队列,通过RNA测序、单细胞RNA测序和空间转录组学分析 ,比较高低Rad-ITF评分组间血管生成相关基因表达、内皮细胞及成纤维细胞浸润水平,并定量分析微血管密度(MVD),从而验证Rad-ITF评分与血管生成水平的相关性,为后续联合TACE与抗血管生成治疗提供理论依据。
03
数据和方法
研究数据
总样本量:1675例HCC患者(1406男,269女)
多中心队列:
训练集:653例
内部验证集:371例
外部验证集:173例
结局测试集:427例(接受TACE的中期HCC)
TCGA测试集:39例(CT + RNA-seq)
基因组测试集:12例(前瞻性,单细胞RNA-seq + 空间转录组)
病理金标准:Sirius red 和 HE 染色评估ITF分级
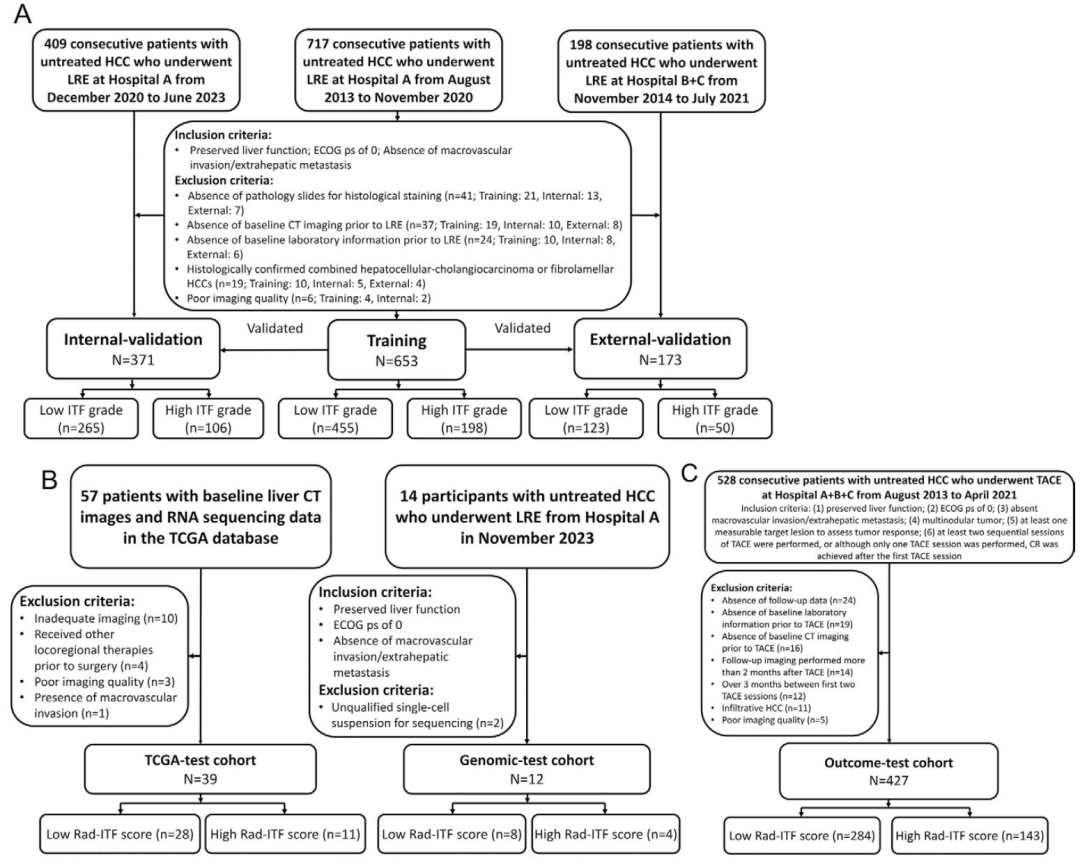
图 1:研究流程图
技术方法
影像组学:从动脉期和门静脉期CT中提取3668个特征,筛选出17个用于建模。
机器学习模型:XGBoost(最优模型),输出Rad-ITF评分。
预后分析:Kaplan-Meier、Cox回归、倾向评分匹配(PSM)、逆概率加权(IPTW)。
分子分析:
TCGA:血管生成相关基因表达
单细胞RNA-seq + 空间转录组:细胞类型富集、基因空间定位
免疫组化:CD34染色评估微血管密度(MVD)
04
实验结果
模型性能:
训练集AUC:0.86
内部验证集AUC:0.85
外部验证集AUC:0.82
预后价值:
高Rad-ITF评分组:
肿瘤应答率更低(46.2% vs 62.0%)
PFS更差(6.8月 vs 11.2月,P < 0.001)
血管生成关联:
高Rad-ITF评分组中VEGFR3、PDGFRA等基因表达显著上调
内皮细胞和成纤维细胞富集
MVD显著升高(55.0 vs 45.0,P < 0.001)
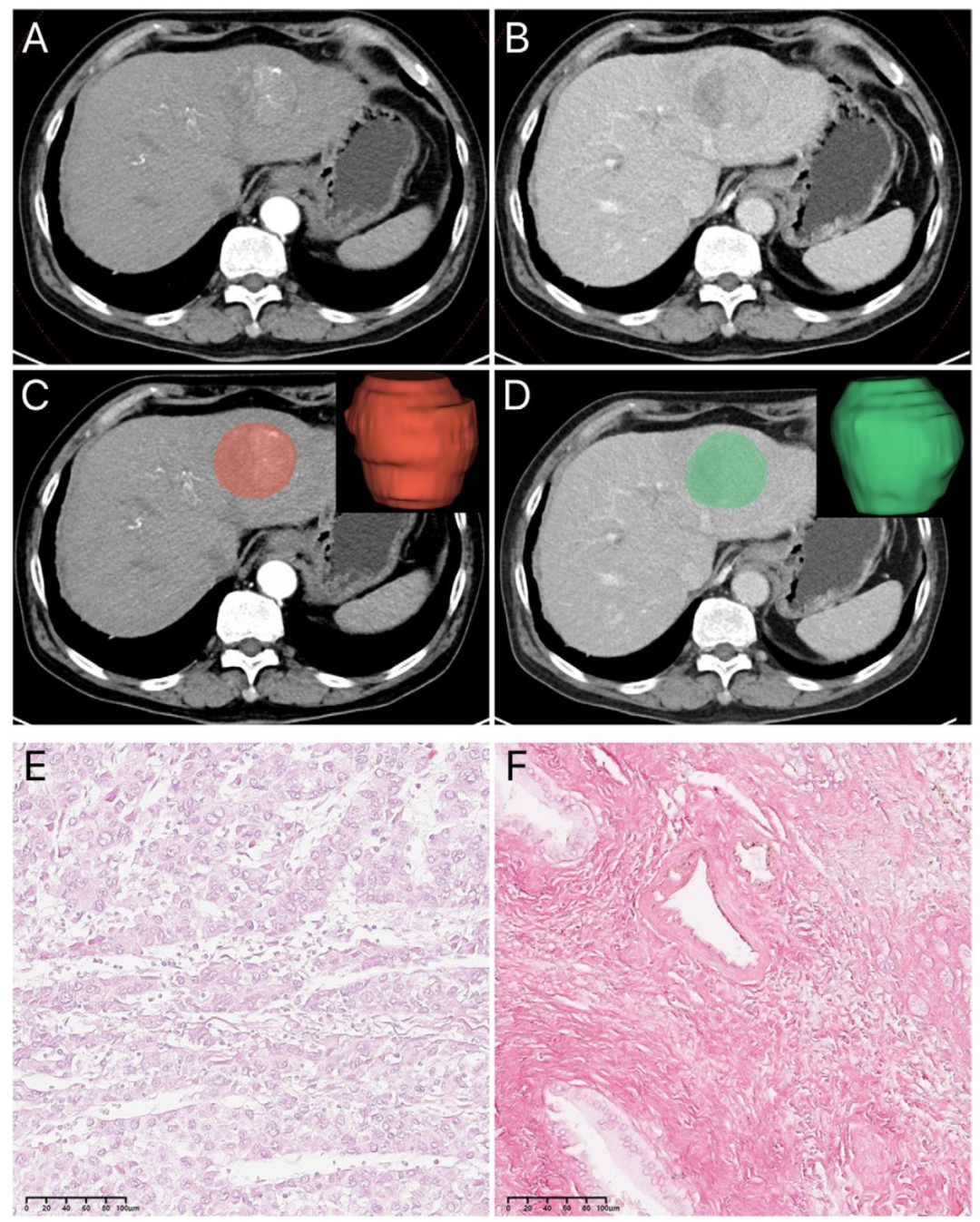
图 2:低/高ITF分级的CT图像分割与病理染色示例
该图展示了低ITF与高ITF肝细胞癌(HCC)的CT图像、肿瘤分割掩模及Sirius红染色 。A-B为41岁男性患者(瘤径46 mm)的动脉期和门静脉期轴位CT ;C-D分别用红色和绿色掩模 标注了动脉期与门静脉期的肿瘤轮廓;E-F为对应病理图像,低ITF组(E) 显示稀疏胶原纤维,而高ITF组(F) 呈现密集的红色胶原沉积。该图直观体现了放射组学特征提取的基础以及ITF分级的组织学参考标准。
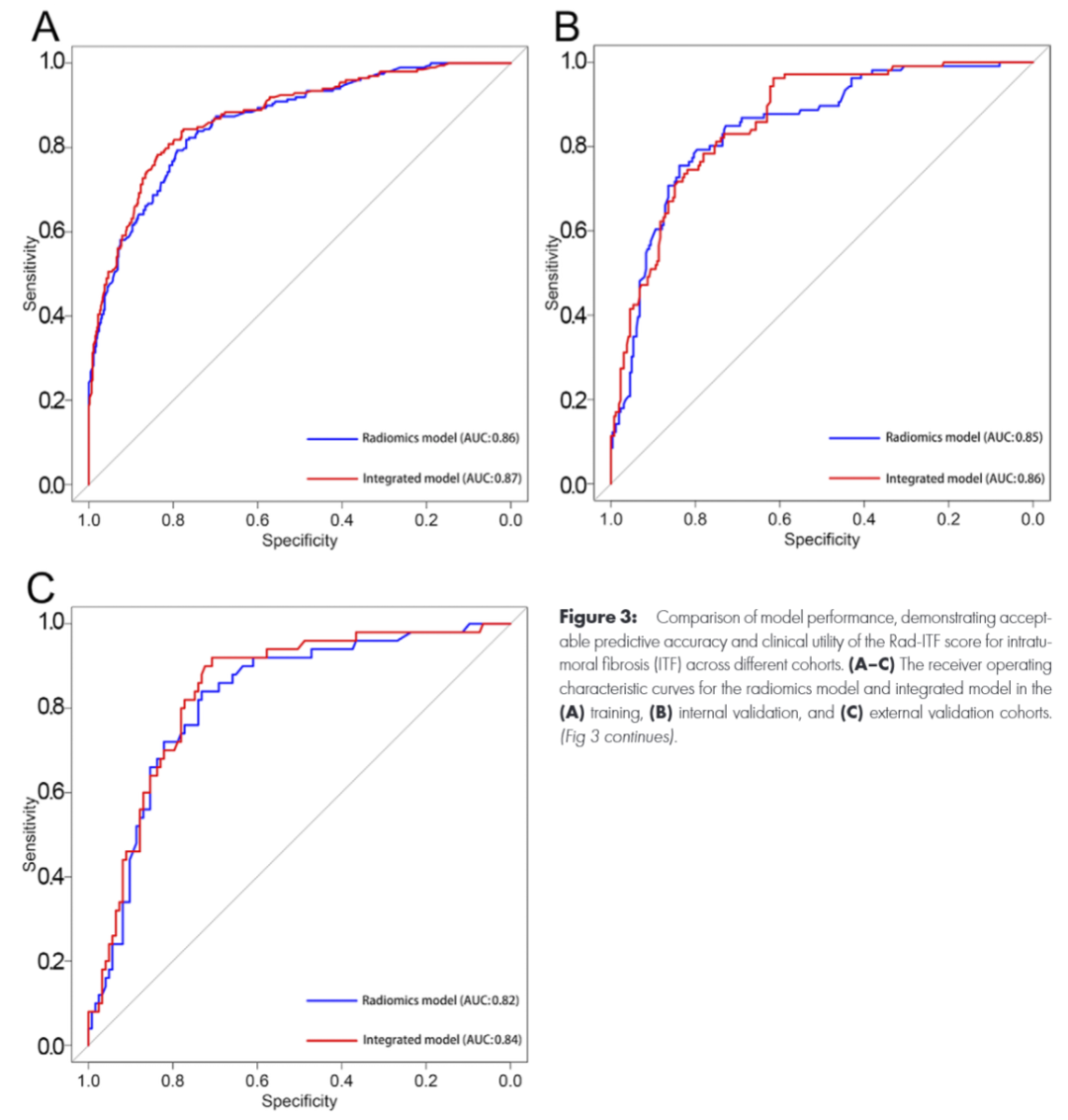
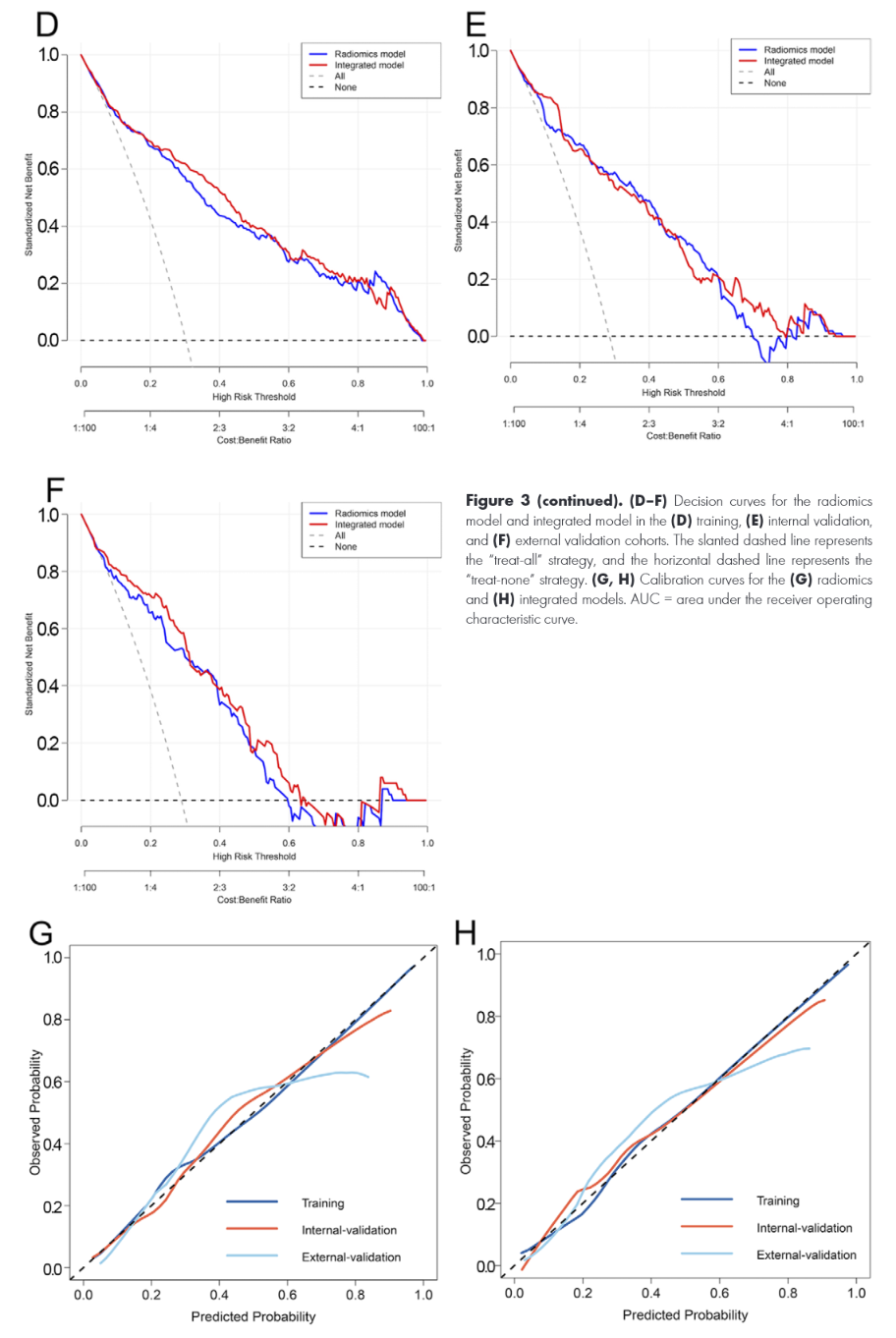
图 3:Rad-ITF评分模型的诊断性能对比
该图评估了放射组学模型(仅Rad-ITF评分)与综合模型(联合肝硬化)的效能。A-C 为ROC曲线,在训练、内部验证、外部验证队列中,放射组学模型的AUC分别为0.86、0.85和0.82 ,与综合模型无显著差异(P均>0.05)。D-F 决策曲线显示,在较宽阈值概率范围内,Rad-ITF评分的净获益优于"全治疗"或"不治疗"策略 。G-H 校准曲线表明预测概率与实际观测概率高度一致,证实模型具有良好的校准度和临床实用性。
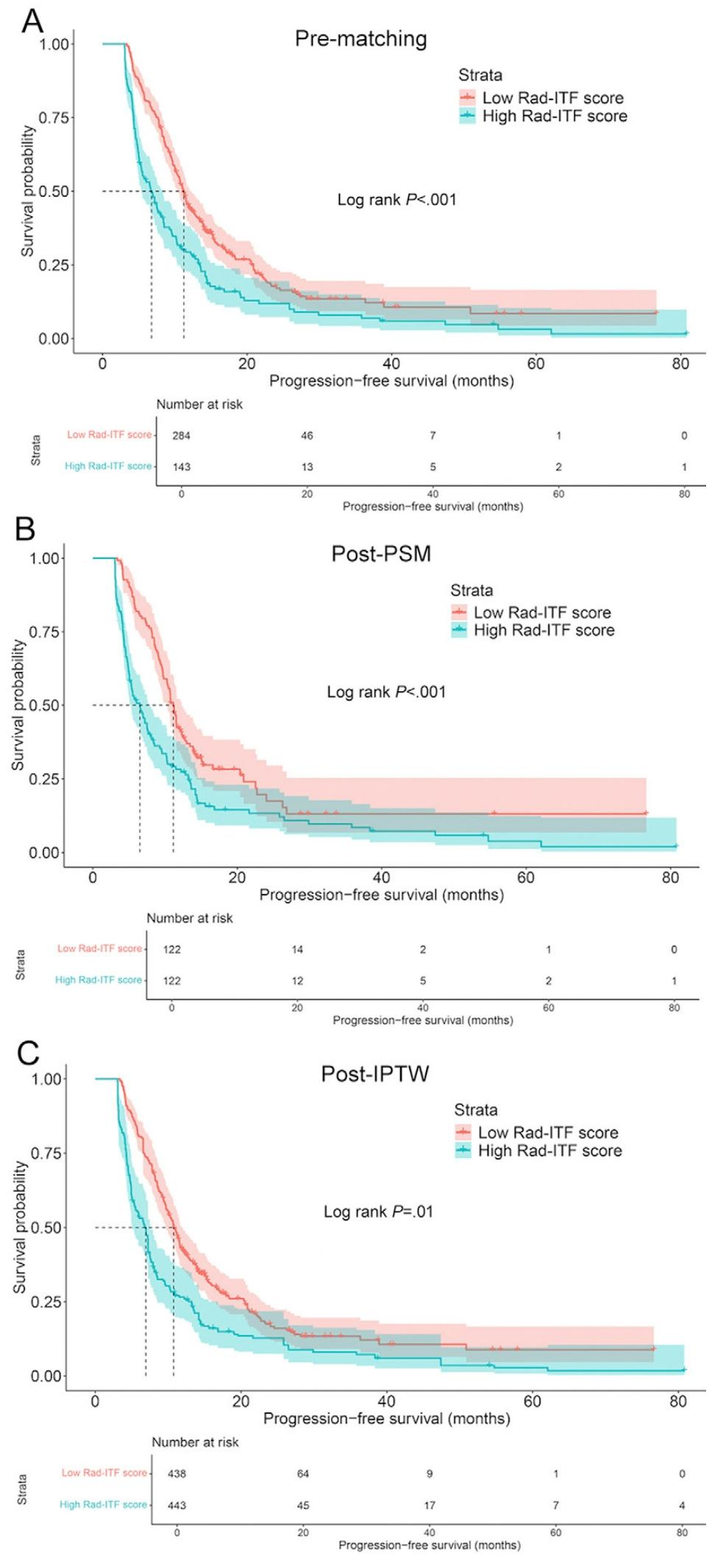
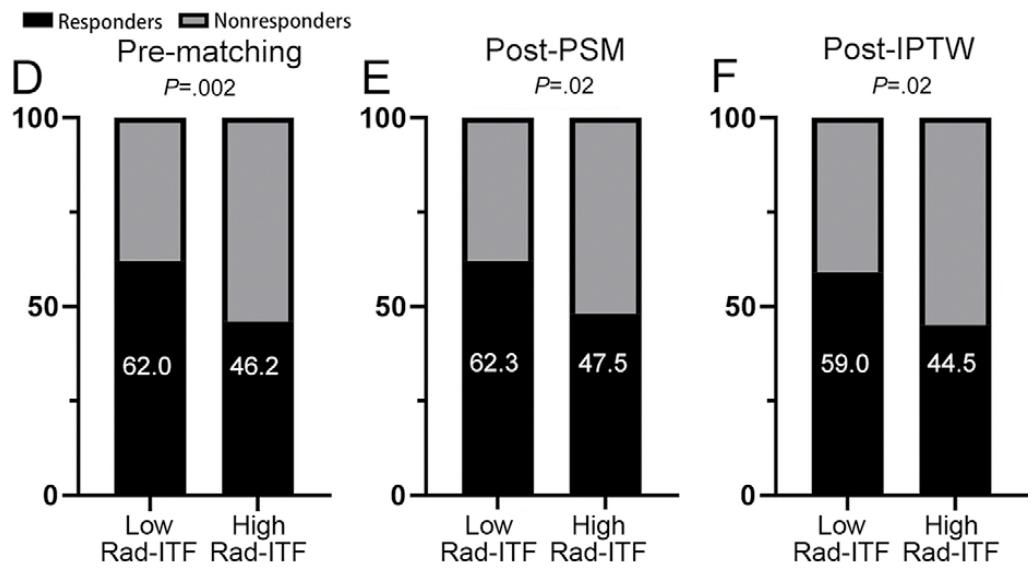
图 4:Rad-ITF评分与TACE预后关系的生存曲线及响应率
该图比较了高低Rad-ITF评分组患者的无进展生存期(PFS)和肿瘤缓解率 。A-C 为Kaplan-Meier曲线:高评分组中位PFS显著劣于低评分组(原始队列:6.8月 vs 11.2月,P<0.001);经倾向评分匹配(PSM) 和逆概率处理加权(IPTW) 后,差异依然显著。D-F 条形图显示,高评分组的客观缓解率(ORR) 在匹配前后均低于低评分组(如匹配前:46.2% vs 62.0%,P=0.002)。结果提示高Rad-ITF评分预示TACE疗效更差、进展更快。
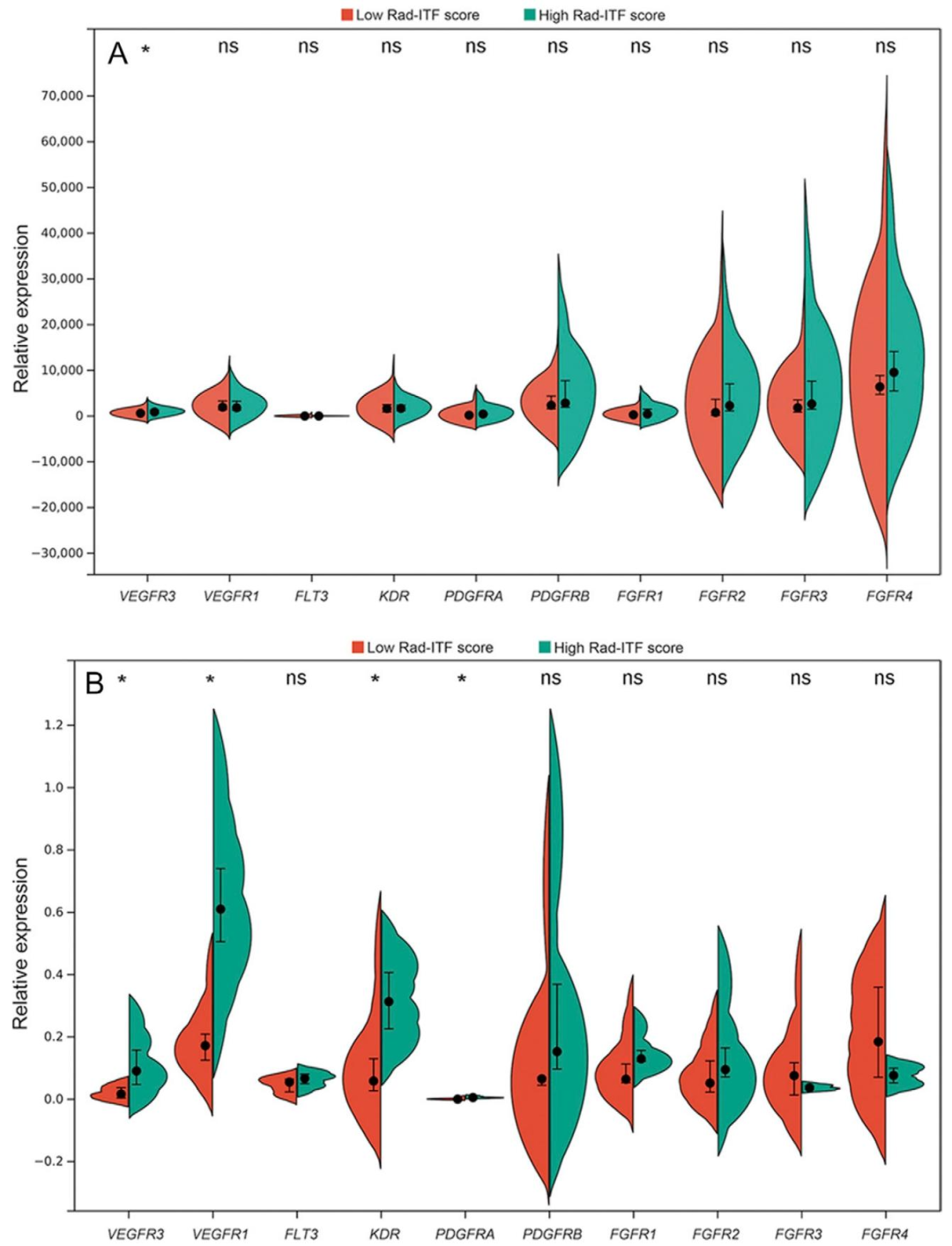
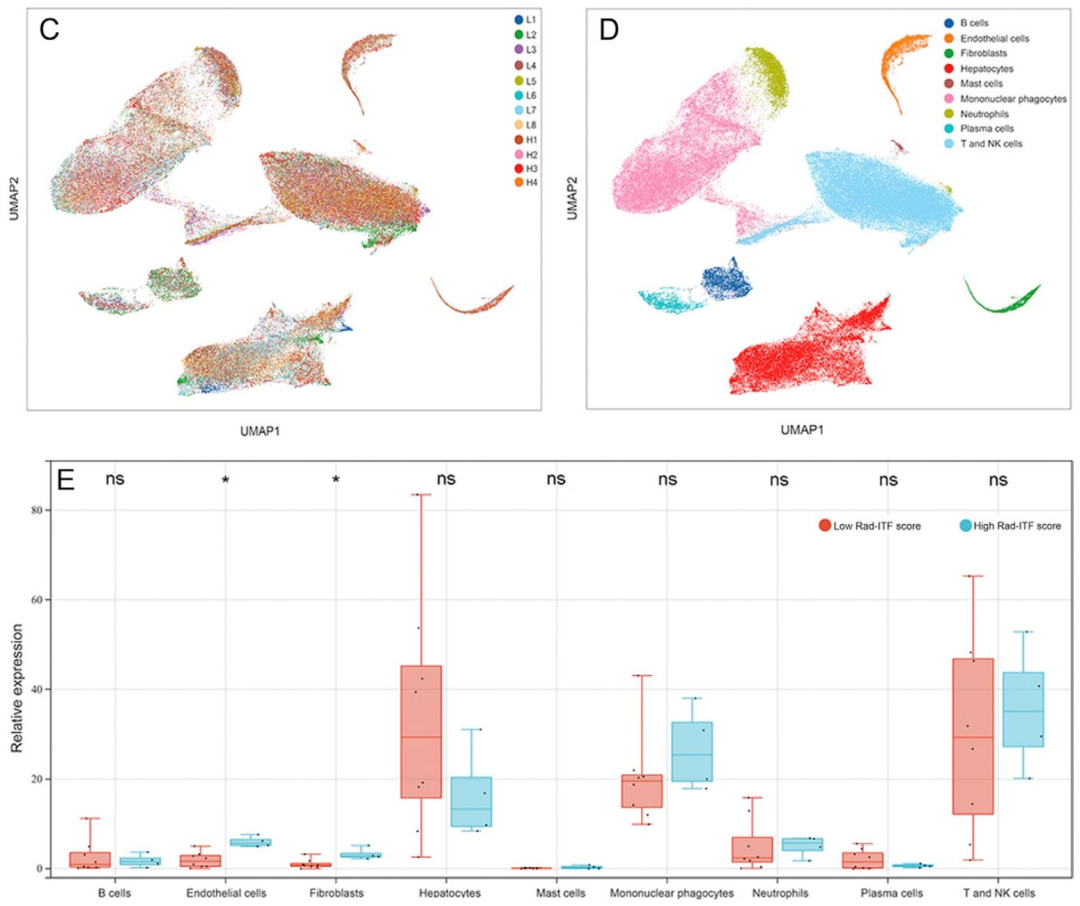
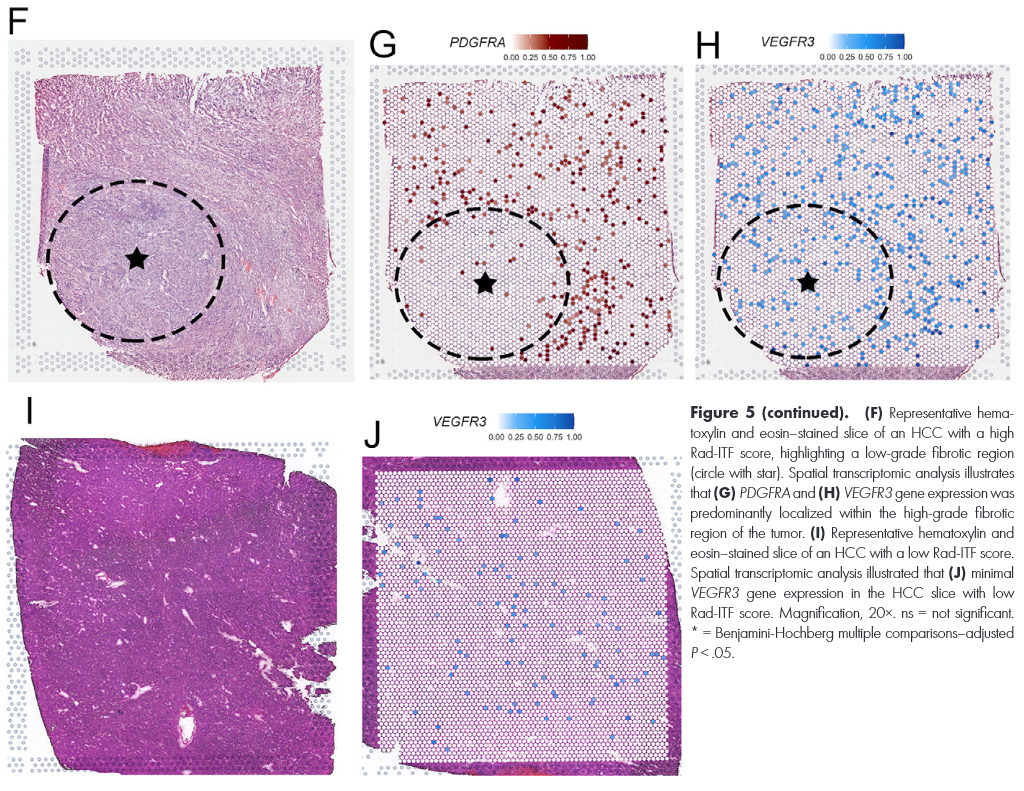
图 5:Rad-ITF评分与血管生成水平的多组学关联分析
该图通过单细胞测序和空间转录组揭示高Rad-ITF评分与血管生成上调 的关系。A-B 小提琴图显示,高评分组中VEGFR3、VEGFR1、KDR、PDGFRA 等基因表达显著升高(校正P=0.04)。C-E 展示内皮细胞和成纤维细胞在高评分组中显著富集 (校正P分别为0.02和0.03)。F-H 空间转录组定位显示VEGFR3和PDGFRA高表达集中于高纤维化区域 ;低评分肿瘤(I-J)则几乎无表达。该图从分子和细胞层面证实Rad-ITF评分可作为血管生成的替代标志物。
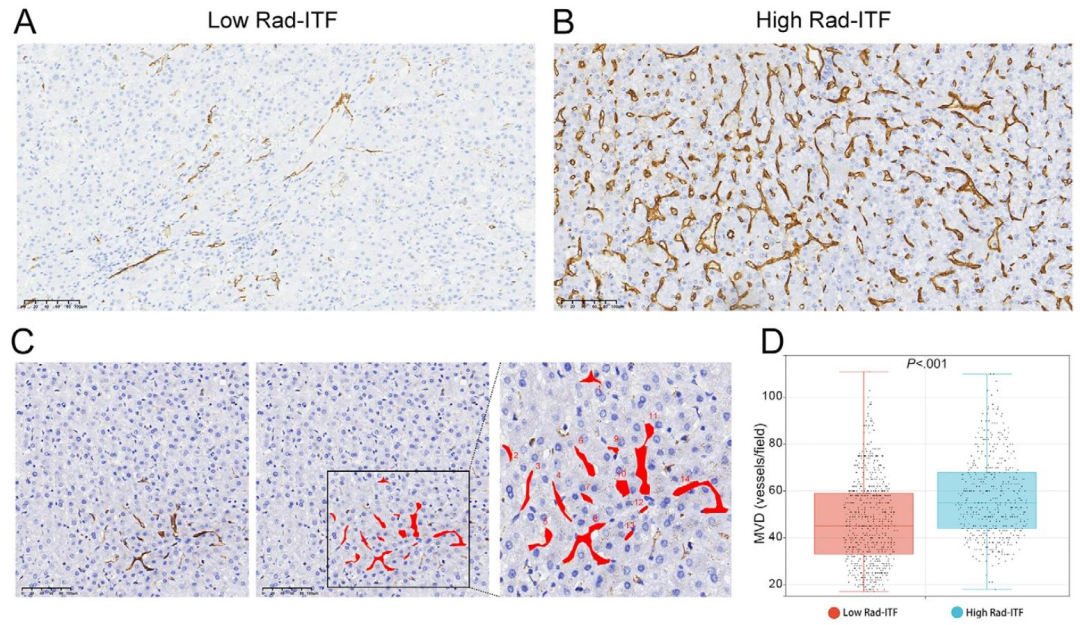
图 6:Rad-ITF评分与微血管密度(MVD)的组织学验证
该图通过CD34免疫组化染色验证高Rad-ITF评分与血管生成增加 的相关性。A 和B 分别为低、高Rad-ITF评分HCC的代表性CD34染色图像(200×),高评分组显示更密集的微血管网络 。C 图解了MVD计数方法------在热点区域内手动标记并计数微血管(示例中标记14条)。D 箱线图汇总了三个验证队列共715例低评分与482例高评分的MVD数据:高评分组中位MVD为55.0(IQR 44.0-68.0) ,显著高于低评分组的45.0(IQR 33.0-59.0) (P<0.001)。该图为Rad-ITF评分反映肿瘤血管生成水平提供了直接病理学证据。
05
研究结论
该研究基于CT放射组学构建了名为Rad-ITF评分 的机器学习模型,用于术前无创评估肝细胞癌(HCC)的瘤内纤维化(ITF) 等级。研究在多个独立队列中验证了该模型的诊断性能,训练、内部验证和外部验证队列的AUC分别达到0.86、0.85和0.82 ,显著优于传统影像特征(如靶样外观)。进一步分析表明,高Rad-ITF评分与更差的TACE治疗反应和更短的无进展生存期(PFS)显著相关 ,提示其在预后分层中的价值。此外,研究还发现,高Rad-ITF评分组中血管生成相关基因(如VEGFR3、PDGFRA)表达上调 ,内皮细胞和成纤维细胞浸润增加,微血管密度升高,表明该评分能间接反映肿瘤的血管生成水平。综上,Rad-ITF评分不仅可作为HCC中ITF等级的有效替代标志物,还能为TACE疗效预测和联合抗血管生成治疗策略的制定提供理论依据。
06
Q&A
Q1:什么是Rad-ITF评分?
**A1:**Rad-ITF评分是一种基于CT影像的放射组学机器学习模型,采用XGBoost算法构建。研究从动脉期和门静脉期CT图像中提取3668个特征,最终筛选出17个关键特征用于计算该评分,用于无创性区分肝细胞癌(HCC)的瘤内纤维化(ITF)高分级与低分级(病理金标准为Sirius red染色)。
Q2:Rad-ITF评分与接受TACE治疗的中期HCC患者的预后有何关联?
A2: 在包含427例接受TACE治疗的中期HCC患者的结局测试队列中,高Rad-ITF评分(≥0.34)与显著更差的预后相关:①肿瘤应答率 :高评分组为46.2%(66/143),低评分组为62.0%(176/284),P=0.002②中位无进展生存期(PFS) :高评分组为6.8个月(95% CI: 5.4, 8.3),低评分组为11.2个月(95% CI: 10.4, 12.3),P<0.001
经倾向评分匹配(PSM)和逆概率加权(IPTW)校正后,上述差异仍然显著。提示Rad-ITF评分可作为TACE术前预后分层的有力工具。
Q3:高Rad-ITF评分与HCC肿瘤血管生成水平之间存在怎样的关联?
A3: 多组学分析一致表明,高Rad-ITF评分与更高的肿瘤血管生成活性显著相关:①基因表达层面 (TCGA队列,n=39):高评分组中VEGFR3等血管生成相关基因表达显著上调(adjusted P=0.04)。②单细胞RNA测序 (前瞻性队列,n=12):高评分组中内皮细胞(adjusted P=0.02)和成纤维细胞(adjusted P=0.03)显著富集,且VEGFR3、PDGFRA等基因表达升高。③空间转录组 (2例):VEGFR3和PDGFRA主要表达于高纤维化区域。④组织学验证 (全体训练+验证集):高评分组的微血管密度(MVD,CD34染色)中位数为55.0,显著高于低评分组的45.0(P<0.001)。
这些结果表明,Rad-ITF评分可间接反映HCC的血管生成状态,为联合抗血管生成治疗提供理论依据。
参考文献:Wang TC, Wei N, Bao Y, Li JX, Zhou P, Sun Y, Wang LZ, Cai WW, Chang DH, Xiao YD. CT Radiomics-based Machine Learning to Identify Intratumoral Fibrosis and Underlying Angiogenesis in Hepatocellular Carcinoma. Radiology. 2026 May;319(2):e250736. doi: 10.1148/radiol.250736.