01
实验原理
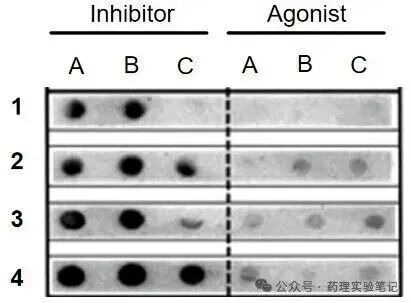
将含有目标分泌型蛋白的样品直接点在固相载体(如 PVDF 膜)上,使蛋白质吸附在膜表面。随后,利用特异性抗体识别并结合目标蛋白。一抗与目标蛋白结合后,再通过与二抗结合,二抗通常连接有酶或荧光标记物。最后,通过化学发光底物反应或荧光检测等可视化手段,根据显色信号的有无和强度来判断目标蛋白是否存在以及相对含量。
02
实验步骤
-
裁剪与活化 PVDF 膜:根据血清数量和样品数量,将 PVDF 膜裁剪成长方形,并减去一个小角作为起始标记。使用甲醇浸泡 PVDF 膜 1 分钟,随后转移到 TBST 中浸泡 15 分钟。

-
晾干 PVDF 膜:取出 PVDF 膜,置于干净自封袋上,晾干至半干状态,即看到水膜消失即可。(晾干可以使 PVDF 膜表面的水分或溶液挥发,使样品中的蛋白质更紧密地吸附在膜上,从而增强结合能力,防止样品在后续操作中移动或扩散。)
-
点样:将样品点于每格的中央,控制样品蛋白浓度在 2mg/mL,每点 1μL,室温晾干。

-
封闭:将 PVDF 膜浸入含 5% 脱脂奶粉的 TBST 溶液中,用量以浸没为准,室温下摇床放置 1 小时。
-
洗涤:回收封闭液,使用 TBST 溶液清洗 PVDF 膜 5 次,每次 5 分钟。
-
一抗孵育:加入稀释后的一抗,确保 PVDF 膜被溶液完全浸没,4℃摇床孵育过夜。
-
洗涤:回收一抗,使用 TBST 溶液清洗 PVDF 膜 5 次,每次 5 分钟。
-
二抗孵育:用含 2% 脱脂奶粉的 TBST 溶液以 1:5000 的比例稀释二抗,确保 PVDF 膜被溶液完全浸没,室温孵育 1.5 小时。
-
洗涤:回收二抗,使用 TBST 溶液清洗 PVDF 膜 5 次,每次 5 分钟。
-
显色:将 ECL 超敏显色剂(A 液:B 液 =1:1)混匀后,按适当体积滴加至 PVDF 膜上,室温反应 10 秒后显色,提前将化学曝光仪预冷,进行曝光,观察并记录结果。