01
文献学习

今天分享的文献是由广东省人民医院放射科刘再毅、南方医科大学南方医院梁莉等团队于2026年5月11日在柳叶刀旗下数字健康领域顶刊《The Lancet Digital Health 》(中科院1区top,IF=24.1)上发表的研究"Molecular alterations prediction in gliomas via an interpretable deep learning model: a multicentre and retrospective study" 即基于可解释深度学习模型的胶质瘤分子改变预测:一项多中心回顾性研究,该研究开发并验证了一种基于基础模型的可解释深度学习框架------GMAP,用于从常规HE染色病理全切片图像中预测胶质瘤的四种关键分子改变(IDH突变、1p/19q共缺失、TERT启动子突变、+7/-10染色体改变)。研究使用了来自14个队列的6298张全切片图像(4024例患者),是目前最大的胶质瘤多中心病理数据集。GMAP在内部测试集和外部验证集中均表现出优异的预测性能,尤其对IDH和1p/19q共缺失具有高准确性。通过多层级可解释性分析,模型识别出与分子改变相关的已知和新型组织形态特征。
创新点:①最大规模多中心验证 :收集14个中心、超4000例患者的6298张WSI,系统评估模型在不同人群、设备与染色方案 下的泛化能力。②覆盖最新WHO分子标志物 :除IDH和1p/19q外,首次在深度学习中系统探索TERT启动子突变和+7/-10 ,贴合2021版分类标准。③多尺度可解释性分析 :从细胞核形态、组织学特征到全片热图,揭示基因型-表型新关联(如+7/-10与短梭形细胞相关),提升模型透明度。
临床价值:①资源匮乏地区的新选择 :无需昂贵基因检测,仅用常规HE切片即可快速推断IDH和1p/19q状态 ,降低精准诊疗门槛。②优化分子检测流程 :作为预筛查分诊工具 ,对高预测评分病例优先行FISH确认,减少不必要的检测成本与等待时间。③推动精准分型与治疗 :提供符合WHO标准的分子信息,辅助胶质母细胞瘤等高级别肿瘤的个体化治疗决策,改善患者管理。
02
研究背景和目的
研究背景
胶质瘤是中枢神经系统最常见的恶性肿瘤,其临床诊疗已进入分子病理学时代 。根据2021年第五版WHO中枢神经系统肿瘤分类指南,IDH突变、1p/19q共缺失、TERT启动子突变及7号染色体扩增/10号染色体缺失(+7/-10) 等分子标志物是胶质瘤诊断、分级和预后判断的核心依据。然而,目前获取这些分子信息的金标准方法(如免疫组化、Sanger测序、FISH)成本高昂、操作复杂、周期较长 ,在资源有限的中低收入国家及基层医疗机构难以普及。近年来,深度学习技术在病理图像分析中展现出巨大潜力,有望从常规HE染色切片中直接推断分子改变。但现有研究多局限于单一或少数的分子标记(尤其是IDH) ,缺乏大规模、多中心的外部验证 来证明模型的泛化能力,同时模型决策的可解释性不足 ,难以获得临床医生的信任。因此,亟需开发一种低成本、高精度、具备良好泛化性且可解释的人工智能系统,用于胶质瘤分子改变的快速预测,以推动精准肿瘤学在更广泛医疗环境中的落地应用。
研究目的
本研究旨在开发并验证一个名为GMAP(胶质瘤分子改变预测器) 的可解释深度学习模型,其核心目标是直接从常规HE染色的全切片病理图像中预测四种关键的分子改变 :IDH突变、1p/19q共缺失、TERT启动子突变及+7/-10状态。为实现这一目标,研究团队构建了迄今为止规模最大的多中心胶质瘤病理数据集 ,涵盖14个独立队列、超过4000例患者的6000余张全切片图像。模型采用基础模型UNI提取特征 ,并结合自主设计的全局-局部Transformer(GLTrans)架构 ,以同时捕捉图像的全局组织背景和局部细胞形态特征。此外,研究特别强调多尺度可解释性分析 ,从细胞核形态、组织病理特征到全切片热力图,系统揭示模型关注的形态学依据及其与分子改变之间的潜在关联。最终目标是验证GMAP在内部测试集和13个外部独立验证集 上的预测性能与泛化能力,并与现有弱监督学习方法进行对比,评估其作为经济、快速、可靠的分子检测分诊工具在临床实践中的应用潜力。
03
数据和方法
研究数据
总样本量:6298张全切片图像,4024例患者
数据来源:14个独立队列(包括TCGA、EBRAINS公共数据集和12家中国医院)
分子标记:IDH突变、1p/19q共缺失、TERT突变、+7/-10改变
数据划分:TCGA作为发现队列(训练:验证:测试=8:1:1),其余13个队列用于外部验证
技术方法
模型架构:GMAP = UNI基础模型(特征提取) + GLTrans(全局-局部Transformer)
任务类型:弱监督多实例学习,每个分子改变为独立二分类任务
比较方法:与TransMIL、ABMIL、CLAM等现有方法对比
可解释性分析:
细胞层级:核形态、染色、纹理特征分析
组织层级:10种组织学特征的病理学家评估
全片层级:热图与免疫组化空间一致性分析
04
实验结果
****①内部测试集AUC:
IDH: 0.939
1p/19q: 0.955
TERT: 0.944
+7/-10: 0.886
****②外部验证集AUC:
IDH: 0.870
1p/19q: 0.885
TERT: 0.694
+7/-10: 0.672
③GMAP在所有分子任务上均显著优于现有方法(p < 0.0001)
④可解释性分析显示模型关注特征与病理学知识一致,如IDH突变型中"煎蛋样细胞"更常见
⑤模型热图与IDH1-R132H免疫组化染色强度空间一致(Moran's I > 0.9)
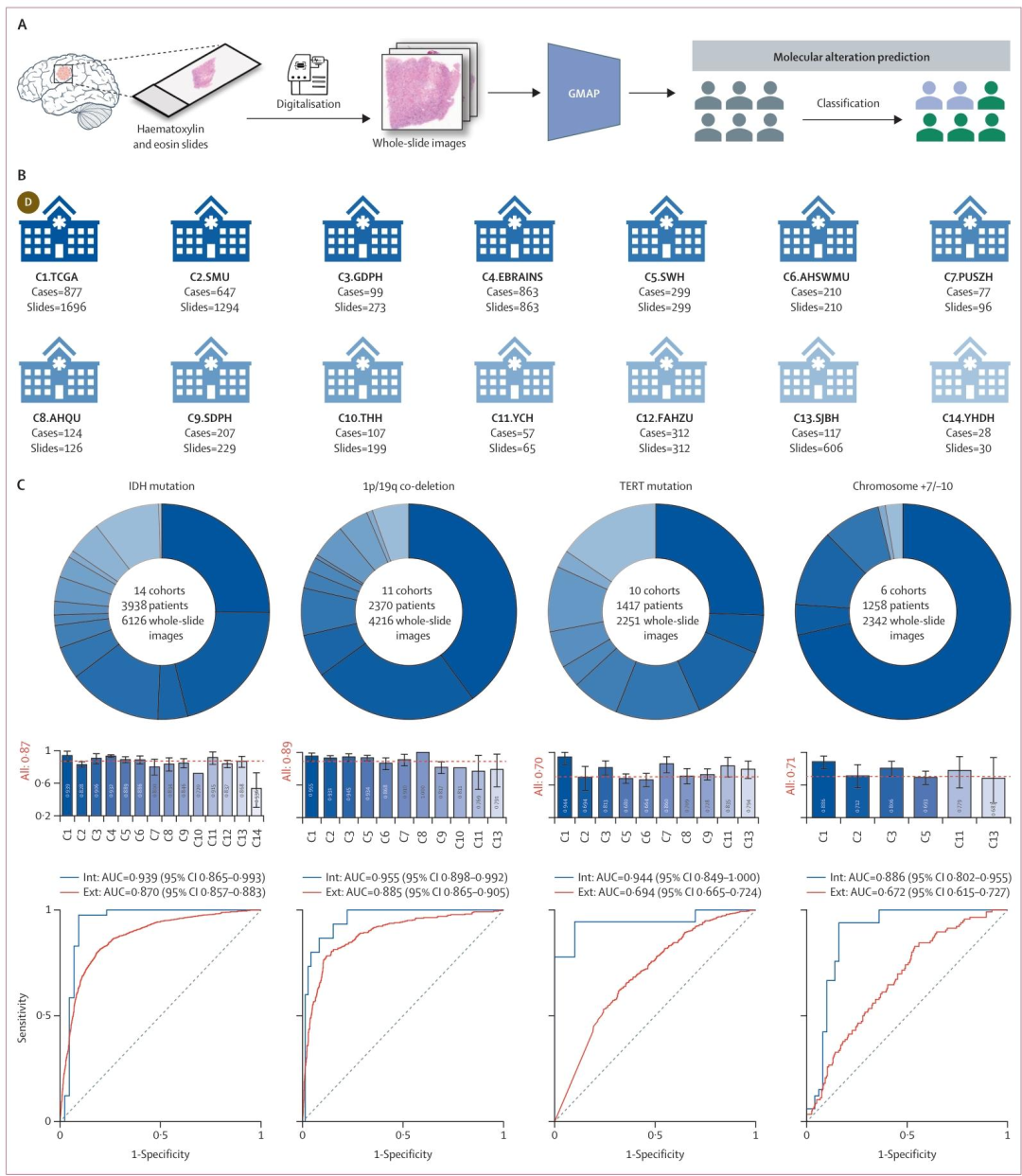
图 1:研究设计与模型泛化性能
该图展示了GMAP模型的整体研究流程与泛化评估结果。图A 呈现了模型开发流程:从TCGA队列的877例患者共1696张全切片图像中提取特征,基于UNI基础模型和GLTrans架构进行弱监督学习,独立预测IDH、1p/19q共缺失、TERT和+7/-10四种分子标志物。图B 条形图汇总了14个医疗中心的患者与WSI分布,总样本量达4024例患者、6298张WSI,其中外部验证集涵盖12家中国医院及EBRAINS公共数据集。图C 通过AUC值展示了GMAP在内部测试集与分组外部验证集上的性能:内部测试集上IDH、1p/19q、TERT、+7/-10的AUC分别达0.939、0.955、0.944、0.886 ;外部验证集上IDH和1p/19q仍保持0.870和0.885的高AUC,而TERT和+7/-10性能有所下降(0.694和0.672),提示后两者泛化性受限于样本异质性。
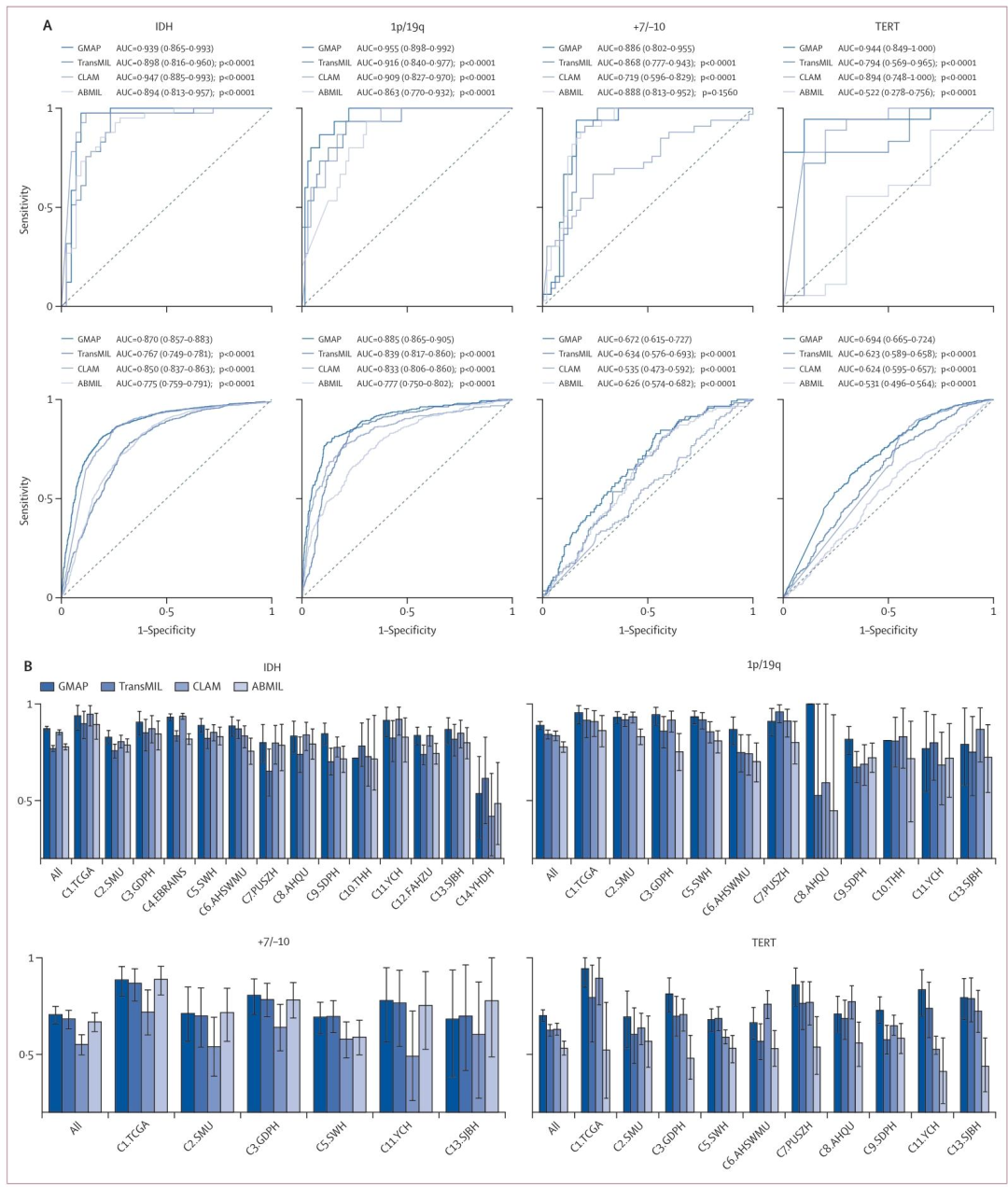
图 2:模型性能对比与ROC曲线
该图比较了GMAP与三种主流多实例学习方法(ABMIL、CLAM、TransMIL)的预测能力。图A 展示了内部测试集(上排)和外部验证集(下排)的ROC曲线:GMAP(红色曲线)在所有四个分子任务中均显著优于对比方法,例如外部验证集上IDH的AUC为0.870(对比模型最高仅0.850),1p/19q为0.885(对比模型最高0.839)。图B 以点图形式展示各模型在独立外部数据集上的AUC值,GMAP在绝大多数数据集上占据领先,且统计检验p值均<0.0001。值得注意的是,对于TERT和+7/-10这类更具挑战性的标志物,GMAP虽性能中等(AUC分别为0.694和0.672),但仍显著超越现有方法,体现了基础模型与GLTrans架构的优势。
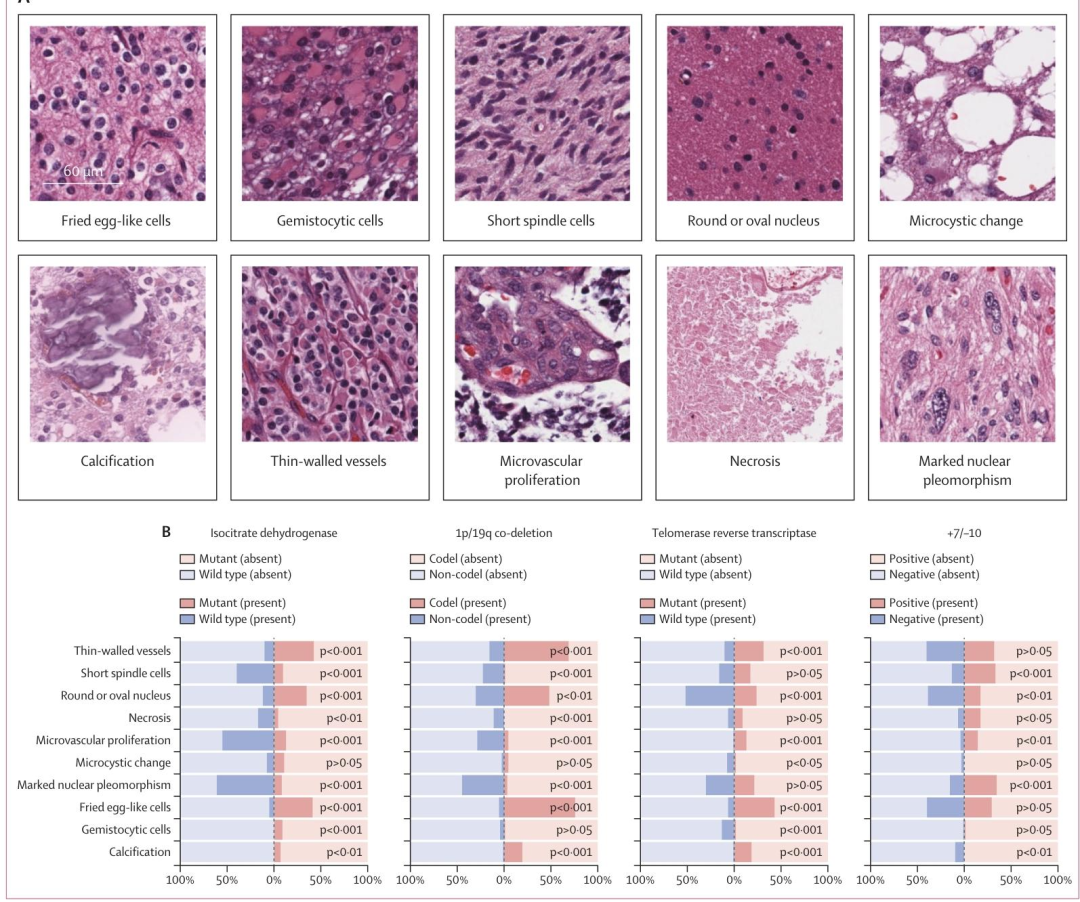
图 3:组织水平的可解释性分析
该图基于广东人民医院队列(C3.GDPH)评估GMAP关注的组织形态学特征。图A 列举了10种胶质瘤相关病理模式,包括微血管增殖、坏死、卵圆形核、"煎蛋样"细胞、钙化、薄壁血管等。图B 通过百分比条形图展示了不同分子状态下这些特征在高贡献图块中的出现率。结果显示:IDH突变型样本中**"煎蛋样"细胞(41.29% vs 5.08%)、卵圆形核(34.84% vs 11.86%)、薄壁血管(42.58% vs 10.17%)** 显著富集,而IDH野生型则更常出现坏死(16.95% vs 4.52%)和微血管增殖(55.08% vs 12.90%)。1p/19q共缺失和TERT突变体的特征分布与IDH突变型高度一致,符合寡突胶质细胞瘤的病理学认知。+7/-10阳性样本则突出显示核多形性(34.67% vs 15.31%)和坏死等高等级特征。
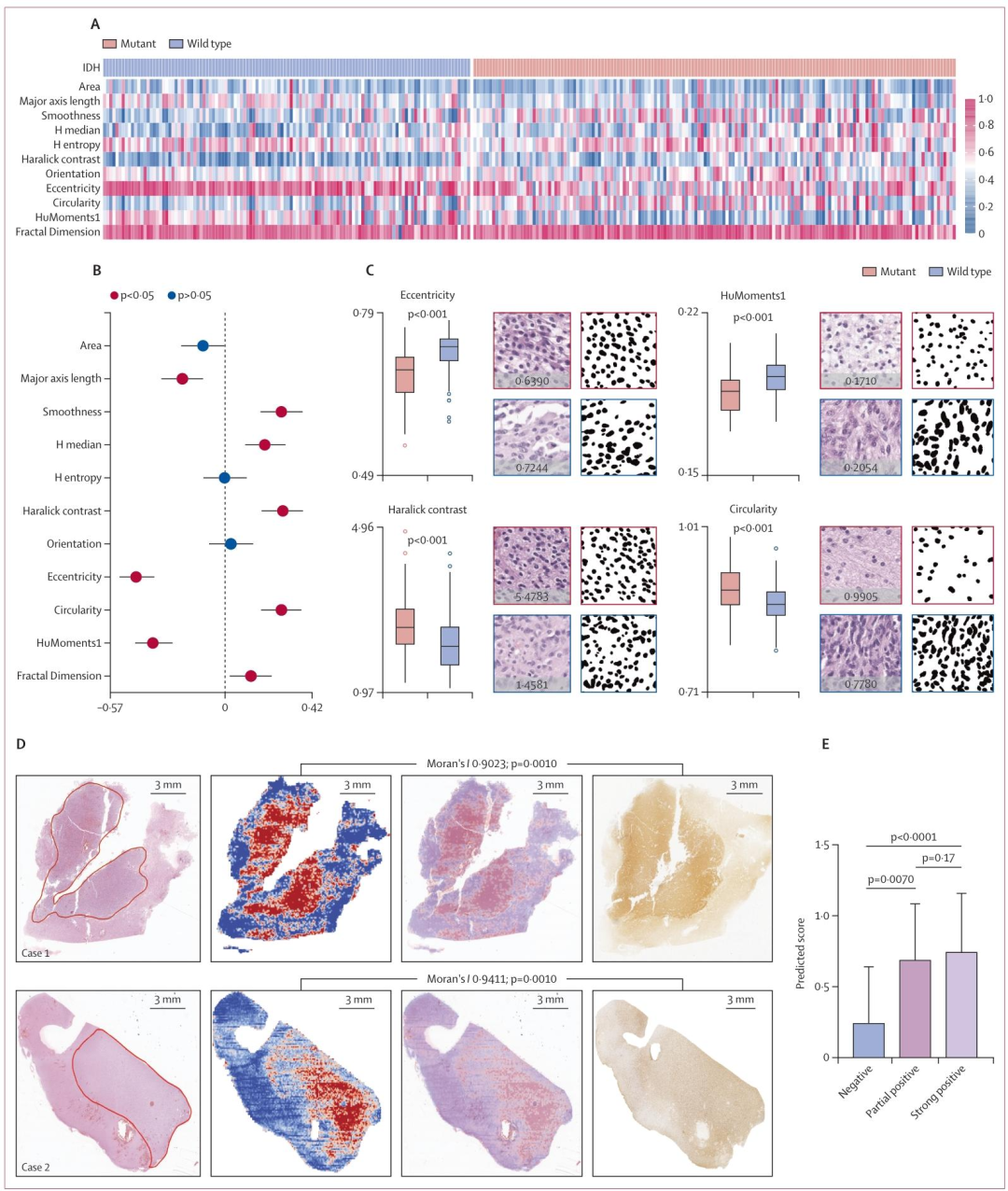
图 4:细胞和切片水平的IDH可解释性分析
该图深入解析GMAP对IDH状态预测的细胞学与空间学依据。图A 展示IDH突变型与野生型在top100高贡献图块中的11种核特征分布差异。图B 的Spearman相关性分析表明,IDH突变型预测与核偏心率呈负相关(r=-0.484) ,与圆度(r=0.306)和Haralick对比度(r=0.314)正相关。图C 箱线图进一步证实:IDH突变型细胞的核更圆、更规则,而野生型核更长、异型性更高。图D 将HE切片、模型注意力热图与IDH1-R132H免疫组化染色进行空间对比,Moran's I >0.9表明两者高度一致。图E显示:随着免疫组化染色强度从阴性到强阳性,GMAP预测分数从0.24±0.40显著升至0.74±0.42(p<0.0001),证明模型捕捉到了真实的生物学特征而非伪影。
05
研究结论
该研究提出的胶质瘤分子改变预测器(GMAP)是一个基于病理学基础模型的可解释深度学习框架,能够从常规苏木精-伊红染色全切片图像中预测四种关键分子改变。在内部测试集中,GMAP对IDH突变、1p/19q共缺失、TERT启动子突变和+7/-10染色体改变的AUROC分别达到0.939、0.955、0.944和0.886,展现出优异的预测性能 。在包含12家中国医院及公共数据集的13个独立外部验证集中,模型对IDH和1p/19q共缺失保持较高的泛化能力(AUROC分别为0.870和0.885),而对TERT和+7/-10的预测性能为中等水平(AUROC分别为0.694和0.672),但仍显著优于现有的多种多示例学习方法 。多尺度可解释性分析表明,模型关注的特征与已知的病理形态学关联高度一致(如IDH突变型富集"煎蛋样细胞"),并揭示了新的基因型-表型相关性(如+7/-10与短梭形细胞形态的潜在关联)。该模型为资源有限地区提供了一种低成本、快速、无需人工标注的分子分型筛查工具,在整合到临床工作流后有望优化胶质瘤的精准诊疗决策。
06
Q&A
Q1:GMAP模型主要预测胶质瘤的哪些分子改变?
A1: GMAP模型预测胶质瘤的四种关键分子改变:①IDH突变 (异柠檬酸脱氢酶突变)②1p/19q共缺失 (染色体臂1p和19q共缺失)③TERT启动子突变 (端粒酶逆转录酶启动子突变)④+7/-10(7号染色体扩增和10号染色体缺失)
Q2:与其他深度学习方法相比,GMAP的主要创新和优势体现在哪些方面?
A2: ①模型架构创新 :采用病理图像基础模型UNI 进行特征提取,结合自研的全局-局部Transformer(GLTrans) ,同时捕捉全片级的全局上下文和局部细胞形态特征。②大规模多中心验证 :收集了14个队列、6298张WSI、4024例患者,是目前最大的胶质瘤病理多中心数据集,显著提升了模型的泛化能力评估可信度。③多尺度可解释性 :从细胞、组织、全片三个层级解释模型决策,例如发现IDH突变型倾向于更圆、形态规则的细胞核,并与IDH1-R132H免疫组化染色空间一致。④临床适用性设计:无需人工标注,直接基于常规HE切片预测,可作为资源受限地区的分子检测分流工具。
Q3:该研究有哪些主要局限性?未来改进方向是什么?
A3:局限性 :①样本不平衡与缺失 :TERT和+7/-10的分子标注缺失率高达65%~69%,且不同中心间预测性能异质性明显(如+7/-10的I²=59.24%)。②未纳入全部关键标志物 :如EGFR扩增(2021 WHO分类中用于IDH野生型胶质母细胞瘤的诊断)。③单一任务独立建模 :目前将各分子改变作为独立二分类任务,未利用标记间的生物学关联(仅16.6%患者有完整四标记信息)。④空间验证局限 :免疫组化与热图的一致性分析仅针对IDH1-R132H变异型,未覆盖其他IDH突变亚型。未来方向:① 扩大数据集,尤其补充TERT和+7/-10标记完整样本。② 开发多任务或多标记联合预测模型,模拟真实整合诊断流程。③ 增加EGFR扩增等新兴诊断标志物。④开展前瞻性临床研究、工作流程评估及成本-效果分析,推动临床转化。
参考文献:Han C, Li D, Zhao B, Zhang X, Lin J, Yan X, Mao N, Lin J, Deng T, Huang J, Zhang J, Li J, Li X, Li H, Yan Y, Zhu X, Yao X, Yan H, Zhao S, Wang L, Ming Y, Liu X, Li S, Fan C, She H, Dai Y, Ye L, Wang J, Liu F, Guo X, Cui Y, Zhang Q, Ping Y, Liu Y, Bian X, Liu Z, Liang L. Molecular alterations prediction in gliomas via an interpretable deep learning model: a multicentre and retrospective study. Lancet Digit Health. 2027 Mar 19:100977. doi: 10.1016/j.landig.2025.100977.