在日常生活中,从婴儿奶瓶到食品包装袋,从医用输液管到儿童玩具,一种名为邻苯二甲酸二(2 - 乙基己基)酯(DEHP)的塑化剂几乎无处不在。这种被广泛应用的化工原料,正随着塑料的老化和分解,悄然渗入空气、水源和土壤,成为威胁人类健康的 "隐形杀手"。当我们在不知不觉中接触 DEHP 时,肝脏这个默默承担代谢重任的器官,正面临着胆汁淤积性损伤的严峻挑战。好在,安徽医科大学的研究团队最近在《Basic & Clinical Pharmacology & Toxicology》上发表的一项研究,为破解这一难题带来了新的希望 ------ 他们发现,三羧酸(TCA)循环的中间体衍生物富马酸二甲酯(DMF),能够通过激活 Nrf2/NQO1 信号通路,有效减轻 DEHP 诱导的肝损伤,而 AbMole 的 ML385 抑制剂则在机制解析中扮演了关键角色。
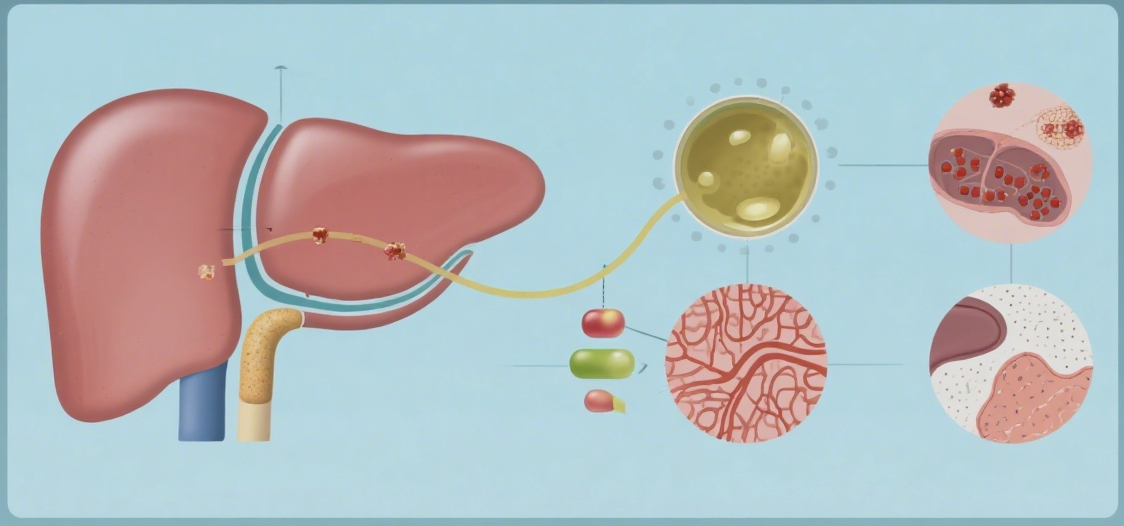
一、暗藏危机的日常接触:DEHP 与肝损伤的隐秘联系
DEHP 作为全球使用最广泛的塑化剂之一,其化学结构决定了它极易从塑料制品中迁移到外界环境。研究表明,人体通过呼吸、饮食和皮肤接触,每天都会摄入一定量的 DEHP,而肝脏作为主要的代谢器官,首当其冲成为 DEHP 毒性作用的靶器官。早期研究发现,DEHP 不仅会引发肝脏炎症、脂质代谢紊乱,甚至可能促进肝癌的发生。近年来,越来越多的证据显示,DEHP 还会干扰胆汁酸代谢,导致胆汁在肝脏内异常淤积,引发胆汁淤积性肝损伤(CLI)。
胆汁淤积性肝损伤的核心特征是胆汁酸在肝脏内过度积累,有毒的胆汁酸会引发氧化应激和炎症反应,进而导致肝细胞坏死、胆管细胞损伤和肝纤维化。临床数据显示,全球每年新诊断的 CLI 病例呈上升趋势,但目前针对这类疾病的有效干预手段却非常有限。因此,深入探究 DEHP 诱导 CLI 的分子机制,并寻找安全有效的干预策略,成为当下肝病研究领域的紧迫课题。
在细胞的能量代谢网络中,TCA 循环被誉为 "代谢中枢",负责将营养物质转化为能量,并为生物合成提供前体物质。最新研究发现,DEHP 能够破坏肝脏中的 TCA 循环,导致富马酸、苹果酸等关键中间体水平下降,进而影响能量代谢和抗氧化防御。而 DMF 作为富马酸的衍生物,能够补充 TCA 循环中间体,这为干预 DEHP 诱导的肝损伤提供了全新的思路。
二、抽丝剥茧的实验设计:从动物模型到细胞机制的层层解析
(一)体内实验:构建 DEHP 诱导的肝损伤模型
研究团队选取 8 周龄的雌性 ICR 小鼠,随机分为 5 组,分别进行不同处理:对照组、DEHP 组(200mg/kg/day)、DMF 组(100mg/kg/day)、DEHP+DMF 低剂量组(30mg/kg/day)和 DEHP+DMF 高剂量组(100mg/kg/day)。通过灌胃给药持续 4 周后,收集血液和肝脏组织,进行多项指标检测。
在生化指标检测中,研究人员发现 DEHP 组小鼠血清和肝脏中的总胆汁酸(TBA)水平显著升高,碱性磷酸酶(ALP)和谷氨酰转肽酶(GGT)活性异常增强,这些都是胆汁淤积的典型标志。而 DMF 干预组的这些指标则呈现剂量依赖性下降,尤其是高剂量组,几乎恢复到了对照组水平。
病理分析显示,DEHP 组小鼠肝脏出现明显的胆管细胞损伤、炎性细胞浸润和胶原沉积,肝细胞坏死区域广泛分布。相比之下,DMF 处理组的肝脏病理损伤明显减轻,胆管结构趋于正常,炎性细胞浸润减少,胶原纤维沉积显著降低。
(二)体外实验:AML-12 细胞模型验证分子机制
为了排除体内复杂环境的干扰,研究团队采用小鼠肝细胞 AML-12 细胞进行体外实验。将细胞分为对照组、DEHP 组(250μM)、DEHP+DMF 低剂量组(10μM)、中剂量组(25μM)和高剂量组(50μM),处理 24 小时后检测细胞活力和相关基因表达。
CCK-8 实验显示,DEHP 处理显著降低了 AML-12 细胞的存活率,而 DMF 预处理则能够显著提高细胞存活率,呈现明显的保护效应。进一步的 RT-qPCR 检测发现,DEHP 诱导了 IL-1β、IL-6 和 TNF-α 等促炎因子的大量表达,而 DMF 能够剂量依赖性地抑制这些炎症因子的转录。
(三)关键工具的助力:AbMole ML385 解析 Nrf2 信号通路
在探究 DMF 作用机制时,研究人员聚焦于 Nrf2/NQO1 信号通路。Nrf2 是调控细胞抗氧化和解毒反应的核心转录因子,其激活能够诱导 NQO1 等抗氧化酶的表达,减轻氧化应激损伤。为了验证 DMF 是否通过激活 Nrf2 发挥作用,研究团队使用了 AbMole 的 ML385(Nrf2 抑制剂,货号 M8692)。
实验中,先用 ML385 预处理 AML-12 细胞 2 小时,再加入 DEHP 和 DMF 进行处理。结果令人振奋:当 Nrf2 被抑制后,DMF 对炎症因子的抑制作用明显减弱,IL-1β、IL-6 和 TNF-α 的表达水平显著回升。这表明 DMF 减轻炎症反应的效果,至少部分依赖于 Nrf2 信号通路的激活。
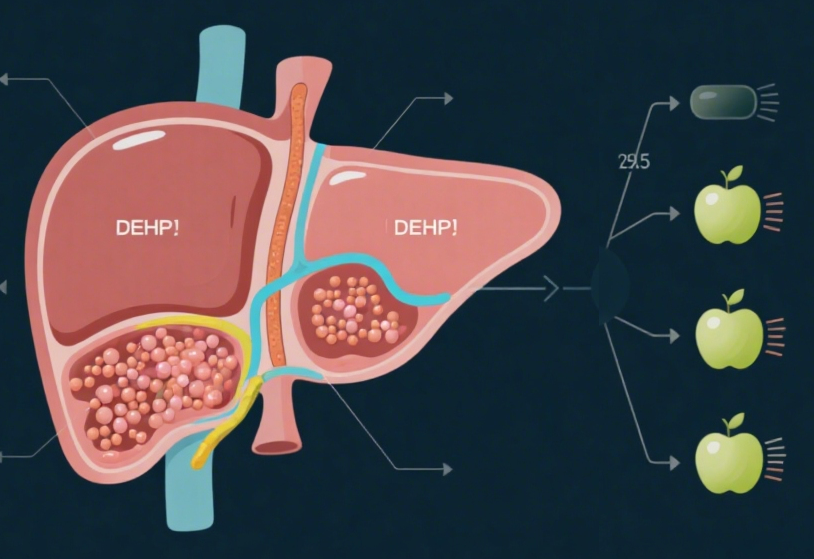
三、数据背后的科学故事:从代谢紊乱到信号激活的连锁反应
(一)DEHP 对 TCA 循环的破坏:能量代谢失衡的开端
通过 LC/MS 检测肝脏中的 TCA 循环代谢物,研究人员发现 DEHP 处理导致富马酸和苹果酸含量显著降低,而其他代谢物如柠檬酸、琥珀酸等则无明显变化。这说明 DEHP 特异性地干扰了 TCA 循环中的富马酸 - 苹果酸代谢节点,导致能量生成减少,抗氧化物质合成受阻,进而引发氧化应激和炎症反应。
(二)DMF 的多重保护效应:从胆汁酸代谢到氧化应激调控
DMF 作为富马酸的酯类衍生物,能够补充 DEHP 导致的 TCA 循环中间体不足,恢复富马酸水平,从而改善能量代谢。更重要的是,DMF 能够调节胆汁酸代谢,降低血清和肝脏中有毒的疏水性胆汁酸(如脱氧胆酸、鹅脱氧胆酸)水平,减少其对肝细胞膜的损伤。
在氧化应激和炎症调控方面,DMF 显著降低了肝脏中丙二醛(MDA)水平,提高了超氧化物歧化酶(SOD)活性,表明其能够减轻脂质过氧化损伤,增强抗氧化能力。同时,DMF 抑制了促炎因子的表达,减轻了肝脏内的炎症反应,为肝细胞创造了有利的修复环境。
(三)Nrf2/NQO1 通路:DMF 发挥作用的核心枢纽
Western blot 和免疫荧光实验显示,DMF 能够促进 Nrf2 蛋白从细胞质转移到细胞核,增强其转录活性,进而上调 NQO1 等下游基因的表达。当使用 ML385 抑制 Nrf2 后,DMF 对 NQO1 的诱导作用消失,再次证实了 Nrf2 通路的关键作用。这一系列实验表明,DMF 通过激活 Nrf2,启动了细胞内的抗氧化和抗炎防御机制,从而减轻 DEHP 诱导的肝损伤。
四、科研工具的幕后贡献:AbMole 产品助力机制精准解析
在整个研究过程中,AbMole 的 ML385 抑制剂发挥了至关重要的作用。在体外实验中,研究人员面临着如何准确验证 Nrf2 信号通路作用的难题。传统的信号通路抑制剂往往存在特异性不足的问题,而 ML385 作为高特异性的 Nrf2 抑制剂,能够精准阻断 Nrf2 的核转位和转录活性,为确定 DMF 的作用机制提供了可靠的工具。
当研究人员发现 DMF 能够上调 Nrf2 和 NQO1 的表达时,他们需要确认这种效应是否是 DMF 发挥保护作用的必要条件。通过 ML385 预处理细胞,观察到 DMF 的保护效应被逆转,这才确凿地证明了 Nrf2 通路的核心作用。可以说,没有 ML385 的助力,就难以如此精准地解析 DMF 的分子机制,这充分体现了高质量科研工具对科学发现的重要性。
五、未来展望:从基础研究到应用转化的无限可能
这项研究的意义远远超出了基础科学的范畴,它为 DEHP 诱导的肝损伤提供了全新的干预思路。DMF 作为 TCA 循环中间体衍生物,通过激活 Nrf2/NQO1 通路,展现出了多靶点的保护效应,为开发针对胆汁淤积性肝损伤的新型干预策略奠定了坚实的基础。