小罗碎碎念
当病理医生面对一张包含数十亿像素的全切片病理图像(WSI)时,就像在茫茫沙漠中寻找特定沙粒------不仅要在海量组织细节中精准识别病变,还要区分形态相似的亚型、判断病变层级,稍有疏忽就可能影响诊断结果。
传统病理诊断依赖医生的经验积累,而AI辅助诊断技术虽已取得进展,却在处理复杂层级分类任务时力不从心。
如今,一种名为PathTree的诊断文本引导表征学习技术横空出世,它模仿病理医生的分层诊断思维,让AI真正读懂病理图像的"语言",为精准医疗打开了新大门。

该研究针对病理全切片图像(WSI)复杂层级分类难题,提出了一种诊断文本引导的表征学习方法PathTree,核心创新在于将多类别病理分类转化为二叉树结构的层级任务,并融合专业病理文本描述实现跨模态引导。
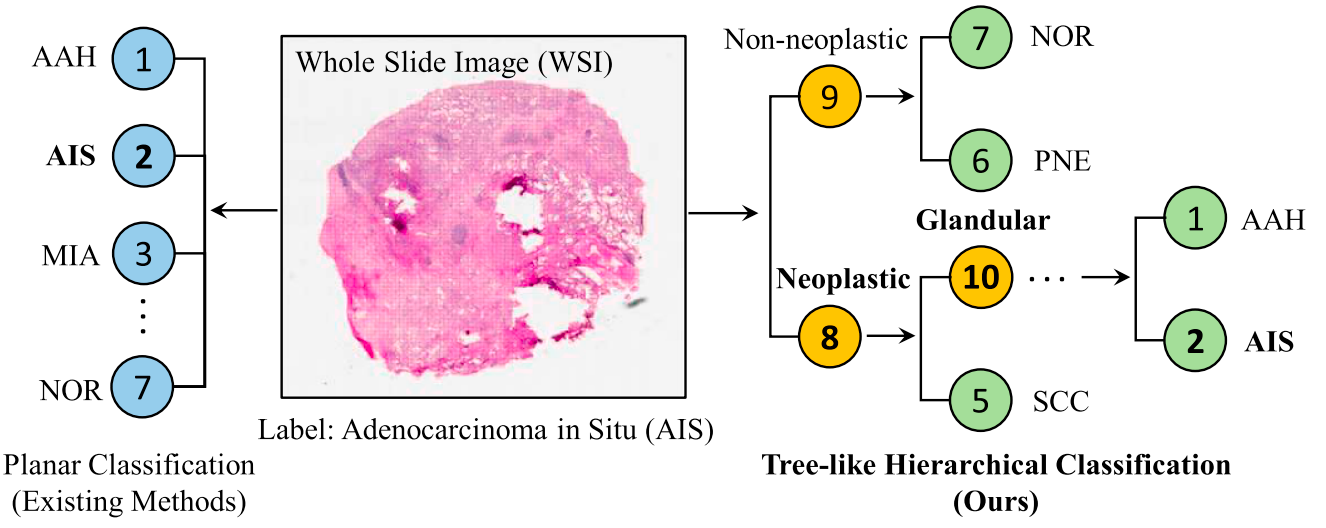
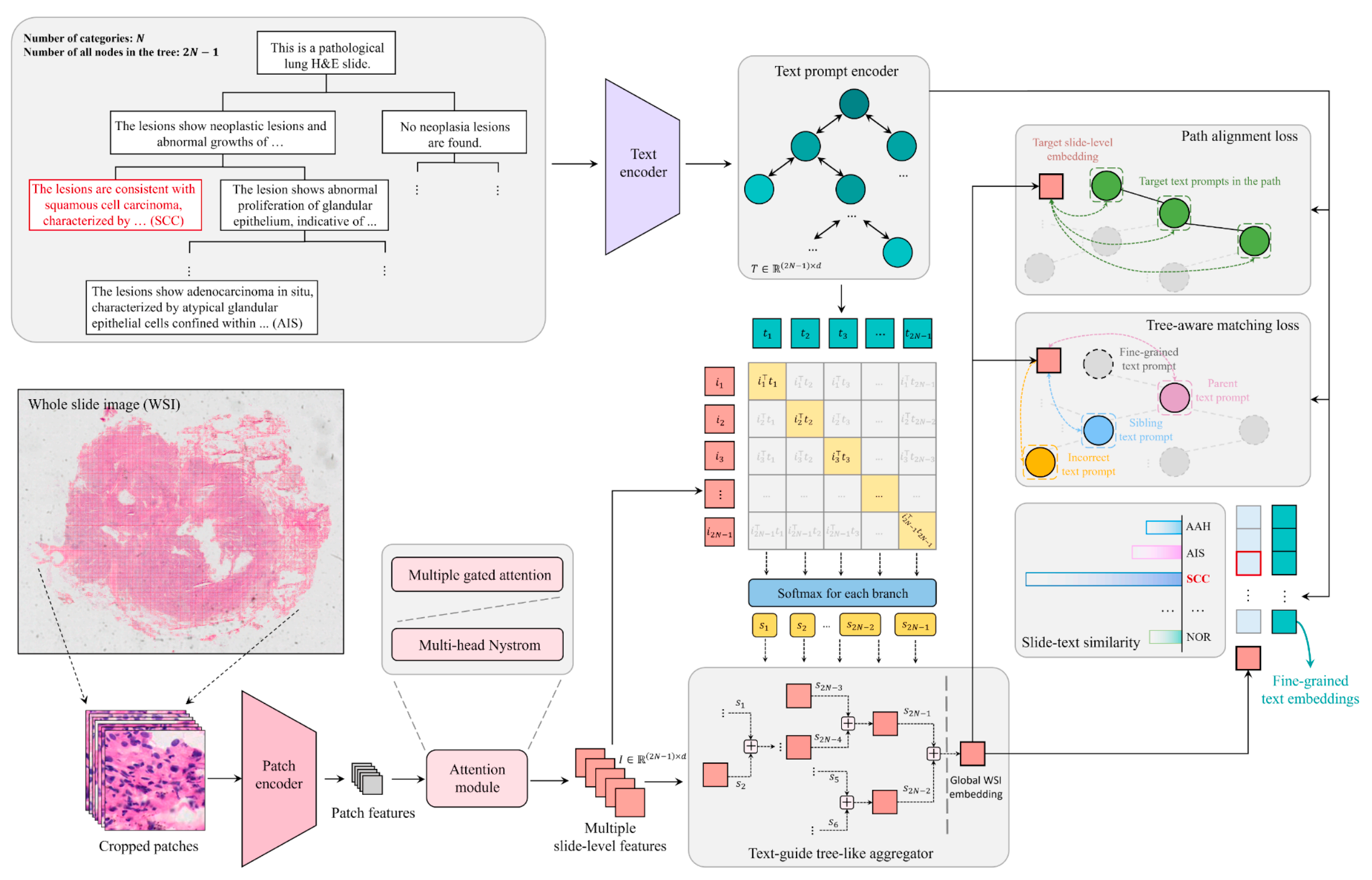
PathTree通过树形图神经网络编码层级文本语义,利用多门控注意力与多头Nystrom注意力双模块提取图像特征,再通过文本引导的树形聚合器实现从细粒度到粗粒度的特征融合,同时引入路径对齐损失与树形匹配损失约束文本-图像语义一致性,有效解决了传统方法忽略类别层级关系、难以利用病理语义信息的局限。
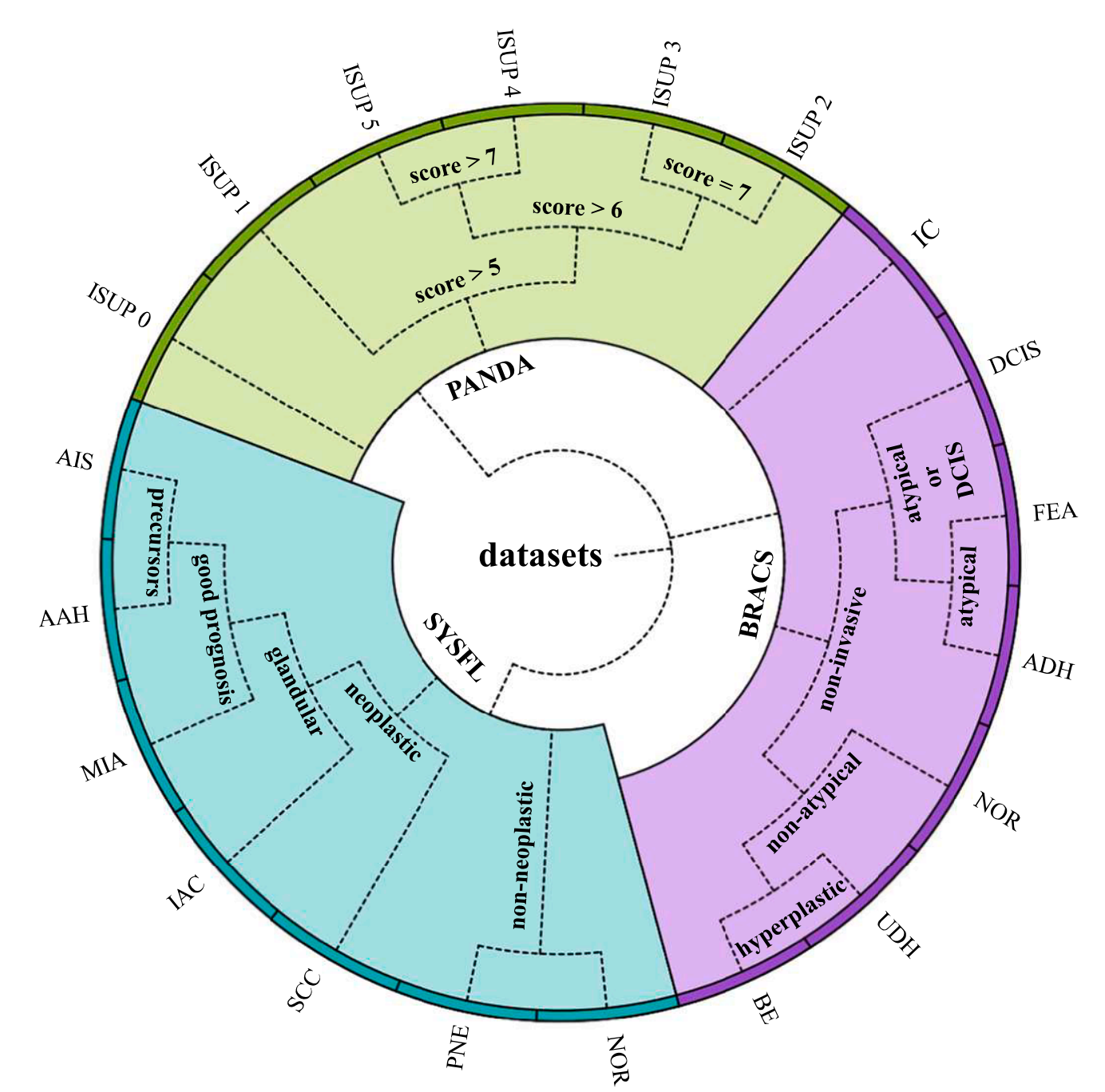
在实验验证方面,研究团队在SYSFL、PANDA、BRACS三大数据集上开展了全面评估,涵盖肺组织冰冻切片病变识别、前列腺癌分级、乳腺癌亚型分类等典型临床场景。
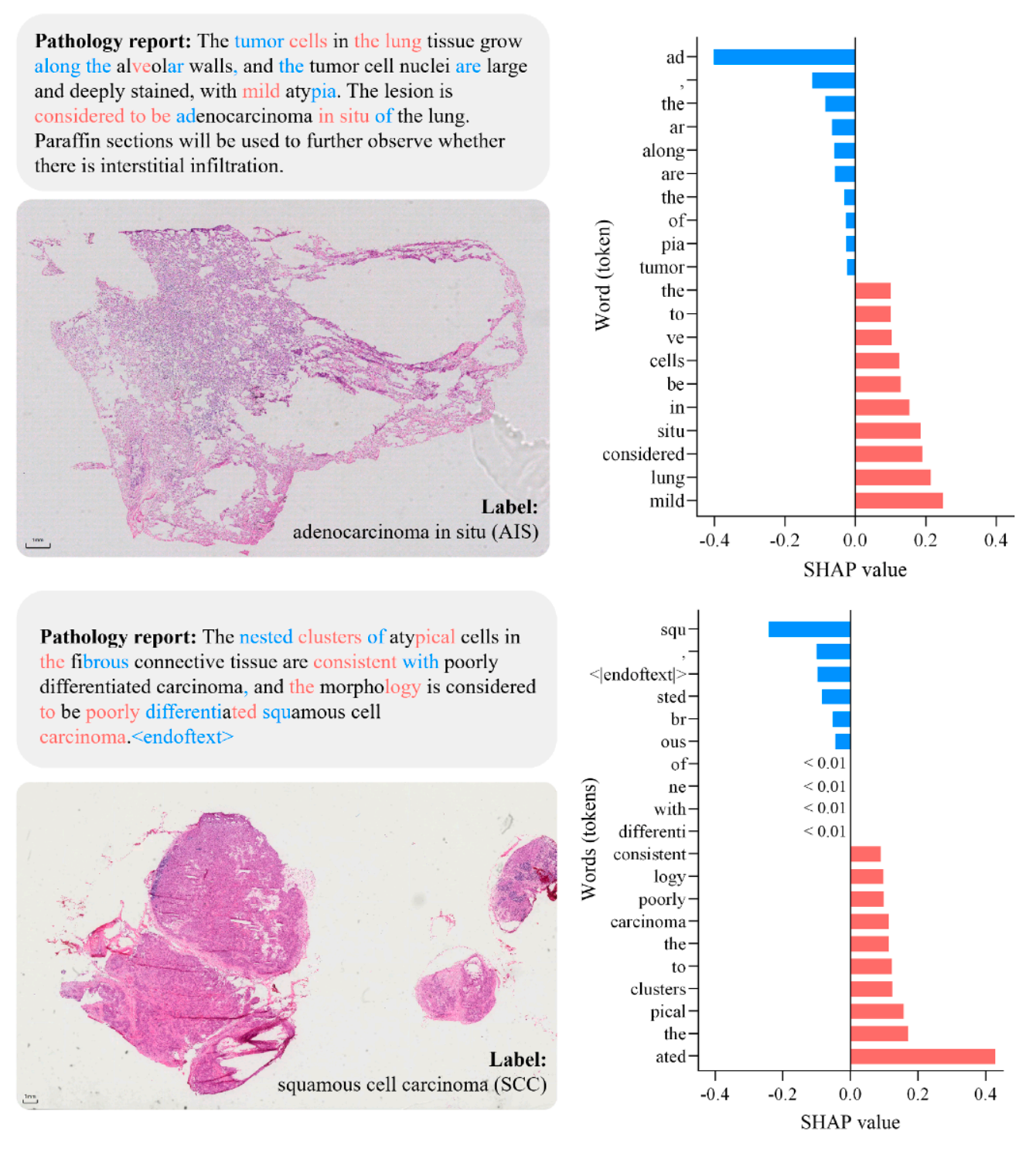
结果显示,PathTree及其变体PathTree-Ny在细粒度分类任务中表现突出,SYSFL数据集加权F1分数达62.04%,PANDA数据集准确率达62.35%,均优于ABMIL、CLAM等主流基线方法;在层级指标H-F1上,模型整体领先约2个百分点,且在少样本学习场景中展现出稳健性能,4-shot及以上设置下优势显著,同时通过SHAP分析验证了模型对病理关键术语的有效捕捉,确保了结果的可解释性。
该研究为复杂病理图像分析提供了新范式,其层级分类框架与文本-图像融合思路不仅突破了现有技术在模糊类别边界、细微形态差异识别上的瓶颈,还为临床实际应用提供了更贴合病理医生诊断逻辑的解决方案。
研究还通过消融实验验证了专业文本描述、树形约束损失等核心组件的有效性,同时指出未来可结合大语言模型生成更丰富的文本提示、构建跨癌种大规模层级数据集预训练基础模型,进一步拓展技术的适用范围与泛化能力,为精准医疗中的AI辅助诊断提供更强有力的技术支撑。
医学AI交流群
目前小罗全平台关注量120,000+,交流群总成员3000+,大部分来自国内外顶尖院校/医院,期待您的加入!!
由于近期入群推销人员较多,已开启入群验证,扫码添加我的联系方式,备注姓名-单位-科室/专业,即可邀您入群。
团队介绍
罗小罗团队是一支以国内外硕博为主的科研团队,覆盖影像组学、病理组学以及基因组学等医学AI主流研究领域。
980+医学图像公开数据集查询系统,680+医工交叉开源代码仓库,最新的医学AI前沿论坛回放等你来探索!
团队的宗旨是汇聚国内外顶尖人才,构建医学AI生态,推动医学AI从实验室走向临床,期待您的加入!
一、病理诊断中的"层级迷宫"与AI瓶颈
病理诊断的核心挑战,在于病变类型的复杂性与关联性。
以肺癌为例,从癌前病变到浸润性癌,存在多个渐进式亚型,它们的形态特征高度相似,却对应着截然不同的治疗方案和预后判断。
这就像区分一系列外观相近的水果------不仅要分清是苹果还是梨,还要判断苹果的成熟度、是否有病虫害。
传统AI技术在处理这类问题时,往往采用"平面分类"思路,将每个病变类型视为独立类别逐一识别。这种方法存在两大局限:
- 一是忽略了病变之间的层级关系,无法利用"癌前病变与早期癌形态相似"这类关键诊断知识;
- 二是过度依赖像素级标注,而高质量的病理标注需要耗费大量时间和专业资源,难以规模化应用。
更棘手的是,复杂病理诊断中,单一词汇难以描述病变特征。
病理医生通常用"腺体结构紊乱、细胞异型性中等、局部浸润间质"这类多维度文本描述辅助判断,但现有AI模型无法有效整合这些语义信息,只能依赖图像特征进行"盲判"。
这些瓶颈导致AI在处理前列腺癌分级、乳腺癌亚型分类等复杂任务时,准确率和泛化能力始终难以达到临床要求。
二、PathTree的"分层诊断"蓝图
PathTree的核心创新,是将病理医生的诊断逻辑转化为可计算的AI框架------它把复杂的多分类问题拆解为二叉树结构的层级任务,用专业诊断文本引导图像特征学习,就像给AI配备了一本"病理诊断手册"和一套"分层推理流程"。
让AI学会"逐层推理"
传统AI是"一眼定生死",直接判断图像属于哪一类病变;而PathTree则像病理医生一样"循序渐进":
- 先区分是良性还是恶性(粗粒度分类)
- 再判断具体亚型(细粒度分类),每一步都基于上一层的判断结果深化分析
这种层级结构不仅符合临床诊断逻辑,还能让模型在每个节点聚焦关键特征,减少干扰信息的影响。
文本与图像的"双向对话"
PathTree的灵魂在于文本与图像的深度融合,其核心组件可通俗理解为三个部分:
病理文本"说明书"
为每个层级的病变节点撰写专业文本描述,比如"癌前病变:腺体结构轻度紊乱,细胞异型性不明显,无间质浸润"。
这些文本由两名以上病理专家验证,确保语义准确性,它们就像AI的"诊断指南",明确每个节点的判断标准。
树形语义"连接器"
通过树形图神经网络(GAT)让不同层级的文本信息互通。
比如"浸润性癌"的文本描述会参考其上层"恶性病变"的特征,同时向下传递给更细分的亚型节点,形成语义关联。
这就像企业的层级汇报体系,基层信息向上汇总,高层指令向下传达,确保整个诊断逻辑的一致性。
双注意力"探测器"
采用两种注意力机制从图像中提取特征:
- 一种是"多门控注意力",给每个图像补丁分配不同权重,聚焦关键区域;
- 另一种是"多头Nystrom注意力",捕捉全局上下文信息。
这两种机制协同工作,既不会错过细微病变(如微小浸润灶),也能把握整体组织形态,就像病理医生用显微镜观察时,既要看局部细节,也要扫视整体切片。
四步完成精准诊断
PathTree的工作过程清晰易懂,就像一场"图像与文本的对话":
第一步,图像切片与文本准备
将WSI切割成256×256像素的小补丁,同时构建包含粗粒度到细粒度的树形文本体系,形成"图像补丁+文本描述"的数据对。
第二步,特征编码与语义交互
用预训练模型分别提取图像补丁和文本的高维特征,再通过树形图神经网络让文本特征互通有无,形成带有层级关系的语义嵌入。
第三步,文本引导的特征聚合
在文本特征的引导下,将分散的图像补丁特征逐层聚合------从叶子节点(细粒度亚型)向上汇总到根节点(粗粒度分类),每一步聚合都参考对应层级的文本描述,确保特征与语义对齐。
第四步,双重约束与预测
通过"路径对齐损失"确保图像特征与层级文本特征一致,用"树形匹配损失"区分相似病变类型,最后通过计算图像与文本的相似度得出诊断结果。
三、三大数据集见证"诊断实力"
为了验证PathTree的性能,研究团队在三个挑战性数据集上进行了全面测试,既包括内部构建的肺组织冰冻切片数据集(SYSFL),也包括公开的前列腺癌分级数据集(PANDA)和乳腺癌亚型分类数据集(BRACS),覆盖了临床中典型的复杂病理诊断场景。
基准测试
在细粒度分类任务中,PathTree表现亮眼:
- 在SYSFL数据集上,加权F1分数达到62.04%,比当前最优方法高出3.38%;
- 在PANDA数据集上,准确率达到62.35%,相当于在1万多张图像中多正确识别了128张病变切片。
更重要的是,在衡量层级分类性能的H-F1指标上,PathTree在三个数据集上均排名第一,证明其层级推理能力的优越性。
这些数据背后,是PathTree对细微差异的精准捕捉。
以前列腺癌分级为例,ISUP 2级(Gleason评分3+4=7)和ISUP 3级(Gleason评分4+3=7)的形态差异极小,传统AI容易混淆,而PathTree通过文本引导的层级对比,能准确区分癌细胞的排列方式和浸润程度,分类准确率提升明显。
真实场景
在肺组织冰冻切片诊断中,由于样本制备时间短、形态不如石蜡切片清晰,诊断难度远高于常规切片。
PathTree在该场景下的加权F1分数达到62.04%,比传统方法高出3个百分点以上,能有效辅助医生快速判断病变性质,为术中决策争取时间。
在乳腺癌亚型分类中,PathTree能准确区分良性病变、癌前病变和恶性肿瘤,其中对扁平上皮不典型性(FEA)这类易误诊亚型的识别准确率提升最为显著。
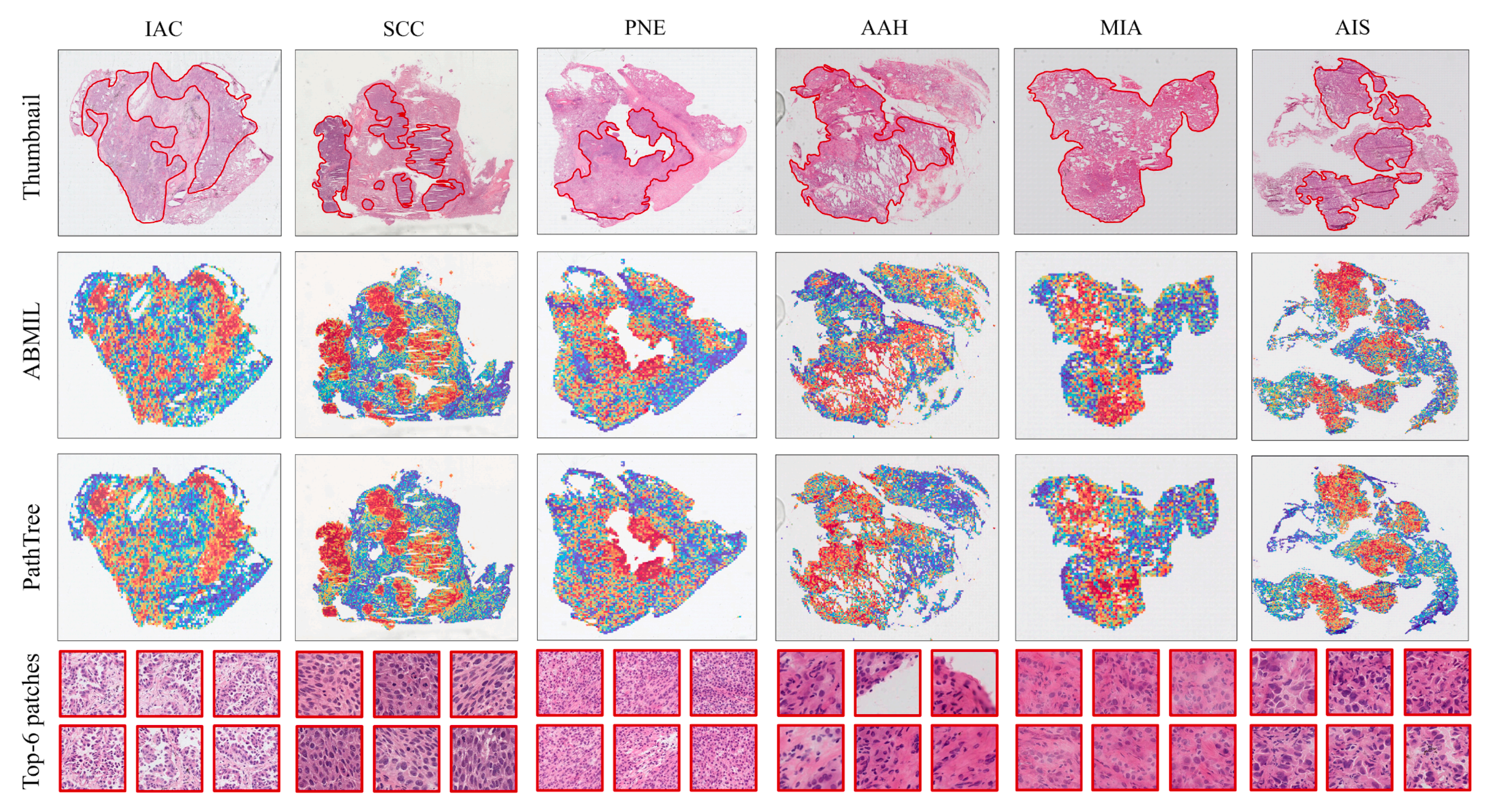
病理医生反馈,PathTree的注意力热图能精准定位病变区域,与医生标注的感兴趣区域重合度高达80%以上,可作为诊断参考。
少样本学习与可解释性
PathTree的另一大亮点是出色的少样本学习能力。
在仅提供16个训练样本的情况下,其AUC分数仍能达到80%以上,这意味着在罕见病诊断等样本稀缺场景中,它依然能发挥作用。
这就像新手医生通过少量典型病例快速掌握诊断要点,大大降低了对大规模标注数据的依赖。
同时,PathTree具备良好的可解释性------通过SHAP分析发现,模型决策主要依赖"腺体结构紊乱""细胞异型性"等病理关键术语,而非无关文本;注意力热图能直观展示模型关注的病变区域,让医生清楚AI的判断依据,避免"黑箱决策"。
四、总结
PathTree的出现,不仅推动了AI病理诊断技术的进步,更在多个层面重塑了病理诊断的生态。
对于临床诊断而言,它解决了复杂亚型分类这一"老大难"问题。
以前AI难以区分的癌前病变与早期癌、不同分级的前列腺癌,现在通过层级推理和文本引导能实现精准识别,这将帮助医生减少误诊漏诊,为患者争取最佳治疗时机。
例如,在肺腺癌诊断中,精准区分原位癌(AIS)和微浸润癌(MIA),能决定患者是否需要术后辅助治疗,直接影响预后。
对于病理研究而言,PathTree提供了"文本-图像"融合的新范式。它证明了专业诊断文本中蕴含的语义信息,能有效提升AI对病理图像的理解能力,为多模态病理分析开辟了道路。
未来,结合病理报告、基因组数据等多源信息,有望实现"图像+文本+基因"的综合诊断,进一步提升精准医疗水平。
对于技术推广而言,少样本学习能力降低了临床应用门槛。许多医院由于样本量有限、标注资源不足,难以部署传统AI模型,而PathTree仅需少量标注数据就能实现较高性能,更适合在基层医院推广,助力医疗资源均等化。
展望未来,PathTree还有巨大的发展空间。
研究团队计划利用大语言模型的医疗知识,自动生成更丰富的病理文本描述;构建跨癌种的大规模层级数据集,训练通用型病理AI模型;探索与基因组数据的融合,实现从病理图像直接预测基因变异、治疗响应等关键信息。
正如病理诊断从光学显微镜发展到数字病理,AI辅助诊断也正在从"平面识别"走向"层级推理",而PathTree正是这一变革的重要推动者。
PathTree的创新,本质上是让AI学会了病理医生的"思维方式"------不仅看图像,更懂诊断逻辑。当技术与临床思维深度融合,精准医疗便有了更坚实的支撑。
或许在不久的将来,每个病理科都将配备这样一位"数字助手",与医生并肩作战,让疾病诊断更精准、更高效,为患者带来更多希望。
参考资料
(本文基于Jiawen Li等人发表于Medical Image Analysis的研究成果,论文题目:Diagnostic text-guided representation learning in hierarchical classification for pathological whole slide image,代码已开源:https://github.com/WonderLandxD/PathTree)