论文总结
1、分析方法较多:
-
结构方程模型分析器官间衰老关联;
-
Cox回归评估年龄差与疾病/死亡的关联;
-
LightGBM用于疾病风险预测;
-
蛋白质组与血液代谢组关联分析;
-
全表型关联分析识别可调节因素;
-
孟德尔随机化分析筛选潜在药物靶点。
2、研究结论:
1. 器官衰老时钟的构建与表现
-
各器官的年龄预测精度差异显著:大脑灰质、白质、心脏、身体成分预测精度较高(R² 0.71--0.81),而肝脏、肾脏、胰腺、眼睛精度较低(R² 0.27--0.34)。
-
模型在性别间表现一致,但在不同年龄层和种族间存在偏差,提示需在多人群中外验证。
2. 器官间衰老的相互关联
-
心脏与身体成分的衰老与其他器官关联最为广泛。
-
结构方程模型揭示了器官间衰老的统计关联网络,如身体成分年龄每增加1年,胰腺、肾脏、心脏年龄分别增加0.26、0.24、0.06年。
3. 器官衰老与疾病、死亡风险的关联
-
器官特异性年龄差越大,相应器官相关疾病风险越高:
-
大脑灰质年龄差与痴呆风险(HR=1.81)、神经系统死亡(HR=1.90)显著相关;
-
心脏年龄差与高血压、心律失常、循环系统疾病相关;
-
肾脏年龄差与肾衰竭相关;
-
胰腺与糖尿病、眼睛与青光眼相关。
-
-
多器官平均年龄差可预测多种疾病及全因死亡,预测性能优于单一蛋白衰老时钟。
4. 影像特征与生物标志物的器官特异性
-
各器官年龄预测中贡献最大的影像特征具有生物学意义,如大脑灰质体积、白质ICVF、视网膜厚度等。
-
血液标志物(如肌酐、胱抑素C)与相应器官年龄差显著相关,体现器官特异性。
-
蛋白质组分析发现966个共享蛋白和507个器官特异性蛋白,如GDF15与脑衰老、PLA2G1B与胰腺衰老相关。
5. 可调节因素与药物靶点
-
生活方式、认知功能、心理社会因素等与器官衰老密切相关,如看电视时间长、吸烟、饮酒等加速多器官衰老;体力活动、谷物摄入等延缓衰老。
-
通过孟德尔随机化识别出14个潜在药物靶点,如TIE1与脑衰老、UMOD与肾脏衰老,部分已在临床研究中被探索。
摘要
器官特定的衰老时钟在反映器官健康方面具有巨大潜力。体内成像本质上是器官特异性的,能够更客观地描述结构和功能特征。 然而,目前尚无系统性评估基于影像的老化时钟。我们利用了来自11,000名健康参与者的1,777个影像衍生表型(IDP),并评估了七个器官的特定器官生物年龄。器官特异性年龄差距主要与相关器官相关的疾病和死亡率相关。器官特定生物年龄贡献最大的IDP成为预测突发疾病的生物标志物,痴呆症曲线下面积(AUC)大于0.8(AUC=0.82)。后续蛋白质组分析显示,不同器官衰老有966个共享分子特征,器官特异性507个特征。最后,我们确定了关键的可调节因子和14个针对器官特异性衰老的药物靶点。基于影像的衰老时钟在宏观和微观尺度上展现了器官特异性,有助于个性化干预和治疗器官衰老。
引言
人类衰老,通常被称为生物年龄,是一个异质性过程,不仅因个体而异,也因不同器官而异。通过比较生物学年龄与真实年龄的差值(即年龄差距),可以洞察特定器官相对于正常同龄人是否表现出加速或延迟衰老2,3。阐明此类器官衰老模式有助于了解未来器官特异性疾病的风险,并促进潜在的早期干预以延缓衰老过程2。 虽然有相当多研究聚焦于全身衰老的测量,但很少有研究考虑到不同器官间的异质性。近年来,器官特异性的生物年龄是基于对预定器官标记的经验知识4或利用体外组织进行的器官富集分子开发的5,6。通过利用更客观的器官标志物,这些框架可以进一步完善。具体来说,体内成像测量具有器官特异性,可以更客观地界定结构和功能特征。特别是基于磁共振成像(MRI)的测量技术越来越多地用于捕捉脑部衰老7-9,这些技术在识别高风险神经退行性疾病个体和监测疾病进展方面具有临床潜力8,10。然而,其他器官缺乏基于影像的衰老时钟。我们预计,利用影像衍生表型(IDP)进行年龄建模,能够增强器官特异性并强化其临床相关性。 在这种情况下,许多重要问题待解决,以全面探讨器官特异性衰老时钟在大规模纵向队列中的适用性。 不同器官的衰老时钟之间有什么关系?器官特异的衰老时钟是否对相关器官的疾病和死亡率贡献更大?基于影像的器官衰老时钟是否也会与外周器官特异性分子表现出关联?不同器官衰老时钟有哪些潜在可调性因素和药物靶点?
为解答上述问题,本研究利用了英国生物样本库(UKB)中11,000名健康个体通过MRI、光学相干断层扫描(OCT)和双能量X射线吸收术(DXA)获得的1,777名IDP。通过机器学习建立了七个针对大脑、心脏、肝脏、肾脏、胰腺、眼睛和体成分的器官特异性衰老时钟。本研究旨在(1)量化多个器官年龄差距之间的相互关系;(2)评估器官年龄差距是否与48种突发疾病和5种死亡相关并预测;(3)识别相关的血浆生物标志物(n=313,生物化学、血细胞计数和代谢标志物)和蛋白质(n=2,920);(4)发现可用于干预和治疗器官特异性衰老的可调节因子和药物靶点。本研究强调,基于影像的器官衰老时钟为识别加速衰老个体、告知未来健康风险及促进长期健康结果提供了关键视角。
结果
研究人群
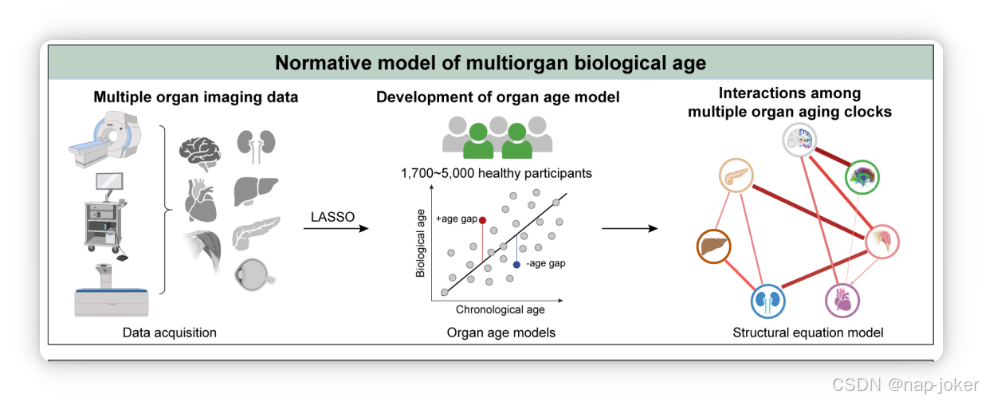
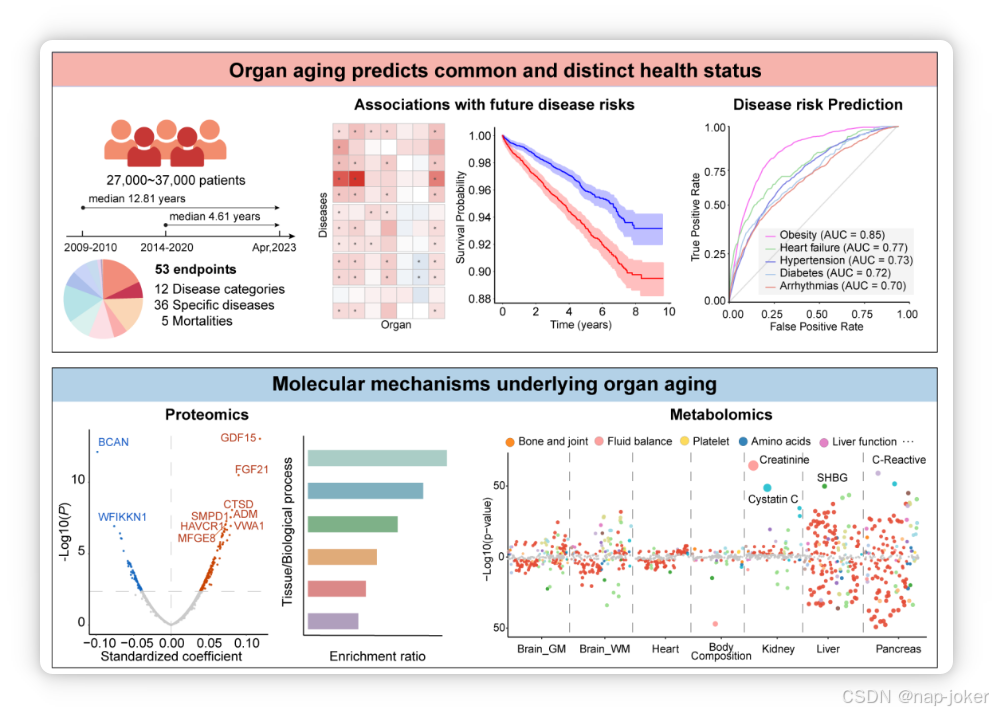
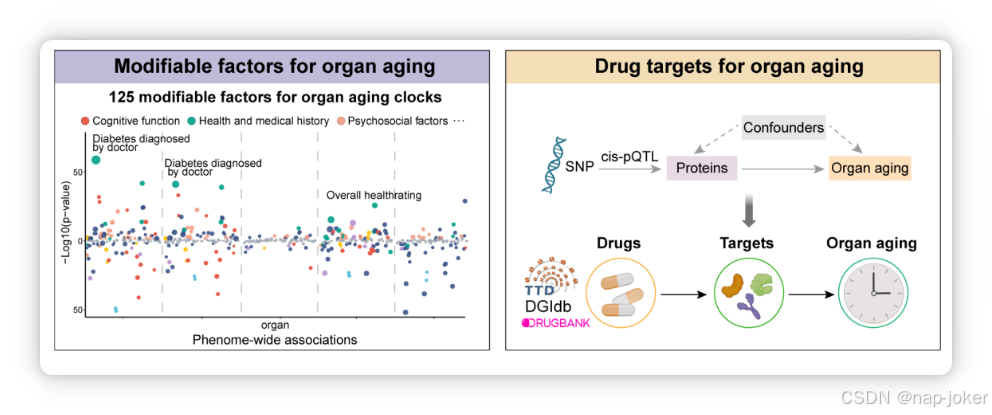
图1 研究设计概述。(a)基于影像衍生表型构建了七个不同器官的生物年龄预测模型,并对器官间年龄差的关系进行了通路分析。(b)考察器官特异性生物衰老是否与主要针对相应器官的疾病未来风险相关并预测相关。(c)识别与器官衰老相关的蛋白质和血液生物标志物是否表现出器官特异性模式。(d) PheWAS分析调查了器官衰老是否与器官特异性可调节因素相关。(e)识别相应器官衰老的药物靶点。图片是用 BioRender.com 创作的。
本研究包含五项聚焦基于影像的生物年龄的研究内容,如图1研究设计流程图所示。基于影像的衰老时钟最初基于1,777名IDP构建(补充表1),共计11,000名健康参与者,中位年龄为61.0岁(四分位数范围,54.0-67.0),其中51.9%(n=5,712)为女性,98.0%(n=10,781)为白人血统。具体地,脑灰质(n=5,190)、脑白质(n=4,943)、心脏(n=2,818)、体成分(n=1,739)、肾脏(n=4,379)、肝脏(n=3,361)、胰腺(n=3,595)和眼睛(n=5,397)等健康参与者数量略有不同。有关研究人群的详细信息可见方法部分和补充表2。
通过影像学特征描述的器官衰老
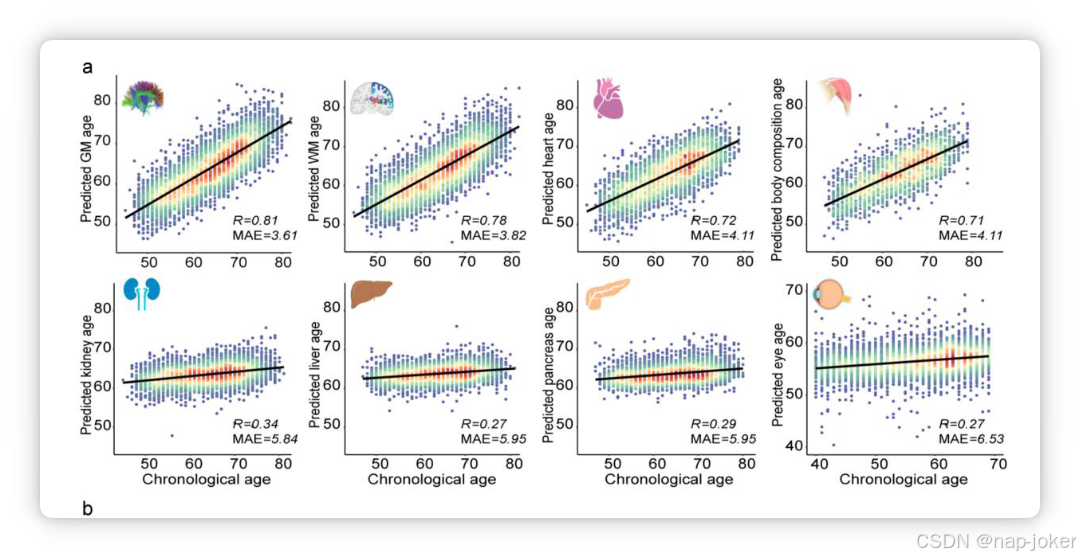
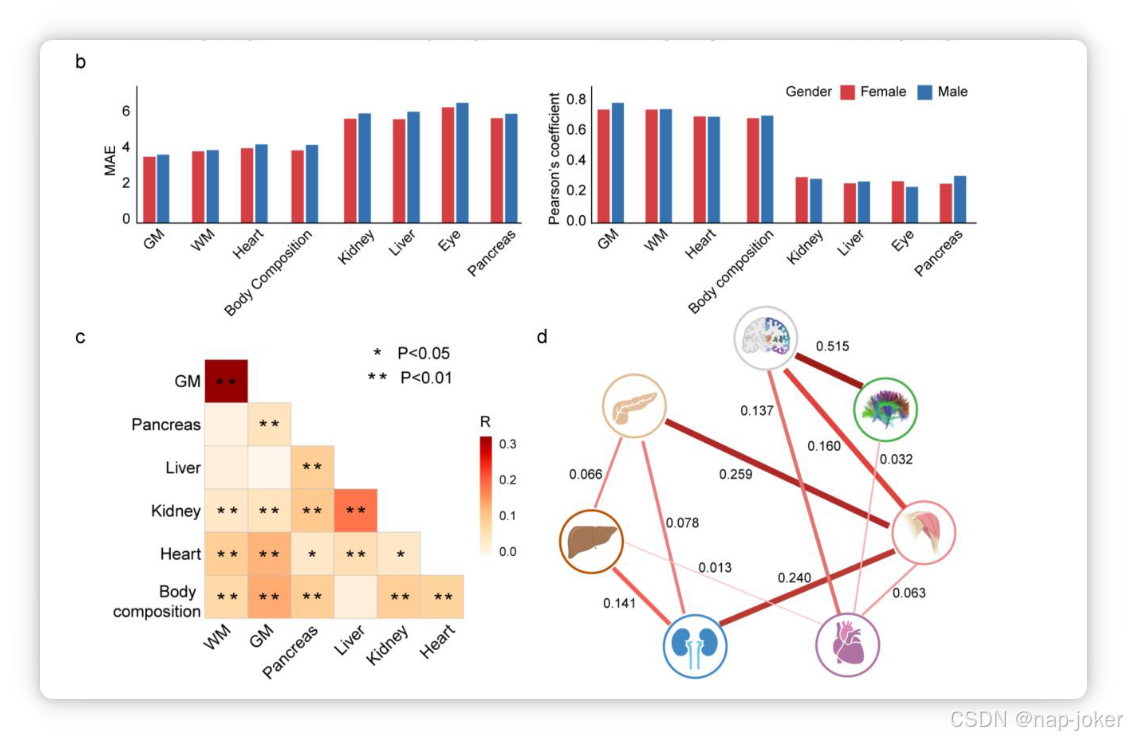
图2 多器官衰老模型的性能。(a)散点图展示了八个不同器官的时间年龄与预测年龄之间的关联。黑色实线表示最合身的型号。选用皮尔逊系数(R)和均方误差(MAE)来衡量器官年龄预测模型的性能。(b) 与A相似,但按性别分层,以考察器官年龄预测模型的潜在性别差异。 不同性别以不同颜色展示。(c) 器官年龄差被定义为差异介于预测年龄和按时间年龄之间。皮尔逊对不同器官年龄差关联系数显示,颜色越深代表关系较高,* < 0.05, ** < 0.01。 (d) 多器官衰老网络描述了器官年龄差距与器官之间的统计关联。SEM在Bonferroni校正P <阈值(0.05/11对)时推断出显著关联,粗暗线代表更强影响。
利用嵌套交叉验证框架,LASSO回归估算了每个器官的生物年龄,其性能评估在保留测试数据中。训练数据与测试数据表现相当,显示无显著过拟合。不同器官的年代预测准确度不一(见图2a)。具体来说,脑灰质(GM;R=0.81,MAE=3.61),脑白质(WM;R=0.78,MAE=3.82)、心脏(R=0.72,MAE=4.11)和体成分(R=0.71,MAE=4.11)。与此同时,在肾脏(R=0.34,MAE=5.84)、肝脏(R=0.27,MAE=5.95)、胰腺(R=0.29,MAE=5.95)和眼球(R=0.27,MAE=6.53)的准确性相对较低。 不同性别的预测准确率相当(图2b)。训练数据与测试数据表现相当,显示无显著过拟合现象(补充表3)。在敏感性分析中,我们发现模型在不同祖先间具有强的普遍性,但在不同年龄段的泛化性较弱(补充表4和表5)。这意味着仅在子样本上训练器官特异性生物年龄模型可能会引入偏差。这些模型基于成年中晚期和白人血统,可能无法完全捕捉早期生活变化,可能导致年龄差距和疾病风险估计不够准确。未来的研究将受益于在祖先、人口统计和临床特征更为多样化的队列中外部验证这些器官特异性衰老时钟。 通过SEM估算不同器官年龄差之间的相互关系(见图2c和2d)。具体来说,心脏和身体组成与其他器官之间表现出最广泛的相互关系。体成分年龄增加1年,胰腺年龄增加0.259年,肾脏年龄增加0.240年,心率增加0.063年。脑年龄方面,GM年龄增加1年,白细胞年龄增加0.515年,心脏年龄增加0.137年,体成分增加0.160年。在剔除年龄、性别和影像部位后,这些关联模式依然保持一致(补充图1)。
**在所有参与年龄建模的IDP中,与灰质体积相关的IDP是脑灰质生物年龄变化最重要的贡献者。对于大脑白质,白质束的ICVF对生物年龄预测贡献最大。**在眼睛中,ISOS-RPE层的厚度是生物年龄的关键贡献者,中央和内侧分区则观察到相反的贡献。升主动脉和降主动脉的动态区域对心脏年龄差影响最大。在肝脏和胰腺中,体积对年龄差距负面贡献,而脂肪分数和铁水平则为正向贡献。肾脏的实质体积与年龄差呈负相关(见图3及补充图2)。
器官衰老预测疾病和死亡的风险
采用Cox比例风险模型,研究了器官特定年龄差距与12大类疾病(40种特定疾病)及所有致病死亡率(4种特定原因死亡率)风险之间的关联,详见补充表6。一般来说,年龄差距越大,疾病或死亡的风险越高,风险比大于1(见图4a,补充图3和补充表7)。由于器官特异性年龄差在生存分析前已转换为z-score,即标准差=1,报告的心率已为年龄差的心率对应标准差。换句话说,z变换后的年龄差距增加1单位,正好对应于原始年龄差距的1-SD增加。器官特异性年龄差距与主要针对该器官的疾病密切相关(图4b)。脑转基因患者的年龄差与痴呆风险的关联最强(HR=1.81,标准差=5.46,95% CI=[1.69, 1.93],PFDR=1.62×10-66,ΔC指数=0.06,P=3.26×10-5)及神经系统导致的死亡(HR=1.90,标准差=5.46,95% CI=[1.62, 2.23],PFDR=4.99×10-13,ΔC指数=0.08,P=5.40×10-3)。脑白细胞疾病的年龄差与脑血管疾病风险相关最为显著(HR=1.46,标准差=6.67,95% CI=[1.33, 1.60],PFDR=4.99×10-13,ΔC指数=0.02,P=4.60×10-3),痴呆(HR=1.99,标准差=6.67,95% CI=[1.67, 2.38],PFDR= 1.08×10-12,Δ C指数=0.03,P= 2.54×10-3)以及精神和行为障碍(HR=1.25,标准差=6.12,95% CI=[1.17, 1.34],PFDR=3.22×10-9,ΔC指数=0.01,P=9.75×10-3)。换句话说,脑转基因年龄差距增加6.67年(即1标准差)的参与者,发生痴呆的风险几乎是其的两倍,脑血管疾病发生风险则高出46%。心脏年龄差与心脏相关疾病风险的关联最为显著,包括高血压(HR=1.31,标准差=7.11,95% CI=[1.22, 1.40],PFDR=4.99×10-13,ΔC指数=0.01,P=6.17×10-4),循环系统疾病(HR=1.21,SD=7.03,95% CI=[1.15, 1.28],PFDR=6.51×10-11,ΔC指数=0.01,P=4.24×10-3)和心律失常(HR=1.22, SD=7.17,95% CI=[1.13, 1.32],PFDR=9.22×10-6,ΔC指数=0.004,P=0.10)。肾脏年龄差与肾衰竭的关联最为显著(HR=1.18,标准差=21.19,95% CI=[1.13, 1.32],PFDR=1.24×10-5,ΔC指数=0.004,P=0.02)。此外,胰腺和眼部的年龄差与胰腺特异性疾病(如糖尿病)的风险密切相关(HR=1.20,标准差=23.65,95% CI=[1.08, 1.34],PFDR=0.00435,ΔC指数=0.009,P=0.08),以及眼部特异性疾病(如青光眼,HR=1.17,SD=27.23,95% CI=[1.10, 1.25],PFDR=3.11×10-5,ΔCindex=0.006,P=0.02), 分别。 与此同时,器官特异性的年龄差距也导致了非器官特有的疾病(见图4a及补充表7)。除脑部特异性疾病外,脑部年龄差也与循环系统疾病风险密切相关(HR=1.14,标准差=5.33,95% CI=[1.09, 1.19],PFDR=2.03×10-8,ΔC指数=0.004,P=3.58×10-3)。体成分年龄差不仅与骨关节炎相关(HR=1.13,标准差=6.77,95% CI=[1.05, 1.23],PFDR=0.01,ΔC指数=0.003,P=0.21),还与周围动脉疾病风险密切相关(HR=1.32,标准差=6.81,95% CI=[1.15, 1.53],PFDR=8.45×10-4,ΔC指数=0.01,P=0.11)、精神和行为障碍(HR=1.16, 标准差=6.74,95% CI=[1.05, 1.28],PFDR=0.02,ΔCindex=0.006,P=0.21)。此外,七个器官的平均年龄差距作为整体健康状况的指标,与多种结局类别的疾病风险密切相关(见图4c),如痴呆(HR=1.62,95% CI=[1.49, 1.76],PFDR=1.61×10-28,Δ C指数=0.03,P= 1.09×10-3)、肾功能衰竭(HR=1.25,95% CI=[1.19, 1.32],PFDR=7.81×10-16,ΔC指数=0.008,P=7.43×10-4),以及全因死亡率(HR=1.23,95%)CI=[1.16, 1.31], PFDR=1.15×10-10, ΔC-index=0.009, P=5.82×10-4)。在两项敏感性分析中,去除了生存分析前的年龄、性别和扫描部位的影响(补充表8),并将器官特异性年龄差距分组为四分位数(补充图4和补充表9),年龄差与疾病关联的方向和效应大小基本保持不变。此外,在明确区分确认性与探索性结果的敏感性分析中,我们发现原始结果中32个显著关联(PFDR<0.05)中有24个在确认分析中存活,181个显著关联中有134个(PFDR<0.05)仍为显著,表明多重检测控制更为严格(补充表10和表11)。通过比较高精度和低精度衰老钟的心率估计,我们发现低精度衰老钟在突发疾病(T = -9.11, P = 5.16×10-18)中表现出较低的疾病风险(HR),而高精度衰老钟可能源于目前这些器官可用的影像特征稀少且有限。 预测分析评估了器官特异性生物年龄(BA)是否能预测疾病和死亡发生的发生,超出了年龄(CA)的影响。我们建立了LightGBM预测模型,IDP对生物器官年龄贡献最大,并将这些模型与仅包含年龄和性别的基线模型进行比较。我们观察到,通过纳入除眼睛外所有器官的信息,预测模型在多种疾病(补充图5和补充表12)中表现优于基线模型,包括肥胖(AUCBA=0.78,AUCCA=0.54)、痴呆(AUCBA=0.80,AUCCA=0.73)、心力衰竭(AUCBA=0.75,AUCCA=0.72)、糖尿病(AUCBA=0.71,AUCCA=0.59)以及全因死亡率(AUCBA=0.71, AUCCA=0.70)。此外,对于许多器官特异性疾病和死亡率,包含器官特异性生物年龄信息的预测模型也表现出优于基线模型的表现(见图4d,补充图5和补充表12)。具体来说,基于基因年龄的模型优于痴呆基线模型(AUCBA=0.82,AUCCA=0.71),纳入心率的模型超过了心力衰竭基线模型(AUCBA=0.78,AUCCA=0.71)和高血压模型(AUCBA=0.74,AUCCA=0.64),基于体成分年龄的模型优于肥胖基线模型(AUCBA=0.86,AUCCA=0.52)。我们还进行了敏感性分析,将70%的数据作为训练数据,剩余30%的数据作为保留测试集。观察到预测模式与10倍交叉验证一致相符(补充图5和表13)
器官衰老与血液生物标志物的关联
在考虑血液与器官之间频繁物质交换的过程中,我们进一步识别出七个器官年龄差与299项血液生物化学、血细胞计数和代谢标志物之间的1,198项显著关联,这些参与者具有可用器官特异性数据(脑GM,N = 25,241;脑WM,N = 23,617;心脏,N = 14,112;肾脏,N = 20,218;体成分,N = 8,975;肝脏, N = 14,420;胰腺,N = 15,892;补充表14、15和16)。总体来看,血液生物标志物与肝脏年龄差之间的显著关联最多(247),其次是胰腺(245)、脑GM(198)、脑WM(196)、肾(128)、心脏(127)、体成分(57)(PFDR < 0.05)。与此同时,299个血液生物标志物中有290个与至少两个器官相关,且这些关联在七个器官中以脂蛋白、脂质和脂肪酸为主导。特别是,白细胞计数是显示最多显著正相关总数(六个器官)的生物标志物,而欧米伽-3脂肪酸与总脂肪酸的比例,IGF-1是显示最多显著负相关数的生物标志物(六个器官)。 在相关的血液生物标志物中,若干生物标志物表现出器官特异性关联(图5a):肌酐(肌肉产生的废物,肾脏清除)是与体组成年龄差关联最显著的负相关(标准化β=-0.19,PFDR= 1.90×10-45),与肾脏年龄差呈最显著的正相关(标准化β=0.31,PFDR=4.76×10-292)。半抑素C作为肾功能评估的敏感标志物12,也与肾脏年龄差呈强正相关(标准化β=0.25,PFDR=1.59×10-244)。极大极低密度脂蛋白(VLDL)中甘油三酯与总脂脂比例较高,反映了甘油三酯在VLDL中占主导地位,并与心血管疾病风险相关(例如动脉粥样硬化)13,14,显示与心脏年龄差呈正相关(标准化β=0.05,PFDR=6.49×10-8)。
发现器官年龄差与血液生物标志物之间存在一致关系,扫描部位作为额外协变量(补充表17)。通过比较高准确率和低精度衰老钟的绝对贝塔估计值,我们发现低精度衰老钟在与代谢物关联方面表现出更强的绝对效应量(β)(T = 3.60,P = 3.60×10-63)。
器官衰老与蛋白质组学标志物的关联
通过使用具有现有蛋白质组和器官特异性数据的参与者,描述了2,920个血浆蛋白与七个器官年龄差之间的关联(脑GM,N=5,525;脑WM,N=5,219;心脏,N=2,878;肾脏,N=4,417; 体型组成,N = 1,673;肝脏,N = 3,392;胰腺,N=3,608;补充表18)。 总体而言,七个器官和1174个蛋白质之间发现了2230个显著关联。 具体来说,胰腺(627个)和肾脏(620个)关联最多,其次是肝脏(367)、基因大胆(249)、白杨白细胞(222)。与此同时,1174种蛋白质中有676种被至少两个器官鉴定。CXCL17、FGF21和LAMP3为总共显著阳性关联最多的蛋白质(六个器官),CA14、CD93和GSN为总共显著负相关数最多的蛋白质(四个器官)。 然而,我们发现表现出最显著关联的蛋白质存在明显的异质性(图5b及补充表19)。具体来说,脑部中BCAN和GDF15与GM和WM系统的年龄差呈出最显著的正负相关。PLA2G1B和CELA3A由胰腺细胞特异分泌,是与胰腺年龄差负相关最显著的蛋白质。ADAMTS15在心脏早期发育期间表达,是与心脏年龄差负相关最显著的蛋白质之一。发现了一致的关系在器官年龄差和蛋白质浓度,扫描位点作为额外协变量(补充表20)。
在组织富集分析中,大多数器官中,负相关蛋白在对应器官过度表达的基因中显著富集(图5c及补充表21)。特别是,蛋白质与GM呈负相关(PFDR=3.26×10-6),白细胞蛋白(WM)(PFDR=3.30×10-6)则富集于脑组织中过度表达的基因。这种器官特异性模式也在体成分(PFDR=0.02)、肝脏(PFDR=2.16×10-21)和胰腺(PFDR=7.41×10-13)中观察到。 同样,在 GO 生物过程富集中,表现出负相关性的蛋白质在与相应器官相关的生物过程中显著富集(补充图6和补充表22)。特别是,我们观察到肾衰老中轴突和突触的富集,含酚化合物代谢过程(PFDR=0.006)及前列腺素-E合酶活性调控(PFDR=0.006),肝脏中血液凝固时纤维蛋白形成(PFDR=0.009),肝脏中血液凝固内因子(PFDR=0.009),胰腺消化(PFDR=0.012)。相反,对于大多数器官,具有阳性关联的蛋白质在免疫相关过程中显著富集,如对革兰氏阴性菌的防御反应和炎症反应。通过比较高准确率和低精度老化时钟的绝对β估计值,我们发现低精度老化钟在与血浆蛋白质组水平相关时显示出更强的绝对效应量(β值)(T = 27.01,P = 5.95×10-156)。
器官衰老的可调节因素
在PheWAS分析中,我们研究了器官特异性年龄差距与143个可调节因素之间的关联,合格参与者人数范围为2416至41871人。总体来看,基因转基因(n=91)、白细胞(n=67)、心脏(n=23)、体成分(n=63)、肾脏(n=50)、肝脏(n=85)和胰腺(n=86)等显著关联数量存在明显多样性。
在所有显著关联中,6个早年生活和家族史因素、59个生活方式和环境因素、14个认知功能、11个健康与医疗史、2个身体指标、27个心理社会因素和6个社会人口学因素与器官年龄差相关(补充表23)。 在所有检查的因素中,143个因素中有114个导致了多个器官的年龄差距(见图6a)。具体来说,更长时间看电视、通常随餐饮酒、吸烟年数更长以及整体健康评分较差,都与几乎所有器官的加速衰老有关;而更多麦片摄入、更强的握力以及更多中等强度的体育活动天数/周数(10+分钟)则是大多数器官衰老减缓的因素。 同时,也观察到年龄差距的器官特异性关联模式。特别是与其他因素相比,认知功能与大脑系统的年龄差距相关性更大。同样,体育活动的天数/周数明显与体成分和胰腺的年龄差相关。此外,在包含眼部的分析中(补充图7和补充表24),关联最显著的因素是母亲出生时的吸烟(标准化β=0.15,PFDR= 2.86×10-36)。 与此同时,观看电视时间更长也是与眼睛衰老关联最显著的因素之一(标准化β=0.05,PFDR=1.85×10-7)。
器官衰老的优先药物靶点
我们进一步采用顺式磁共振分析,定位具有药物干预器官衰老调节潜力的药物靶点。对于血浆蛋白与器官特异性衰老之间的15项顺式-磁共振关系,以及脑脊液蛋白与器官特异性衰老之间的2项顺式-磁共振关系,大多数都得到了至少三种磁共振方法的有力支持。我们未观察到显著的顺式-磁共振关系的水平和方向多效性(均为PFDR>0.05)(补充表25)。共有14种血浆蛋白被发现与器官衰老有显著因果关系(FDR校正P < 0.05,补充表25)。其中,CHRDL2、ITIH4、LRRC37A2、SEMA3F和TIE1蛋白与脑衰老有因果关系,TIE1蛋白通过脑脊液进一步证实。对人脑微血管的转录组分析显示,与内皮衰老和粘连相关的基因,包括TIE1,在tau病理升高时上调,表明TIE1表达与年龄相关神经退行性疾病脑血管变化之间存在关联15。ABO、CLPS和GRP蛋白与胰腺衰老有因果关系,而CLPS是胰脂肪酶在高效膳食脂质水解过程中所需的辅因子。GRP及其受体在正常人类胰腺组织中内源性表达,表明其在局部胰腺信号中起作用16。 除了生理功能外,循环中的GRP水平还被报道与胰腺炎后葡萄糖代谢改变和促炎细胞因子增加有关。这些特征------代谢失调、慢性炎症信号传递以及内分泌-副分泌通信障碍------是与年龄相关的胰腺功能衰退的典型特征17。ERI1、MSRA和SPINK8与眼睛衰老有因果关系,其中MSRA是一种能保护视网膜和晶状体细胞免受氧化应激的酶18。LAMB1和UMOD与肾脏衰老有因果关系,UMOD编码正常尿液中最丰富的蛋白------尿调节蛋白19。实验模型中,UMOD启动子中常见的非编码变异与慢性肾病和年龄依赖性肾病病变的易感性增加相关,支持UMOD在肾衰老相关病理中作用的遗传基础20。肾脏衰老和疾病的蛋白质组学分析显示,基底膜成分的变化,包括层联锁链的变化(如LAMB1)的变化,是衰老和进行性肾病的共同特征21。六个蛋白质------ADH4、LAMB1、ABO、GRP、UMOD 和 TIE1------均为获批药物靶点或正在临床试验中,详见 DrugBank、治疗靶点数据库和药物-基因相互作用数据库(图6b)。值得注意的是,磁共振识别的蛋白与器官衰老相关的候选药物靶点。这些发现具有假设性质,需要功能性随访,包括体外/体内实验、组织特异性敲低/过度表达研究,理想情况下还包括干预性试验以验证治疗潜力。
讨论
我们的研究是首次全面分析基于影像的七个器官衰老时钟,利用了来自英国11,000名健康个体的1,777个器官特异性IDP数据。本研究结果显示,基于影像的生物器官衰老表现出独特的器官特异性模式。具体来说,发现了器官间的选择性相互关系,其中心脏和体组成的相互关系比其他器官更为广泛。器官特异性生物衰老可影响并预测突发疾病和死亡率,主要影响相应器官,痴呆和肥胖的AUCs>0.8。同时,识别出966个共享分子特征和507个器官特异性分子特征,用于不同器官的生物衰老。在多个器官中发现了不同的可调节因素,其中认知功能与大脑更为密切相关,身体活动则更多地与身体组成相关。此外,还识别出14个可用于器官特异性衰老干预的潜在药物靶点。总体而言,我们新型基于影像的衰老时钟为推进人类衰老的理解提供了替代途径,并激发针对性干预措施以降低器官特异性疾病风险。 与现有依赖实证知识或外部体外数据来估算器官衰老的血浆蛋白组4,5,22、代谢2,23、表观遗传24和面部25老化时钟不同,我们的基于影像的衰老时钟展示了更高的器官特异性和减少对人工选择依赖的优势。与此同时,与体外细胞老化估计为单细胞分辨率26相比,体内成像在特异性和可行性之间提供了折中,使得基于影像的建模能够实现更客观、具体且实用的估计器官年龄。此外,虽然我们在构建年龄预测模型时未引入器官富集蛋白的信息,但我们发现与影像定义的器官年龄相关的蛋白质和血液生物标志物表现出器官特异性模式,这凸显了我们的模型不仅在宏观尺度(通过影像显示)具有器官特异性,在微观尺度上也具有特异性。这种双层次特异性强调了基于影像的方法在捕捉器官特异性生物衰老过程方面的稳健性。 早期的研究要么在推断关联方向性时引入偏倚,要么单独描述了身体系统和大脑系统内多器官衰老网络结构27。通过利用同一次影像检查中收集的大脑及其他器官的UKB影像数据,本研究提供了关于大脑与其他器官衰老过程如何相互影响的互补视角。特别是,我们发现了大脑衰老与心脏和身体组成之间存在选择性关联。 脑与心脏年龄差距之间的统计关联与假设的脑心连接是一致的,因为大脑通过自主神经系统的交感神经和副交感神经分支调节心脏活动28,且精神疾病(如创伤后应激障碍)与冠心病风险(HR = 1.61)增加相关29。本研究结果与以往研究共同推动了统计推断多器官衰老网络的新兴格局。值得注意的是,与提供因果洞见的磁共振分析不同,SEM分析通过描述器官特异性年龄差距间的关联模式,这些模式与某些网络结构相兼容,而非建立因果关系,起到补充和探索的作用。 尽管以往研究暗示了液体性衰老与疾病之间的器官特异性关联模式4,5,但对于器官特定衰老如何促成突发疾病,尚缺乏系统性的评估。与之前的报告相比,我们的发现揭示了大脑和心脏更多器官特异的模式,进一步完善了之前对肾脏与代谢疾病之间与更具体的肾脏与肾功能衰竭联系的关系。此外,我们通过展示器官特异性模式对糖尿病和青光眼风险的预测能力,扩展到了胰腺和眼睛。对于大多数疾病,我们的基于影像的衰老时钟显示出的危险比通常高于之前的单一蛋白质组衰老时钟(所有疾病H<R1.2)在UKB22中。先前确立的器官特异性蛋白质组衰老时钟显示,LonGenity队列5中心力衰竭风险更高(心率:HR=2.37)和死亡率(所有蛋白质:HR=1.54),而UKB-PPP队列6则更高的肾衰竭风险。然而,鉴于队列间潜在的系统性差异,例如, 在比较前,需要考虑发病率、人口统计特征和仔细考虑。 此外,通过估计所有器官的平均年龄差,我们证明了这一简单代理指标能预测影响多个器官的突发疾病风险,并优于单一蛋白质组衰老时钟(所有疾病心率<1.2)22。通过监测这一生物标志物,医疗人员可以早期发现多器官功能障碍的迹象,并实施预防策略以减轻健康整体恶化。更重要的是,我们发现与器官生物年龄相关的IDP信息能够预测疾病和死亡率的发生,超出年龄和性别的统计,进一步凸显了基于影像的生物年龄在揭示衰老异常中的潜力。与现有的简单痴呆风险预测模型(CAIDE30、DRS31和ANU-ADRI32)相比,后者受限于可能有偏的自我报告和临床变量,我们的基于影像的风险预测模型不仅实现了更优异的预测性能,还在客观性和生物学相关性方面表现更为出色,成为早期痴呆风险评估的更稳健工具。 如前所述,肝脏33、肾脏34和胰腺35是调节新陈代谢的重要器官。因此,我们发现这三个器官------肝脏、肾脏和胰腺------与血液生物标志物和血浆蛋白的显著关联最多。 此外,我们证明了蛋白质和血液生物标志物最显著与器官年龄的关联显示出明显的器官特有模式。其中,血浆GDF1536------与加速脑部衰老有最强正相关性的蛋白质------成为血管性痴呆发作最强的预测因子37。肌酐和胱抑素C水平升高与肾脏加速衰老相关,这两者都是临床上最广泛使用的肾功能测量指标38。与此同时,对于大多数器官来说,与免疫反应相关的蛋白质表达升高与加速器官衰老有关,这也重新证明了因炎症水平升高而导致的低度和慢性损伤是衰老的标志性特征39,40。 总体而言,这些发现从微观视角阐明了基于影像年龄的器官特异性特征。对这些器官衰老相关生物标志物的进一步评估,有望激发新的目标,以有效预防和干预衰老。 尽管某些器官(如肾脏、肝脏、胰腺)的衰老时钟预测效果适中,但仍可能为器官特异性衰老过程提供宝贵见解。这一点得到了以下支持:(1)尽管这些器官在预测年龄方面表现较低,但其衰老对器官特异性疾病的风险比高于大多数其他疾病,表明其在宏观尺度上具有器官特异性。例如,胰腺衰老表现出更强的糖尿病风险,青光眼的衰老显示出更高的眼部风险,而肾脏衰老则表现出更高的肾衰竭风险;(2)这些器官的加速衰老与临床验证的器官特异性血浆生物标志物之间存在强烈关联,这些标志物反映了其功能状态,进一步暗示了微观尺度上的器官特异性。例如,肌酐和胱氨酸C与肾脏衰老呈阳相关性最强,SHBG与肝脏衰老关联最强。(3)此前基于原始腹部MRI和深度学习的胰腺衰老时钟实现了更高的性能(MAE=2.94±0.03),但器官特异性低于我们,这与近期倡导平衡模型表现和临床相关性的观点一致10。总体来看,我们发现低精度的衰老时钟确实捕捉了特定器官的特征宏观和微观尺度的模式。虽然这些功能较低的器官未来模型性能提升至关重要,但它们表现出有意义的器官特异性模式,并有助于反映相应器官的衰老和健康状况在解读我们的研究结果时,应考虑几个问题。首先,尽管我们利用了大量多模态影像衍生的表型,但某些器官------尤其是肾脏、肝脏和胰腺------可用的IDP仍然相对粗略,这可能限制了器官特定衰老估计的精确性。其次,研究人群来自英国生物样本库成像队列,主要为4096岁的白人欧洲人。因此,所提出的基于影像的衰老时钟主要捕捉晚年衰老模式,可能无法完全推广到年轻人群。由于现有多模态和多器官数据集有限,目前研究范围内无法进行外部验证,但未来研究将受益于在祖先、人口统计和临床特征更多样化的独立队列中外部验证这些器官特异性衰老时钟,以进一步评估其泛化性和转化潜力。第三,大多数参与者的器官仅拍摄一次,因此衍生的器官特异年龄差距代表的是与正常衰老的横断面偏差,而非个体内的纵向变化,无法直接建模衰老速率或时间动态。最后,虽然我们对广泛的人口统计学、生活方式和社会经济共同变量进行了调整,但残余混杂因素------如共病或用药------仍无法完全排除,观察到的关联应进一步验证。 本研究是首次基于多模态成像对器官特异性衰老时钟的全面评估。本研究建立的基于影像的衰老时钟不仅在宏观和微观尺度上展现出器官特异性,还高度预测影响相关器官的突发疾病,凸显其临床应用潜力。此外,我们识别出器官特异性分子基础和可调节因素,可能激发创新策略以减缓衰老
方法
参与者
英国生物样本库是规模最大的基于人群的生物医学队列之一,涵盖40至96岁的50万多名参与者,遍及英国41,42岁。本研究最初纳入了所有基线视网膜OCT或参与脑MRI、心脏MRI、腹部MRI及全身双能量X射线吸收测量(DXA)影像就诊的患者。根据赫尔辛基宣言,UKB获得了国家信息治理委员会(国家卫生与社会护理信息治理委员会)和国家卫生服务西北研究伦理委员会(参考:11/NW/0382)的批准,并从所有参与者那里获得了书面知情同意。临床试验编号不适用。所有方法的详细描述可见补充信息。
多器官影像表型
基于1777个相关器官的IDP构建了七个器官的时间年龄预测,包括大脑、心脏、体质、肾脏、肝脏、胰腺和眼睛。脑灰质和白质分别进行了评估。仅从英国银行选拔并获取结构性和功能性器官的IDP(补充表1)。 具体来说,针对大脑,利用T1加权MRI量化了1010个与区域灰质体积、皮层平均厚度和表面积相关的IDP。扩散加权MRI产生了443项白质体积和主要白质束微观结构测量。微观结构测量通过扩散张量成像(DTI)拟合和神经突体取向色散与密度成像(NODDI)建模进行了表征43,包括分数各向异性(FA)、平均扩散率(MD)、张量模(MO)、L1、L2、L3、细胞内体积分数(ICVF)、各向同性或游离水体积分数(ISOVF)以及取向分散指数(OD)。对于心脏,一组心血管MRI序列被用于评估106个与心脏和主动脉结构及功能相关的IDP44。此外,腹部多序列MRI被用于生成肝脏、肾脏、胰腺和脂肪组织的体积、脂肪和铁含量测量45,46。同时,通过DXA仪器测量了138名体质内流离者。骨面积、骨矿物质含量、骨密度、瘦体重和脂肪质量的测量数据直接推导。最后,64个眼部IDPs来自视网膜OCT47,该数据提供了视网膜层厚度和子场的信息,以及垂直杯与盘比和盘径。 对于每个器官,仅纳入了所有分析中所有IDP中非缺失值的参与者。换言之,排除了任何与器官相关的IDP缺失数据的参与者,导致符合进一步年龄建模的健康参与者数量略有差异(补充表2)
规范性器官老化模型
在健康参与者中训练了最小绝对缩小和选择算子回归(LASSO)模型,预测参与者的年龄,并以脑GM、脑WM、心脏、体成分、肾脏、肝脏、胰腺和眼睛等影像表型为潜在预测因子(补充表1)。健康状态被定义为在关联的初级护理、住院患者、死亡登记册和自我报告的医疗状况来源中无终生发生记录(类别1712)。对于每个器官,LASSO预测模型均采用嵌套的10折交叉验证构建。内环包括交叉验证,选择最佳超参数λ,而外环通过在包含最优λ的九个折叠上训练模型,并在剩余一个折叠上测试模型,评估模型的泛化性能。该交叉验证过程为每位健康者得出了预测年龄个体。按照该建议,训练数据中也将年龄从预测年龄回归,并将相同的回归模型应用于测试数据48,49。通过计算测试集中预测年龄与时间年龄之间的皮尔逊相关系数(R)和平均绝对误差(MAE)来评估模型性能。 最后,在健康参与者中创建了八个最优的器官特异性生物年龄预测模型,并将这些模型应用于剩余的UKB参与者,以获得每个器官的预测年龄。每个器官的预测年龄(即生物年龄)与实际年龄之间的差异被视为器官特异的年龄差距,从而判断该器官相比健康同龄人是加速还是减缓衰老过程。偏倚调整步骤显著减少了脑GM(未校正斜率:-0.34;修正斜率:-0.04)、脑功能(未校正斜率:-0.36;修正斜率:-0.04)、心脏(未校正斜率:-0.45;修正斜率:-0.02)、体成分(未校正斜率:-0.46;修正斜率:-0.04)、肾脏(未校正斜率:-0.89; 修正斜率:-0.04)、肝脏(未矫正斜率:-0.92;修正斜率:-0.06)、胰腺(未矫正斜率:-0.91;修正斜率:-0.09)和眼睛(未矫正斜率:-0.92;修正斜率:-0.07)。在敏感性分析中,分别训练了健康男性和女性的模型,以考察性别差异在年龄预测中的潜在影响。此外,为了评估模型在不同年龄段和祖先间的普遍适用性,我们将健康参与者分为两个年龄组(≤65岁和>65岁)和两个祖先组(白人和非白人)。对于每个分层,模型在一个子组训练,在另一个子组中评估。
结构方程模型(SEM)
结构方程建模(SEM)被用于评估器官年龄差距与器官之间的关联。由于眼睛的扫描与其他器官不同,扫描电子显微镜仅限于除眼睛外的六个器官。在确定最优模型结构时,Tetrad v7.6.550 中的快速贪婪等价搜索(FGES)启发式算法被用来确定得分最高的因果贝叶斯网络,这在探索性分析中非常有用,用于构建关于横断面数据网络结构的假设。基于所得的网络结构,利用lavaan v0.6.17进行了路径分析,以估算最终网络中边缘关联的强度和显著性。在敏感性分析中,进一步回归了所有器官特异性年龄差距的影像访问年龄、性别和成像部位,并对所得残差进行了搜索算法。由于反复影像访问的可用性有限,SEM分析仅限于横断面关联,无法推断纵向效应或因果通路。 FGES--SEM分析依赖若干假设,包括因果充分性(即无未测量混杂因素)、无反馈环的无环关系,以及有向无环图是否足以表示条件依赖关系。在多器官衰老等复杂生物系统中,由于反馈机制和潜在因素,这些假设不太可能被完全满足。因此,推断出的网络结构和路径系数应被解释为与某些依赖结构兼容的统计关联,而非因果效应的证据,旨在探索性和假设生成。
疾病和死亡风险的预测
从UKB中选出了共13类发病结局(补充表6),包括12类疾病(36种特定疾病)和全因死亡率(4种特定原因死亡)。使用Cox比例风险模型,使用R组件生存率v3.5.5测试了器官特异年龄差距与事件结局之间的关联。对于13个类别的所有发病结局,生存模型包括器官特异性年龄差、生理年龄、性别、教育年限、身体质量指数(BMI)、吸烟和饮酒状况作为预测因子。年龄差距效应的显著性通过FDR校正的P < 0.05在所有范围内确定器官成对和结果。通过器官间的平均年龄差距来证明整体年龄差距与事故风险之间的关联。利用哈雷尔C指数评估模型区分经历事件患者与未经历事件的能力,数值越高表示表现越好。我们进一步计算了将每个器官年龄差距纳入基线模型(包括年龄、性别和既定常规风险因素)时哈雷尔C指数(ΔC指数)的变化,显著性通过1000条自助法进行了分析。通过回归年龄、性别和扫描部位的影响进行敏感性分析,以进行生存分析。为提高结果的可靠性,我们还通过将器官特异性年龄差距按低至高分为四分位,构建了生存模型,并评估了年龄差距对疾病和死亡率风险分层的能力。为了严格,我们进一步进行了敏感性分析,明确区分了确认性结果和探索性结果。具体来说,在确认性分析中,七个器官特异性年龄差与预先指定的器官特异性疾病之间的关联经历了严格的邦费罗尼修正P < 0.05。在探索性分析中,我们通过考虑检验间固有依赖性进行了层级FDR纠正,并在各器官内控制了假发现率。具体来说,针对八个器官,每个器官都基于疾病特异性p值,使用Simes检验计算出综合p值。这八个综合p值随后在5%处进行了罗斯福修正。仅考虑具有显著综合性检测的器官,且在每个重要器官内,在FDR校正P的5%下测试关联性<。最后,我们比较了高精度与低精度老化时钟之间的关联强度。特别是,使用R阈值0.5,我们将器官分为高准确率组和低准确率组。两组的生存率估计值进行了比较。 为了进一步说明器官特异年龄差距的临床意义,我们开发了疾病和死亡率的预测模型。在疾病预测分析中,发病病例定义为在影像学随访中首次确诊的参与者。对于每个疾病对照组定义为在随访期间未发病的参与者。排除影像检查前发生的事件,以确保预测因素与结局之间的时间性清晰区分。该设计确保所有预测模型均使用基线影像衍生指标进行训练和评估,以预测未来疾病风险。 具体来说,结局定义为UKB中终生的疾病发病率和死亡率。 对于每个器官,选择了对生物年龄模型贡献最多的50%的IDP作为预测变量,并采用10折交叉验证框架构建了LightGBM预测模型,以避免潜在的过拟合。为减少潜在高度相关或冗余特征,利用LASSO模型在疾病预测前进行特征选择。此外,在涵盖所有器官的整体预测中,我们利用usdm软件包进一步处理了潜在共线性,仅保留方差膨胀因子小于10的特征。 由此产生的特征被用来构建疾病预测模型。整体模型表现通过平均10个折叠的AUC进行评估。利用同一框架,还进行了包含所有器官预测因子的整体预测模型。通过将既有模型的性能与仅包含年龄和性别的基线模型进行比较,我们评估了包含器官特定生物年龄信息的模型是否比传统年龄更准确地预测疾病和死亡风险。为进一步评估模型的稳健性,我们进行了敏感性分析,将70%的数据作为训练数据,30%的静态数据作为保留测试集。采用了类似10折交叉验证的特征选择。
与蛋白质和血液生物标志物的关联
基线血浆样本采用NovaSeq 6000测序系统处理,Olink Explore 3072用于定量2923种独特蛋白的浓度51,52。三种缺失率达到或更高的蛋白质(GLIPR1、NPM1和PCOLCE)被丢弃。血浆样本还被准备和处理,以量化血液生化、血细胞计数,以及代谢生物标志物53。最后,不同器官中,纳入了530至5,525名含全部2,920种蛋白质的参与者(补充表18)和2,569至25,241名含全部310项血液生物标志物的参与者(补充表14和补充表15)。蛋白质组和代谢物均对生物标志物浓度进行了反级归一化,且去除了年龄和性别的影响。 对于每个器官,采用广义线性模型考察血浆蛋白与器官特异年龄差距之间的关联,包含影像学时的年龄、性别、教育年限、汤森指数、影像学中的吸烟状况、影像中的饮酒状况、族裔以及基线与影像之间的间隔作为协变量。显著性通过FDR修正的P <0.05在所有2,920×7对蛋白质-器官中确定。对于每个器官,通过ToppGene的过代表分析进行了去氧膜生物过程富集。组织富集分析采用FUMA v1.5.2超几何测试,并利用GTEx v8的基因表达进行。进行了以扫描位作为额外协变量的线性模型的敏感性分析。血液生物化学、血球计数和代谢生物标志物也采用了类似的广义线性模型。显著性通过FDR校正的P <0.05确定,涵盖所有310×7对血液生物标志物-器官对。与上述类似,将高准确率和低精度老化时钟与生物标志物相关的β估计值进行了比较。
按现象的关联分析
采用与以往研究类似的UKB可变因子领域54,排除多项表型后,除眼睛外的器官获得了143个共同因子,所有器官均获得了139个共同因子。 在R55中,PHESANT包对PheWAS的关联进行了研究。本研究考察了器官特异性年龄差距与各器官因素之间的关联,年龄和性别为协变量。显著性由FDR校正后的P <0.05在143×7中确定因子-器官对。在敏感性分析中,我们对八个器官的139个可调节因子进行了PheWAS,显著性由FDR校正的P<确定,涵盖139×8因子-器官对。
遗传关联与药物靶点鉴定
为评估我们的发现是否能为器官衰老的潜在药物靶点提供参考,我们采用了TwoSampleMR R软件包,采用两样本顺式磁共振分析,以蛋白质与基于影像的器官特异性衰老之间的因果关系进行分析,统计显著性在FDR校正的P < 0.05阈值下确定。在排除具有蛋白质组数据的受试者后,PLINK2进行了器官特异性衰老的GWAS分析。血浆与脑脊液蛋白定量性状位点关系分别来自英国生物样本库制药蛋白质组学项目(http://ukb-ppp.gwas.eu)52和Cruchaga等56。 我们选择了与P阈值P<5×10-8显著相关的顺式单核苷酸(位于蛋白编码基因转录起始位点1 Mb以内)。 应用了四种MR方法:反方差加权法(IVW)、MR-Egger法、加权中位数法和加权模式,IVW为主要结果报告方法。当只有单一静脉注射可用时,采用了瓦尔德比率。进行了反向磁共振分析以确认该蛋白对器官衰老的因果关系。为解决潜在多效性,我们采用MR-PRESSO的敏感性分析检测水平多效性,MREgger分析方向多效性。为了进一步探索我们发现的治疗潜力,我们利用了基因组重塑药物(GREP)软件和药物-基因相互作用数据库(https://dgidb.org/),分析了核磁共振识别蛋白编码基因在获批药物靶基因中的富集情况。
我们研究中使用的所有软件和方法均公开,并在方法中进行了描述。 本研究的主要分析代码公开于 https://github.com/hitrp/MultiOrganImagingAging