01
文献学习

今天分享的文献是由首都医科大学附属北京友谊医院放射科等团队于2026年1月26日在《Insights into Imaging》(中科院2区,IF=4.5)上发表的研究"CT-based deep learning signatures associated with transcriptomic heterogeneity and combined with nutritional biomarkers improve prediction of 3-year overall survival in esophageal squamous cell carcinoma"即基于CT的深度学习特征结合转录组异质性与营养生物标志物改善食管鳞状细胞癌3年总生存期的预测,该研究开发并验证了一种基于CT图像的深度学习特征(DLS)结合营养生物标志物(如低骨骼肌质量)的预测模型,用于食管鳞状细胞癌(ESCC)患者术后3年总生存期的个体化预测。研究还通过转录组分析揭示了DLS定义的风险组之间的代谢通路差异,增强了模型的生物学可解释性。
创新点:①首次整合 CT深度学习特征与营养生物标志物(LSMM) ,构建多模态预后模型,提升预测性能。②揭示DLS风险分组的转录组代谢异质性 ,关联胆固醇合成、氧化磷酸化等通路,增强生物学可解释性。③采用Crossformer架构 提取多尺度特征,结合注意力图可视化,提高深度学习模型的可解释性。
临床价值:①术前无创预测 3年总生存期,辅助个体化治疗决策,避免依赖术后病理。②联合营养指标(LSMM) 改善风险分层,识别高危营养不良患者,指导预康复干预。③模型C-index达0.753(内部)和0.725(外部),优于传统模型,具备较好的泛化能力。
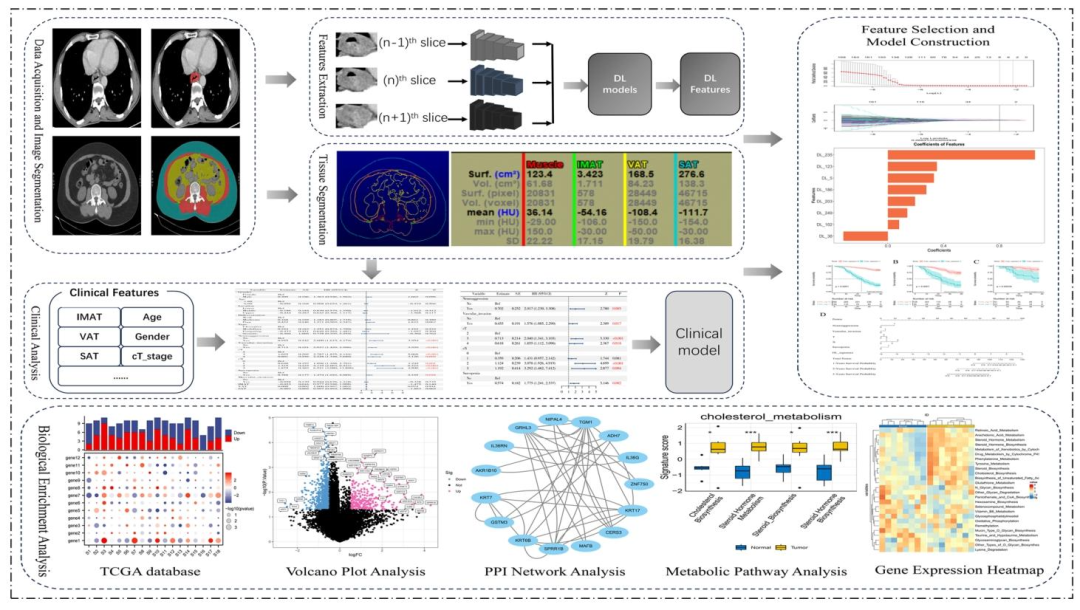
图 2:研究整体工作流程图
数据采集
临床:基线资料、病理、随访、营养指标(L3-SMI评估LSMM)
影像:增强CT静脉期图像
组学:TCGA转录组数据
影像处理与特征提取
手动分割肿瘤3D-ROI
Crossformer架构提取多尺度深度学习特征
PCA降维至256维
模型构建
临床模型:Cox回归筛选独立预后因子
DL模型:LASSO-Cox筛选关键深度学习特征(DLS)
组合模型:DLS+临床/营养因子联合建模
模型验证
评价指标:C-index、KM曲线、校准曲线、DCA、时间依赖ROC
验证队列:内部验证+外部验证
生物学机制解析
TCGA队列:差异基因(DEGs)、PPI网络、代谢通路ssGSEA
建立CT影像表型 ↔转录组代谢异质性的关联
02
研究背景和目的
研究背景
食管癌是全球第六大癌症相关死亡原因,其中食管鳞状细胞癌(ESCC) 是最常见的病理亚型,5年总生存率低于20% ,3年生存率多不足50% ,预后极差。目前,ESCC的预后评估主要依赖术后病理指标如TNM分期、分化程度和脉管侵犯等,但这些指标难以反映患者间的肿瘤生物学异质性 ,导致相同分期的患者生存差异显著。近年来,营养不良和低骨骼肌质量(LSMM) 被证实是ESCC等实体瘤的重要独立预后因素,但多数深度学习(DL)生存模型未整合此类宿主营养状态信息。另一方面,基于CT图像的深度学习特征(DLS)可非侵入性地捕获肿瘤形态与异质性 ,具备预后预测潜力。然而,现有DL模型多局限于影像特征,缺乏与转录组代谢异质性的关联分析,限制了其生物学可解释性和临床推广。因此,亟需构建融合影像、临床与营养指标的多模态模型,并探索其背后的分子机制。
研究目的
本研究旨在开发并验证一种基于CT图像的深度学习特征(DLS)与术前营养生物标志物(尤其是LSMM)相结合的联合模型 ,用于术前预测ESCC患者术后3年总生存期(OS) ,以提升个体化风险分层能力。研究进一步探索DLS所定义的高危与低危组之间的转录组差异 ,特别是代谢相关通路(如胆固醇合成、氧化磷酸化、谷胱甘肽代谢等)的活性变化,揭示影像表型背后的肿瘤代谢重编程异质性 ,增强深度学习模型的可解释性。通过整合影像、临床病理及营养指标,该研究希望弥补现有模型忽略宿主状态的不足 ,提供一种术前即可获取、非侵入性、具备生物学依据的预后评估工具,为ESCC患者的个体化治疗决策和围手术期营养干预提供理论依据。
03
数据和方法
研究数据
总样本量:662例ESCC术后患者(来自三个医疗中心)
训练集:402例
内部验证集:172例
外部验证集:88例
转录组分析:16例来自TCGA数据库的ESCC患者
数据来源:CT影像(增强与非增强)、临床病理资料、TCGA转录组数据
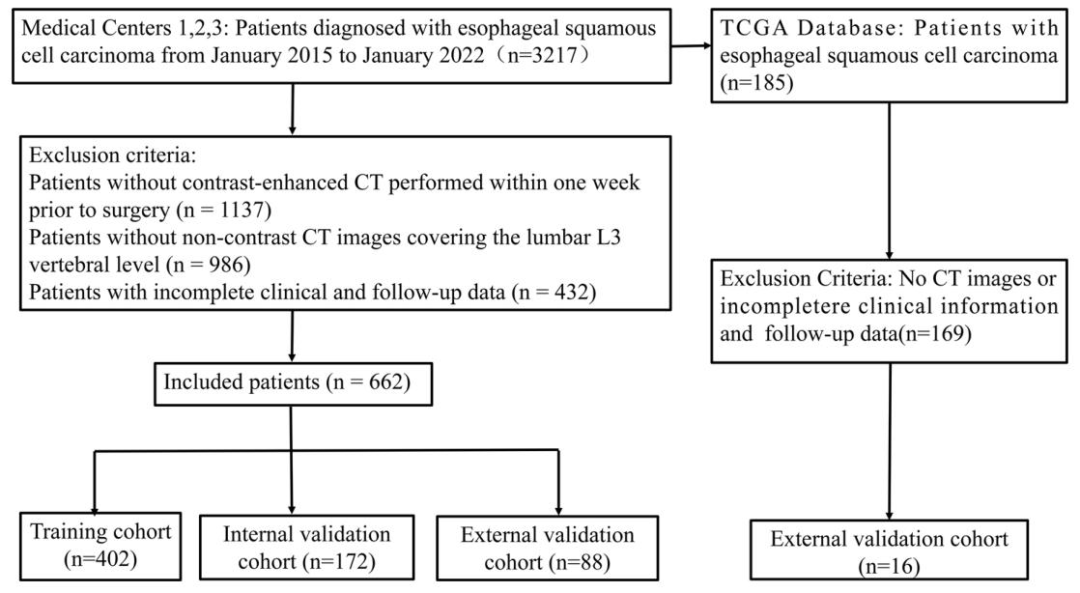
图 1:患者筛选流程图
技术方法
深度学习特征提取:基于Crossformer架构,从CT图像中提取多尺度特征,PCA降维。
营养评估:L3椎体骨骼肌指数(SMI),定义低骨骼肌质量(LSMM)。
建模方法:LASSO-Cox回归筛选特征,构建临床模型、DLS模型和联合模型。
模型评估:C-index、校准曲线、决策曲线分析(DCA)、Kaplan-Meier生存曲线。
转录组分析:差异表达基因(DEGs)、PPI网络、ssGSEA代谢通路分析。
04
实验结果
临床模型:C-index 内部0.687,外部0.645
DLS模型:C-index内部0.743,外部0.692
联合模型:C-index 内部0.753,外部0.725,优于前两者
风险分层:KM曲线显示高风险组与低风险组生存差异显著(p < 0.05)
转录组分析:高风险组在胆固醇合成、氧化磷酸化、谷胱甘肽代谢等通路显著富集,提示代谢重编程
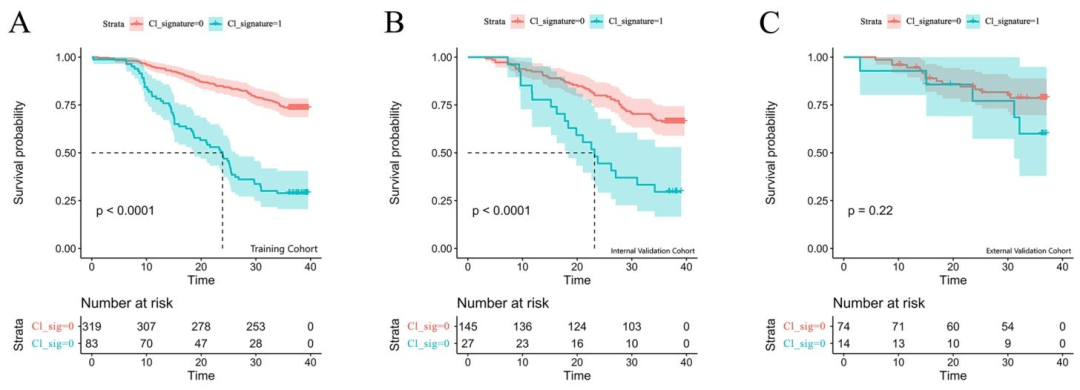
图 3:临床模型的Kaplan--Meier生存曲线
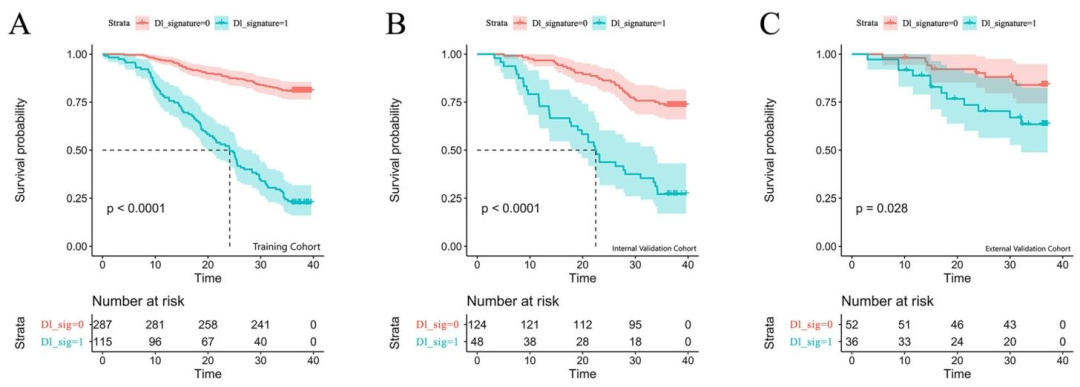
图 4:深度学习模型的Kaplan--Meier生存曲线
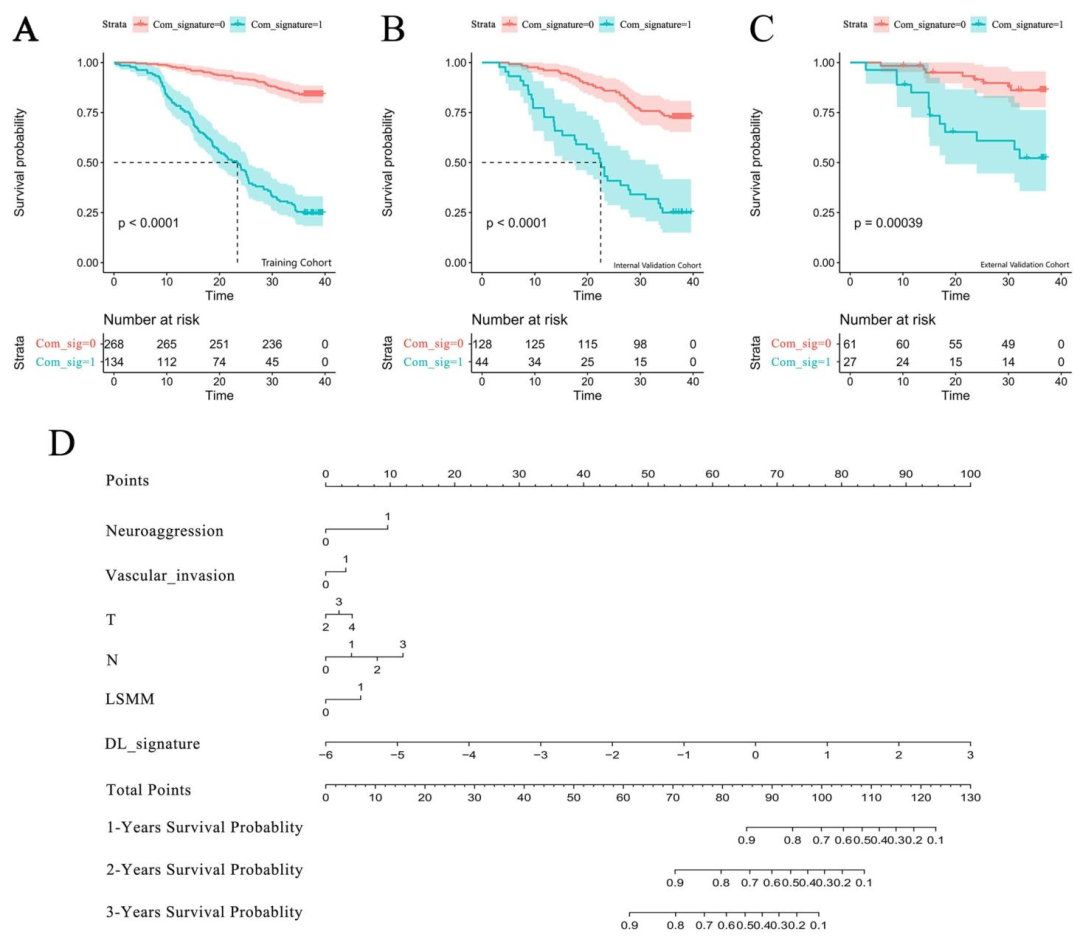
图 5:组合模型生存分析与可视化
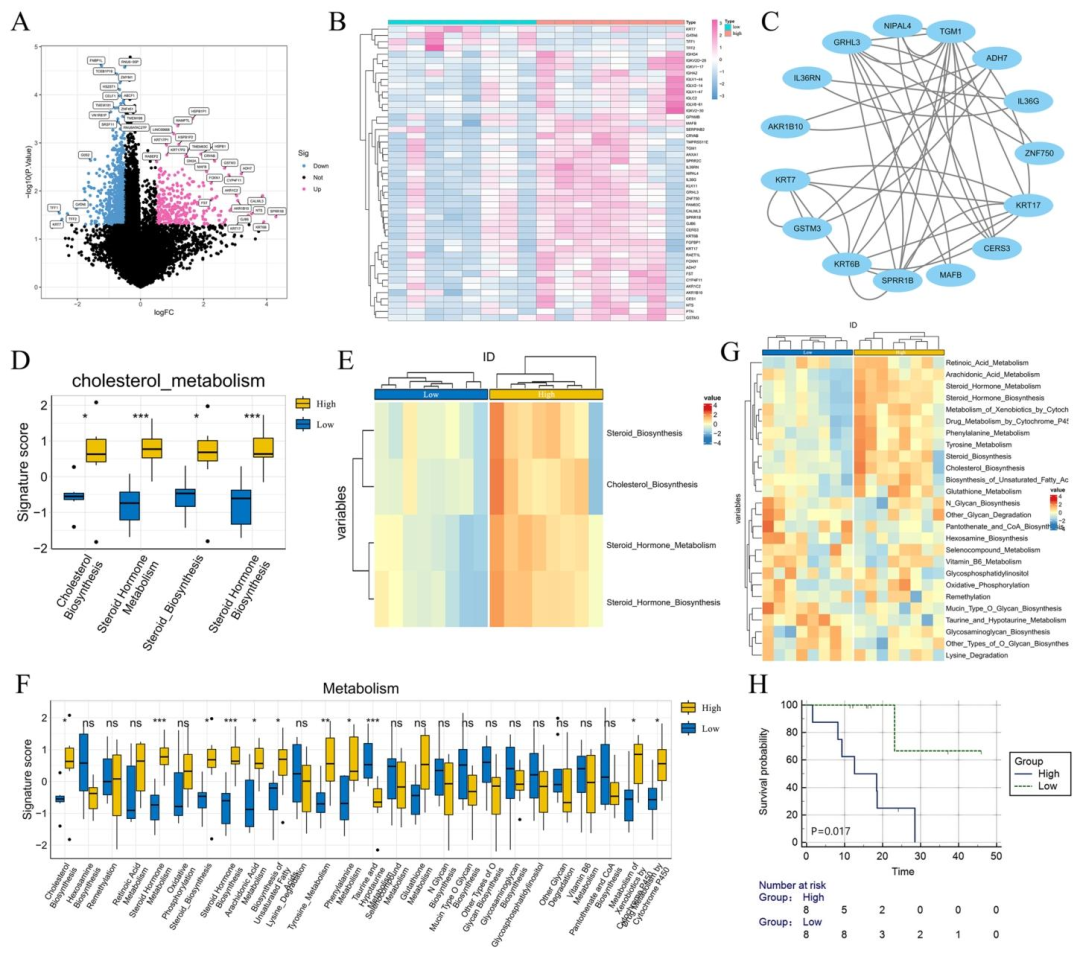
图 6:基于DLS风险分组的ESCC转录组代谢异质性分析
05
研究结论
该研究成功构建并验证了一种结合CT深度学习特征与营养生物标志物(低骨骼肌质量,LSMM)的多模态预测模型 ,用于食管鳞癌(ESCC)患者术前3年总生存期的个体化评估。结果表明,深度学习模型在内部和外部验证队列中的C-index分别达0.743和0.692 ,而整合了病理T/N分期、神经浸润、血管侵犯及LSMM的联合模型表现更优 ,内部和外部验证C-index提升至0.753和0.725,且校准曲线和决策曲线分析证实其临床净获益。尤为重要的是,基于深度学习特征的风险分层揭示了显著的转录组代谢异质性 :高风险组中胆固醇生物合成、氧化磷酸化及谷胱甘肽代谢等通路活性明显升高,而低风险组则相反,这为影像表型提供了生物学注解,支持深度学习特征作为"数字活检 "反映肿瘤代谢重编程。尽管模型在外部验证中C-index有所下降,且受限于回顾性设计和小样本转录组分析,但该联合模型实现了术前预后预测、风险分层与生物学可解释性的统一,为食管鳞癌的精准治疗决策提供了有前景的工具。
参考文献:Jia J, Cheng Y, Wang J, Bai G, Han L, Xu L, Niu Y. CT-based deep learning signatures associated with transcriptomic heterogeneity and combined with nutritional biomarkers improve prediction of 3-year overall survival in esophageal squamous cell carcinoma. Insights Imaging. 2026 Jan 26;17(1):22. doi: 10.1186/s13244-025-02189-x.