01
文献学习

今天分享的文献是由广东省人民医院放射科刘再毅教授团队联合南方医科大学、昆明医科大学第三附属医院、广州医科大学第一附属医院、中山大学等多中心团队近日(2026年1月5日)在肿瘤学领域顶刊《npj Precision Oncology》(中科院1区top,IF=8)上发表的研究"Longitudinal MRI-based deep learning model for predicting pathological complete response in breast cancer: a multicenter, retrospective cohort study"即基于纵向MRI的深度学习模型预测乳腺癌病理完全缓解:一项多中心回顾性队列研究,该研究提出了一种名为BSTNet的自监督时序学习框架,利用纵向动态增强MRI数据,预测乳腺癌患者在接受新辅助治疗后的病理完全缓解情况。该模型在多个独立队列中表现出优异的预测性能和良好的泛化能力。
创新点:①采用自监督学习处理纵向MRI :提出BSTNet框架,通过时间序列重排实现无监督预训练,有效捕捉肿瘤动态变化,减少对标注数据的依赖。②融合多头自注意力与LSTM机制 :结合时序特征提取与长短期记忆网络,提升模型对不规则扫描间隔与缺失时间点的适应能力。③跨中心泛化能力强:在多个独立外部验证中表现稳定,适应不同扫描协议与分子亚型,具备良好的临床适用性。
临床价值:①早期识别治疗反应不佳患者 :高特异性辅助临床及时调整治疗方案,避免无效治疗与毒副作用,推动个体化治疗决策。②非侵入性预测替代有创检查 :基于MRI的深度学习模型减少对组织活检的依赖,提升患者依从性与诊疗体验。③优化医疗资源分配:准确预测pCR可指导手术降级或强化治疗,合理分配医疗资源,提高整体治疗效率与效果。
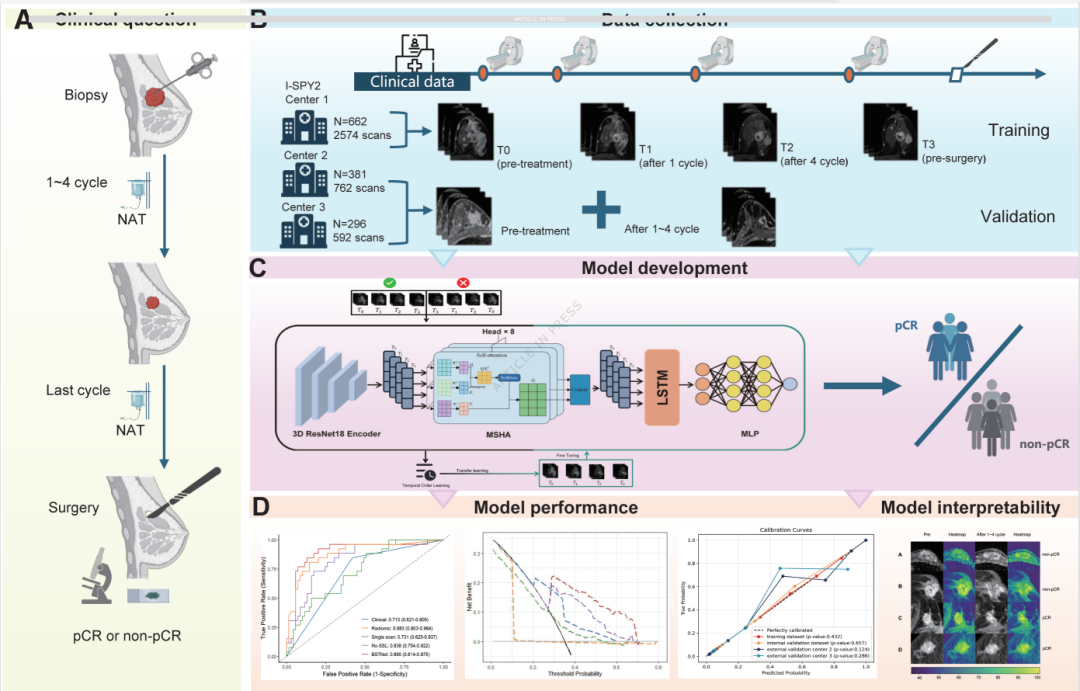
图 5:研究整体设计流程图
A:患者诊疗流程
关键节点:活检确诊→1-4周期新辅助治疗(NAT)→末次NAT→手术→病理评估(pCR/Non-pCR),明确纳入患者的治疗轨迹。
B:数据队列来源
训练+内部验证集:I-SPY2试验(Center 1,2010-2016),按8:2随机分配;外部验证集:Center 2(广东省人民医院,2015-2022)、Center 3(云南肿瘤医院,2020-2021)。
C:模型核心框架
核心技术:基于纵向MRI的乳腺自监督时间学习框架(BSTNet),聚焦pCR预测。
D:性能与可解释性评估
评估方法:ROC曲线(AUC)、决策曲线分析(DCA)、校准曲线;可解释性工具:Grad-CAM热力图。
02
研究背景及目的
研究背景
乳腺癌是全球女性最常见的恶性肿瘤,也是癌症相关死亡的主要原因。新辅助治疗已成为当前乳腺癌系统治疗的关键组成部分,而实现病理完全缓解不仅是手术降级(如保乳手术替代乳房切除)的关键前提,更是一个经验证的替代终点,能显著预测患者长期生存的改善。然而,尽管具有重要临床价值,仅有约19-30%的患者能够达到病理完全缓解 ,凸显了早期预测治疗反应的紧迫性,以便及时调整治疗方案、改善患者结局。现有预测方法存在明显局限:基于血液或组织活检的生物标志物具有侵入性、成本高且缺乏大规模验证;传统的动态对比增强磁共振成像分析则准确性不足。近年来,基于单时间点医学影像的深度学习模型展现出潜力,但未能充分利用治疗过程中肿瘤生物学与形态学的动态演变信息 。纵向影像数据虽能捕捉这些时序变化,但现有分析方法多依赖固定时间点的简单特征拼接,难以有效建模复杂的肿瘤演进模式,且对临床实践中多变的扫描间隔适应性差。因此,迫切需要一种能够灵活、鲁棒地分析纵向影像数据的新方法,以克服现有技术的不足,实现更早期、更准确的病理完全缓解预测,从而指导个体化的临床决策。
研究目的
本研究旨在开发并验证一个新颖的、基于自监督时序学习的深度学习框架 ,用于早期预测乳腺癌患者在新辅助治疗后的病理完全缓解状态。该框架的核心目标是克服现有单时间点模型无法捕捉治疗动态变化,以及传统纵向分析方法对固定扫描间隔和简单特征拼接依赖的局限性 。具体而言,研究试图通过构建名为BSTNet的模型 ,利用治疗前及治疗期间多个时间点的纵向MRI数据,自主学习肿瘤在治疗过程中的时序演变特征 。研究目的包括:验证该模型在预测病理完全缓解方面的判别性能与泛化能力 ,在一个包含1339名患者的多中心回顾性队列中进行内部与外部验证;评估其在不同分子亚型和不同扫描时间间隔下的性能稳定性 ;并通过与临床模型、放射组学模型、单时间点深度学习模型以及无自监督的时序模型进行比较,系统证明其优越性 。最终,本研究希望提供一个强大、实用且可解释的工具,能够适应多变的临床影像采集协议,辅助临床医生早期识别可能无法达到病理完全缓解的患者,从而为及时调整治疗策略、避免无效治疗及减少相关毒性提供依据,推动乳腺癌个性化治疗的发展。
03
数据和方法
研究数据
数据来源:3个独立多中心队列,共1339例患者、3928次MRI扫描。
训练集+内部验证集:来自I-SPY2试验(Center 1,2010-2016),529例训练集(pCR率34.0%)、133例内部验证集(pCR率33.8%)。
外部验证集1(Center 2):广东省人民医院,381例(pCR率35.2%,2015年3月-2022年9月)。
外部验证集2(Center 3):云南肿瘤医院,296例(pCR率34.1%,2020年4月-2021年11月)。
纳入标准:病理确诊浸润性乳腺癌、NAT后接受手术、具有治疗前及1-4周期治疗后MRI扫描、术后病理评估pCR状态。
关键变量:患者年龄、激素受体(HR)状态、人表皮生长因子受体2(HER2)状态、Ki-67指数、肿瘤分期等临床病理特征;纵向DCE-MRI影像数据(1.5T或3.0T扫描仪,峰值强化期图像)。
终点定义:pCR定义为乳腺及腋窝淋巴结无浸润性肿瘤细胞(ypT0/N0或ypTis/N0)。
技术方法
影像预处理:
半自动化肿瘤分割(nnU-Net模型+放射科医生手动调整,ICC=0.952,DSC=0.944)。
图像重采样、肿瘤中心化3D感兴趣区(VOI)提取、z-score强度归一化。
模型构建(BSTNet):
核心架构:3D ResNet18 CNN(空间特征提取)+多头自注意力机制(MHSA)+长短期记忆网络(LSTM)(时间特征建模)。
自监督预训练:通过662例患者的3-4个时间点序列(T0:治疗前;T1:1周期后;T2:4周期后;T3:术前),生成2648个增强样本(原始序列+随机排列序列),学习时间依赖关系。
监督微调:冻结编码器层,优化时间处理模块和分类层,采用加权交叉熵损失函数。
对比模型:临床模型(基于多变量逻辑回归)、放射组学模型(预处理与末次影像差异特征)、单扫描深度学习模型(仅用术前或1-4周期影像)、无自监督学习的多时间点模型(No-SSL)。
评估指标:主要指标为受试者工作特征曲线下面积(AUC),次要指标包括准确率、灵敏度、特异度、阳性预测值(PPV)、阴性预测值(NPV);校准曲线、决策曲线分析(DCA)评估临床效用;Grad-CAM可视化模型可解释性。
统计分析:Shapiro-Wilk正态性检验、t检验/秩和检验、卡方检验、多变量逻辑回归、DeLong检验(模型AUC比较)、1000次bootstrap抽样计算95%CI,P<0.05为差异有统计学意义。
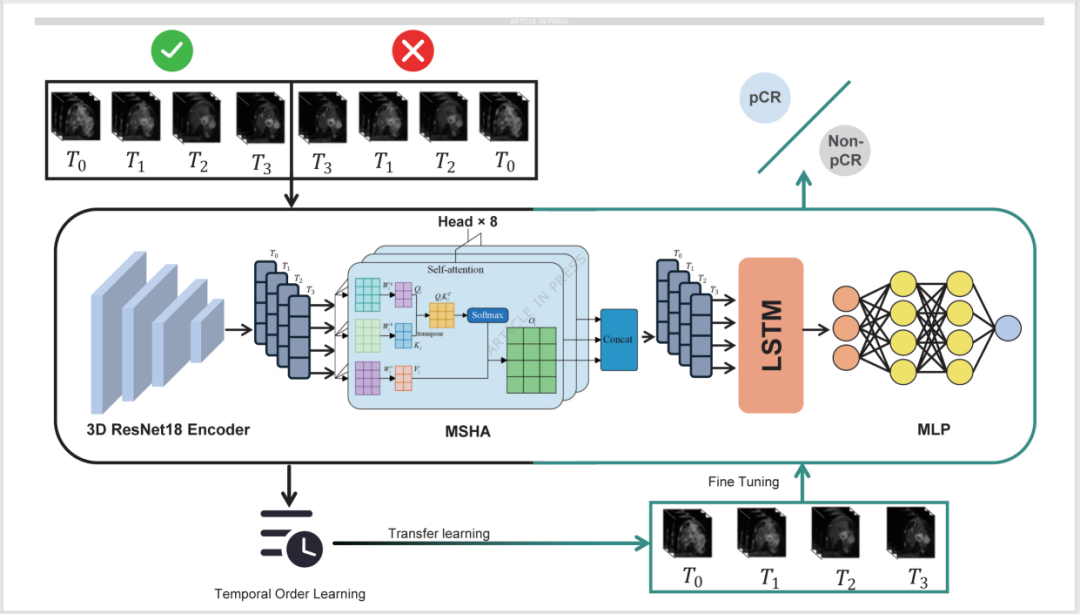
图 6:BSTNet的架构与模型训练流程
架构组件
空间特征提取:3D ResNet18 CNN骨干网络,对每个时间点的MRI扫描图独立处理,生成256维特征向量。
时间特征建模:集成多头自注意力机制(MHSA,8头)和长短期记忆网络(LSTM),捕捉多时间点间的动态依赖关系。
分类输出:全连接层(256神经元)+二分类输出层(pCR/Non-pCR),损失函数为二元交叉熵。
训练流程(两阶段)
自监督预训练:利用662例患者的3-4个时间点序列(T0:治疗前;T1:1周期后;T2:4周期后;T3:术前),通过"时间序列置换"生成2648个增强样本(1个原始序列+3个随机排列序列),让模型学习时间逻辑关系,无需额外标注。
监督微调:冻结CNN编码器层,仅更新时间处理模块和分类层,采用加权交叉熵损失函数,适配pCR预测任务;对缺失时间点数据采用零填充处理,保证输入结构一致性。
04
实验结果
①模型性能:
- BSTNet表现优异:内部验证AUC=0.882(95% CI:0.816-0.948),外部验证Center 2 AUC=0.857(95% CI:0.819-0.895),Center 3 AUC=0.854(95% CI:0.802-0.906)。
- 显著优于对比模型:在外部验证中,BSTNet AUC显著高于No-SSL(0.783/0.759)、放射组学模型(0.602/0.710)、临床模型(0.705/0.733)及单扫描模型(0.643/0.613)(P<0.05)。
②亚组与稳定性:
- 分子亚型一致性:HR±、HER2±亚组AUC分别为0.827-0.886、0.818-0.895,无显著差异。
- 扫描时间点适应性:Center 2中1-4周期扫描AUC=0.841-0.893(稳定);Center 3中4周期扫描AUC达0.970(最优)。
- 非pCR识别能力:内部验证特异度=86.4%,Center 2=74.5%,Center 3=85.1%。
③临床效用:决策曲线分析显示,在0.3-0.7阈值概率范围内,BSTNet在外部验证队列中的净获益显著高于其他模型,优于"治疗所有患者"或"不治疗任何患者"的基线策略。
④可解释性:Grad-CAM可视化显示,pCR患者治疗后激活集中于肿瘤核心区(与同心收缩模式相关),非pCR患者激活集中于肿瘤周边区(与非同心收缩模式相关)。
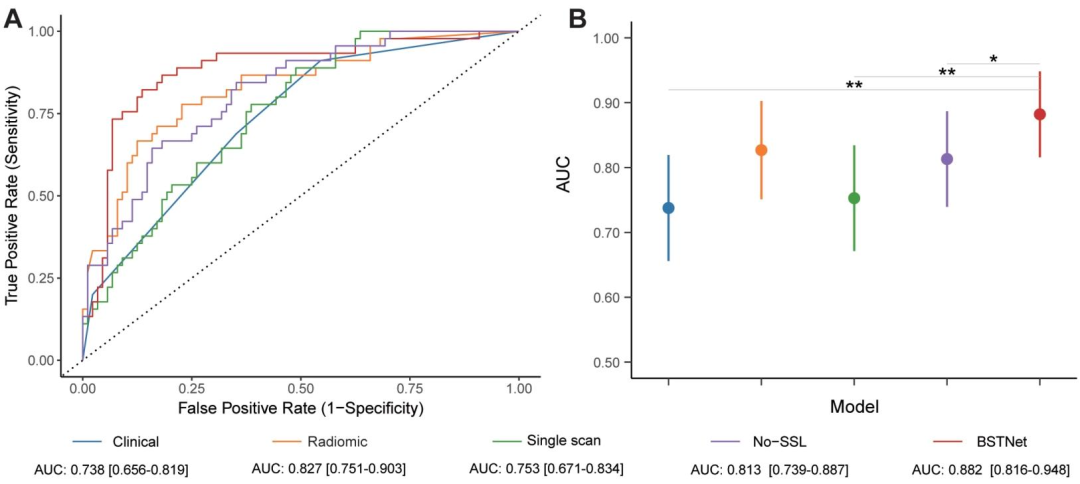
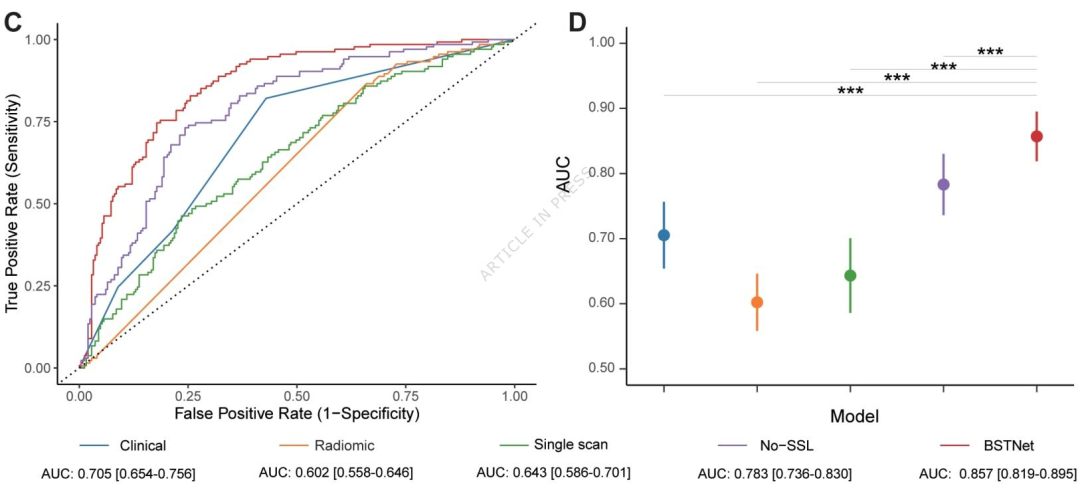
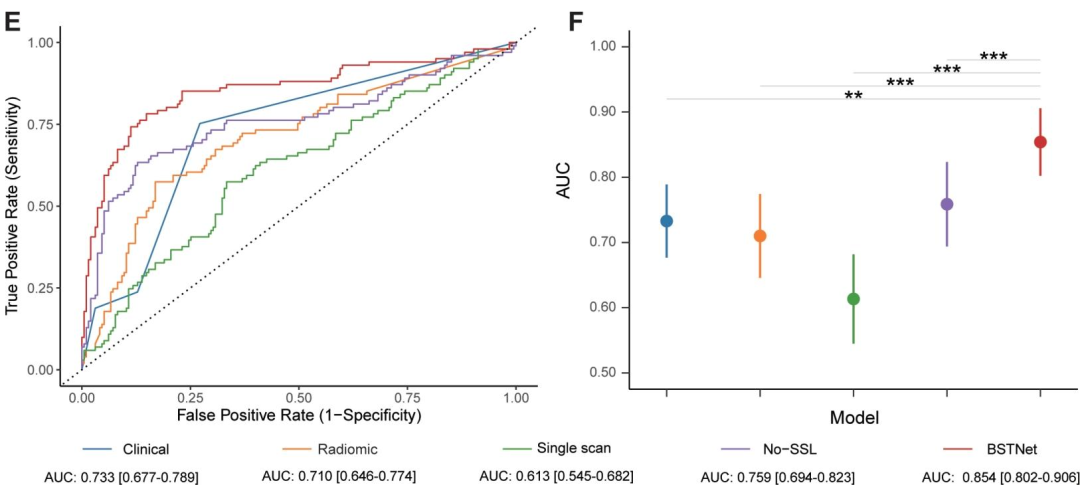
图 1:不同模型在内部及外部验证队列中的ROC曲线与AUC值对比
展示了BSTNet与4种基准模型(临床模型、放射组学模型、单扫描深度学习模型、无自监督学习的多时间点模型(No-SSL))的预测性能差异,以AUC(受试者工作特征曲线下面积)为核心指标。
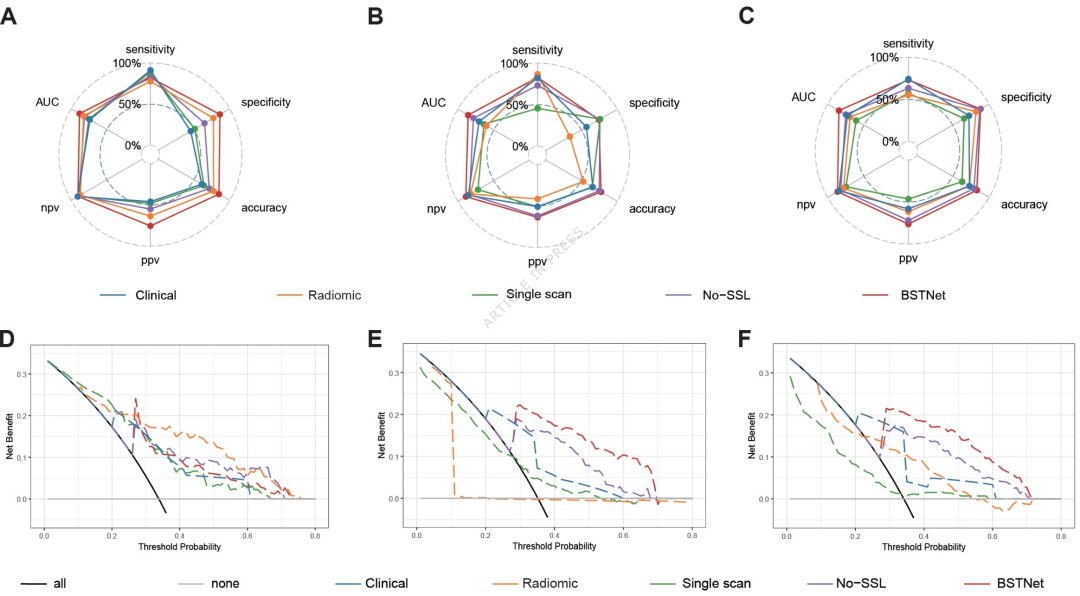
图 2:不同模型的综合性能雷达图与决策曲线分析(DCA)
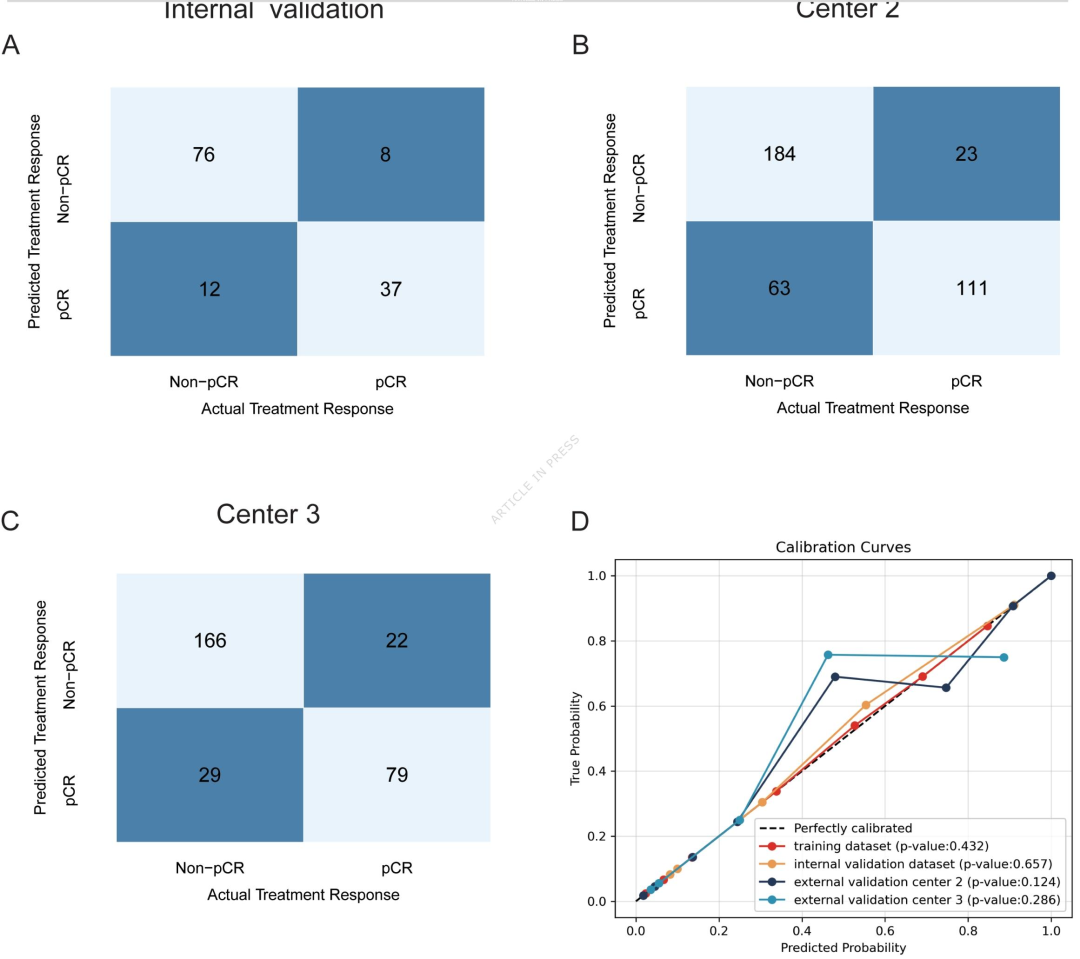
图 3:BSTNet的混淆矩阵与校准曲线

图 4:BSTNet的Grad-CAM可视化(模型可解释性)
通过热力图展示模型预测时关注的MRI区域,揭示pCR与Non-pCR患者的肿瘤影像特征差异。
05
研究结论
本研究成功开发了一种基于纵向MRI的自监督时序深度学习模型(BSTNet),用于早期预测乳腺癌新辅助治疗后的病理完全缓解(pCR)。该模型在包含1339例患者的多中心回顾性队列 中表现出优异且稳定的预测性能 :内部验证AUC为0.882,外部验证AUC分别为0.857和0.854。BSTNet在不同分子亚型(HR+/HR-、HER2+/HER2-)中均保持一致的预测能力 ,且对非pCR患者具有较高的特异性 (内部验证86.4%,外部验证74.5%和85.1%),有助于临床早期识别治疗反应不佳的患者并调整策略。与单时间点模型、影像组学模型及无自监督的时序模型相比,BSTNet显著优于现有方法 ,尤其擅长捕捉治疗过程中肿瘤的动态变化,并具备良好的跨中心泛化能力。该研究为乳腺癌个体化治疗提供了一种稳健、可解释且临床适用性强的AI辅助决策工具,但其临床效用仍需前瞻性研究进一步验证。
参考文献:Huang X, Xu Z, Zhao Y, Wang Y, Liu Y, Hu W, Zhao K, Yao L, He J, Yu Y, Deng T, Wu L, Zhang W, Liang C, Liu Z. Longitudinal MRI-based deep learning model for predicting pathological complete response in breast cancer: a multicenter, retrospective cohort study. NPJ Precis Oncol. 2026 Jan 5. doi: 10.1038/s41698-025-01256-2.