01
文献学习

今天分享的是由北京大学人民医院洪楠团队联合山西人民医院放射科等团队于2026年1月8日在《Radiology: Imaging Cancer 》(中科院2区,IF=6.3)上发表的研究"Assessing an Automated Noncontrast CT--based Pipeline for Sacral Tumor Classification Using a Hip Bone Reference Frame"即基于髋骨参考框架的非增强CT自动骶骨肿瘤分类流程评估,本研究开发了一种全自动混合深度学习流程** ,用于基于术前非增强CT图像对骶骨肿瘤进行六分类。该流程整合了肿瘤与髋骨自动分割模型 和多模态分类模型 ,首次引入髋骨参考坐标系以提升定位与分类准确性,并在多中心数据集中验证其性能优于放射科医生。**
创新点 :①首创髋骨坐标系 :首次采用髋骨作为解剖参考框架定位骶骨肿瘤,提升空间定位精度。②多模态融合模型 :整合影像、临床与位置信息构建CL-MedImageNet,实现六类肿瘤同步分类。③全自动一体化流程:从分割到分类全程自动化,避免人工干预,提高处理效率与一致性。
临床价值 :①辅助术前精准分型 :提供非侵入性诊断工具,减少活检依赖,支持个体化治疗决策。②提升诊断效能 :尤其在转移瘤诊断中优于放射科医生,弥补临床诊断难点。③促进多中心应用:经外部验证的自动化系统适应不同机构,提升诊断可及性与标准化。
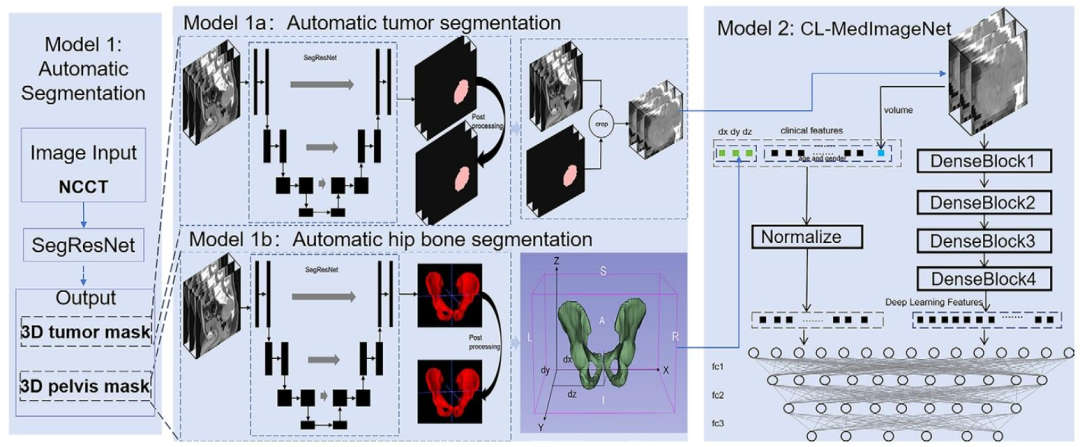
图 1:研究整体流程图
输入数据:非增强CT(NCCT)影像。
模型1(SegResNet):自动分割肿瘤和髋骨,生成3D肿瘤掩码与3D髋骨掩码;以髋骨为参考框架,计算肿瘤质心的相对位置(Dx、Dy、Dz)。
模型2(CL-MedImageNet):创新型6分类模型,同时接收三类输入------模型1裁剪的肿瘤影像、肿瘤相对髋骨的位置信息、临床数据(年龄、性别、肿瘤体积),最终输出肿瘤分类结果。
02
研究背景及目的
研究背景
骶骨肿瘤作为一类特殊的骨肿瘤亚型,在临床诊断与治疗中面临显著挑战。这类肿瘤类型多样,主要包括脊索瘤、巨细胞瘤、软骨肉瘤、骨肉瘤、神经源性肿瘤及转移瘤 ,其中脊索瘤最为常见。由于早期症状不典型且病例相对罕见,骶骨肿瘤常被延误诊断或误诊,导致患者可能接受不必要的侵入性活检或治疗延迟,从而增加病痛、医疗成本及死亡风险。目前,术前肿瘤类型的准确鉴别对于制定个体化治疗方案(如脊索瘤的广泛切除与巨细胞瘤的病灶内刮除)至关重要,但传统依赖组织活检的方法具有侵入性、存在采样误差及并发症风险 ,并非理想选择。影像学检查,尤其是非增强CT(NCCT),因能清晰显示骨质破坏、钙化等关键特征而成为首选初步评估手段,但其诊断效能受限于医生经验与主观判断。尽管人工智能(AI)技术在医学影像领域迅速发展,卷积神经网络(CNN)已在多种肿瘤诊断中展现出潜力,但现有针对骶骨肿瘤的AI研究仍存在明显局限:多数模型依赖内部验证,缺乏外部测试以验证泛化能力;未能有效整合影像特征与临床、空间位置信息;且多依赖于人工分割,流程非全自动化,效率低且易引入人为误差 。因此,开发一种能够自动化、多模态整合且经过外部验证的AI系统,以提升骶骨肿瘤术前分类的准确性、客观性和临床可行性,成为亟待解决的重要课题。
研究目的
本研究旨在开发并验证一种全自动的混合深度学习流程,仅基于术前非增强CT(NCCT)图像实现对骶骨肿瘤类型的自动、准确分类 。具体而言,该研究设计并构建了一个集成两个串联卷积神经网络模型的全自动化管线 。第一个模型(模型1)负责从NCCT图像中自动分割肿瘤区域与髋骨结构 ,生成对应的掩膜;其中一项关键创新是首次将髋骨作为解剖参考框架 ,用于精确定义肿瘤的空间位置。第二个模型(模型2,即CL-MedImageNet分类器)是一个创新的六分类模型 ,其能够同步接收并融合三类输入信息 :由模型1提取的肿瘤区域图像、计算得到的肿瘤相对于髋骨的空间位置坐标(Dx, Dy, Dz)、以及患者的临床数据(年龄、性别、肿瘤体积)。该研究的目标是通过这种自动化、多模态(影像+临床+位置)融合的策略 ,克服现有研究手动操作繁琐、数据利用单一、缺乏外部验证等缺陷,从而建立一个高效、客观且可推广的辅助诊断工具。最终,研究通过内部及外部独立数据集验证,旨在证明该全自动混合模型的分类性能能够达到甚至超越放射科医生的诊断水平,为骶骨肿瘤的术前无创精准分型、个性化治疗规划提供可靠的技术支持。
03
数据和方法
研究数据
总样本:690例患者(2011--2024年)
数据来源:三中心多中心回顾性数据
中心1:630例(训练/验证/内部测试)
中心2 & 3:60例(外部测试)
肿瘤类型:转移瘤、软骨肉瘤、骨肉瘤、脊索瘤、神经源性肿瘤、巨细胞瘤
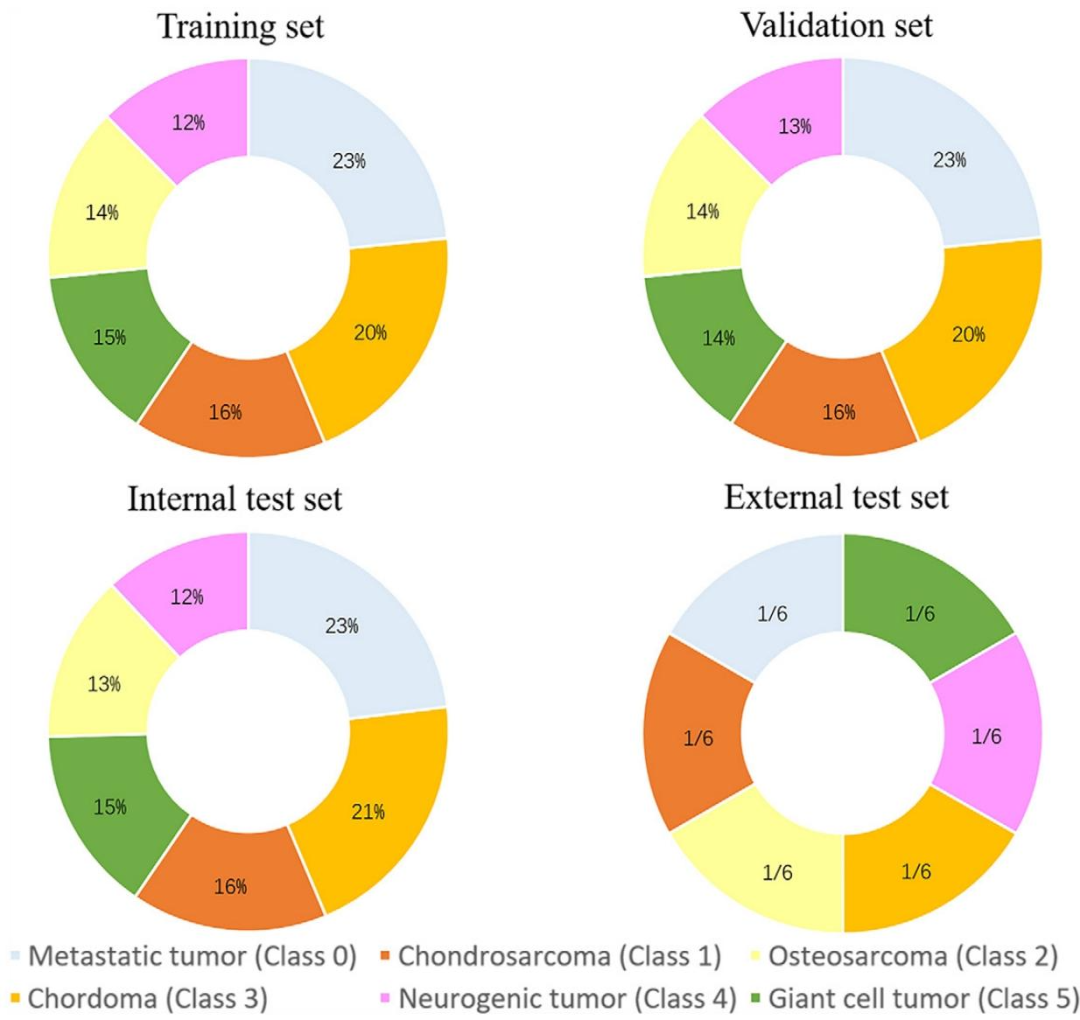
图 2:各数据集肿瘤类型分布
技术方法
1. 模型架构(全自动混合pipeline)
模型1(SegResNet):自动分割肿瘤与髋骨,生成3D肿瘤掩码和髋骨掩码;以髋骨为参考框架,计算肿瘤质心的相对坐标(Dx、Dy、Dz),实现肿瘤定位。
模型2(CL-MedImageNet):基于DenseNet-121改进的6分类模型,输入包括:①模型1裁剪的肿瘤影像;②临床数据(年龄、性别、肿瘤体积);③肿瘤相对位置信息。
2. 对比模型构建
构建3类核心模型:C-MedImageNet(影像+临床数据)、L-MedImageNet(影像+位置信息)、CL-MedImageNet(影像+临床+位置信息)。
对照模型:支持向量机(SVM,仅临床数据/临床+位置数据)、DenseNet-121(仅影像数据)。
3. 性能评估
分割性能:Dice系数(验证集、内部测试集、外部测试集)、观察者间一致性(Dice系数)。
分类性能:宏平均AUC、宏平均F1分数、微平均AUC、微平均F1分数、混淆矩阵。
对照实验:与两名具有5年肌肉骨骼影像诊断经验的放射科医生进行盲法对比(仅提供临床数据及原始CT影像)。
4. 统计分析
连续变量:方差分析或Kruskal-Wallis检验;分类变量:χ²检验或Fisher精确检验。
显著性水平:P<0.05,使用IBMSPSSStatistics进行分析。
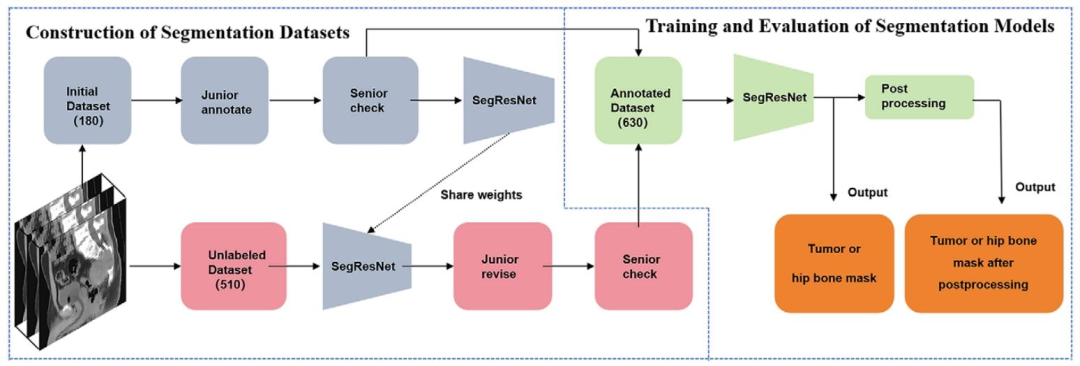
图 3:分割数据集构建与模型评估流程
04
实验结果
1. 分割性能
经后处理后,肿瘤分割Dice系数:验证集0.82±0.11、内部测试集0.81±0.12、外部测试集0.81±0.12;髋骨分割Dice系数均≥0.94。
观察者间分割一致性:Dice系数0.96,提示人工分割一致性优异。
2. 分类性能
CL-MedImageNet表现最优:
宏平均AUC:验证集0.89(95% CI:0.83-0.93)、内部测试集0.88(95% CI:0.84-0.92)、外部测试集0.87(95% CI:0.79-0.92)。
宏平均F1分数:验证集0.63、内部测试集0.63、外部测试集0.56。
对神经源性肿瘤(AUC0.97)和脊索瘤(AUC0.94)分类效果最佳。
3. 与放射科医生对比
外部测试集:CL-MedImageNet宏平均AUC(0.87)显著优于放射科医生1(0.80,P=0.002),优于放射科医生2(0.83,P=0.45)。
优势领域:对转移性肿瘤诊断提升最显著(模型AUC0.91 vs 医生10.65、医生20.77,P<0.001)。
4. 不同模型对比
整合多维度数据的模型(CL-MedImageNet)性能优于单一数据模型;位置信息与临床数据的加入均能提升分类效果(CL-MedImageNet>C-MedImageNet>L-MedImageNet>仅影像/仅临床模型)。
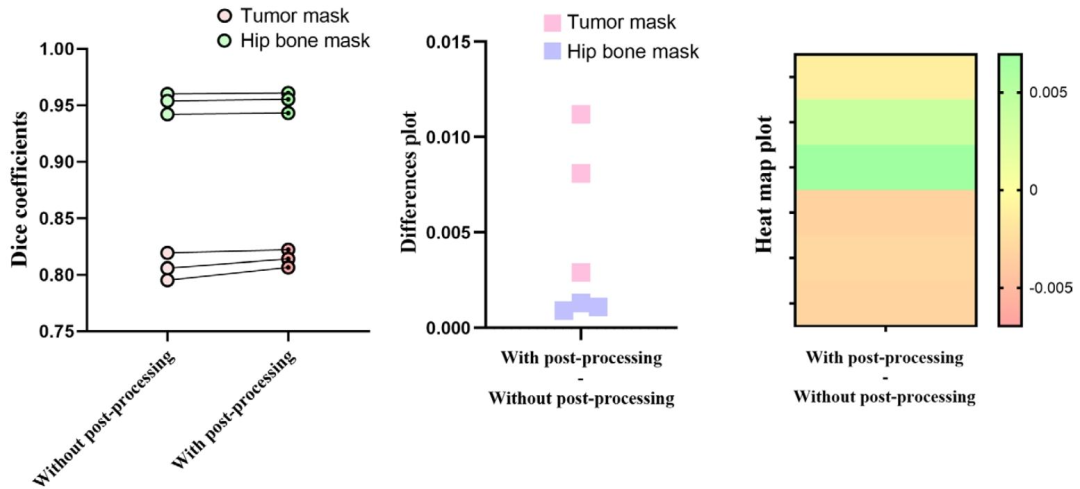
图 4:有无后处理的分割Dice系数对比
对比肿瘤掩码和髋骨掩码在"无后处理"与"有后处理"条件下的分割精度(Dice系数)
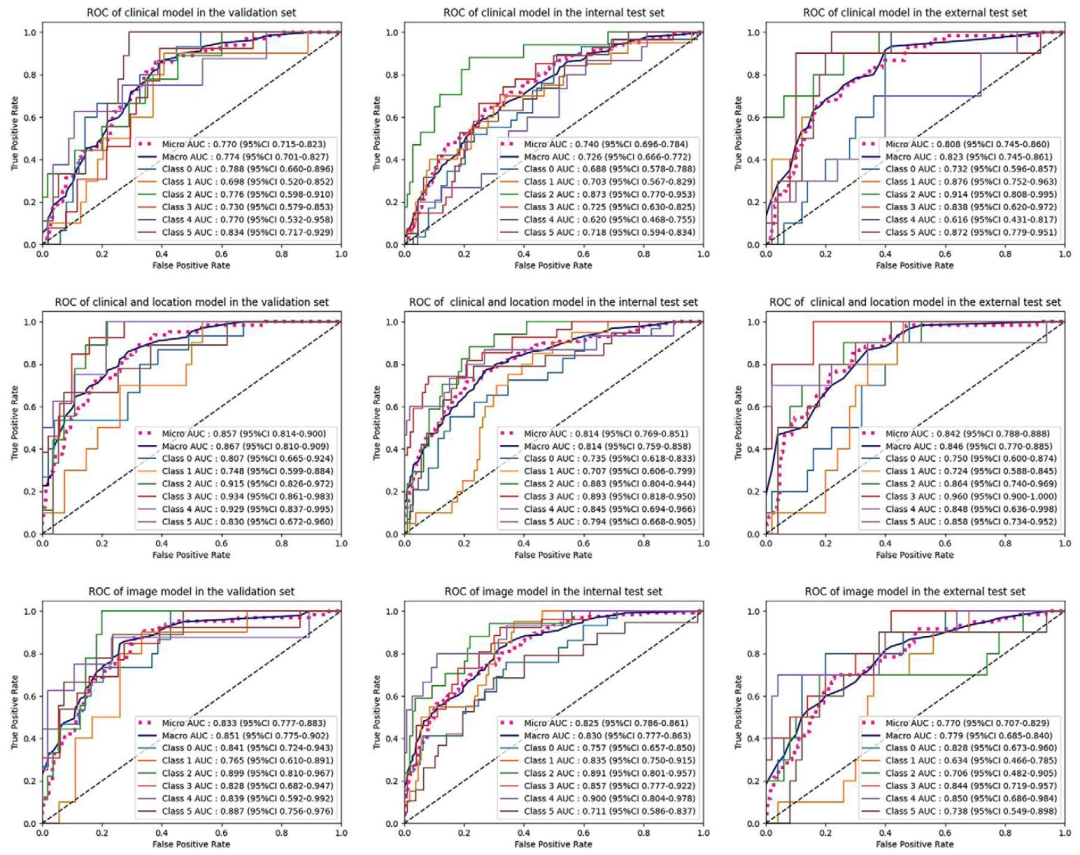
图 5:SVM与DenseNet121模型的ROC曲线
展示三类模型在验证集、内部测试集、外部测试集的ROC曲线(AUC值
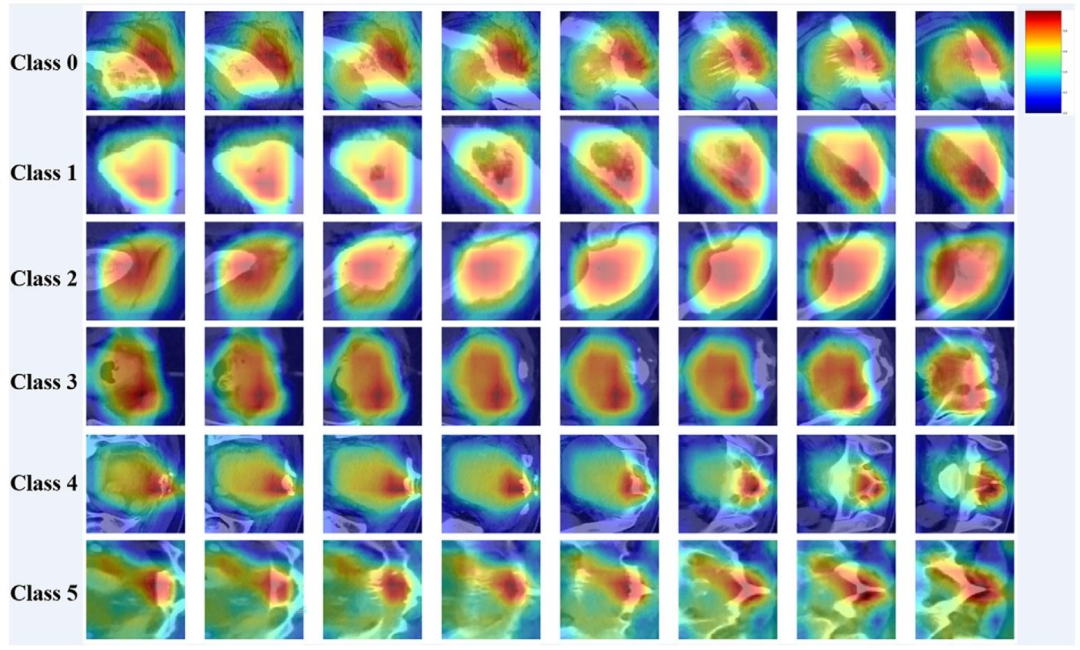
图 6:DenseNet121的注意力图
展示DenseNet121模型对6类肿瘤影像的注意力分布,颜色从红色到蓝色表示模型分类决策的贡献度递增
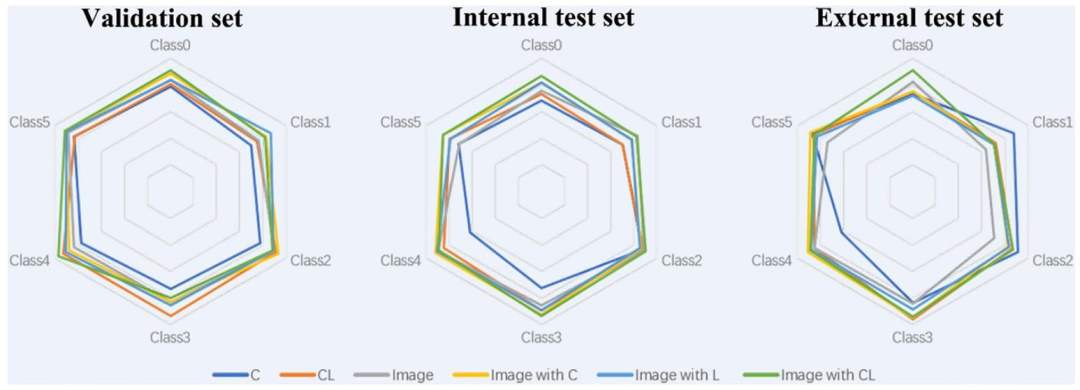
图 7:不同模型区分6类肿瘤的雷达图
在验证集、内部测试集、外部测试集三个场景下,对比6种模型对6类肿瘤的分类性能
模型类型:仅临床数据(C)、临床+位置数据(CL)、仅影像数据(Image)、影像+临床数据(Image+C)、影像+位置数据(Image+L)、影像+临床+位置数据(Image+CL,即CL-MedImageNet)。
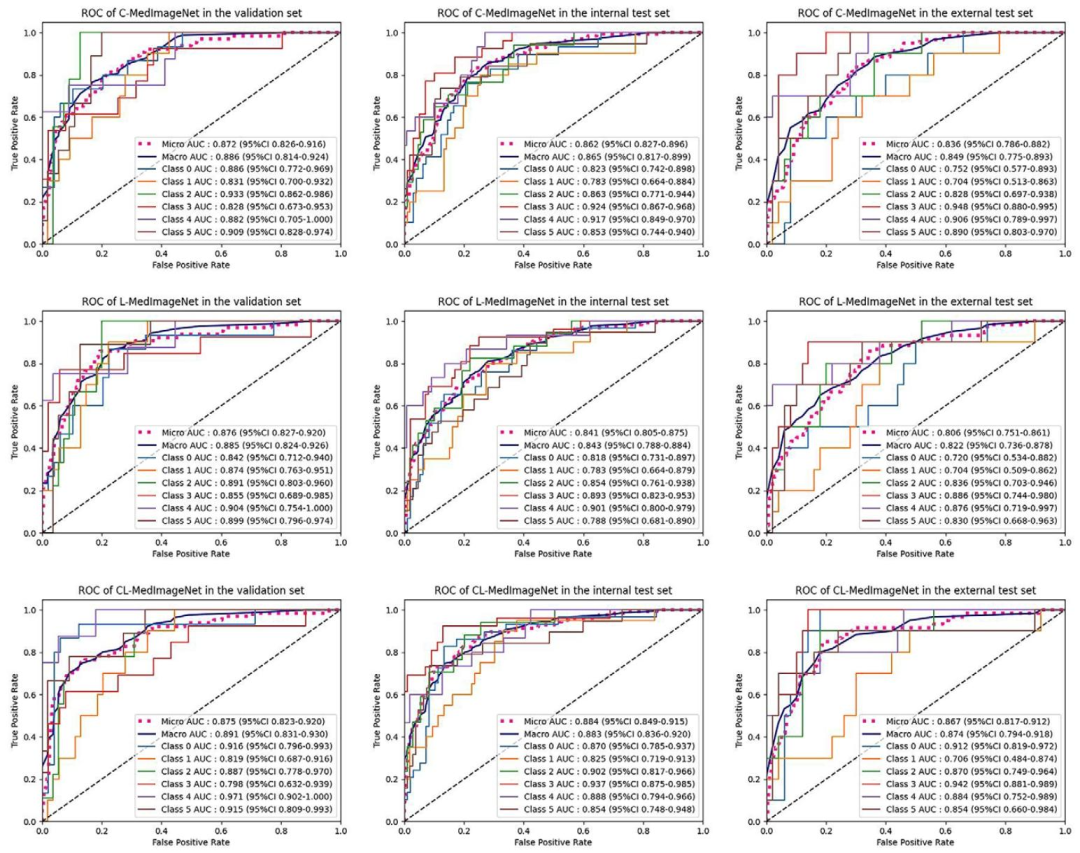
图 8:C-MedImageNet等模型的ROC曲线
展示三类融合模型在验证集、内部测试集、外部测试集的ROC曲线(AUC值)图 9:放射科医生读数的AUC与混淆矩阵
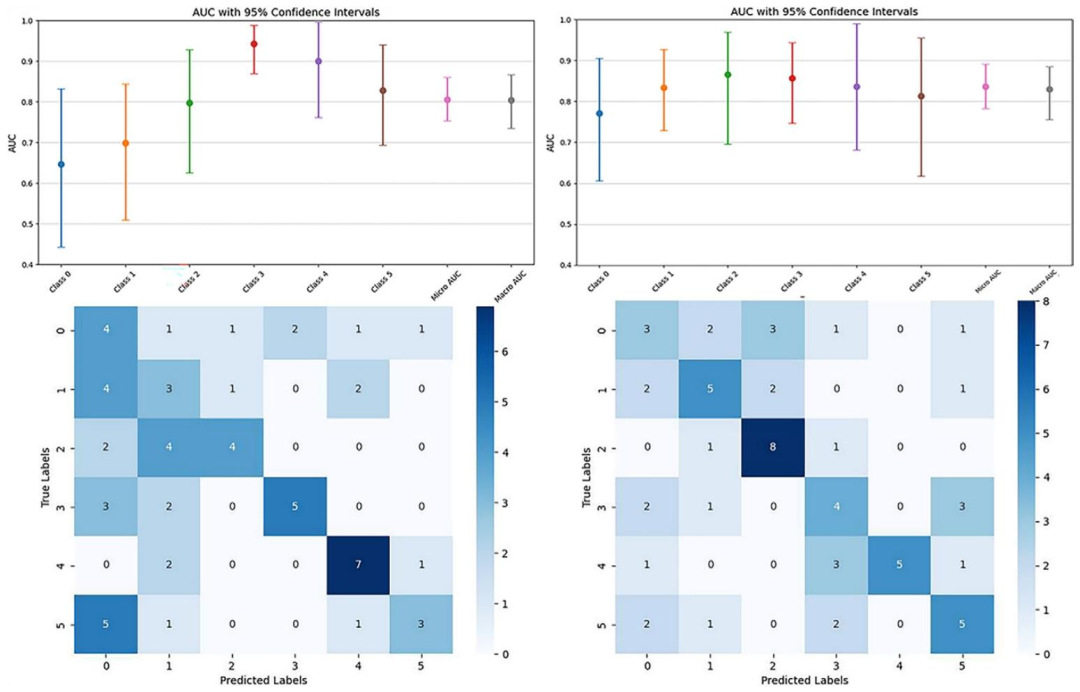
图 9:放射科医生读数的AUC与混淆矩阵
展示两名放射科医生(5年肌肉骨骼影像诊断经验)对外部测试集(60例)的诊断性
05
研究结论
本研究成功开发并验证了一种基于非增强CT(NCCT)的全自动深度学习混合模型(CL-MedImageNet),用于骶骨肿瘤的六分类诊断。该模型创新性地以髋骨为参考坐标系进行肿瘤定位 ,并整合了影像、临床(年龄、性别、肿瘤体积)与位置信息,实现了端到端的全自动分割与分类流程。在包含690例患者的回顾性多中心研究中,模型表现出优异的分割性能 (Dice系数达0.81--0.82)和稳健的分类能力 (宏观平均AUC为0.87--0.89,宏观平均F1分数为0.56--0.63),且在外部测试中显著优于两名放射科医生 (宏观平均AUC:0.87 vs. 0.80,P=0.002),尤其在转移瘤诊断方面优势明显(AUC 0.91 vs. 0.65--0.77)。研究结果表明,该全自动、多模态AI系统能够提升骶骨肿瘤术前诊断的准确性与一致性 ,为非侵入性辅助诊断和个体化治疗规划提供了可行工具。尽管存在外部验证样本量有限、回顾性设计可能引入偏倚等局限性,但其方法学创新与临床实用性已得到初步验证,未来需通过更大规模前瞻性研究进一步优化与推广。
参考文献:Zheng F, Yin P, Liang K, Yang L, Liu T, Zhang W, Wang Y, Hao W, Hao Q, Hong N. Assessing an Automated Noncontrast CT-based Pipeline for Sacral Tumor Classification Using a Hip Bone Reference Frame. Radiol Imaging Cancer. 2026 Jan;8(1):e250098. doi: 10.1148/rycan.250098.