01
文献学习

今天分享的文献是由广东省人民医院放射科刘再毅教授、阿里巴巴达摩院等团队于2026年4月21日在肿瘤学领域顶刊《Annals of Oncology 》(中科院1区top,IF=65.4)上发表的研究"Colorectal cancer detection using non-contrast CT and deep learning: a multicenter and international cohort study "即基于非增强CT与深度学习的结直肠癌检测:一项多中心国际队列研究,该研究开发并验证了一个名为 COCA 的深度学习模型,用于在常规非增强CT扫描中检测结直肠癌。研究涵盖多中心、国际队列,并进行真实世界验证。COCA在检测CRC方面表现出优异的性能,显著优于放射科医生,并能在胸部CT等非完整肠道覆盖的扫描中实现有效筛查。****
创新点:①首创非增强CT筛查结直肠癌 :首次验证平扫CT结合深度学习可精准检测CRC,突破传统需增强或肠道准备的局限 。②联合分割与分类的多任务框架 :采用混合监督学习与双版本模型 (高特异/高灵敏),适配大规模机会性筛查与高危人群早筛。③拓展至胸部CT与持续学习 :验证胸部CT(部分肠段可见)的可行性,并引入困难样本挖掘与增量学习实现模型动态升级。
临床价值:①提升检出率并减少漏诊 :AI辅助下医生敏感性提升20.4%,发现真实世界中多次漏诊的CRC ,避免治疗延误。②覆盖现有筛查盲区人群 :适用于<45岁年轻人群、急诊/住院等场景,无需额外检查或患者配合 ,扩大筛查覆盖面。③效能优于主流非侵入性检测 :高特异性版达99.8%,显著降低不必要的结肠镜转诊,兼具成本效益与高依从性。
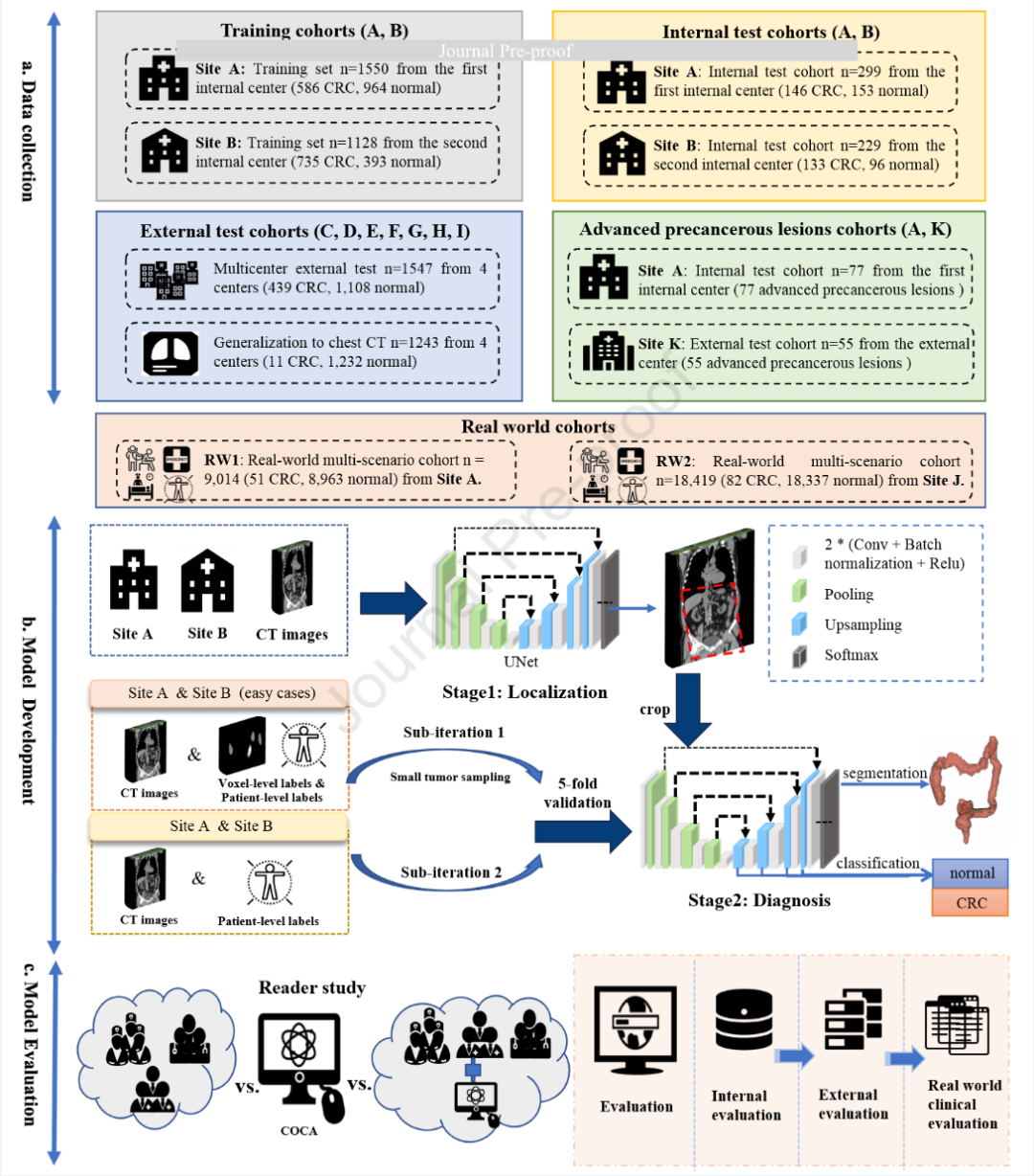
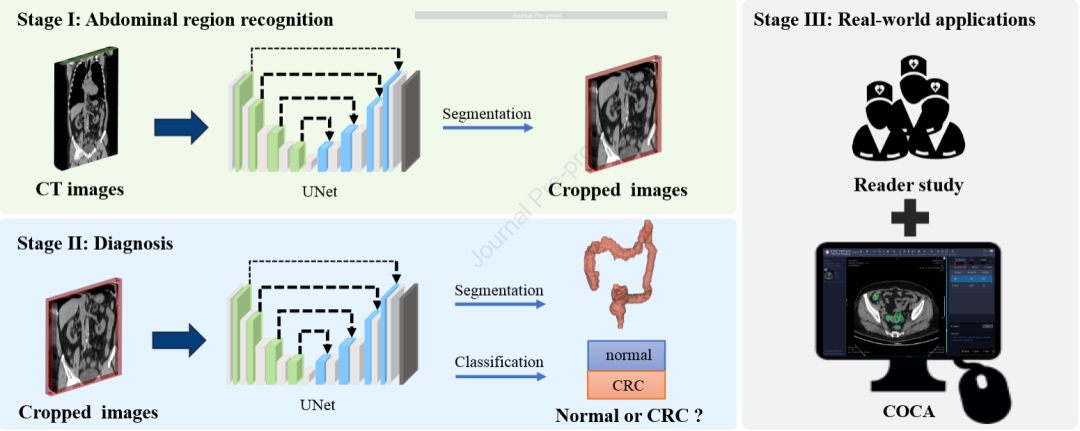
图 1:研究整体工作流程图
02
研究背景和目的
研究背景
结直肠癌(Colorectal Cancer, CRC)是全球癌症相关死亡的第二大原因,尽管存在结肠镜、CT结肠造影、胶囊结肠镜、多靶点粪便DNA检测及cfDNA血检等多种筛查手段,但它们的应用均面临显著挑战。结肠镜作为金标准具有侵入性,患者常因疼痛和尴尬感而依从性低 ;CT结肠造影虽创伤较小,但仍需肠道充气,造成不适;粪便DNA检测和cfDNA血检虽为非侵入性,但前者因粪便采集意愿低而导致依从性差,后者对早期癌前病变的灵敏度不足(文献报道仅13.2%),增加了漏诊风险。此外,当前筛查指南主要覆盖45岁以上人群,年轻人群CRC发病率正在上升 ,而经济欠发达地区医疗资源匮乏、认知度低,进一步限制了筛查覆盖率。值得注意的是,每年有数千万例常规非增强腹部盆腔CT扫描 (用于创伤、腹痛或肿瘤分期等适应症),这些扫描常包含结直肠区域,但传统上认为非增强CT因软组织对比度差、影像特征不特异,未被用于CRC筛查 。近年来,人工智能在非增强CT上检测胰腺癌、食管癌等挑战性癌症方面展现出潜力,然而利用非增强CT进行CRC检测尚未被探索。因此,开发一种无创、无需肠道准备、无需额外辐射、且可规模化的CRC筛查方法具有迫切的临床需求。
研究目的
本研究旨在开发并验证一种名为COCA(COlorectal Cancer detection with AI) 的深度学习模型,利用常规非增强CT (包括腹部/盆腔及胸部CT)实现高精度的结直肠癌检测。具体目标包括:构建一个联合病灶分割与分类的多任务学习架构 ,并通过混合监督策略利用来自两个中心的1,321例CRC患者和1,357例正常对照进行模型训练。研究首先评估COCA在内部测试队列中的诊断性能,并与十名不同年资放射科医生 (包括结直肠专家、普通放射科医生和住院医师)进行对比,随后在国际多中心外部验证队列 (涉及中国和捷克共和国的四个中心,共1,547例患者)中评估其泛化能力。此外,研究将COCA的应用扩展至胸部CT (部分结直肠区域可见),并检测晚期癌前病变 。最关键的是,通过在两个医院的真实世界多场景连续患者队列 (共27,433例)中部署COCA,验证其在急诊、门诊、住院及体检等场景中的实际效能,评估其减少漏诊、辅助临床决策的安全性及经济性。最终目标是提供一种无创、低成本、可规模化的机会性CRC筛查工具,克服现有方法在依从性和覆盖率上的根本障碍。
03
数据和方法
研究数据
训练集:2,678例(1,321例CRC,1,357例正常),来自两个中心
内部测试集:528例
外部国际测试集:1,547例(4个中心)
胸部CT测试集:1,243例
真实世界验证集:RW1(9,016例)、RW2(18,427例)
癌前病变测试集:内部77例,外部55例
技术方法
模型架构:两阶段深度学习
定位阶段:UNet粗分割结直肠区域
诊断阶段:多任务框架(分割 + 分类),使用混合监督学习
训练策略:五折交叉验证 + 困难样本挖掘 + 持续学习(COCA Plus)
读者研究:10名不同经验的放射科医生,评估有无AI辅助下的诊断表现
统计方法:AUC、敏感性、特异性、PPV、Bootstrap置信区间、Permutation test、DeLong test
04
实验结果
内部测试集:AUC 0.992,敏感性 91.8%,特异性 98.8%
外部多中心测试集:AUC 0.979,敏感性 86.1%,特异性 99.5%
胸部CT测试集:敏感性81.8%,特异性 99.9%
读者研究:AI辅助提升敏感性 +20.4%,特异性 +5.4%
真实世界验证:
RW1:敏感性 88.2%,特异性 99.5%,PPV 48.4%
RW2(COCA Plus):敏感性 86.6%,特异性 99.8%,PPV 63.4%
癌前病变检测:敏感性 61.0%(内部),45.5%(外部)
早期CRC检测:Stage I 敏感性 ≥ 83.3%
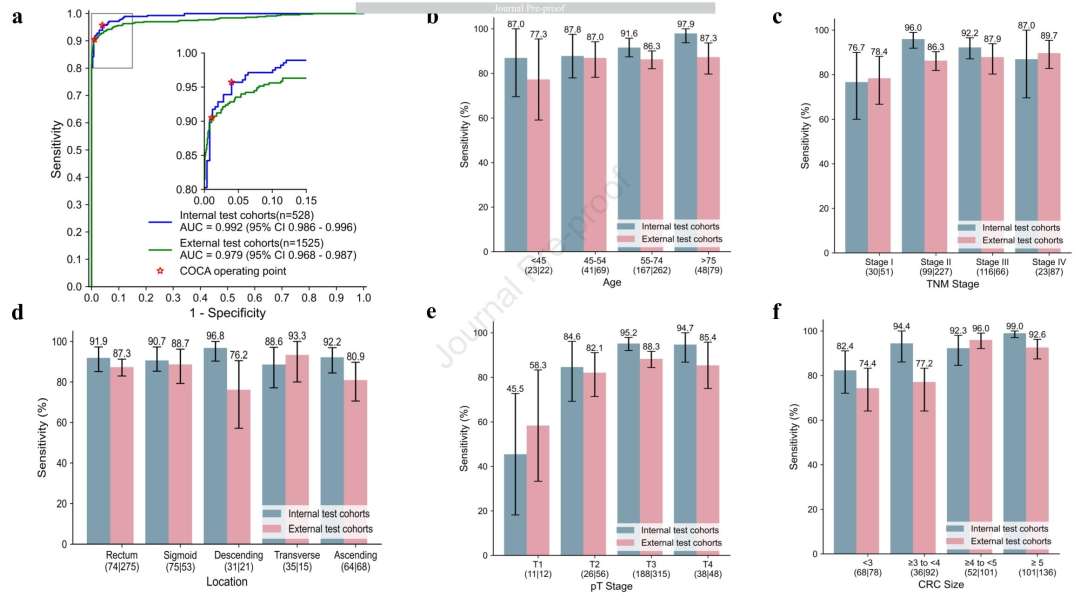
图 2-高特异性版COCA的CRC检测性能: 该图展示了内外部测试集上模型的诊断能力。a. ROC曲线 :内部测试集AUC达0.992 (95% CI 0.986-0.996),外部多中心AUC为0.979 (0.968-0.987),表现优异。b-f 分别按年龄、肿瘤位置、TNM分期、T分期和肿瘤大小展示敏感性:早期(I期)敏感性76.7% ,<3cm小肿瘤82.4% ,<45岁年轻患者87.0%。直肠和乙状结肠敏感性均>90%,表明模型在不同亚组中具有稳健的检测能力。
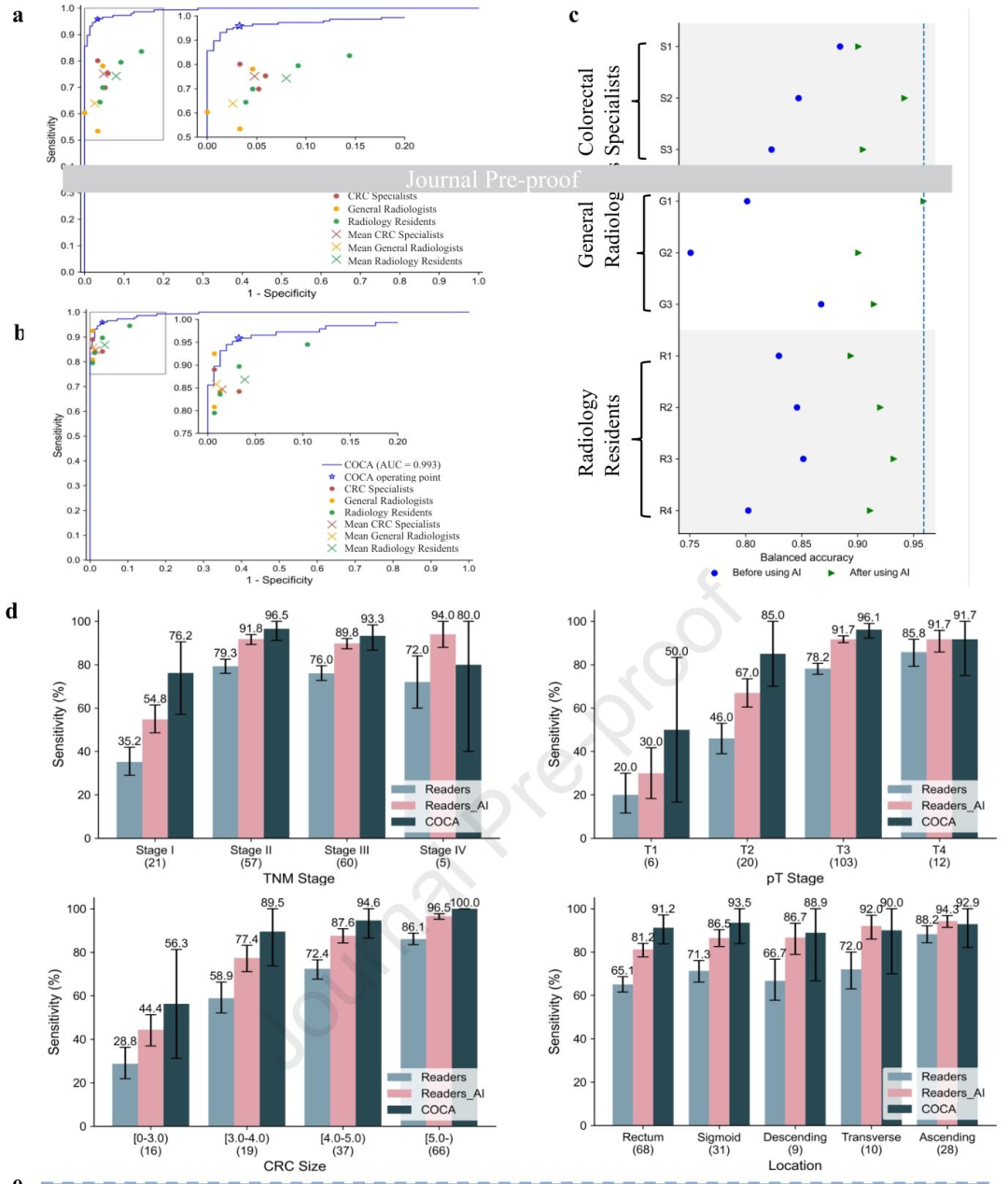
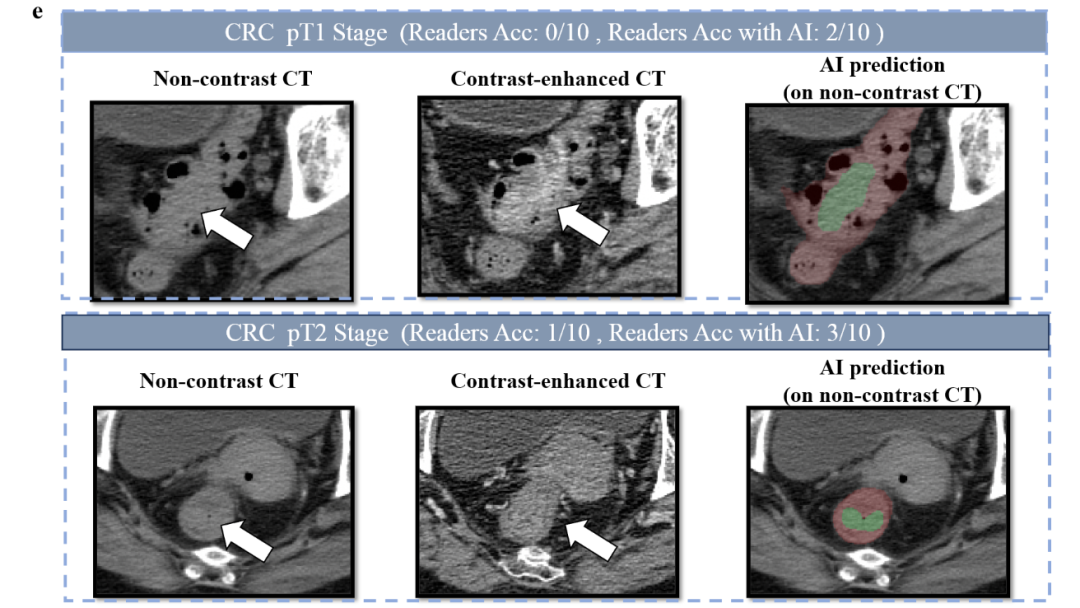
图 3-读者研究与AI辅助效果: 该图对比了10名放射科医生(专科、普放、住院医师)单独及在COCA辅助下的CRC检出性能。a :COCA独立诊断较医生平均敏感性提高20.4% ,特异性提高5.4%。b :AI辅助后医生平均敏感性提升14.5%,特异性提升3.1%。c :各经验层级医生的平衡准确率均有改善 ,普放医师提升最显著(75.6%→90.3%)。d :亚组分析显示AI辅助对早期(pT1/pT2)和直肠乙状结肠肿瘤的检出帮助最大。e:展示了两个被医生遗漏但AI成功检出的早期CRC案例,突显辅助价值。
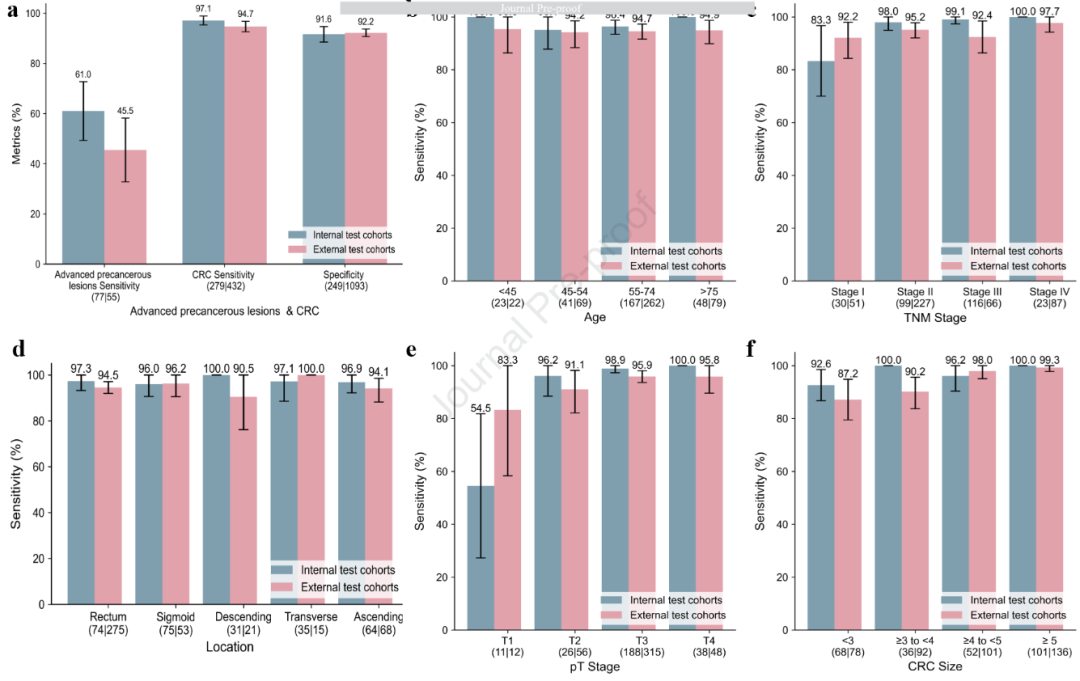
图 4-高灵敏度版COCA对早期CRC和癌前病变的检测: 该图评估了专为平均风险人群筛查设计的高灵敏度模型(验证集敏感性>95%)。a :对晚期癌前病变 ,内部测试敏感性为61.0% ,外部为45.5%;对I期CRC 敏感性分别达83.3% 和92.2% ,远超cfDNA血液检测(13.2%)和多靶点粪便DNA检测(43.4%)。b-f 按年龄、位置、分期、T分期和肿瘤大小展示敏感性:<3cm肿瘤敏感性92.6% (内部)和87.2%(外部),<45岁人群敏感性100%(内部)。证明该模型能显著提升早期病变的检出机会。
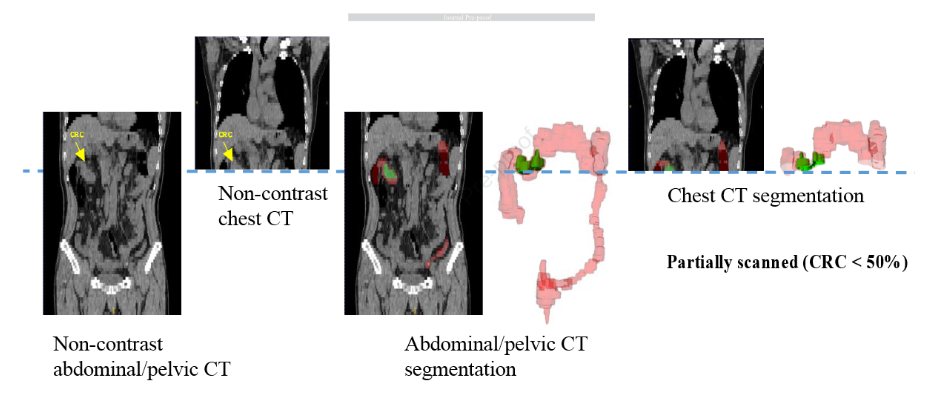
图 5-胸部CT中的CRC检测可行性: 该图示例展示了一名CRC患者的非增强CT图像,包括腹部/盆腔CT和胸部CT,并分别用红色(肠管) 和绿色(肿瘤) 显示了COCA的分割结果。尽管胸部CT仅扫及部分横结肠(肿瘤体积<50%),模型仍能成功检测出CRC成分。在11例胸部CT测试中,COCA达到81.8%敏感性 和99.9%特异性;同一患者腹部CT扫描时敏感性升至90.9%。这表明即使肠道显示不全,COCA也能从常规胸部CT中实现机会性CRC筛查,扩大了应用场景。
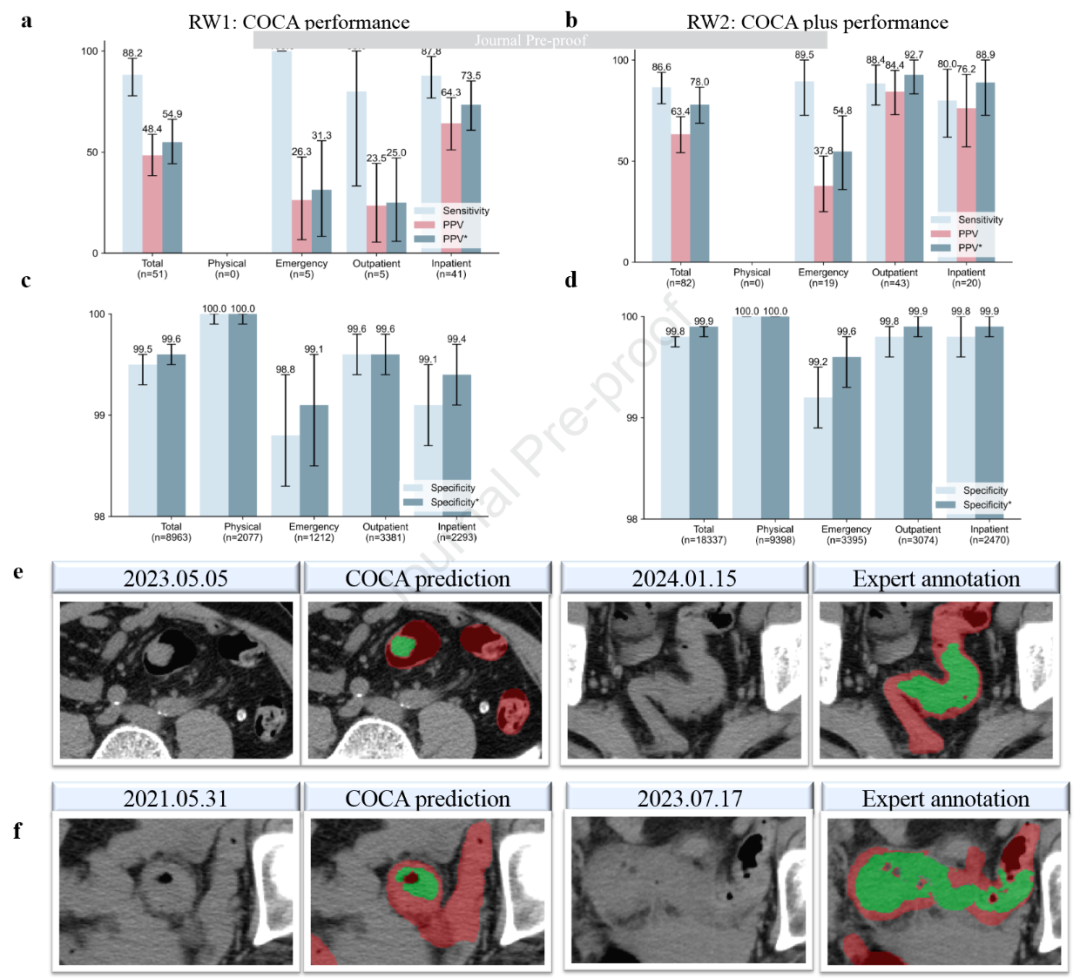
图 6-真实世界临床评估: 该图展示了两个大型连续患者队列(RW1 n=9,016;RW2 n=18,427)中的验证结果。a-d :RW1中COCA敏感性88.2%、特异性99.5%、阳性预测值48.4%;排除有临床意义假阳性后PPV升至54.9%。RW2(COCA Plus) 敏感性86.6%、特异性99.8% 、PPV显著提升至63.4% 。e-f 展示了两个初始报告漏诊的CRC病例:e中肿瘤在2023年CT未被发现,至2024年明显增大;f中肿瘤被漏诊两年。COCA均成功识别,证明了其在真实临床场景中减少漏诊、改善患者管理的潜力。
05
研究结论
该研究开发了一种基于非增强CT和深度学习的新型结直肠癌(CRC)筛查模型COCA,并在多中心、国际队列中进行了系统验证。研究结论表明:COCA在内部和外部验证集中均表现出极高的诊断性能 (AUC 0.967--0.996),显著优于不同年资放射科医生 ,可提高敏感性20.4%、特异性5.4%。在真实世界连续27,433例患者 中,COCA保持敏感性86.6%--88.2%、特异性99.5%--99.8% ,并成功检出了5例初始影像报告漏诊的CRC 。高灵敏度版本对早期CRC(I期敏感性83.3%--92.2%)及晚期癌前病变(敏感性45.5%--61.0%) 具有检测能力,且模型在胸部CT部分肠段覆盖下仍可行 (敏感性81.8%)。通过增量学习升级的COCA Plus进一步降低漏诊率、提高阳性预测值。综上,COCA利用常规非增强CT实现非侵入性、无需肠道准备、低成本、可大规模部署的机会性CRC筛查,弥补了现有筛查手段依从性低、覆盖不足的缺陷,有望显著降低CRC漏诊率并改善患者预后。
06
Q&A
Q1:与放射科医生相比,COCA表现如何?
A1: 在读者研究中,COCA的检测敏感性比10位不同年资的放射科医生平均高出20.4% ,特异性高出5.4% ,定位准确率高出22.0% 。在AI辅助下,医生们的平均敏感性提升了14.5% ,特异性提升了3.1%,尤其对早期、小肿瘤和直肠/乙状结肠部位提升明显。
Q2:COCA在实际临床中的应用价值是什么?
A2: 在两个真实世界队列中,COCA成功检测出多例被初次报告漏诊的CRC ,部分病例因此避免了数月至一年的诊断延迟。模型可作为预读系统嵌入PACS,自动标记可疑病灶,辅助医生尤其是非专科医生提高诊断质量。其高特异性(>99%)也有助于减少不必要的肠镜转诊。
Q3:COCA的局限性和未来方向是什么?
A3:局限性 :当前模型仅针对CRC检测,无法识别其他肠道疾病(如炎症性肠病、良性息肉);部分假阳性对应临床有意义但非CRC的病变;模型对某些CT扫描协议存在性能下降。未来方向:计划开展前瞻性机会性筛查研究 和人群筛查项目 ;进一步扩展模型对多种肠道病变的识别能力;推动FDA等监管批准,并解决患者知情同意、数据隐私等伦理与合规问题。
参考文献:Chen X, Qiu MY, Zhang JP, Xia YD, Cao K, Cao WW, Yao LS, Lambert L, Li SY, Liang YT, Lin H, Yu YF, Yao JW, Guo WC, Xu J, Zheng ZL, Mao Y, Chen ZW, Shi Y, Kovarnik T, Vocka M, Ye XH, Zhou J, Xie CM, Wang QF, Guo YM, Liang D, Ma ZL, Lai LS, Huang X, Jia YL, Zhang L, Liu ZY. Colorectal cancer detection using non-contrast CT and deep learning: a multicenter and international cohort study. Ann Oncol. 2026 Apr 21:S0923-7534(26)00150-X. doi: 10.1016/j.annonc.2026.04.009.