01
文献学习

今天分享的文献是由广东省人民医院放射科刘再毅等团队于2024年10月在《Science Bulletin》(中科院1区top,IF=21.1)上发表的研究"Integrated analysis of radiomics, RNA, and clinicopathologic phenotype reveals biological basis of prognostic risk stratification in colorectal cancer "即放射组学、RNA与临床病理表型的整合分析揭示结直肠癌预后风险分层的生物学基础,该研究提出并验证了一种基于CT影像的放射组学预后签名,用于结直肠癌患者的风险分层。通过多阶段放射基因组学分析(包括前向与反向工程验证、宏观与微观生物学关联验证),揭示了该放射组学签名与肿瘤增殖、免疫炎症等相关分子通路的关联。研究还验证了该签名在不同人群和外部数据集中的泛化能力,并探讨了其在II期结直肠癌患者辅助化疗决策中的潜在临床价值。
关键词:结直肠癌、放射组学、放射基因组学、预后风险分层、肿瘤微环境、CT影像、RNA测序、多模态整合分析
创新点:①首次提出"正向-反向影像基因组学"紧密整合策略 ,系统解析影像、基因与表型关联,突破单一方向分析局限。②从宏观影像到微观分子通路进行多层次生物学验证 ,揭示免疫-炎症-增殖 等关键通路与影像风险的关联。③构建具有生物学可解释性的泛化预后影像组学标志物,在多中心及外部队列中验证稳定,填补临床转化空白。
临床价值:①指导II期结直肠癌辅助化疗决策 ,识别低风险患者避免过度治疗,实现精准分层与个体化治疗 。②基于常规CT影像实现无创预后风险分层 ,C-index达0.864,为术前评估提供便捷、可重复工具。③揭示影像组学风险背后的免疫微环境与增殖表型,为联合靶向/免疫治疗策略提供生物标志物依据。
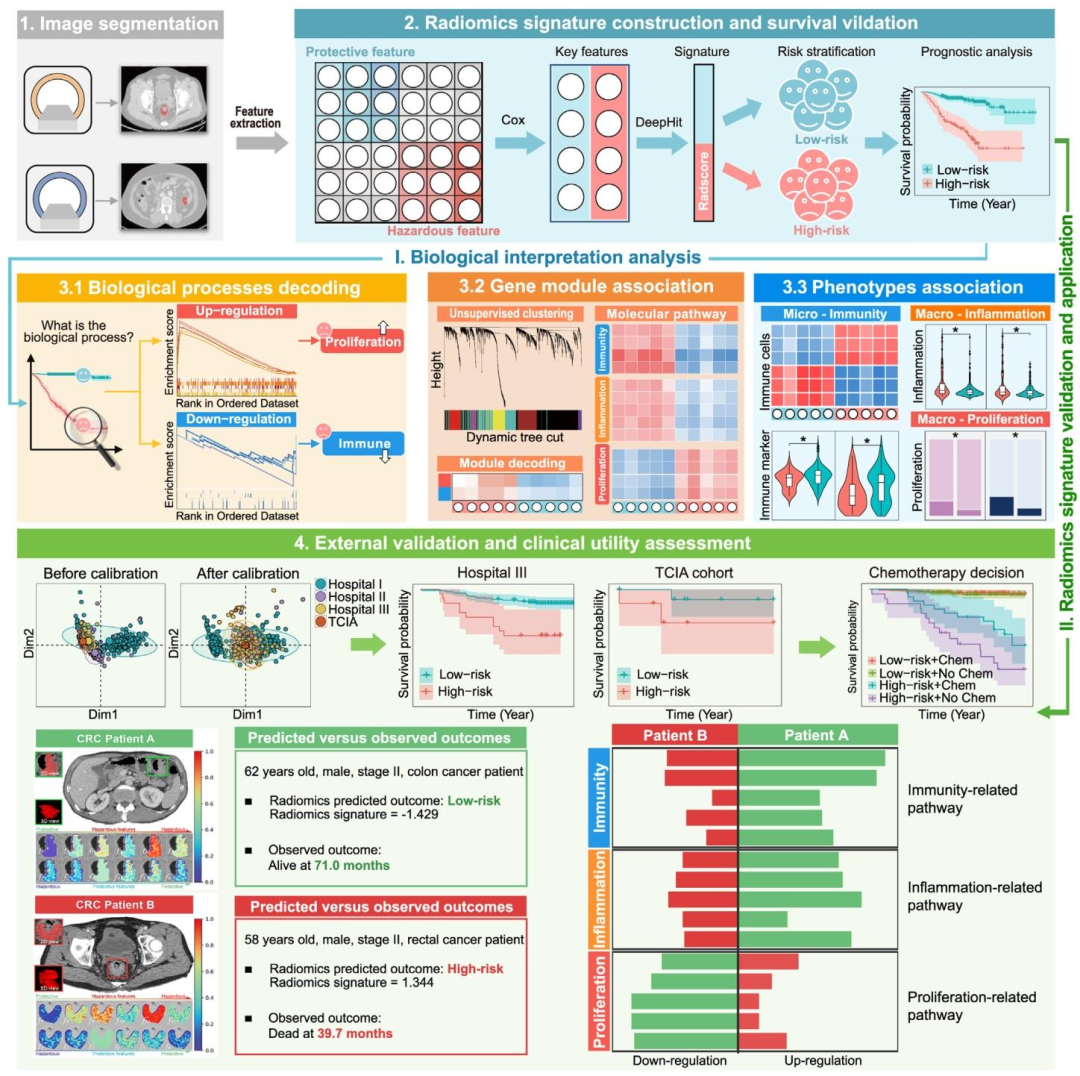
图 1:研究整体工作流程图
图像分割
操作:使用自研DeepCRC自动化工具完成CT肿瘤靶区分割,由2名高年资放射科医师复核。
影像组学特征构建与生存验证
流程:特征筛选→构建影像组学签名→风险分层→预后分析。
算法:采用DeepHit(竞争风险生存分析)、Cox回归模型。
输出:将患者分为高风险/低风险组,完成预后效能验证。
生物学解析分析
3个维度:
①生物学过程解码(分子通路差异);
②基因模块关联(WGCNA共表达网络);
③表型关联(微观免疫+宏观增殖)。
核心:打通影像表型→分子机制→临床表型的关联链条。
外部验证与临床效用评估
验证:多中心队列(国内3家医院+TCIA)、模型校准前后对比。
临床应用:指导Ⅱ期结直肠癌化疗决策。
典型病例展示(2例Ⅱ期CRC患者)
病例A(低风险):62岁男性结肠癌,免疫相关通路激活;随访71.0个月仍生存。
病例B(高风险):58岁男性直肠癌,增殖/炎症相关通路激活;随访39.7个月死亡。
02
研究背景和目的
研究背景
结直肠癌(colorectal cancer, CRC)是全球常见的恶性肿瘤,其预后评估对于个体化治疗决策至关重要。近年来,放射组学 (radiomics)作为一种从医学影像中高通量提取定量特征的技术,展现出预测CRC预后的巨大潜力。然而,放射组学的临床转化面临关键障碍------风险分层的生物学基础尚不明确 ,即影像特征与肿瘤潜在分子机制之间的关联缺乏系统解释。为此,研究者转向放射基因组学(radiogenomics),试图通过整合影像与基因组数据揭示二者关系。但现有研究多采用单向关联分析 ,仅从影像到基因或从基因到影像的单向推断,证据力度不足,难以真正阐明微观分子事件与宏观影像表型之间的因果联系。此外,不同医疗中心、不同扫描设备带来的批次效应 也严重影响放射组学模型的泛化能力。因此,亟需发展一种多阶段、双向整合的放射基因组学策略,通过前向与反向工程相结合的方法,验证微-宏观生物学关联,并在多中心数据集中进行外部验证,从而为放射组学特征赋予明确的生物学解释,推动其向临床实践转化。
研究目的
本研究旨在实现双重目标。第一,建立一种基于CT图像的、具有泛化能力的结直肠癌预后放射组学特征 ,能够在多个独立数据集中稳定地对患者进行高、低风险分层,并评估其作为独立预后因子的价值。第二,通过多阶段放射基因组学分析,深入揭示放射组学、基因组学与临床病理表型之间的复杂相互作用 ,弥补现有研究在生物学解释上的不足。具体而言,研究采用前向与反向放射基因组学工程相结合的方法,首先识别与放射组学风险分组相关的关键分子通路和核心基因 (如C5AR1、MIF、CSF1、AURKA、PLK4等),进而验证这些分子变化与免疫微环境表型、炎症指标、病理增殖特征 等宏观表型的关联。最终,研究还探索了该放射组学特征在指导II期CRC患者辅助化疗决策中的潜在临床应用价值,旨在识别可能从强化治疗中获益的高危亚群,同时避免低危患者接受不必要的治疗。通过系统性整合影像、转录组和临床数据,本研究期望为放射组学的临床转化提供坚实的生物学基础,推动结直肠癌的精准医学发展。
03
数据和方法
研究数据
放射组学训练集:来源于广东省人民医院(GDPH)和重庆医科大学附属第一医院(FAHCMU),共 676 例患者,用于构建放射组学预后签名。
放射组学内部验证集:同样来源于 GDPH 和 FAHCMU,共 291 例患者,用于内部验证签名性能。
放射组学外部验证集 1:来源于云南肿瘤医院(YNCH),共 169 例中国结直肠癌患者,用于外部验证(中国人群)。
放射组学外部验证集 2:来源于癌症影像档案馆(TCIA),共 20 例国际患者,用于外部验证(国际人群)。
放射基因组学发现集:来源于 GDPH 中有 RNA-seq 数据的患者,共 150 例,用于探索放射组学风险分层的生物学机制。
放射基因组学内部验证集:同样来源于 GDPH 中有 RNA-seq 数据的患者,共 58 例,用于验证生物学发现。
**影像数据:**术前CT图像
分子数据: RNA-seq
临床数据: OS、病理、实验室指标等
技术方法
**影像预处理:**重采样、灰度离散化、ComBat去批次效应
肿瘤分割: DeepCRC自动分割 + 放射科医生验证
特征提取: PyRadiomics提取1037个特征
**特征选择:**重复性分析、单变量Cox、LASSO回归
模型构建: DeepHit算法(生存分析)
放射基因组学分析:
签名水平:GSEA富集分析
特征水平:加权基因共表达网络分析 + GSVA
表型水平:免疫细胞浸润、实验室指标、病理标志物
临床验证: Kaplan-Meier、C-index、亚组分析(II期CRC)
04
实验结果
放射组学签名性能:
训练集 C-index = 0.864(95% CI: 0.838--0.890)
内部验证集 C-index = 0.734(95% CI: 0.662--0.806)
外部验证集(YNCH)C-index = 0.704
TCIA队列 C-index = 0.848
生物学机制:
高风险组:肿瘤增殖通路(如细胞周期)上调
低风险组:免疫相关通路(如巨噬细胞、NK细胞趋化)上调
关键基因:C5AR1, MIF, CSF1, AURKA, PLK4
免疫与病理表型:
低风险组:更高的淋巴细胞、CD4+/CD8+ T细胞
高风险组:更高的中性粒细胞、NLR、SII、Ki67、LVI、PNI
临床决策支持:
高风险II期CRC患者可能从化疗中获益
低风险II期患者可避免不必要的化疗

图 2:影像组学预后特征构建及潜在生物学过程探究
(a):DeepHit算法构建影像组学特征流程(b):Kaplan--Meier生存曲线(c):高风险组上调/下调通路富集(d):5个核心基因表达箱线图(e):WGCNA基因聚类树与模块划分(f):关键影像特征-通路富集分数相关性热图(g):风险组-微观免疫表型关联(h):影像特征-28种免疫细胞浸润相关性热图(i):风险组-宏观免疫炎症表型关联(j):风险组-病理增殖表型关联
05
研究结论
该研究通过整合CT影像组学、RNA测序及临床病理表型 ,首次采用正向与反向放射基因组学联动策略,系统揭示了结直肠癌(CRC)预后风险分层的生物学基础 。研究构建了一个基于DeepHit算法的预后影像组学特征,在训练、内部验证及外部验证队列中均表现出稳定的风险分层能力(C-index分别为0.864、0.734和0.704),并能将患者显著区分为高、低风险组(HR=4.912~1.962)。多阶段分析发现,高风险组富集了细胞周期、趋化因子信号及补体激活 等通路,且与C5AR1、MIF、CSF1、AURKA、PLK4 等核心基因表达上调相关。此外,该影像组学特征与微免疫表型 (如免疫细胞浸润减少)、外周血炎症指标 (中性粒细胞/淋巴细胞比值、系统性免疫炎症指数)以及病理增殖特征 (淋巴血管侵犯、神经侵犯)显著关联,从而从宏观影像到微观分子层面验证了其生物学合理性。临床转化价值 方面,在II期CRC患者中,低风险组接受化疗未改善预后,而高风险组(尤其II期结肠癌)可从化疗中获益,提示该特征有助于指导个体化辅助治疗 ,避免低风险患者过度治疗。尽管存在回顾性设计及TCIA样本量小等局限,该研究为影像组学的临床落地提供了可解释的生物学依据,并推动了CRC精准预后评估的发展。
参考文献:Chen X, Huang Y, Wee L, Zhao K, Mao Y, Li Z, Yao S, Li S, Liang Y, Huang X, Dekker A, Chen X, Liu Z. Integrated analysis of radiomics, RNA, and clinicopathologic phenotype reveals biological basis of prognostic risk stratification in colorectal cancer. Sci Bull (Beijing). 2024 Dec 15;69(23):3666-3671. doi: 10.1016/j.scib.2024.10.005.