研究背景
生命活动离不开蛋白质之间、蛋白质与核酸之间的精细互作。这些互作的异常往往与癌症、神经退行性疾病等密切相关。然而,传统研究手段各有短板:亲和纯化依赖高质量抗体,细胞裂解和洗涤过程容易丢失弱或瞬时的结合;化学交联虽能稳定部分互作,却可能引入假阳性,且难以处理不溶性靶点。酵母双杂交及蛋白片段互补法虽适合高通量筛选,但受限于细胞器类型(如膜蛋白不适),过表达易造成假阳性,标签的空间位阻又可能导致假阴性。因此,研究者迫切需要能够在生理条件下原位解析分子互作的新型工具。
一、两种核心酶学标记策略
邻近标记(Proximity Labeling, PL)技术依赖两类工程化酶产生短寿命活性中间体,从而实现空间受限的标记。
过氧化物酶系统(APEX、HRP):在过氧化氢存在下,该类酶将外加的生物素-苯酚转化为高反应活性的苯氧自由基。自由基只能标记与酶(即诱饵蛋白)空间上邻近的内源蛋白,距离稍远的蛋白则几乎不被标记。标记范围受自由基半衰期及细胞内淬灭剂(如谷胱甘肽)的调控。
生物素连接酶系统(BioID、TurboID):该酶利用ATP和生物素催化生成活性中间体生物素-5'-AMP,该中间体扩散后同样优先标记邻近蛋白质。与过氧化物酶不同,其活性受细胞内胺类物质的影响。
两类方法的共同逻辑是:酶促产生的活性物种寿命极短,标记严格限定在诱饵蛋白周围。标记结束后裂解细胞,用链霉亲和素磁珠富集生物素标记的蛋白,经胰酶消化成肽段,再通过液相色谱-串联质谱(LC-MS/MS)鉴定。结合"诱饵-酶融合组"与"仅表达酶的空间参照组"的定量比率分析,即可筛选出真正的互作蛋白。
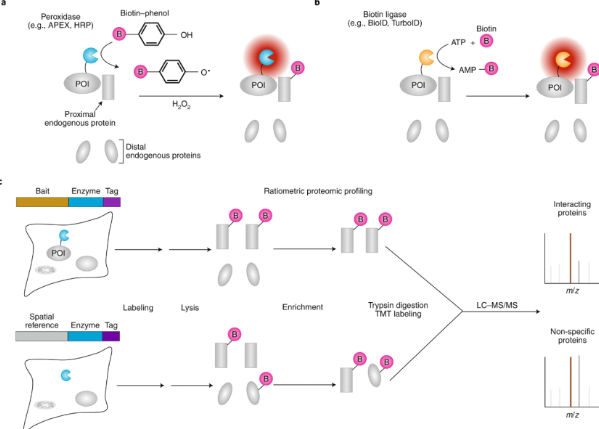
图1 基于过氧化物酶和生物素连接酶的邻近标记方法
二、邻近标记在蛋白质-核酸(RNA/DNA)互作中的应用
蛋白质-RNA互作:
-
间接标记(需交联):将APEX2靶向特定亚细胞区室,先标记邻近蛋白,再通过甲醛(APEX-RIP)或紫外线(Proximity-CLIP)使蛋白与RNA交联,最后用链霉亲和素富集蛋白-RNA复合物,从而捕获特定区域的蛋白-RNA互作。
-
直接标记(无需交联):以蛋白为中心的方法如APEX-seq、CAP-seq,分别利用APEX2直接标记邻近RNA,或利用miniSOG光产生活性氧标记RNA碱基,富集后测序即可鉴定互作RNA。以RNA为中心的方法如RaPID、MS2标签介导的PL及dCas13-based PL,通过BoxB适配体、MS2茎环或dCas13将生物素连接酶(BASU)或过氧化物酶(APEX2)靶向特定RNA(外源标记或内源RNA),实现对RNA结合蛋白的原位标记。
蛋白质-DNA互作 :
以DNA为中心的邻近标记主要基于CRISPR靶向。dCas9-based PL将PL酶与dCas9融合,靶向特定基因组位点,标记邻近的DNA结合蛋白。ChromID则将PL酶(如BASU)与识别特定染色质修饰的"阅读器"结构域融合,从而标记与特定组蛋白修饰相关的蛋白质,弥补了传统ChIP-seq依赖抗体且难以靶向非特异性修饰的不足。
这些方法的设计精髓在于:利用邻近标记"原位标记"的特性,避开传统核酸互作研究中细胞裂解和交联的弊端;同时借助CRISPR或结构域融合实现空间精准靶向,形成适用于多种研究场景的PL技术体系。
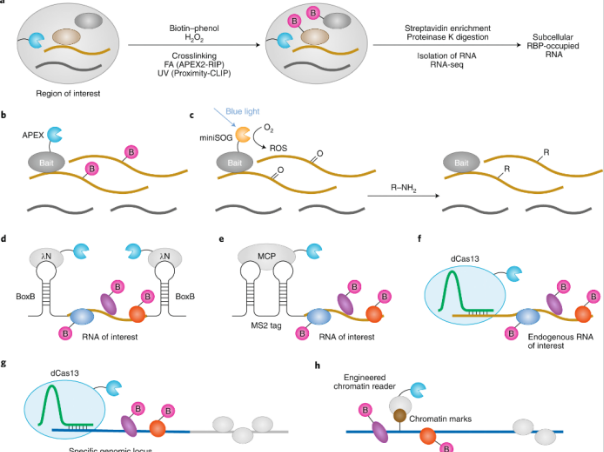
图2 邻近标记(PL)技术在蛋白质-核酸(RNA与DNA)相互作用研究中的应用
三、邻近标记技术的核心优势
-
活细胞/活体原位捕获:在生理状态下发挥作用,能够保留传统方法易丢失的弱互作和瞬时互作,且不依赖高亲和力抗体。
-
灵活的时空分辨率:过氧化物酶类(如APEX2)可实现分钟级快速标记,适合追踪动态过程;生物素连接酶类(如TurboID)无显著细胞毒性,适合长期体内研究(小鼠、植物等)。结合诱导二聚化、分裂酶等策略,可进一步提升亚细胞特异性,精细解析核膜、线粒体膜等区域的互作网络。
-
广泛的适用性:不仅用于蛋白质-蛋白质互作,还可通过适配交联、CRISPR靶向等策略,拓展至蛋白质-RNA、蛋白质-DNA互作,适用于从体外细胞系到多个物种体内系统的多层次研究。