导读
骨质疏松症的诊断不足是一个全球性难题。虽然双能X线吸收测定法(DXA)是被广泛认可的筛查手段,但由于筛查率低、受退行性改变干扰等原因,临床应用存在局限。
近日,发表在 Radiology 上的一项研究不仅开发了一种鲁棒的自动3D ROI放置方法,还提出了一套针对不同CT扫描仪和管电压的标准化校正方案,并建立了大规模多样化人群的骨密度基准值。
研究背景
骨质疏松症(Osteoporosis)虽然可防可治,但长期面临诊断不足的困境。DXA检查虽然普及,但在脊柱退行性改变(如骨赘、血管钙化)存在时,往往会错误地升高骨密度(BMD)读数,从而低估骨折风险。
定量CT(QCT)虽然更准确,但需要校准体模。机会性筛查(Opportunistic Screening)------即利用患者因其他临床指征(如肺结节、肾结石等)拍摄的常规CT进行骨密度分析,成为近年来的研究热点。
然而,AI辅助的机会性筛查面临三大挑战:
1. ROI选择的变异性: 传统的2D ROI易受层面选择影响。
2. 成像参数的不一致: 不同管电压(kVp)和扫描仪型号会导致CT值(HU)漂移。
**3. 基准数据的缺乏:**缺乏基于CT的大规模、多种族人群的正常值参考。
研究方法
本研究纳入了283,499名患者的538,946次非增强CT检查,时间跨度从2003年至2024年。
1. 自动化图像分割与3D ROI放置
研究团队开发了一个卷积神经网络(CNN),用于自动分割脊柱解剖结构。
3D vs 2D: 不同于传统的单层2D ROI,该算法自动计算椎体体积,并放置一个体积为椎体5%的球形 3D ROI 。
**定位策略:**ROI自动定位在分割出的椎体内部CT值最低的区域(避开致密骨岛),且位于椎体基底静脉孔的前方。
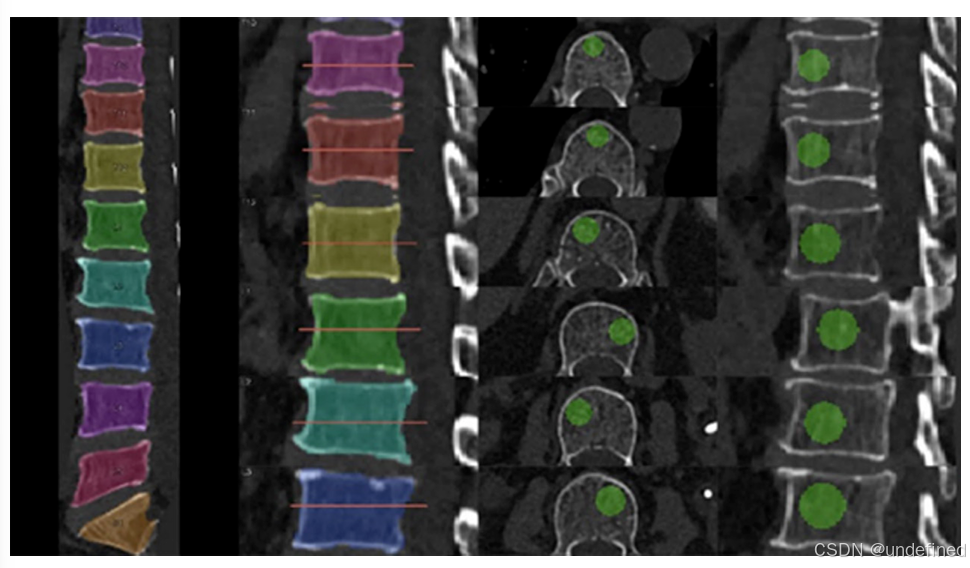
图1:胸椎和腰椎椎体内3D ROI的放置示意图。
2. 跨设备的统计学校正(Harmonization)
由于数据来自 43种 不同的CT扫描仪型号和 6种 不同的管电压,研究提出了一种线性缩放方法将所有HU值校准至 120 kVp 和参考扫描仪标准。
3. 验证与基准建立
验证: 由3名资深放射科医生对1496个椎体的自动ROI放置进行人工审核。
**基准:**根据WHO定义的骨质疏松患病率,计算特定年龄段女性的CT值百分位数,从而反推基于CT值的诊断阈值。
研究结果
1. 技术鲁棒性与一致性
算法准确性: 放射科医生与AI算法在ROI放置上的一致性高达99.9%。
参数影响: 研究发现,管电压(kVp) 对CT值的影响显著,80 kVp与120 kVp下的CT值差异高达 23% ;而不同 扫描仪型号 带来的差异相对较小,普遍 <10% 。
**ROI方法差异:**3D ROI测得的CT值平均比传统2D方法低35 HU。这意味着不能直接沿用以往文献中的2D阈值。
2. 骨密度随年龄变化的趋势
数据清晰地展示了骨密度随年龄下降的轨迹:
女性: 绝经期前后出现陡峭的下降趋势。
男性: 呈近乎线性的下降。
**性别差异:**50岁以下,女性骨密度高于男性;50岁以上,男性骨密度高于女性(P < .001)。
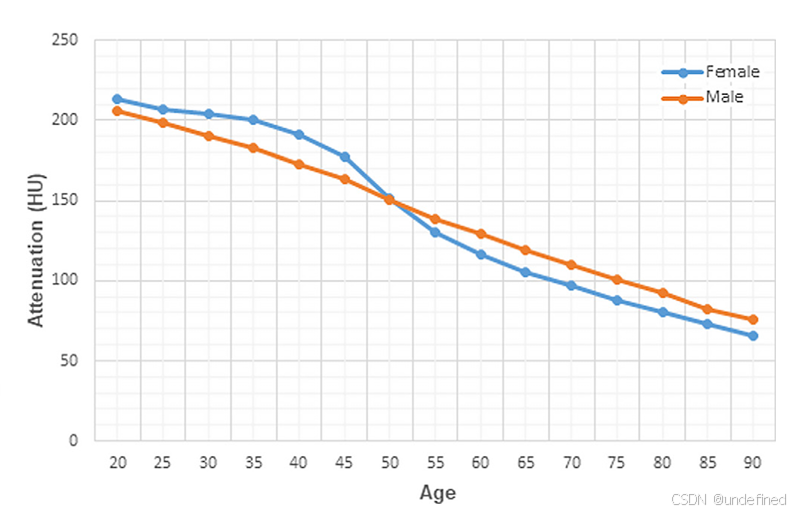
图3:L1椎体平均骨小梁衰减值(HU)随年龄和性别的变化曲线。
3. 基于种族的骨密度差异
本研究提供了基于种族的详细统计数据。在控制变量后,不同种族群体的骨密度表现出显著差异(P < .001):
黑人(Black)患者: 骨小梁衰减值最高。
65-69岁女性 L1均值:131 ± 44 HU
65-69岁男性 L1均值:146 ± 47 HU
亚裔(Asian)患者: 居中。
65-69岁女性 L1均值:108 ± 42 HU
65-69岁男性 L1均值:120 ± 41 HU
白人(White)患者: 骨小梁衰减值最低。
65-69岁女性 L1均值:98 ± 32 HU
65-69岁男性 L1均值:111 ± 37 HU
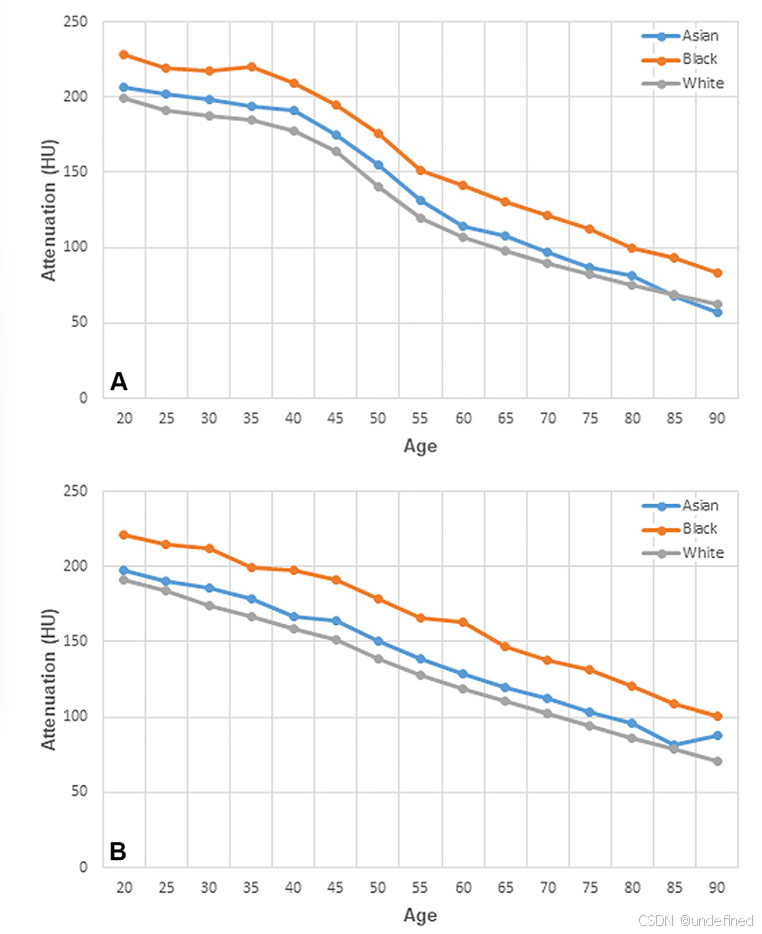
图5:不同种族患者L1椎体骨小梁衰减值的差异(A为女性,B为男性)。
此外,在西班牙裔(Hispanic)与非西班牙裔(Non-Hispanic)的对比中,男性群体表现出显著差异(西班牙裔男性骨密度更高),而女性群体差异无统计学意义(P = .36)。
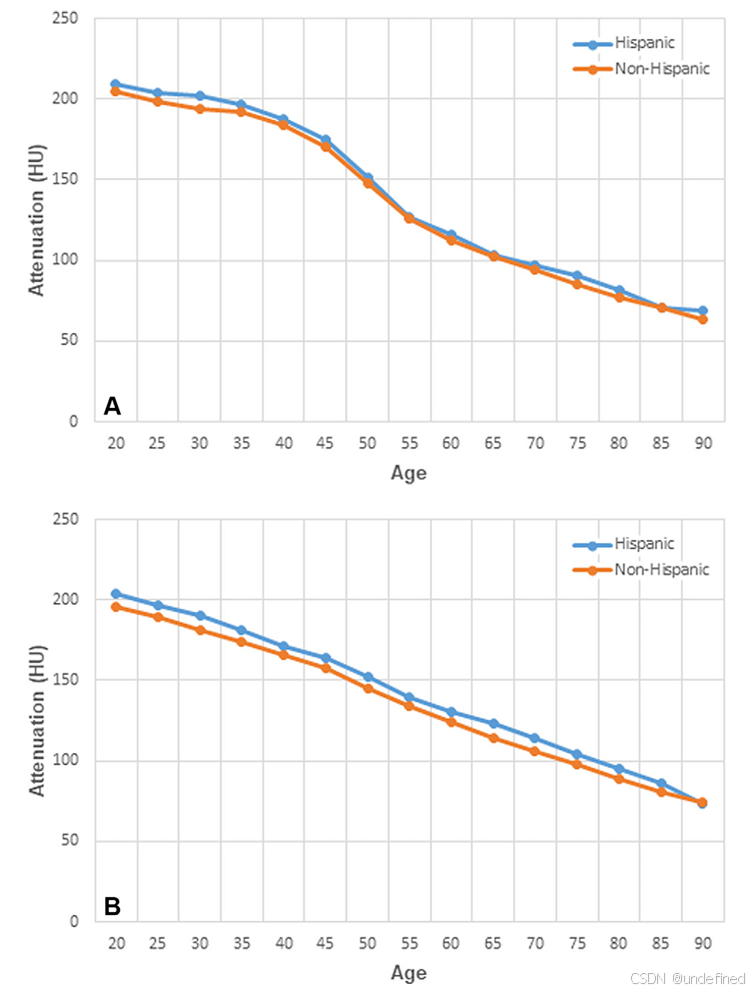 图6:西班牙裔与非西班牙裔患者的骨密度对比(A为女性,B为男性)。
图6:西班牙裔与非西班牙裔患者的骨密度对比(A为女性,B为男性)。
4. 诊断阈值的确立
基于3D ROI方法,研究确定了针对 L1椎体 的骨质疏松症诊断阈值:
|---------------------|------------|
| 分类 | CT值阈值 (L1) |
| 骨质疏松 (Osteoporosis) | < 80 HU |
| 骨量减少 (Osteopenia) | < 117 HU |
*注:该阈值低于既往2D方法通常引用的100-115 HU,临床应用时需注意测量方法的匹配。
讨论与总结
这项研究不仅仅是一次大规模的数据回顾,它为人工智能与医学结合的落地应用提供了两个重要的工程化思路:
1. 数据标准化的重要性: 在缺乏体模校准的回顾性数据集中,利用统计学方法对管电压和机型进行校正,是实现跨中心AI模型泛化能力的关键步骤。
**2. 精细化的基准值:**AI的应用不能脱离流行病学背景。该研究建立的分性别、分年龄、分种族的基准数据库,揭示了黑人患者骨密度普遍高于白人和亚裔患者的生理性差异。这提示我们在未来的算法设计中,可能需要考虑种族特异性的风险阈值,以避免算法偏见。
局限性提示: 虽然样本量巨大,但数据主要来自美国东北部的医疗机构,且未排除服用骨代谢药物的患者。此外,3D ROI取最低值的策略导致其阈值与其他研究不可直接互换。
结论: 基于深度学习的自动化CT机会性筛查,能够有效利用现有的临床CT影像识别低骨量人群。通过标准化的校正方法和细分人群的基准值建立,该技术有望在不增加辐射剂量和患者成本的前提下,大幅提高骨质疏松症的检出率。
点击文末 "阅读原文"查看全文
|----------------------------------------------------------------|
| European Radiology | GPT-4o能否替代人工标注?基于LLM的不确定性标签提取在上肢X光中的应用研究 |
| Medical image analysis | BUFNet:融合边界感知与不确定性量化,攻克MR脑肿瘤分割难题 |
| MICCAI | 首个全身PET/CT病灶自动描述框架:结合CLIP与位置引导策略,实现精准高效的病灶描述 |